Mitotan
Mitotan ist ein Arzneistoff, der als Zytostatikum selektiv die Zellteilung in der Nebennierenrinde hemmt. Er wird in der Humanmedizin bei nichtoperablen Nebennierenrindenkarzinomen, in der Veterinärmedizin zur Therapie des Cushing-Syndroms eingesetzt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-Mitotane_Enantiomers_Structural_Formulae.png.webp) | ||||||||||||||||||||||
| (R)-Form (links) und (S)-Form (rechts) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Mitotan | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C14H10Cl4 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 320,04 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
in Wasser 0,1 mg·l−1, löslich in Ethanol, Isooctan und Tetrachlormethan[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Humanmedizin
In der Humanmedizin sind Tabletten mit dem Wirkstoff Mitotan zur symptomatischen Behandlung des fortgeschrittenen, nicht-operablen, metastasierenden oder rezidivierenden Nebennierenrindenkarzinoms zugelassen. Da es nur wenige Patienten mit einem Nebennierenrindenkarzinom gibt, gilt die Krankheit als selten, und das Medikament wurde am 12. Juni 2002 als Arzneimittel für seltene Leiden („Orphan-Arzneimittel“) ausgewiesen.[4]
Veterinärmedizin
In der Veterinärmedizin wird Mitotan zur Therapie einer Überfunktion der Nebenniere, des sogenannten Cushing-Syndroms, eingesetzt. Es kann sowohl zur Behandlung des primären (adrenokortikalen) als auch des sekundären (hypophysären) Cushings eingesetzt werden. Der Wirkstoff wirkt selektiv zytotoxisch auf die Zona fasciculata und Zona reticularis der Nebennierenrinde und bewirkt eine Nekrose der glukokortikoidproduzierenden Zellen und damit eine verminderte Ausschüttung von Cortison. Die Therapie mit Mitotan kann dauerhaft erfolgen und damit eine Einschränkung der Funktionsfähigkeit der Nebenniere bewirken. Alternativ ist eine kurzzeitige hochdosierte Anwendung zur Zerstörung des Organs möglich, ein eventuell dadurch ausgelöster Morbus Addison ist medikamentös zu behandeln.[5]
Infolge der potenziellen Toxizität auch für Menschen müssen im Umgang mit Mitotan Vorsichtsmaßnahmen getroffen werden, die eine ungewollte Aufnahme verhindern. Dazu gehört, neben dem Tragen von Gummihandschuhen bei der Applikation, die konsequente Beseitigung des vom Tier gebildeten Kotes; Schwangere sollten mit dem behandelten Tier nicht in Kontakt kommen.
Mitotan kann auch zur Behandlung einer Alopecia X angewendet werden.[6]
In den letzten Jahren wurde Mitotan nahezu vollständig durch Trilostan verdrängt. Es gibt kein in Deutschland zugelassenes Präparat auf der Basis von Mitotan, so dass das zugelassene Präparat auf Trilostan-Basis (Handelsname Vetoryl) gemäß § 56a Abs. 2 des Arzneimittelgesetzes vorzuziehen ist. Zudem hat Trilostan eine wesentlich kürzere Wirkdauer und ist damit verträglicher.[7] Die Anwendung von Mitotan bei Lebensmittel liefernden Tieren ist verboten, da der Wirkstoff nicht in der Verordnung (EU) Nr. 37/2010 aufgeführt ist. Auch in der Schweiz ist Mitotan kein Wirkstoff, der als Bestandteil eines zugelassenen verwendungsfertigen Tierarzneimittels verkehrsfähig ist.[8]
Synthese
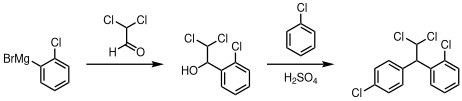
Mitotan kann ausgehend von (2-Chlorphenyl)mangesiumbromid synthetisiert werden. In einem ersten Schritt erfolgt die Umsetzung mit Dichloracetaldehyd, in einer weiteren Reaktion mit Chlorbenzol und Schwefelsäure wird Mitotan als Produkt erhalten.[9]
Sonstiges
o,p′-DDD ist im technischen DDT als Nebenprodukt mit einem Anteil von etwa 0,1 % enthalten, sein Isomer p,p′-DDD wurde in den USA in den 1950er-Jahren als Insektizid verwendet.[2]
Handelsnamen
- Lysodren
Weblinks
- Eintrag zu Mitotan bei Vetpharm
- Government of Canada: Benzene, 1-chloro-2-[2,2-dichloro-1-(4-chlorophenyl)ethyl]- (Mitotane)
- Environment Canada & Health Canada: RISK MANAGEMENT SCOPE for Benzene, 1-chloro-2-[2,2-dichloro-1-(4-chlorophenyl)ethyl]- (Mitotane), 2013.
Einzelnachweise
- Datenblatt 1-(2-Chlorophenyl)-1-(4-chlorophenyl)-2,2-dichloroethane bei Sigma-Aldrich, abgerufen am 9. November 2021 (PDF).
- U.S. Department of Health and Human Services, Agency for Toxic Substances and Disease Registry: Toxicological profile for DDT, DDE and DDD. (PDF; 5,6 MB), 2002.
- The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1073, ISBN 978-0-911910-00-1.
- Lysodren: Europäischer öffentlicher Beurteilungsbericht (EPAR) und Produktinformation, Übersicht auf der Website der Europäischen Arzneimittelagentur.
- Eintrag zu Mitotan bei Vetpharm, abgerufen am 24. September 2018.
- Meike Horn: Post-clipping Alopezie vs. Alopecia X – Fakten, Diagnostik und Therapieansätze. In: veterinärspiegel Heft 4, 2017, S. 135–140.
- Eintrag zu Trilostan bei Vetpharm, abgerufen am 26. September 2018.
- Swissmedic: Zugelassene Verfahren und Wirkstoffe (Memento vom 27. September 2018 im Internet Archive), Stand 31. August 2018.
- Axel Kleemann: Pharmaceutical Substances. 5th ed. Thieme, Stuttgart 2009, ISBN 978-1-62198-377-4.