Arginin
L-Arginin ist eine proteinogene α-Aminosäure. Für den Menschen ist sie semi-essentiell. Der Name leitet sich vom lateinischen Wort argentum (Silber) ab, da die Aminosäure zuerst als Silber-Salz isoliert werden konnte. Diese Aminosäure hat den höchsten Masseanteil an Stickstoff von allen proteinogenen Aminosäuren. Im Dreibuchstabencode wird L-Arginin mit Arg und im Einbuchstabencode als R abgekürzt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
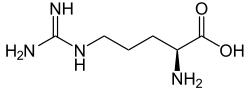 | ||||||||||||||||||||||
| Strukturformel von L-Arginin, dem natürlich vorkommenden Enantiomer | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Arginin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
| |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
0,7 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
| |||||||||||||||||||||
| Löslichkeit |
gut in Wasser (150 g·l−1 bei 20 °C)[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Enantiomere
Arginin besitzt ein Stereozentrum, somit existieren zwei chirale Enantiomere.
In den Proteinen kommt ausschließlich L-Arginin [Synonym: (S)-Arginin] peptidisch gebunden vor. Enantiomer dazu ist das spiegelbildliche D-Arginin [Synonym: (R)-Arginin], das in Proteinen nicht vorkommt. Racemisches Arginin [Synonyma: DL-Arginin und (RS)-Arginin] besitzt geringe Bedeutung.
Wenn in Texten oder in der wissenschaftlichen Literatur „Arginin“ ohne weiteren Namenszusatz (Präfix) erwähnt wird, ist L-Arginin gemeint.
| Enantiomere von Arginin | ||
| Name | L-Arginin | D-Arginin |
| Andere Namen | (S)-Arginin | (R)-Arginin |
| Strukturformel |  | 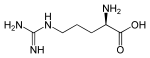 |
| CAS-Nummer | 74-79-3 | 157-06-2 |
| 7200-25-1 (Racemat) | ||
| EG-Nummer | 200-811-1 | 205-866-5 |
| 230-571-3 (Racemat) | ||
| ECHA-Infocard | 100.000.738 | 100.005.334 |
| 100.027.793 (Racemat) | ||
| PubChem | 6322 | 71070 |
| 232 (Racemat) | ||
| DrugBank | DB00125 | DB04027 |
| − (Racemat) | ||
| FL-Nummer | 17.003 | – |
| Wikidata | Q173670 | Q27076987 |
| Q27104032 (Racemat) | ||
Vorkommen
L-Arginin ist weit verbreitet. Die folgenden Beispiele geben einen Überblick über Arginingehalte und beziehen sich jeweils auf 100 g des Lebensmittels, zusätzlich ist der prozentuale Anteil von gebundenem Arginin am Gesamtprotein angegeben.[5]
| Lebensmittel | Protein | Arginin | Anteil |
|---|---|---|---|
| Buchweizenkörner | 13,25 g | 982 mg | 7,4 % |
| Erbsen, getrocknet | 24,55 g | 2188 mg | 8,9 % |
| Erdnuss, geröstet | 23,68 g | 2832 mg | 11,9 % |
| Hähnchenbrustfilet, roh | 21,23 g | 1436 mg | 6,8 % |
| Hühnerei | 12,57 g | 820 mg | 6,5 % |
| Kuhmilch, 3,7 % Fett | 3,28 g | 119 mg | 3,6 % |
| Kürbiskerne | 30,23 g | 5353 mg | 17,7 % |
| Lachs, roh | 20,42 g | 1221 mg | 6,0 % |
| Mais-Vollkornmehl | 6,93 g | 345 mg | 5,0 % |
| Pinienkerne | 13,69 g | 2413 mg | 17,6 % |
| Reis, ungeschält | 7,94 g | 602 mg | 7,6 % |
| Schweinefleisch, roh | 20,95 g | 1394 mg | 6,7 % |
| Walnüsse | 15,23 g | 2278 mg | 15,0 % |
| Weizen-Vollkornmehl | 13,70 g | 642 mg | 4,7 % |
Alle diese Nahrungsmittel enthalten praktisch ausschließlich chemisch gebundenes L-Arginin als Proteinbestandteil, jedoch kein freies L-Arginin.
Geschichte
L-Arginin wurde 1886 erstmals durch den deutschen Chemiker Ernst Schulze und seinen Doktoranden Ernst Steiger aus Lupinenkeimlingen isoliert.[6] 1894 gelang dann dem schwedischen Chemiker Sven Gustaf Hedin die Isolierung von Arginin aus tierischem Material durch die hydrolytische Spaltung von Hornsubstanz.[7] Durch einen Vergleich seines „tierischen“ Arginins mit ihm zur Verfügung gestellten Proben aus dem Labor Schulzes gelang Hedin der Nachweis der Übereinstimmung der beiden Substanzen.[8]
Eigenschaften
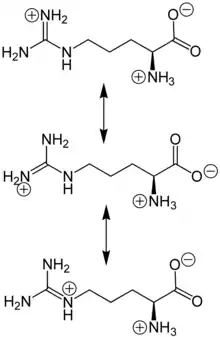
Arginin ist eine α-Aminosäure, die in ihrer Seitenkette eine hydrophile, basisch reagierende Guanidinogruppe enthält. Diese liegt im sauren, neutralen und schwach basischen Milieu protoniert vor, wobei die positive Ladung zwischen den Aminogruppen delokalisiert ist. Gemeinsam mit L-Lysin und L-Histidin gehört L-Arginin zur Gruppe der basischen Aminosäuren oder Hexonbasen.
Arginin liegt im neutralen pH-Bereich überwiegend als „inneres Salz“ bzw. Zwitterion vor, da die α-Aminogruppe und die Guanidinogruppe protoniert vorliegen, wogegen die Carboxygruppe deprotoniert vorliegt. In diesem Zustand trägt Arginin eine positive Netto-Ladung.[9] Die Guanidinogruppe ist eine sehr starke Base, da sie in ihrer protonierten Form als Guanidinium-Ion delokalisierte π-Elektronen besitzt. Sie liegt erst über einem pH-Wert von 12,1 mehrheitlich deprotoniert vor.
Der isoelektrische Punkt, bei dem Arginin keine Netto-Ladung trägt und somit im elektrischen Feld nicht wandert, liegt bei pH 10,8.[10] Bei diesem pH-Wert besitzt Arginin auch seine geringste Löslichkeit in Wasser.
Freies L-Arginin hat einen bitteren Geschmack.[11]
Biosynthese
L-Arginin wird aus den Vorläufern Carbamoylphosphat, L-Ornithin und L-Aspartat synthetisiert. Im ersten Schritt überträgt das Enzym Ornithin-Transcarbamylase unter Abspaltung von Phosphat die Carbamoylgruppe des Carbamoylphosphats auf die δ-Aminogruppe von L-Ornithin, wodurch L-Citrullin entsteht. Im nächsten Schritt werden durch das Enzym Argininosuccinat-Synthase unter ATP-Verbrauch L-Citrullin und L-Aspartat zu Argininosuccinat verknüpft. Durch die Argininosuccinat-Lyase wird Argininosuccinat in L-Arginin und Fumarat gespalten.[12] In Harnstoff-ausscheidenden Tieren ist die Arginin-Biosynthese ein Teil des Harnstoffzyklus, der zur Ausscheidung von überschüssigem Stickstoff dient.
Industrielle Herstellungsverfahren
Für die Herstellung von L-Arginin gibt es zwei Verfahren:[13]
- „Extraktion“ aus Protein-Hydrolysaten von Gelatine, Haaren oder Federn. Dabei wird das Protein-Hydrolysat (Aminosäuregemisch) durch Kristallisation und Ionenaustauscherchromatographie getrennt und so – neben anderen proteinogenen Aminosäuren – L-Arginin isoliert.
- Fermentation.
Das dabei erhaltene L-Arginin kann ggf. in einem weiteren Produktionsschritt durch Umsetzung mit Salzsäure in das stabilere L-Arginin-Hydrochlorid umgewandelt werden.
Funktionen
Die hauptsächliche Funktion von L-Arginin liegt in der Verwendung zum Aufbau von Proteinen. In Pflanzen-Keimlingen und Speicherzellen dient L-Arginin als Reservoir für organischen Stickstoff. L-Arginin dient als Vorläufer bei der Synthese von Kreatin, das in Form von Kreatinphosphat ein wichtiger Energiespeicher bei Wirbeltieren ist. L-Arginin ist ein Metabolit des Harnstoffzyklus, in dem das Ammonium, das beim Abbau von Stickstoffverbindungen (z. B. Aminosäuren) entsteht, in Harnstoff umgewandelt wird. Durch Decarboxylierung kann L-Arginin in Agmatin und weiter in Polyamine umgewandelt werden, die in der Zelle essentielle Funktionen bei der Stabilisierung von DNA, RNA und Membranen haben. L-Arginin ist beim Menschen und bei vielen anderen Tieren die alleinige Vorstufe von Stickstoffmonoxid (NO), einem der kleinsten Botenstoffe im menschlichen Körper. Durch Stickstoffmonoxid (NO)-Synthase entsteht aus L-Arginin der Endothelium-derived relaxing Factor (EDRF), der als NO identifiziert wurde. EDRF führt physiologisch zu einer Gefäßerweiterung, indem das NO in die Muskelschicht der Gefäße diffundiert. Es aktiviert dort die lösliche Guanylatcyclase und führt so zur Erschlaffung der glatten Muskulatur und zum Nachlassen des Gefäßtonus. Studien zeigen, dass Arginin über diese Gefäßerweiterung einen erhöhten Blutdruck signifikant senken kann.[14]
Aufgrund der gefäßerweiternden Funktion findet Arginin im Bodybuilding als sogenanntes „Pump-Supplement“ Anwendung. Weiterhin führt das NO zur Hemmung der Thrombozytenaggregation und -adhäsion. Dadurch wird die Bereitschaft für thrombotische Veränderungen an Gefäßplaque-Rupturen herabgesetzt, dem häufigsten Grund für zerebrale Insulte (Schlaganfall). Es wird angenommen, dass Arginin die unterdrückte Immunantwort bei schweren Verletzungen, Mangelernährung, Sepsis und nach Operationen positiv beeinflussen kann. Bei zusätzlicher Gabe werden eine verbesserte zelluläre Immunantwort, eine Abnahme verletzungsbedingter Funktionsstörungen der T-Zellen und eine verstärkte Phagozytose beobachtet. Zusätzlich wird die Ausbildung der endothelialen Dysfunktion (gestörten Gefäßfunktion) verhindert.[15][16]
1998 erhielten die Wissenschaftler Robert F. Furchgott, Louis J. Ignarro und Ferid Murad für die Erforschung des Zusammenhangs von Arginin und dem körpereigenen sekundären Botenstoff Stickstoffmonoxid (Stickoxid, NO) den Nobelpreis für Medizin.
Neue Studien zeigen zudem, dass eine Supplementation mit Arginin die Freisetzung von Insulin aus den beta-Zellen der Pankreas fördern kann und gleichzeitig die Insulinresistenz signifikant verringert.[17][18] Neben der positiven Wirkung von L-Arginin auf die Glucosetoleranz sowie auf Insulinsensitivität und -produktion führt eine L-Arginin-Supplementation zusätzlich zu einem verbesserten antioxidativen Status.[19]
Arginin antagonisiert die gefährlichen Wirkungen von asymmetrischem Dimethylarginin (ADMA) auf die Blutgefäße. ADMA entkoppelt die Stickstoffmonoxid-Bildung, wodurch eine endotheliale Dysfunktion mit nitrosativem und oxidativem Stress ausgelöst wird.[20][21][22][23][24][25][26]
Bedarf
Der Mensch kann innerhalb des Harnstoffzyklus Arginin selbst synthetisieren, allerdings sind die entstehenden Mengen nicht ausreichend, um den Bedarf vor allem bei heranwachsenden Menschen vollständig zu decken. Daher ist L-Arginin für Kinder essentiell. Aber auch bei Erwachsenen wird der Bedarf an L-Arginin durch die körpereigene Produktion oft nicht ausreichend abgedeckt. Besonders in der Wachstumsphase, durch Stress, bei diversen Krankheiten (z. B. Arteriosklerose, Bluthochdruck, erektile Dysfunktion, Gefäßerkrankungen) oder nach Unfällen übersteigt der Bedarf an Arginin die vom menschlichen Organismus produzierte Menge.[20][21] Auch im Alter steigt der Bedarf an L-Arginin stark an, da der endogene Gegenspieler, das asymmetrische Dimethylarginin (ADMA), um den Faktor 4 ansteigt und damit 40-fach erhöhte Argininkonzentrationen zur Neutralisierung der gefährlichen Effekte dieses Sterblichkeitsfaktors benötigt werden.[20][21][22][23][24][25] Diese Mengen können nur durch eine diätetische Zufuhr gedeckt werden. Entscheidend für den Bedarf an L-Arginin sind daher auch Faktoren wie oxidativer und nitrosativer Stress sowie die ADMA-Spiegel und damit das L-Arginin-ADMA-Verhältnis.[20][26]
Bei einer Proteinzufuhr von etwa 70–90 g/Tag ergibt sich eine rechnerische tägliche Argininzufuhr von ca. 1–5 g/Tag.[20][27]
Medizinische Verwendung
L-Arginin wird zur Behandlung einer schweren metabolischen Alkalose verwendet. In der Kinderheilkunde ist L-Arginin auch zur Behandlung eines durch eine schwere angeborene Stoffwechselstörung bedingten erhöhten Ammoniakgehaltes im Blut (Hyperammonämie) angezeigt. Diagnostisch wird L-Arginin zur Abklärung eines Wachstumshormonmangels bei Minderwuchs eingesetzt.
Als (semi)essentielle Aminosäure ist L-Arginin obligatorischer Bestandteil einer parenteralen Ernährung. In Elektrolyt-Konzentraten zum Zusatz zu Infusionslösungen und in peroralen Diätetika wird L-Arginin ebenfalls eingesetzt.[28]
Pharmazeutisch verwendet wird meistens das L-Arginin-Hydrochlorid.
Arginin wird auch als Zusatz in Zahnpasta verwendet. Verglichen mit einer herkömmlichen Zahnpasta mit Fluoridzusatz wurde eine verbesserte Remineralisierung der Zähne mit einer Kombination aus Arginin, Calciumcarbonat und Fluorid nachgewiesen.[29][30]
Supplemente
Arginin wird zur Supplementierung bei unzureichender Zufuhr oder erhöhtem Bedarf als diätetisches Lebensmittel, insbesondere als Lebensmittel für besondere medizinische Zwecke, gemäß Diätverordnung für verschiedene Krankheitszustände wie erektile Dysfunktion, Arteriosklerose im Frühstadium, Funktionsstörungen der Blutgefäß-Innenwand (endotheliale Dysfunktion) und Bluthochdruck vermarktet.[20][24][25] Diese Indikationen sind für die diätetische Behandlung von Erkrankten etabliert. Ob bei Patienten mit bestehender Herzschwäche die Einnahme von Arginin die körperliche Belastbarkeit oder die Lebensqualität verbessert, bleibt offen – die Ergebnisse einer kleinen, placebokontrollierten Studie verneinen dies.[31]
Die Verwendung gesundheitsbezogener Angaben (health claims), die hingegen den Beitrag von L-Arginin auf gesunde Menschen zur Unterstützung des Kreislaufsystems (Aufrechterhaltung einer normalen Durchblutung, eines gesunden Blutdrucks und der Hämatopoese), zur Unterstützung und Verbesserung der Erektion sowie zur Kräftigung der Muskeln und zur Bereitstellung von Stickoxid im Stoffwechsel betreffen, beurteilte die europäische Behörde für Lebensmittelsicherheit (EFSA) 2011 als wissenschaftlich nicht gerechtfertigt.[32] Einzelne Arbeiten bestätigen die gesundheitsfördernden Wirkungen von L-Arginin bei Gesunden ebenso wie bei Arteriosklerose, endothelialer Dysfunktion und Bluthochdruck und empfehlen die Aminosäure zur Therapie der Herz-Kreislauf-Erkrankungen zugrundeliegenden Stoffwechselstörungen,[14][23][24][25][33][34][35] auch in Kombination mit Vitamin B6, Vitamin B12 und Folsäure.[36] Die hierbei festgestellte mäßige Absenkung des systolischen Blutdrucks war hinsichtlich der Ausgangswerte signifikant, nicht aber im Vergleich mit einer Placebogruppe.[36] Die Halbwertszeit nach der oralen Einnahme von 6 Gramm L-Arginin liegt bei 1,5 bis 2 Stunden.[37]
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6. Auflage. Spektrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage. John Wiley & Sons, New York 2004, ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell. 5. Auflage. Taylor & Francis, 2007, ISBN 978-0-8153-4106-2.
Weblinks
Einzelnachweise
- Eintrag zu ARGININE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- Datenblatt Arginin (PDF) bei Carl Roth, abgerufen am 13. März 2010.
- K.-J. Teresa u. a.: Nickel Ion Complexes of Amino Acids and Peptides. In: Metal Ions in Life Sciences. Band 2: Nickel and Its Surprising Impact in Nature. John Wiley & Sons, 2007, ISBN 978-0-470-01671-8, S. 67; doi:10.1002/9780470028131.ch3.
- Eintrag zu CAS-Nr. 74-79-3 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. März 2011. (JavaScript erforderlich)
- Nährstoffdatenbank des US-Landwirtschaftsministeriums, 22. Ausgabe.
- E. Schulze: In: Berichte der deutschen chemischen Gesellschaft. Band 19, 1886, S. 1177ff.
- S. G. Hedin: In: Zeitschrift für physiologische Chemie. Band 20, 1895, S. 186.
- Sabine Hansen: Entdeckung der Aminosäuren. Berlin 2015 (arginium.de (Memento vom 15. Juni 2016 im Internet Archive)).
- Hans-Dieter Jakubke, Hans Jeschkeit: Aminosäuren, Peptide, Proteine. Verlag Chemie, 1982, ISBN 3-527-25892-2, S. 42.
- Allinger, Cava, de Jongh, Johnson, Lebel, Stevens: Organische Chemie. 1. Auflage. Walter de Gruyter, Berlin 1980, ISBN 3-11-004594-X, S. 1129.
- W. Ternes, A. Täufel, L. Tunger, M. Zobel (Hrsg.): Lebensmittel-Lexikon. 4. Auflage. Behr’s Verlag, Hamburg 2005, ISBN 3-89947-165-2, S. 62–63.
- MetaCyc L-arginine biosynthesis I (via L-ornithine). Abgerufen am 6. Dezember 2020.
- Otto-Albrecht Neumüller (Hrsg.): Römpps Chemie-Lexikon. Band 1: A–Cl. 8. neubearbeitete und erweiterte Auflage. Franckh'sche Verlagshandlung, Stuttgart 1979, ISBN 3-440-04511-0, S. 263–264.
- J. Y. Dong, L. Q. Qin, Z. Zhang, Y. Zhao, J. Wang, F. Arigoni, W. Zhang: Effect of oral L-arginine supplementation on blood pressure: A meta-analysis of randomized, double-blind, placebo-controlled trials. In: Am Heart. Band 162, 2011, S. 959–965, doi:10.1016/j.ahj.2011.09.012.
- U. Landmesser u. a.: Endothelial function: a critical determinant in atherosclerosis? In: Circulation. 109 (21 Suppl 1), 2004, S. II27–II33. PMID 15173060; PDF (freier Volltextzugriff, engl.).
- P. Fürst, H.-K. Biesalki u. a.: Ernährungsmedizin. Thieme-Verlag, Stuttgart 2004, S. 94–95.
- L. D. Monti, E. Setola, P. C. Lucotti, M. M. Marrocco-Trischitta, M. Comola, E. Galluccio, A. Poggi, S. Mammì, A. L. Catapano, G. Comi, R. Chiesa, E. Bosi, P. M. Piatti: Effect of a long-term oral l-arginine supplementation on glucose metabolism: a randomized, double-blind, placebo-controlled trial. In: Diabetes Obes Metab. 14(10), Okt 2012, S. 893–900. doi:10.1111/j.1463-1326.2012.01615.x.
- L. D. Monti, M. C. Casiraghi, E. Setola, E. Galluccio, M. A. Pagani, L. Quaglia, E. Bosi, P. Piatti: L-arginine enriched biscuits improve endothelial function and glucose metabolism: a pilot study in healthy subjects and a cross-over study in subjects with impaired glucose tolerance and metabolic syndrome. In: Metabolism. 62(2), Feb 2013, S. 255–264. doi:10.1016/j.metabol.2012.08.004.
- S. Fazelian, M. Hoseini, N. Namazi, J. Heshmati, M. Sepidar Kish, M. Mirfatahi, A. S. Some Olia: Effects of L-Arginine Supplementation on Antioxidant Status and Body Composition in Obese Patients with Pre-diabetes: A Randomized Controlled Clinical Trial. In: Adv Pharm Bull. 4(Suppl 1), Okt 2014, S. 449–454. doi:10.5681/apb.2014.066.
- A. Ströhle, A. Hahn: Arginin bei Atherosklerose: Diätetische Maßnahmen bei Atherosklerose – Stellenwert von L-Arginin. In: Deutsche Apotheker Zeitung. Teil 1: Band 20, 2012, S. 97–102 (online, freier Volltext) und Teil 2: Band 21, S. 74–83 (online, freier Volltext).
- I. Seljeflot I., B. B. Nilsson, A. S. Westheim, V. Bratseth, H. Arnesen: The L-arginine-asymmetric dimethylarginine ratio is strongly related to the severity of chronic heart failure. No effects of exercise training. In: J. Cardiac. Fail. Band 17, 2011, S. 135–142, doi:10.1016/j.cardfail.2010.09.003.
- M. Anderssohn, M. Rosenberg, E. Schwedhelm, C. Zugck, M. Lutz, N. Lüneburg, N. Frey, R. H. Böger: The L-Arginine-asymmetric dimethylarginine ratio is an independent predictor of mortality in dilated cardiomyopathy. In: J. Card. Fail. Band 18, Nr. 12, 2012, S. 904–911, doi:10.1016/j.cardfail.2012.10.011.
- F. Pizzarelli, R. Maas, P. Dattolo, G. Tripepi, S. Michelassi, G. D’Arrigo, M. Mieth, S. Bandinelli, L. Ferrucci, C. Zoccali: Asymmetric dimethylarginine predicts survival in the elderly. In: Age. Band 35, Nr. 6, 2013, S. 2465–2475 PMC 3824988 (freier Volltext).
- S. M. Bode-Böger, J. Muke, A. Surdacki, G. Brabant, R. H. Böger, J. C. Frölich: Oral L-arginine improves endothelial function in healthy individuals older than 70 years. In: Vasc. Med. Band 8, 2003, S. 77–81, doi:10.1191/1358863x03vm474oa (freier Volltext).
- K. Jung, O. Petrowicz: L-Arginin und Folsäure bei Arteriosklerose. Ergebnisse einer prospektiven, multizentrischen Verzehrsstudie. In: Perfusion. Band 21, 2008, S. 148–156.
- K. Sydow, R. H. Böger: Reloaded: ADMA and oxidative stress are responsible for endothelial dysfunction in hyperhomocyst(e)inaemia: effects of L-arginine and B vitamins. In: Cardiovasc. Res. 2012, doi:10.1093/cvr/cvs205.
- A. Hahn: Nahrungsergänzungsmittel und ergänzende bilanzierte Diäten. Wissenschaftliche Verlagsgesellschaft, Stuttgart 2006, S. 295.
- S. Ebel, H. J. Roth (Hrsg.): Lexikon der Pharmazie. Georg Thieme Verlag, 1987, ISBN 3-13-672201-9, S. 56.
- R. Cantore, I. Petrou, S. Lavender, P. Santarpia, Z. Liu, E. Gittins, M. Vandeven, D. Cummins, R. Sullivan, N. Utgikar: In situ clinical effects of new dentifrices containing 1.5% arginine and fluoride on enamel de- and remineralization and plaque metabolism. In: The Journal of clinical dentistry. Band 24 Spec no A, 2013, S. A32–A44. PMID 24156138.
- I. Petrou, R. Heu, M. Stranick, S. Lavender, L. Zaidel, D. Cummins, R. J. Sullivan, C. Hsueh, J. K. Gimzewski: A breakthrough therapy for dentin hypersensitivity: how dental products containing 8 % arginine and calcium carbonate work to deliver effective relief of sensitive teeth. In: The Journal of clinical dentistry. Band 20, Nummer 1, 2009, S. 23–31. PMID 19489189.
- Iris Hinneburg: Arginin: Schutz von Herz und Kreislauf nicht belegt. In: Medizin transparent. 30. Juni 2020, abgerufen am 13. Juli 2020.
- Carlo Agostoni, Jean-Louis Bresson, Susan Fairweather-Tait, Albert Flynn, Ines Golly, Hannu Korhonen, Pagona Lagiou, Martinus Løvik, Rosangela Marchelli, Ambroise Martin, Bevan Moseley, Monika Neuhäuser-Berthold, Hildegard Przyrembel, Seppo Salminen, Yolanda Sanz, Sean J. J. Strain, Stephan Strobel, Inge Tetens, Daniel Tomé, Hendrik van Loveren, Hans Verhagen: Scientific Opinion on the substantiation of health claims related to L arginine and “immune system functions” (ID 455, 1713), growth or maintenance of muscle mass (ID 456, 1712, 4681), normal red blood cell formation (ID 456, 664, 1443, 1712), maintenance of normal blood pressure (ID 664, 1443), improvement of endothelium-dependent vasodilation (ID 664, 1443, 4680), “physical performance and condition” (ID 1820), “système nerveux” (ID 608), maintenance of normal erectile function (ID 649, 4682), contribution to normal spermatogenesis (ID 650, 4682), “function of the intestinal tract” (ID 740), and maintenance of normal ammonia clearance (ID 4683) pursuant to Article 13(1) of Regulation (EC) No 1924/2006. In: EFSA Journal. Band 9, Nr. 4, 2011, S. 2051–2081, doi:10.2903/j.efsa.2011.2051 (freier Volltext).
- P. Lucotti, L. Monti, E. Setola, G. La Canna, A. Castiglioni, A. Rossodivita, M. G. Pala, F. Formica, G. Paolini, A. L. Catapano, E. Bosi, O. Alfieri, P. Piatti: Oral L-arginine supplementation improves endothelial function and ameliorates insulin sensitivity and inflammation in cardiopathic nondiabetic patients after an aortocoronary bypass. In: Metabolism. Band 58, Nr. 9, 2009, S. 1270–1276, doi:10.1016/j.metabol.2009.03.029.
- Y. Bai, L. Sun, T. Yang, K. Sun, R. Chen J. Hui: Increase in fasting vascular endothelial function after short-term oral L-arginine is effective when baseline flow-mediated dilation is low: a meta-analysis of randomized controlled trials. In: Am. J. Clin. Nutr. Band 89, Nr. 1, 2009, S. 77–84, doi:10.3945/ajcn.2008.26544 (freier Volltext).
- J. W. Drover, R. Dhaliwal, L. Weitzel, P. E. Wischmeyer, J. B. Ochoa, D. K. Heyland: Perioperative use of arginine-supplemented diets: a systematic review of the evidence. In: J. Am. Coll. Surg. Band 212, Nr. 3, 2011, S. 385–399, doi:10.1016/j.jamcollsurg.2010.10.016.
- Daniel Menzel, Hermann Haller, Manfred Wilhelm, Horst Robenek: l-Arginine and B vitamins improve endothelial function in subjects with mild to moderate blood pressure elevation. In: European Journal of Nutrition. 5. November 2016, S. 1–12, doi:10.1007/s00394-016-1342-6.
- Alexander Ströhle, Andreas Hahn: Diätetische Maßnahmen bei Atherosklerose – Stellenwert von L-Arginin, Teil 2: Vasoprotektive Effekte von L-Arginin. In: deutsche-apotheker-zeitung.de. 24. Mai 2012, abgerufen am 4. Juni 2019.