Decarboxylierung
Als Decarboxylierung bezeichnet man eine chemische Reaktion, bei der aus einem Molekül ein Kohlenstoffdioxid-Molekül abgespalten wird. Durch Erhitzen oder durch enzymatische Katalyse kann eine Decarboxylierung besonders leicht bei Carbonsäuren (bevorzugt: β-Ketosäuren oder Malonsäuren) erfolgen.[1] Dabei tritt ein sechsgliedriger Übergangszustand auf.
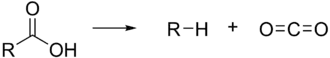
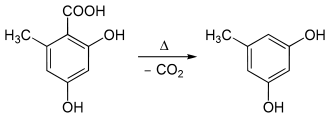
Bei rascher Erwärmung von Orsellinsäure entsteht bei 176 °C Orcin.[2][3]
Eine im Primärstoffwechsel aller Lebewesen zentrale Decarboxylierung ist die oxidative Decarboxylierung des Pyruvats bzw. des α-Ketoglutarats. Ersteres ist das Produkt, das am Ende der Glykolyse beim Abbau der Glucose gebildet wird. Durch einen Multienzymkomplex werden unter Mitwirkung vieler Coenzyme die Substrate um ein Kohlenstoff-Atom verkürzt. Da gleichzeitig zwei Elektronen auf einen zellulären Wasserstoffakzeptor über FAD auf NAD+ übertragen werden, spricht man bei dieser Folgeoxidation auch von oxidativer Decarboxylierung.
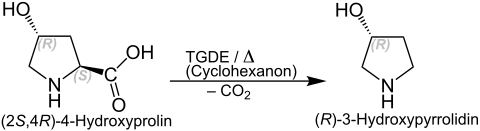
α-Aminosäuren lassen sich durch Erhitzen in Tetraethylenglycoldimethylether (TGDE) in Gegenwart katalytischer Mengen Cyclohexenon decarboxylieren.[4] Beispiel: Bei der Decarboxylierung von (2S,4R)-4-Hydroxyprolin entsteht (R)-3-Hydroxypyrrolidin:
Auch die biogenen Amine entstehen im Stoffwechsel durch Decarboxylierungsreaktionen.
Siehe auch
Weblinks
Einzelnachweise
- Siegfried Hauptmann: Organische Chemie, 2. Auflage, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 403.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-182.
- R. Hegnauer: Chemotaxonomie der Pflanzen, Band 1: Thallophyten, Bryophyten; Pteridophyten und Gymnospermen, Birkhäuser Verlag, Basel 1962, S. 160 (eingeschränkte Vorschau in der Google-Buchsuche).
- Sabine Wallbaum, Thomas Mehler, Jürgen Martens (1994): Decarboxylation of α-Amino Acids containing two and three Stereogenic Centers: A Simple One-Step Procedure to Prepare Two Opticall Active β-Amino Alcohols and a Bicyclic Pyrrolidine Derivative. In: Synthetic Communications, 24 (10); S. 1381–1387; doi:10.1080/00397919408011741.