Asymmetrisches Dimethylarginin
Asymmetrisches Dimethylarginin (ADMA) ist ein methyliertes Derivat der Aminosäure L-Arginin, das im Blutplasma des menschlichen Organismus zu finden ist. Es entsteht durch Protein-Methyl-Transferasen (PRMTs), die in Proteinen gebundenes Arginin methylieren. Diese Methylarginine werden durch Proteolyse freigesetzt. Der Abbau der methylierten Argininderivate wie ADMA erfolgt durch Dimethylarginin-dimethylaminohydrolasen (DDAHs). ADMA gilt als Risikomarker u. a. für die Arteriosklerose. In der Tiermedizin wird Symmetrisches Dimethylarginin als Marker für die Nierenfunktion eingesetzt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
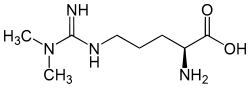 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | asymmetrisches Dimethylarginin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H18N4O2 | |||||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 202,25 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Medizinische Bedeutung
Erhöhte Werte für ADMA werden gefunden bei Menschen mit Bluthochdruck, erhöhten Cholesterin-Spiegeln, Diabetes mellitus und chronischer Nierenkrankheit. Es besteht eine enge Beziehung zwischen ADMA-Spiegeln im Blutplasma und der Dicke von Media und Intima der Arteria carotis communis, einem der Surrogat-Marker für Arteriosklerose in der Allgemeinbevölkerung. Erhöhte ADMA-Spiegel sind bei Menschen mit koronarer Herzkrankheit, Diabetes und chronischer Nierenkrankheit ein starker Risikofaktor für das Auftreten von Herz-Kreislauf-Komplikationen wie z. B. Herzinfarkt oder Schlaganfall.[2][3][4]
Möglicherweise führen erhöhte ADMA-Spiegel zu einer Inaktivierung von Stickstoffmonoxid, das normalerweise eine Entspannung der glatten Gefäßmuskulatur bewirkt, was wieder zu einer Vasodilatation und damit zu einer Absenkung der Nachlast des Herzens und des Blutdrucks führt. ADMA könnte so über eine Senkung der Stickstoffmonoxid-Spiegel an den Endothel-Zellen der Gefäßwand die Entstehung einer Arteriosklerose begünstigen. Der genaue molekulare Mechanismus, der zu einer Erhöhung von ADMA im Blut führt, ist bislang jedoch noch unbekannt (Stand 2014). Allerdings werden zunehmend ein erhöhter oxidativer und nitrosativer Stress sowie damit verbundene Stoffwechselstörungen wie erhöhte Homocysteinspiegel dafür verantwortlich gemacht.[5] ADMA ist der endogene Antagonist von L-Arginin, des Substrats der Stickstoffmonoxidbildung, und damit ein entscheidender Krankheits- und Sterblichkeitsfaktor, der durch die Entkopplung der Synthese von Stickstoffmonoxid und den Verbrauch dieses Radikalfängers einen gefährlichen nitrosativen und oxidativen Stress erzeugen kann.[6][7][8][9][10][11][12]
Messmethoden und Referenzbereich
Die Bestimmung von ADMA erfolgt im analytischen oder klinischen Labor mit Hilfe von HPLC, eines ELISA oder der Massenspektrometrie. Im Blut eines gesunden Menschen gilt eine Konzentration von durchschnittlich 0,7 µmol/l (Mikromol pro Liter) als Normwert.
Quellen
- Datenblatt Dimethyl-L-arginine, ≥95% (HPLC) bei Sigma-Aldrich, abgerufen am 16. Januar 2022 (PDF).
- Matsuguma, K. et al. (2006): Molecular Mechanism for Elevation of Asymmetric Dimethylarginine and Its Role for Hypertension in Chronic Kidney Disease. In: J Am Soc Nephrol. 17, 2176-2183. PMID 16807406 doi:10.1681/ASN.2005121379
- Boger, R.H. et al.: Asymmetric dimethylarginine (ADMA) as a prospective marker of cardiovascular disease and mortality--an update on patient populations with a wide range of cardiovascular risk. Pharmacol Res, 2009. 60(6): p. 481-7.
- Sibal, L. et al.: The role of asymmetric dimethylarginine (ADMA) in endothelial dysfunction and cardiovascular disease. Current cardiology reviews, 2010. 6(2): p. 82.
- I. Seljeflot, B. B. Nilsson, A. S. Westhelm, V. Bratseth, H. Arnesen: The L-arginine-asymmetric dimethylarginine ratio is strongly related to the severity of chronic heart failure. No effects of exercise training. In: J Card Fail 2011, Band 17 (2): S. 135–142, doi:10.1016/j.cardfail.2010.09.003. PIMD 21300303
- Seljeflot I., B. B. Nilsson, A. S. Westheim, V. Bratseth, H. Arnesen: The L-arginine-asymmetric dimethylarginine ratio is strongly related to the severity of chronic heart failure. No effects of exercise training. In: J. Cardiac. Fail. Band 17, 2011, S. 135–142.
- M. Anderssohn, M. Rosenberg, E. Schwedhelm, C. Zugck, M. Lutz, N. Lüneburg, N. Frey, R. H. Böger: The L-Arginine-asymmetric dimethylarginine ratio is an independent predictor of mortality in dilated cardiomyopathy. In: J. Card. Fail. Band 18, Nr. 12, 2012, S. 904–911.
- Pizzarelli, R. Maas, P. Dattolo, G. Tripepi, S. Michelassi, G. D’Arrigo, M. Mieth, S. Bandinelli, L. Ferrucci, C. Zoccali: Asymmetric dimethylarginine predicts survival in the elderly. In: Age, Band 35, Nr. 6, 2013, S. 2465–2475.
- S. M. Bode-Böger, J. Muke, A. Surdacki, G. Brabant, R. H. Böger, J. C. Frölich: Oral L-arginine improves endothelial function in healthy individuals older than 70 years. In: Vasc. Med. Band 8, 2003, S. 77–81.
- K. Jung, O. Petrowicz: L-Arginin und Folsäure bei Arteriosklerose. Ergebnisse einer prospektiven, multizentrischen Verzehrsstudie. In: Perfusion, Band 21, 2008, S. 148–156.
- K. Sydow, R. H. Böger: Reloaded: ADMA and oxidative stress are responsible for endothelial dysfunction in hyperhomocyst(e)inaemia: effects of L-arginine and B vitamins. In: Cardiovasc. Res., 2012, doi:10.1093/cvr/cvs205.
- Tain Y.-L., Huang L.-T. (2014) Restoration of asymmetric dimethylarginine-nitric oxide balance to prevent the development of hypertension. Int. J. Mol. Sci. 15, 11773-11782
Literatur
- Vallance, P. et al. (1992): Accumulation of an endogenous inhibitor of nitric oxide synthesis in chronic renal failure. In: Lancet. 339(8793), 572–575. PMID 1347093