Wasserhärte
Wasserhärte ist ein Begriffssystem der angewandten Chemie, das sich aus den Bedürfnissen des Gebrauchs natürlichen Wassers mit seinen gelösten Inhaltsstoffen entwickelt hat.

In der Wasserchemie bezeichnet der Begriff Wasserhärte die Stoffmengenkonzentration der im Wasser gelösten Kationen der Erdalkalimetalle und in speziellen Zusammenhängen auch die zugehörigen anionischen Partner. Zu diesen „Härtebildnern“ zählen im Wesentlichen Calcium- und Magnesiumkationen sowie die normalerweise nur in Spuren vorhandenen Strontium- und Bariumionen. Diese gelösten sogenannten Härtebildner können schwerlösliche Verbindungen bilden, darunter vor allem mit dem im Wasser gelöstem Kohlendioxid die jeweiligen Carbonate und mit gelösten Fettsäuren oder Tensiden die sog. Kalkseifen. Diese Tendenz zur Bildung von in Wasser schwer löslichen Verbindungen ist der Grund für die Beachtung der im Trinkwasser gelösten Erdalkalien, die zur Entstehung des Begriffs- und Theoriesystems um die Wasserhärte geführt hat.
Geschichte und Herleitung des Begriffs
Schon in den antiken hippokratischen Schriften wurde zwischen weichem (μαλακός) und hartem (σκληρός) Wasser unterschieden. Das harte ist unter anderem „bei Felsquellen, warmer Erde oder mineralreichen Quellen zu finden.“[1] Galenos erläutert hierzu: „Denn Hippokrates nennt ‚hartes Wasser‘ das raue, das beim Trinken die Zunge und beim Waschen den Körper beißt. Das weiche Wasser ist dem entgegengesetzt.“[2]
Für das Wäschewaschen von Hand wird bis heute vorzugsweise Regenwasser genutzt, welches als weich gilt. Quell- oder Brunnenwasser, die als hart gelten, werden dagegen eher gemieden, weil der hohe Anteil gelöster Mineralien im harten Wasser Seife vermehrt zu wasserunlöslicher Kalkseife ausflocken lässt. Die so gebundene Teil der Seife verliert seine Reinigungswirkung. Gleichzeitig lässt die entstandene Kalkseife das gewaschene Waschgut ergrauen und macht das Waschgut nach dem Trocknen auf der Wäscheleine hart und steif. Durch die Nutzung von weichem Wasser fürs Waschen können diese unerwünschten Effekte weitgehend vermieden werden.[3]
Auswirkungen
Niederschlagswasser ist „destilliertes Wasser“ und enthält von Natur aus keine Mineralien, sondern nur Luftbestandteile und Luftverunreinigungen, die beim Fall zur Erdoberfläche aus der Luft herausgewaschen wurden oder selbst kondensierten. Deswegen ist Regenwasser weiches Wasser. In Regionen mit kristallinen Gesteinen im Boden, wie Granit, Gneis und Basalt, kann das Regenwasser nur wenige leichtlösliche Mineralien herauslösen, das Grundwasser ist weiches Wasser. Auch Oberflächenwasser ohne viel Kontakt zu Gesteinen gilt als weich.
Weiches Wasser ist günstiger für alle Anwendungen,
- bei denen das Wasser erhitzt wird,
- zum Waschen,
- zum Gießen von Zimmerpflanzen oder kalkempfindlichen Pflanzen (Moorbeetpflanzen) etc.
Nachteilig kann jedoch starke Schaumbildung bei Waschmitteln sein und die schlechte Entfernbarkeit von Seife z. B. beim Händewaschen.
In Kontakt mit kalkhaltigen Gesteinen (wie beispielsweise Kalkstein, Marmor oder Dolomit) kann Regenwasser mehr Minerale auflösen, es wird zu hartem Wasser.
- Es führt zur vermehrten Bildung von Kesselstein in Haushaltsgeräten, Heizungen und Heißwasserbereitern,
- beeinträchtigt Waschprozesse (erhöht Bedarf und Verbrauch von Spül- und Waschmitteln), dies führte zur Entwicklung von Wasserenthärtern (in Spülmaschinen, Maschinengeschirrspülmitteln, Waschmitteln etc.)
- beeinflusst je nach dem Maß der Härte den Geschmack und das Aussehen bestimmter Speisen und Getränke (z. B. Tee).
Entstehung
Die Wasserhärte entsteht beim Durchtritt von Wasser durch carbonatgesteinhaltige Böden und Gesteine und/oder Grundwasserleiter (Aquifere) durch Lösung von Carbonaten mithilfe von Kohlensäure unter Bildung löslicher Hydrogencarbonate (HCO3−).
Sämtliche gelösten Erdalkalimetalle (die dann als Carbonate, Sulfate, Chloride, Nitrite, Nitrate und Phosphate vorliegen) werden als Gesamthärte bezeichnet.[4], die nur an Kohlensäure gebundenen Anteile als Karbonathärte[4](auch Carbonathärte oder temporäre Härte oder vorübergehende Härte) und deren beider Differenz als Nichtkarbonathärte[4] (permanente Härte oder bleibende Härte).
Der überwiegende Teil der Wasserhärte entsteht als Carbonathärte und ist daher für die Wasserhärte von spezieller Bedeutung. Sie entsteht durch Auflösung von carbonathaltigen Gesteinen, also Kalk (CaCO3) bzw. Dolomit (Ca-Mg-Mischcarbonat) nach folgenden Formeln
Dieselben Reaktionen und Gleichgewichte laufen mit allen Erdalkali- und Mischcarbonaten ab: SrCO3 , BaCO3 ,… Die Carbonathärte entspricht der Hälfte der Konzentration des Anions Hydrogencarbonat (HCO3−).
Magnesium- und Calciumionen können auch durch andere Lösungsvorgänge in das Wasser gelangen, etwa durch Auflösungen von Gips-Mineralien (CaSO4 × 2 H2O). Grundwässer aus gipshaltigen Schichten können im Extremfall die Sättigungskonzentration für Gips erreichen, die einer Härte von 78,5 °fH bzw. 44 °dH entspricht. (Für die Maßeinheiten °dH und °fH siehe unten Abschnitt Einheiten und Umrechnung.)
Die in sauren Niederschlägen enthaltenen Säuren, die durch den Begriff saurer Regen bekannt geworden sind, führen nach Lösung von Carbonatgesteinen zum Anstieg der Gesamthärte. Beteiligt sind vor allem Schwefelsäure (H2SO4), die über Schwefeldioxid und die Bildung von schwefeliger Säure bei der Verbrennung schwefelhaltiger Brennstoffe entsteht, und Salpetersäure (HNO3), die über die Zwischenstufe der Stickoxide bei besonders heißen Verbrennungen gebildet wird. Durch Maßnahmen zur Luftreinhaltung (z. B. Rauchgasentschwefelung und Fahrzeugkatalysatoren sowie DeNox-Anlagen in Kraftwerken) sind diese Belastungen in den vergangenen Jahrzehnten drastisch reduziert worden.
Beim Zerfall von Pflanzenmasse (tote Wurzeln, Falllaub, untergepflügte Halme) im Boden oder bei der Ausbringung landwirtschaftlichen Düngers wird der darin enthaltene Stickstoff zunächst als Ammonium (NH4+) freigesetzt. Daran schließt sich ein bakterieller Oxidationsprozess an, die sog. Nitrifikation. Das Ammonium wird zuerst zu Salpetriger Säure (HNO2) und schließlich zu Salpetersäure (HNO3) oxidiert (und könnte auch weiter zu N2 denitrifiziert werden). Diese Salpetersäure löst aus Kalk – und beim Fehlen von Kalk aus Tonmineralen – Härtebildner auf, der dann den Pflanzen nicht mehr zur Verfügung steht. Deshalb drohen landwirtschaftlich genutzte kalkarme Böden zu versauern. In diesen Fällen ist eine Kalkdüngung erforderlich. Die dann wieder reichlich vorhandenen Carbonate können für einen Härteanstieg in Grundwässern mitverantwortlich sein.
In Grundwässern, die durch landwirtschaftliche Aktivitäten beeinflusst sind, kann die Härte auf über 30 °fH bzw. 17 °dH, in Einzelfällen sogar auf über 40 °fH bzw. 23 °dH, ansteigen. Dies geht sowohl auf vermehrte Kohlensäurebildung als auch auf vermehrte Nitrifikation zurück.
Regenwasser kann nur ausnahmsweise dann Härtebildner aufnehmen, wenn die Atmosphäre kalkhaltige Staubpartikel enthält. Üblicherweise liegt deshalb die Härte von Regenwasser nahe Null. Auch Trinkwasser-Talsperren und Bergseen enthalten selbst in kalkreichen Gegenden oft Wasser von geringer Härte, wenn ihr Einzugsgebiet eine geringe geografische Fläche umfasst und das Regenwasser hauptsächlich oberflächlich zufließt.
Kalk-Kohlensäure-Gleichgewicht
Die Wasserhärte ist durch ein System verschiedener miteinander gekoppelter chemischer Gleichgewichtesreaktionen gekennzeichnet und davon abhängig. Neben den Reaktionsgleichgewichten gehören auch die Löslichkeitsgleichgewichte zwischen den verschiedenen Erdalkali-Ionen und den zugehörigen Carbonat- und Sulfat-Fällungsprodukten (Calcit, Dolomit, Schwerspat, Gips etc.) dazu. Gekoppelt ist auch das Lösungs- und Dissoziationsgleichgewicht des Kohlenstoffdioxid-Kohlensäure-Carbonat-Systems.
Trifft CO2 auf (Regen)Wasser werden mehr als 99 % des Kohlenstoffdioxids nur physikalisch gelöst und weniger als 1 % reagiert temperaturabhängig in einer Gleichgewichtsreaktion (dort erklärt) mit den Wassermolekülen chemisch zu Kohlensäure (H2CO3), die wässrige Lösung reagiert deshalb schwach sauer.
- .
Die gebildete Kohlensäure H2CO3 steht in einer Gleichgewichtsreaktion mit Hydrogencarbonat (HCO3−)-Ionen und Oxonium- (H3O+)-Ionen.
Das Hydrogencarbonat-Ion HCO3− dissoziiert in Wasser weiter zum Carbonat-Ion CO32−
In Wasser liegen diese Gleichgewichtsreaktionen überwiegend auf der Seite des Kohlenstoffdioxids (das dann überwiegend physikalisch im Wasser gelöst vorliegt) und nur in geringem Umfang bilden sich Hydrogencarbonationen.
In der Wasserchemie wird gelöstes CO2 mit der eigentlichen Säure H2CO3 üblicherweise als freie Kohlensäure zusammengefasst, deren Gleichgewichtsreaktionsprodukte, die Summe von Carbonat und Hydrogencarbonat, als gebundene Kohlensäure.
Die Formel
beschreibt das Kalk-Kohlensäure-Gleichgewicht.[5]
Calciumcarbonat selbst ist in reinem Wasser kaum löslich. Die Löslichkeit beträgt gerade einmal 14 Milligramm pro Liter, wobei das Carbonat-Ion als Hydrogencarbonat-Ion in Lösung geht. Bei Anwesenheit von gelöstem Kohlenstoffdioxid steigt die Löslichkeit jedoch um mehr als das Hundertfache, wobei sich das leicht lösliche (dissoziiert vorliegende) Calciumhydrogencarbonat bildet[6]
Wird nun einer dieser Gleichgewichtsreaktionspartner zusätzlich in Wasser eingebracht (oder dem Wasser entzogen), so ist im Gleichgewicht ein "Überhang" (oder "Mangel") an einer Seite, worauf die chemischen Reaktionen in die andere (von der anderen) Richtung der Reaktionsgleichungen ablaufen bis sich mit den Reaktionsprodukten wieder ein Gleichgewicht eingestellt hat (Prinzip vom kleinsten Zwang). Ebenso wenn der pH-Wert oder die Wassertemperatur verändert werden. Auch Wasserverdunstung oder Verdünnung bewirken eine Änderung der CO2-Konzentration und somit eine Gleichgewichtsverschiebung. Regenwasser nimmt temperaturabhängig CO2 aus der Atmosphäre auf. Ein Überhang (oder Mangel) auf der einen Seite der Gleichgewichtsreaktion führt zu einem Ansteigen (oder Absinken) auch auf der anderen Seite, beispielsweise…
- wenn Niederschlagswässer mit anderem pH-Wert in ein Gewässer eingebracht werden (saurer Regen),
- wenn ein Badeteichwasser (etwa mit Huminsäuren aus Torf) angesäuert wird,
- wenn CO2-hältige Luft in Schwimmteich-Badewasser eingeblasen wird
- durch solare Wassererwärmung, wobei nicht umgesetztes physikalisch gelöstes CO2 wegen erhöhter Wassertemperatur ausgast
- immer wenn mineralhaltiges Wasser erwärmt, erhitzt oder abgekühlt wird,
- wenn ein (Kalk)Stein in ein Gewässer geworfen wird (Calcium hat einen Massenanteil von 3,39 % in der Erdkruste,[7] es ist praktisch omnipräsent; siehe dazu Spurenelemente und die Liste der Häufigkeiten chemischer Elemente)
- wenn Badende kalksteinhaltigen Bodenschmutz auf den Füßen haben und im Wasser abwaschen,
- durch biogene Entkalkung, wenn höhere Pflanzen, Wasserpflanzen und Planktonalgen bei der Photosynthese dem Wasser Kohlenstoffdioxid (oder dessen Reaktionsprodukte im Kalk-Kohlensäure-Gleichgewicht) entziehen (beim Entzug des Kohlenstoffdioxids aus dem Dissoziationsgleichgewicht als auch bei der Aufnahme von Hydrogencarbonat durch Algen kommt es zu einer Verminderung der H3O+-Ionen, also zur Steigerung des pH-Wertes (das Wasser wird alkalkischer), mit der Folge einer Verschiebung des Massenverhältnisses zwischen Hydrogencarbonat und Carbonat zugunsten des Carbonats. Dabei überschreiten die Konzentrationen an gelöstem Calcium und Carbonat miteinander multipliziert das Löslichkeitsprodukt von Calciumcarbonat, welches folglich kristallisiert und ausfällt).
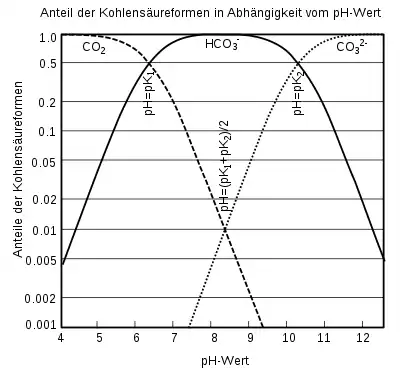
Das Wasser befindet sich in diesem Kalk-Kohlensäure-Gleichgewicht, wenn die Kalkausscheidung gleich groß ist wie die Kalkauflösung, also es genau so viel Kohlenstoffdioxid enthält, dass es gerade keinen Kalk abscheidet, aber auch keinen Kalk lösen kann. Wird einem solchen Wasser Kohlenstoffdioxid entzogen, bilden sich schwer lösliche Verbindungen wie Calcit und Dolomit als besonders schwer lösliches (!) Mischcarbonat. Das Wasser ist dann mit diesen Mischcarbonaten übersättigt, worauf diese ausfallen.
Abscheidung und Ausfällung von Kalk und Mischmineralen
Daneben existiert noch der Carbonat-Silicat-Zyklus der Gesteine, bei dem Silikatgesteine gelöst und wieder abgeschieden werden. Das kohlensäurehaltige Regenwasser erodiert silicatische Gesteine, indem es daraus Calcium-Silicat-Minerale (Verbindungen aus Calcium, Silicium und Sauerstoff) auflöst, wodurch die freigesetzten Calcium- und Hydrogencarbonat-Ionen ins Grundwasser gelangen. Als Beispiel dient die Gleichung der Umsetzung des Feldspats Anorthit durch Kohlensäure unter Bildung von Kaolinit:
Durch weitere Biomineralisation werden mineralische Biominerale aus dem Wasser ausgeschieden. So fällen beispielsweise Armleuchteralgen oder zur Photosynthese fähige Cyanobakterien ("Blaualgen") ebenfalls Calciumcarbonat aus, letztere bilden in Mikrobenmatten mattenförmige Stromatolithen. Die Mikroorganismen in den Biofilmen sind dann an der Basis inaktiv und sterben ab und wachsen an der Filmoberfläche weiter. Kieselalgen (Diatomeen) fällen Kieselsäure aus dem Wasser aus und bilden daraus bei Normaltemperatur und Normaldruck wasserhaltiges amorphes Siliziumdioxid.
Vermeintliche "Kalkablagerungen" in Schwimmteichen oder Schwimmbecken bestehen daher meist aus homogenen Gemischen von Calciumcarbonat, Mischcarbonaten, Apatit, Siliziumdioxid und Silikaten und sind deswegen auch mit Säuren nur schwer lösbar. In Gewässern findet Sedimentation dieser Mineralschichten statt, siehe dazu Mudde-Schlammablagerungen (Mulm) und Seekreide-Kalkablagerungen.
Aufgrund der Temperaturabhängigkeit der gesamten Gleichgewichtssysteme bilden sich beispielsweise auch Kesselstein-Ablagerungen bei Warmwasseranlagen, Kaffeemaschinen oder Kochtöpfen bei der Bereitung von Heißwasser aus kalkhaltigem Wasser.
Pufferkapazität solcher Wässer
Hohe Kalkgehalte und somit hohe Hydrogencarbonatgehalte im Wasser wirken zudem als chemische Puffer (mit der Kohlensäure als Säure und dem Hydrogencarbonat-Ion als Base).
Bei Zugabe von Säure stellt sich das chemische Gleichgewicht ein, indem CO2 freigesetzt wird. Es muss viel Säure zugegeben werden, dass sich der pH-Wert stark ändert, was zugleich eine Schutzfunktion für die Biozönose gegen starke pH-Wert-Schwankungen darstellt.
Zur Bestimmung der Pufferkapazitäten wird einerseits die Säurekapazität bestimmt, wie viel Säurezusatz zu einer Wasserprobe nötig ist, bis der pH-Wert 4,3 erreicht ist, damit wird die gebundene Kohlensäure bestimmt. Die freie Kohlensäure wird über die Basekapazität bestimmt, wie viel Laugenzusatz zu einer Wasserprobe nötig ist, bis der pH-Wert 8,2 erreicht ist.
„Aggressives Wasser“
Wird Leitungswasser in Häusern mittels Ionenaustauscheranlagen entkalkt, kann dieses Wasser mehr Kohlensäure aufnehmen. In der Wasserchemie wird Wasser, das noch Minerale lösen kann (siehe dazu Löslichkeit und Löslichkeitsprodukt), aggressives Wasser genannt.
Kalkhaltige Werkstoffe (Beton, Asbestzement usw.) werden zudem bei überschüssigen CO2–Gehalten im Wasser korrodiert. Auf die Korrosionswahrscheinlichkeit von Werkstoffen, und dies betrifft besonders Werkstoffe aus Eisen, hat die überschüssige Kohlensäure dann Einfluss, wenn sogenannte aggressive Kohlensäure vorhanden ist. Gleichgewichtswässer mit einer Mindesthärte von 1,5 mmol/l neigen zur Bildung einer Kalk-Rostschutzschicht. Siehe dazu auch die Tillmanssche Formel.
Aggressives Wasser mit überschüssiger Kohlensäure hat zur Folge, dass Kalkablagerungen in alten Wasserrohren wieder abgelöst werden und bei Schadstellen der inneren Zinkschicht Rost entstehen kann. Um dies zu verhindern, werden nach einer Entkalkung oft Phosphate als Phosphatierung ins Leitungswasser zudosiert, die wieder eine Beschichtung als Korrosionsschutz hervorrufen und die Kalkablösung verhindern.
Aus Dolomit (CaMg(CO3)2) wird bei geringerer Kalkbrenntemperatur halbgebrannter Dolomit (CaCO3·MgO; auch Magno genannt) hergestellt. Dieser hat sich in der Trinkwasseraufbereitung als kieselsäurefreies (SiO2-freies) Filtergranulat zur Entsäuerung zur Bindung von überschüssigem CO2 bewährt. Genauso wird das Material in Fisch- und Schwimmteichen zur pH-Wert-Anhebung und -stabilisierung und wirksameren Aufkalkung eingesetzt. Mit Wasser reagiert vorzugsweise die MgO-Komponente. Weiteres unter Magno (Chemikalie).
Bedeutung der Gesamthärte
Die Gesamthärte gibt die Summe der Konzentrationen der Kationen von Erdalkalimetallen in Wasser an. Diese Kationen haben eine große, positive physiologische Bedeutung, stören jedoch bei einigen Verwendungen des Wassers.
- Manche anionische Tenside und Seifen bilden mit den Kationen der Erdalkalimetalle unlösliche Kalkseifen. Diese Kalkseifen tragen nichts zur Reinigungswirkung bei, die damit gebundene Menge der Tenside oder Seifen bleibt wirkungslos und belastet sohin bloß das Abwasser, zudem führen die auf der Wäsche abgelagerten Kalkseifen zu einer Verunreinigung und Vergrauung der Textilien. Zur Verbesserung wurden daher kationische Tenside und amphotere Tenside entwickelt, die nicht mit Erdalkali-Ionen reagieren (siehe auch Baukastenwaschmittel und Wasserhärte und Waschen)
- Enthärter: Bei Maschinengeschirrspülmitteln werden Enthärterstoffe zugesetzt (Phosphate oder Citrate) oder Ionenaustauscher-Enthärter eliminieren die Härtebildner aus dem Waschwasser (bei Spülmaschinen oder gewerblichen Waschmaschinen) oder für Prozesswasser (beispielsweise für Verdampfer in Heizkraftwerken).
Physiologische Bedeutung
Magnesium und Calcium sind für den Organismus essentiell. Der menschliche Körper enthält 0,47 g/kg Magnesium und 15 g/kg Calcium. Für die Versorgung des Körpers mit diesen Elementen spielt das Trinkwasser jedoch eine untergeordnete Rolle. Strontium ist ebenso wie Calcium in den Knochen enthalten, hat aber keine spezielle physiologische Bedeutung.
Barium ist in gelöster Form giftig. In sulfathaltigen Wässern werden toxikologisch bedenkliche Konzentrationen aber nicht erreicht, weil das extrem schwerlösliche Bariumsulfat gebildet wird. Bariumsulfat ist Hauptbestandteil oral verabreichter medizinischer Röntgenkontrastmittel.
Nichtcarbonat-Härte
Die bleibende Härte ist nicht an Hydrogencarbonat oder Carbonat gebunden und kann daher prinzipiell nicht als Calcium- oder Magnesiumcarbonat aus dem Wasser entfernt werden. Dieser nicht entfernbare Anteil ist durch Anionen wie z. B. Chloride, Nitrate und Sulfate ausgeglichen („gebunden“). In welchen unterschiedlichen Konzentrationen diese Anionen genau vorliegen, spielt in Bezug auf die Wasserhärte keine Rolle, gibt aber Auskunft über die Herkunft dieser Anteile. Tatsächlich beeinflusst aber diese permanente Härte ganz entscheidend das Fällungsverhalten der Carbonathärte-Anteile, weil die somit erhöhten Konzentrationen an Calcium und Magnesium in die Rechnung der Ionenprodukte mit dem Carbonat eingehen und somit die Schwellenwerte z. B. der „zugehörigen Kohlensäure“ für das Eintreten der härtetypischen Fällungsreaktionen erhöhen.
Oft werden auch die Konzentrationen von Magnesium- und Calciumionen getrennt bestimmt und dann als „Magnesiumhärte“ bzw. „Calciumhärte“ bezeichnet. Ihre Summe entspricht in guter Näherung der Gesamtwasserhärte.
Methoden zur Bestimmung
- Die bekannteste praktikable Bestimmungsmethode für die Gesamthärte ist die komplexometrische Titration mit einer wässrigen Lösung des Dinatriumsalzes der Ethylendiamintetraessigsäure (EDTA, Handelsname: Titriplex III) mit bekannter Konzentration. EDTA bildet mit allen Erdalkali-Härtebildnern Ca2+, Mg2+, Ba2+, Sr2+,… lösliche, stabile Chelatkomplexe. 100 ml der zu untersuchenden Wasserprobe werden mit 2 ml 25%iger Ammoniaklösung, einem pH 11 Puffer (Ammoniak-Ammoniumacetat) und dem Indikator Eriochromschwarz T versetzt. Üblicherweise ist der Indikator mit dem Puffer zusammen als so genannte „Indikator-Puffer-Tabletten“ erhältlich. Der Indikator, wenn mit einem Gelbfarbstoff maskiert, bildet mit den Ca2+ und Mg2+ einen rot gefärbten Komplex. Sind alle Erdalkali-Ionen am Ende der Titration vom EDTA gebunden, liegt das Eriochromschwarz-T frei vor und ist grün gefärbt. Beim unmaskierten Indikator ist der Farbwechsel von magenta bis blau. Die Gesamthärte berechnet sich aus dem verbrauchten Volumen an EDTA-Lösung. Bei einer Wasserprobe von 100 ml entspricht 1 ml verbrauchter EDTA-Lösung (c = 0,1 mol/l) 5,6 °dH (deutsche Härtegrade), das entspricht 1 mmol/l Erdalkaliionen. Um die Calcium- und Magnesiumkonzentration einzeln nachzuweisen, wird bei einem niedrigeren pH von ca. 8 erst gegen Ca2+ mit EDTA titriert, weil bei diesem pH der Mg-EDTA-Komplex noch nicht stabil ist. Am Umschlagspunkt von Calcium wird der pH dann auf 11 eingestellt und mit EDTA gegen Mg2+ titriert.
- Eine etwas ältere Methode ist die hydrolytische Fällungs-Titration mit alkoholischer Kaliumpalmitatlösung, bei der Palmitationen mit Calcium- und Magnesiumionen (resp. allen Erdalkaliionen, die dabei miterfasst werden) zu den entsprechenden unlöslichen Salzen (Kalkseife) der Palmitinsäure reagieren. Bei Überschreiten des Äquivalenzpunktes reagieren Palmitationen hydrolytisch zu Hydroxidionen, die mit Phenolphthalein als Indikator nachgewiesen werden. 1 ml einer Kaliumpalmitatlösung mit der Konzentration 0,1 mol/l entspricht dabei einer Gesamthärte von 1 mval/l.[8]
- Die Carbonathärte wird durch das Salzsäure-Bindungs-Vermögen (SBV) bestimmt, die Carbonathärte entspricht der Säurekapazität (siehe dazu Pufferkapazität). Hierzu werden 100 ml des Wassers mit Salzsäure (c = 0,1 mol/l) bis zum pH-Wert 4,3 titriert (pH-Meter oder Umschlag von Methylorange-Indikator). Hierbei wird (nahezu) alles Carbonat und Hydrogencarbonat zu „freier Kohlensäure“ umgewandelt. Der Säureverbrauch in ml entspricht deshalb der Hydrogencarbonatkonzentration in mval/l. Die Multiplikation mit 2,8 ergibt deutsche Härtegrade (°dH), sofern das Ergebnis der Berechnung nicht die Gesamthärte übersteigt. Die Bestimmung freier Kohlensäure wird durch Bestimmung der Basekapazität ermittelt.
Resultiert bei der Analyse eines natürlichen Wassers für die Carbonathärte ein höherer Wert als für die Gesamthärte, so enthält dieses Wasser auch Natriumhydrogencarbonat. Die Carbonathärte ist in diesem Fall identisch mit der Gesamthärte, da diese nicht größer als die Gesamthärte sein kann. - In analytischen Labors können die Erdalkaliionen wie auch die Anionen der Säurereste mit Hilfe der Ionenchromatografie oder der Kapillarelektrophorese bestimmt werden. Calcium kann auch spektroskopisch mit Hilfe der Flammen-Atomemissionsspektrometrie (F-AES) bestimmt werden.
Einheiten und Umrechnung
Nach dem SI-Maßsystem wird der Gehalt der Erdalkaliionen, also die Gesamthärte, in Mol pro Liter bzw. angesichts der geringen Konzentrationen in Millimol pro Liter (mmol/l) angegeben.
Die Wasserhärte wurde in Deutschland und Österreich früher in Grad deutscher Härte (°dH) angegeben. Dabei war 1 °dH formal als 10 mg CaO je einem Liter Wasser definiert. Die anderen Härtebildner wie Magnesium wurden als hierzu äquivalente Menge (7,19 mg MgO pro Liter) definiert. Später wurde die Angabe der Wasserhärte in der praxisgerechten Stoffmengen-Äquivalenzeinheit Millival pro Liter (mval/l) verwendet. Heute sind gesetzlich die oben genannten molaren Angaben gefordert, ungeachtet der praktischen Erfordernisse.
In der Schweiz sind die französischen Härtegrade °fH maßgebend.
In anderen Ländern waren oder sind andere Maßeinheiten in Gebrauch, die jedoch nur eingeschränkt vergleichbar sind. Vergleichbar werden sie, wenn man ein Standard-Ionenverhältnis annimmt. Das ist möglich, weil die meisten natürlichen Wässer eine relativ ähnliche Kationenverteilung aufweisen, unabhängig vom Gesamtsalzgehalt. Nur unter dieser Voraussetzung ist die folgende Tabelle zur Umrechnung anwendbar:
| °dH | °e (°Clark) | °fH | °rH | ppm (°aH) | mval/l | mmol/l | ||
|---|---|---|---|---|---|---|---|---|
| Deutsche Grad | 1 °dH = | 1 | 1,253 | 1,78 | 7,118 | 17,8 | 0,357 | 0,1783 |
| Englische Grad (Grad Clark) |
1 °e = | 0,798 | 1 | 1,43 | 5,695 | 14,3 | 0,285 | 0,142 |
| Französische Grad | 1 °fH = | 0,560 | 0,702 | 1 | 3,986 | 10 | 0,2 | 0,1 |
| Russische Grad | 1 °rH = | 0,140 | 0,176 | 0,251 | 1 | 0,146 | 0,050 | 0,025 |
| ppm CaCO3 (Amerikanische Grad) |
1 ppm = | 0,056 | 0,07 | 0,1 | 6,834 | 1 | 0,02 | 0,01 |
| mval/l Erdalkali-Ionen | 1 mval/l = | 2,8 | 3,51 | 5,00 | 20,040 | 50 | 1 | 0,50 |
| mmol/l Erdalkali-Ionen | 1 mmol/l = | 5,6 | 7,02 | 10,00 | 40,080 | 100,0 | 2,00 | 1 |
Die Einheit 1 ppm wird hier entgegen dem eigentlichen Wortsinn im Sinne von 1 mg CaCO3 pro Liter Wasser verwendet. CaCO3 hat die Molmasse 100. Damit entspricht 1 ppm CaCO3 = 1/100 mmol/l und ist nicht dimensionslos.
Sind die Werte für Magnesium (Mg) und Calcium (Ca) bekannt, kann die Härte des Wassers (z. B. bei Mineralwasser) wie folgt berechnet werden:
- Härtegrad des Wassers in
- bzw. in
Härtebereiche
Härtebereiche zur Dosierung von Waschmitteln
Auf Verpackungen von Wasch- und Reinigungsmitteln, die Phosphate oder andere härtebindende Stoffe enthalten, mussten nach § 7 Abs. 1 Satz 1 Nr. 5 Wasch- und Reinigungsmittelgesetz (WRMG)[10] seit 1988 abgestufte Dosierungsempfehlungen in Millilitern für die Härtebereiche 1 bis 4 angegeben werden. Gesetzlich vorgegeben waren dabei die Angaben bezüglich Millimol Gesamthärte je Liter. Es wurden die folgenden Härtebereiche definiert:
| Härtebereich | Millimol Gesamthärte je Liter | °dH |
|---|---|---|
| 1 (weich) | bis 1,3 | bis 7,3 |
| 2 (mittel) | 1,3 bis 2,5 | 7,3 bis 14 |
| 3 (hart) | 2,5 bis 3,8 | 14 bis 21,3 |
| 4 (sehr hart) | über 3,8 | über 21,3 |
Neuregelung der Härtebereiche
Am 1. Februar 2007 wurde vom Deutschen Bundestag die Neufassung des Wasch- und Reinigungsmittelgesetzes[11] (WRMG) beschlossen, das am 5. Mai 2007 in Kraft getreten ist. Darin wurden u. a. die Härtebereiche an europäische Standards angepasst und die Angabe Millimol Gesamthärte je Liter wird durch die (aus chemischer Sicht unsinnige) Angabe Millimol Calciumcarbonat je Liter ersetzt. Wasserversorgungsunternehmen werden wohl weiterhin auch die Gesamthärte veröffentlichen, dies ist im Gesetz aber nicht vorgeschrieben. Nach Stellungnahmen des BMU gegenüber der DVGW[12] soll Millimol Calciumcarbonat je Liter unverändert als Millimol Gesamthärte je Liter aufgefasst werden. Die neuen Härtebereiche unterscheiden sich kaum von den bisherigen, nur werden die Bereiche 3 und 4 zum Härtebereich „hart“ zusammengelegt und die Ziffern 1,2,3 und 4 werden durch die – bereits gebräuchlichen – Beschreibungen „weich“, „mittel“ und „hart“ ersetzt. Die neuen Härtebereiche sind wie folgt definiert:
| Härtebereich | Millimol Calciumcarbonat je Liter | °dH |
|---|---|---|
| weich | weniger als 1,5 | weniger als 8,4 °dH |
| mittel | 1,5 bis 2,5 | 8,4 bis 14 °dH |
| hart | mehr als 2,5 | mehr als 14 °dH |
Auf Verpackungen von Waschmitteln müssen laut § 8 Abs. 1 Satz 1 WRMG[13] empfohlene Mengen und/oder Dosierungsanleitung in Milliliter oder Gramm für eine normale Waschmaschinenfüllung bei den Wasserhärtegraden weich, mittel und hart und unter Berücksichtigung von ein oder zwei Waschgängen angegeben werden. Um Waschmittel einzusparen, muss man die örtlich vorhandene Wasserhärte kennen und liest dann auf der Packung die dazugehörende Waschmittelmenge ab. Bei härterem Trinkwasser (ab Härtebereich 3 – „hart“) sollte man bei Temperaturen ab 60 °C einen separaten, phosphatfreien Enthärter dazugeben. Die Wasserversorgungsunternehmen teilen dem Kunden die örtliche Wasserhärte mit oder verschicken Aufkleber, welche man zweckmäßigerweise auf die Waschmaschine klebt.
Für Trinkwasser bestehen Vorschriften bezüglich der Wasserhärte, siehe dort.
Schweiz
Gemäß Lebensmittelgesetz wird das Wasser in der Schweiz in sechs Härtestufen eingeteilt, welche in Millimol pro Liter (Anzahl Kalzium- und Magnesiumteilchen pro Liter Wasser) oder in französischen Härtegraden ºfH angegeben werden.
| Härte in °fH | mmol/l | Bezeichnung |
|---|---|---|
| 0 bis 7 | 0 bis 0,7 | sehr weich |
| 7 bis 15 | 0,7 bis 1,5 | weich |
| 15 bis 25 | 1,5 bis 2,5 | mittelhart |
| 25 bis 32 | 2,5 bis 3,2 | ziemlich hart |
| 32 bis 42 | 3,2 bis 4,2 | hart |
| größer als 42 | größer 4,2 | sehr hart |
Während das Wasser in den Voralpen, in den Alpen und auf der Alpensüdseite üblicherweise sehr weich oder weich ist, ist es im Jura mittelhart und im Mittelland hart bis sehr hart.[14]
Enthärtungsmethoden
Entcarbonisierung: Mit dieser Maßnahme wird nur die Carbonathärte verringert. Dem Wasser wird Calciumhydroxid als „Kalkwasser“ zugegeben, das die folgende Reaktion auslöst:
Eine Entcarbonisierung wird in einigen deutschen Wasserwerken an sehr harten Wässern durchgeführt.
Enthärtung durch Ionenaustausch: Ionenaustauscher, die mit Kochsalz regeneriert werden, sind in der Lage, Calcium- und Magnesiumionen gegen Natriumionen auszutauschen. Dieses Prinzip wird z. B. in Spülmaschinen eingesetzt, um die Heizelemente zu schonen und „Kalkflecken“ auf dem Geschirr zu vermeiden. Wasserenthärtungsanlagen für den nicht-professionellen Gebrauch zur Enthärtung von Trinkwasser verwenden dieses Prinzip. Gelegentlich wird es auch zur Aufbereitung kleiner Wassermengen, etwa zum Blumengießen oder Teekochen, verwendet.
Vollentsalzung: Eine Vollentsalzung beseitigt nicht nur Härtebildner, sondern alle Ionen. Sie wird durch eine Kombination von Kationen- und Anionenaustauscher erreicht. Vollentsalztes Wasser wird überall da eingesetzt, wo Wasser in reiner Form benötigt wird. Die größten Mengen kommen als Kesselspeisewasser zum Einsatz. Ein ähnliches Ergebnis erzielen die Umkehrosmose und die Destillation, bei denen auch nichtionische gelöste Feststoffe entfernt werden.
Andere Methoden: Die Komplexbildung mit Polyphosphaten vermindert die Härte, führt jedoch zur Überdüngung von Oberflächengewässern. Waschmittel enthalten oft noch in kleinen Mengen Komplexbildner, die Enthärtung erfolgt jedoch heute im Wesentlichen durch Kationenaustauscher wie Zeolith A. Damit wird die Bildung von Kalkseifen verhindert, die Stabilität der für den Waschgang notwendigen Emulsion erhöht und die Heizelemente der Waschmaschine geschont.
Bei Dampflokomotiven wird auch die Innere Speisewasseraufbereitung verwendet.
Geräte mit elektrischen oder magnetischen Feldern führen zu keiner Beseitigung der Härte, und ihre Wirkung ist umstritten. Bestenfalls ist denkbar, dass bei der Kristallisation des überschüssigen Calciumcarbonates unter dem Einfluss dieser Felder die instabile Aragonit-Form gebildet wird, die aus feinen nadelförmigen Kristallen besteht und suspendiert bleibt. Die normale Kristallisation zu dem stabileren Calcit dagegen bildet die bekannten Verkrustungen (Kesselstein). Die Wirkung dieser Art von Wasserbehandlung ist zeitlich begrenzt und geht deshalb nach einer gewissen Fließstrecke hinter dem Gerät wieder verloren. Eine Voraussetzung für die beschriebene Wirkung scheint zu sein, dass Wechselfelder benutzt werden oder dass Wasser in einem statischen Feld verwirbelt wird. Deshalb bleiben z. B. auf der Wasserleitung aufgesetzte Magnetschuhe ohne jede Wirkung.
Siehe auch
Literatur
- Walter Kölle: Wasseranalysen – richtig beurteilt. Grundlagen, Parameter, Wassertypen, Inhaltsstoffe, Grenzwerte nach Trinkwasserverordnung und EU-Trinkwasserrichtlinie. 2. aktualisierte und erweiterte Auflage. Wiley-VCH, Weinheim 2003, ISBN 3-527-30661-7.
- Hanns-J. Krause: Aquarienwasser. Diagnose, Therapie, Aufbereitung. 2. verbesserte Auflage, Neuauflage. bede-Verlag, Kollnburg 1993, ISBN 3-927997-00-5
Weblinks
- Übersichtskarte der Wasserhärte deutschlandweit
- Ausfindigmachen der Wasserhärte nach Postleitzahl in der Schweiz. Schweizerischer Verein des Gas- und Wasserfaches SVGW
- Übersichtskarte der Wasserhärte in Österreich (PDF; 397 kB)
- Wasserhärte-Verzeichnis vieler deutschen Städte
- Verzeichnis der Wasserhärte vieler deutschen Städte
Einzelnachweise
- Anne Liewert: Die meteorologische Medizin des Corpus Hippocraticum. De Gruyter, Berlin/München/Boston 2015, ISBN 978-3-11-041699-2, S. 98, Google-Books-Ansicht
- Anne Liewert: Die meteorologische Medizin des Corpus Hippocraticum. De Gruyter, Berlin/München/Boston 2015, ISBN 978-3-11-041699-2, S. 98, Fußnote 109; Google-Books-Ansicht
- Wilhelmine Buchholz: Wasser und Seife, oder, Allgemeines Wäschebuch. Hamburg / Leipzig 1866 (eingeschränkte Vorschau in der Google-Buchsuche).
- Karl Höll, Helmut Peter, Dietrich Lüdemann: Wasser. ISBN 3-11-125936-6 (eingeschränkte Vorschau in der Google-Buchsuche).
- Angewandte Chemie und Umwelttechnik für Ingenieure. S. 340 (eingeschränkte Vorschau in der Google-Buchsuche).
- Wolfgang F. Tegethoff: Calciumcarbonat Von der Kreidezeit ins 21. Jahrhundert. Springer-Verlag, 2013, ISBN 978-3-0348-8259-0, S. 3 (eingeschränkte Vorschau in der Google-Buchsuche).
- Harry H. Binder: Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- Jander/Jahr/Knoll: Maßanalyse, Sammlung Göschen Band 221, de Gruyter Berlin 1966, S. 209 ff.
- Tabelle nach: Hanns-J. Krause: Aquarienwasser. Diagnose, Therapie, Aufbereitung. 2. verbesserte Auflage, Neuauflage. bede-Verlag, Kollnburg 1993, ISBN 3-927997-00-5, S. 35.
- aus dem Jahr 1987, BGBl. I S. 875
- Wasch- und Reinigungsmittelgesetz.
- Neue Härtebereiche für Trinkwasser.
- i. Verb. m. der Verordnung (EG) Nr. 648/2004 (PDF) (zuletzt geändert durch EG-Verordnung Nr. 907/2006) Art. 11 Abs. 4 und gemäß Anhang VII Abschnitt B derselben.
- Wasserhärte: Was muss beachtet werden? (PDF; 333 kB) Schweizerischer Verein des Gas- und Wasserfaches; abgerufen am 8. Mai 2017.