Emulsion
Unter einer Emulsion (lateinisch ex und mulgēre ‚herausgemolken‘) versteht man ein fein verteiltes Gemisch zweier normalerweise nicht mischbarer Flüssigkeiten ohne sichtbare Entmischung. Beispiele für Emulsionen sind zahlreiche Kosmetika, Milch oder Mayonnaise.


Struktur der Emulsion
In einer Emulsion liegt ein fein verteiltes Gemisch zweier Flüssigkeiten, wie Öl und Wasser, vor. Eine Flüssigkeit (Phase) bildet kleine Tröpfchen, verteilt in der anderen Flüssigkeit. Die Phase, die Tröpfchen bildet, nennt man innere Phase oder auch disperse Phase. Die Phase, in der die Tröpfchen schwimmen, wird äußere Phase oder kontinuierliche Phase genannt. Emulsionen gehören zu den dispersen Systemen und unterscheiden sich von Gemischen mischbarer Flüssigkeiten, wie zum Beispiel Ethanol und Wasser. Emulsionen sind in der Regel trübe, milchige Flüssigkeiten.
Emulsionen aus Wasser und Öl unterscheidet man in Wasser-in-Öl-Emulsion (W/O-Emulsion) und Öl-in-Wasser-Emulsion (O/W-Emulsion). Ein weiterer wichtiger Bestandteil von Emulsionen ist der Emulgator (Tensid), der die Bildung von Tröpfchen erleichtert und einer Entmischung (Phasentrennung) entgegenwirkt.
Chemische Betrachtung einer Emulsion
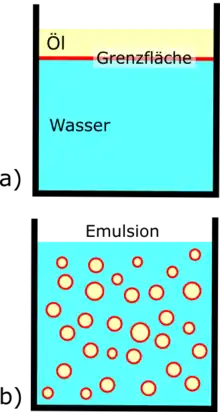
Viele Flüssigkeiten können entweder gut mit Wasser (sie sind hydrophil) oder gut mit Öl (sie sind lipophil) mischbar sein. Hydrophile Flüssigkeiten bilden hauptsächlich zwischenmolekulare Kräfte in Form von Wasserstoffbrücken aus. Bei lipophilen Flüssigkeiten bilden sich hingegen hauptsächlich zwischenmolekulare Van-der-Waals-Kräfte aus. Gibt man etwas Öl in Wasser, wird das Öl aufschwimmen. Zwischen den beiden Phasen können sich die obengenannten Kräfte nicht recht ausbilden. An der Grenzfläche bildet sich hingegen eine Grenzflächenspannung aus. Die Grenzflächenspannung ist der Antrieb, eine möglichst kleine Grenzfläche zu bilden, und verhindert damit die Existenz einer Emulsion.
Zur Herstellung und Stabilisierung einer Emulsion sind grenzflächenaktive Substanzen, die Tenside (Emulgatoren), notwendig. Die Grenzflächenspannung an der Öl-Wasser-Phasengrenzfläche wird durch das Tensid deutlich gesenkt. Sie vermitteln zwischen den beiden Phasen und haben einen polaren (hydrophilen) und einen unpolaren (lipophilen) Teil. Der polare Teil kann Wasserstoffbrücken ausbilden und sich mit hydrophilen Stoffen verbinden, während der unpolare Teil des Moleküls Van-der-Waals-Kräfte ausbildet und sich mit lipophilen Stoffen verbindet.
Emulsionen sind trotzdem instabile Systeme, haben also eine begrenzte Lebensdauer. Das sogenannte Brechen der Emulsion erfolgt, da die Größe der Grenzflächen durch Zusammenfließen von Tröpfchen zu größeren Tröpfchen verringert wird (siehe Stabilität von Emulsionen). Butter, eine Wasser-in-Milchfett-Emulsion, wird aus Sahne, einer Milchfett-in-Wasser-Emulsion, durch Emulsionsbrechen hergestellt.[1]
Zur zusätzlichen Stabilisierung einer Emulsion können Hydrokolloide als Stabilisatoren eingesetzt werden. Diese Stoffe erhöhen die Viskosität der kontinuierlichen Phase, verzögern die Aufrahmung und dadurch das Brechen der Emulsion.
Obwohl eine Emulsion aus Flüssigkeiten besteht, kann sie auch fest sein und wird dann als feste Emulsion bezeichnet. Wird eine Suspension einemulgiert, spricht man von einer Suspo-Emulsion.[2]
Physikalische Betrachtung
Die wichtigsten Größen bei der Betrachtung von Emulsionen sind das Phasenvolumenverhältnis (der Quotient aus dem Volumen der inneren Phase zu jenem der äußeren), die mittlere Teilchengröße (Dm) sowie die Teilchengrößenverteilung.
Phasenvolumenverhältnis
Bis zu einem Phasenvolumenverhältnis von 0,3/0,7 (30 % innere Phase, 70 % äußere Phase) hängen die Eigenschaften der Emulsion im Wesentlichen von den Eigenschaften der äußeren Phase ab. Die Tröpfchen können sich fast unabhängig voneinander in der äußeren Phase bewegen und auch die Viskosität entspricht ungefähr jener der äußeren Phase.
Mit steigendem Phasenvolumenverhältnis kommen die Eigenschaften der inneren Phase deutlich mehr zum Tragen. Wird der Volumenanteil der inneren Phase zu hoch, so kann die Phasenlage umschlagen. Eine O/W-Emulsion wird zu einer W/O-Emulsion und umgekehrt. Man spricht von einer sogenannten Phaseninversion. Zur Inversion einer O/W-Emulsion kann es auch durch Temperaturerhöhung kommen, da höhere Temperaturen die hydrophilen Wechselwirkungen des Emulgators mit dem Wasser schwächen, so dass die lipophilen Wechselwirkungen relativ gestärkt werden. Somit lässt sich eine energetisch günstigere Situation im System vorfinden, indem die Ölphase die kontinuierliche Phase bildet, in der die Wasserphase emulgiert vorliegt. Das (effektive) Phasenvolumenverhältnis kann außerdem durch kontrollierte Aggregation der dispergierten Phase erhöht werden. Dies geht einher mit einem starken Anstieg der Viskosität und dem Auftreten von scherverdünnendem Fließverhalten.[3]
Tröpfchengröße
Emulsionen, die durch Scheren (z. B. Rotor-Stator-System) und Hochdruck-Emulgiermaschinen hergestellt werden, sind nicht monodispers. Die Tröpfchengrößen sind innerhalb einer gewissen Spanne verteilt (siehe auch Dispersitätsanalyse). Die Herstellung monodisperser Emulsionen ist durch Dispergieren mittels Mikroporen (mikroporöse Festkörper, Membranen oder Mikrokanäle) möglich.
Polydisperse Emulsion lassen höhere Raumerfüllungen realisieren, als dies in einer monodispersen, hexagonal dichtesten Packung möglich wäre. Zwischenräume zwischen den größeren Tropfen werden dabei mit kleineren Tröpfchen aufgefüllt.
Der mittlere Teilchendurchmesser (Dm) in Emulsionen liegt normalerweise zwischen 100 Nanometer und 1 Millimeter. Je größer der mittlere Teilchendurchmesser und je breiter die Teilchengrößenverteilung, desto stärker ist die milchig-weiße Trübung der Emulsion. Emulsionen wie zum Beispiel Milch wirken im Auflicht bläulich, im Durchlicht teils deutlich rot. Ursache davon ist die Abhängigkeit der Streuung vom Teilchendurchmesser (siehe dazu Mie-Streuung, elektromagnetische Streuung an Objekten in der Größenordnung der Wellenlänge und Rayleigh-Streuung).
Emulsionen mit einem Tröpfchendurchmesser[4]
- größer 1 Mikrometer nennt man Makroemulsionen,
- im Bereich von 1 Mikrometer oder kleiner nennt man Miniemulsion oder submikrone Emulsion (letztere sind thermodynamisch stabiler),
- unterhalb von 100 Nanometern nennt man Nanoemulsion
Stabilität von Emulsionen
Überwiegend sind Emulsionen thermodynamisch instabil: Die disperse Phase ist bestrebt, sich durch Koaleszenz zu größeren Bereichen zu vereinigen – dabei wird die Grenzflächenenergie zwischen den beiden Phasen verringert.[4]
Emulsionen sollen meist für einen bestimmten Zeitraum (zwischen wenigen Stunden und einigen Jahren) und unter bestimmten Bedingungen (Temperaturbereich, pH-Bereich) erhalten bleiben. Zerfällt eine Emulsion, so geschieht dies in einzelnen Phasen, die oft jedoch gleichzeitig ablaufen.
- Phase: Kurzzeitig stabile Emulsion
Beispielsweise Fetttröpfchen sind in der äußeren Phase (Wasser) dispergiert. - Phase: Aufrahmung oder Sedimentation (reversibel)
Aufgrund der Gravitationskraft erfolgt eine Trennung der gemischten Phasen in die spezifisch leichtere und die spezifisch schwerere. - Phase: Ostwald-Reifung (Ripening)
- Phase: Aggregation (reversibel)
Die Fetttröpfchen bilden Aggregate, der Teilchendurchmesser wird vergrößert und nach dem Stokes’schen Gesetz erhöht sich die Sedimentationsgeschwindigkeit der dispergierten Fetttröpfchen. - Phase: Koaleszenz
Die Fetttröpfchen vereinigen sich; dies kann im Extremfall zum Brechen der Emulsion führen.
Herstellung von Emulsionen
Durch Verkleinerung der Tropfen bei der Herstellung einer Emulsion erhöht sich die Grenzfläche zwischen den beiden Phasen. Dabei muss die Grenzflächenspannung überwunden und eine neue Grenzfläche geschaffen werden. Dies erfordert Arbeit, die mechanisch in das System eingebracht werden muss. Durch dabei auftretende Scherkräfte werden die Tröpfchen immer kleiner.
Tenside (nieder- und höhermolekular) und hochmolekulare Emulgatoren
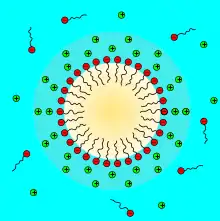
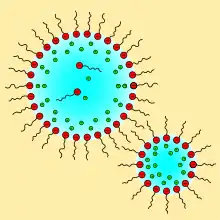
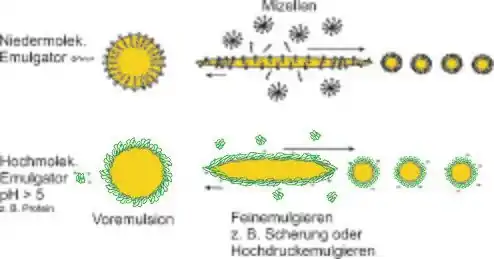
Durch Tenside bzw. Emulgatoren, die häufig auch als Surfactants (surface active agents) bezeichnet werden, lässt sich die Grenzflächenspannung en drastisch senken. Das Tensid soll auch verhindern, dass die neu entstandenen Tröpfchen wieder koaleszieren (zusammenfließen). Dazu muss das Tensid möglichst schnell an die neue Grenzfläche der gebildeten Tropfen diffundieren und einen Grenzflächenfilm bilden. Synthetische Tenside schaffen dies in wenigen Millisekunden.
Hochmolekulare grenzflächenaktive Substanzen werden aufgrund ihrer amphiphilen und überwiegend leichten molekularen Umordnung bzw. Flexibilität an der Grenzfläche (ionische Molekülreste zur Wasserphase gerichtet) ebenfalls als Emulgatoren bezeichnet (z. B. Proteine, Polyvinylalkohole mit hohem Polymerisationsgrad). Diese adsorbieren etwas langsamer (aber ebenfalls in Millisekunden) und bilden gegenüber den Tensiden stabilere und höher viskose Grenzflächen (siehe nachfolgende Abbildung). Dadurch weisen diese Emulsionen gegenüber den niedermolekularen Emulgatoren eine höhere Koaleszenzstabilität auf.
Eine genauso zu beachtende Eigenschaft bei der Auswahl eines geeigneten niedermolekularen Tensids ist seine Spreitungsgeschwindigkeit (Ausbreitungsgeschwindigkeit). Die Grenzfläche eines neuen Tropfens ist zunächst nur teilweise von Tensid belegt. Dieses spreitet nun zu jenem Teil der Grenzfläche, der zunächst noch unbelegt war. So entsteht zunächst ein Tensidkonzentrations-Gradient an der Grenzfläche, der je nach Spreitungsgeschwindigkeit mehr oder weniger schnell zu einer gleichmäßigen Tensidverteilung ausgeglichen wird.
Mit zunehmender Tropfenzerkleinerung und ansteigender Grenzfläche nimmt die Tensidkonzentration in der kontinuierlichen Phase ab. Ist nicht ausreichend Tensid zur Belegung der Grenzfläche vorhanden, kann keine kleinere stabile Tropfengröße erzielt werden.
Aus dem Volumen der zu dispergierenden Phase und dem angestrebten Tröpfchendurchmessser kann für die zu belegende Grenzfläche die notwendige Emulgatormenge kalkuliert werden. Hierfür muss bekannt sein, welche Fläche durch 1 g Emulgator belegbar ist (niedermolekulare Emulgatoren etwa 10 mg pro ml Öl,[5] Proteine etwa 15 mg pro ml Öl). Mit Abnahme der Partikelgröße steigt die Grenzfläche pro ml Öl, dies führt zu einem höheren Emulgatorbedarf.
Bei höhermolekularen Emulgatoren wird zur Absicherung der Emulsionsbildung etwa die doppelte Menge eingesetzt.
Beim Einsatz von niedermolekularen Tensiden liegt die notwendige Konzentration allgemein deutlich oberhalb der erforderlichen bzw. des Mizellbildungspunktes cmc (engl.: critical micelle concentration). Aus den Mizellen werden mit Zunahme der Grenzfläche die notwendigen Emulgatormoleküle nachgeliefert.
Normalerweise ist jene Phase, in der sich der Emulgator besser löst, die äußere bzw. kontinuierliche Phase. Bei einem HLB-Wert von 3 bis 6 wird die Emulsion eine W/O-Emulsion, von 8 bis 18 eine O/W-Emulsion (Bancroft-Regel).
Hochmolekulare Emulgatoren an Grenzflächen
Während Polyglycerin-Polyricinoleat (PGPR, M 1200-2000 g/mol), ein Emulgator für Wasser-in-Öl-Emulsionen, eine höhere molare Masse aufweist, werden die polymeren Emulgatoren mit etwa M < 10 000 g/mol zu den hochmolekularen gerechnet. Aufgrund des unterschiedlichen Gehaltes an nichtgeladenen und geladenen Aminosäuren und eines pH-abhängigen Ladungszustandes adsorbieren die entfalteten amphiphilen Proteinmoleküle mit unterschiedlicher Aktivität an den Grenzflächen (Luft/Wasser, Wasser/Öl). Mit Zunahme der Ladung und der Löslichkeit steigt an der Grenzfläche auch die Affinität zur wässrigen Phase (hohe Hydrophilie), gleichzeitig lagern sich die ungeladenen lipophilen Aminosäurereste an der Luft- bzw. Ölphase an und unterstützen bei Eintrag von Scherenergie die Bildung von Luftblasen oder Öltropfen.
Da Proteine überwiegend oberhalb des isoelektrischen Punktes (IP) negativ und unterhalb des IP (im stärker sauren pH-Bereich) positiv geladen sind, ändert sich durch Einstellung des pH-Wertes der wässrigen Phase der Ladungszustand an der Grenzfläche. So kann die Proteingrenzfläche z. B. bei einem pH-Wert unter 4,0 bei positiver Ladung mit negativ geladenen Polymeren (Polyelektrolyten) komplexieren. Dies kann genutzt werden, um Grenzflächen zusätzlich mit negativ geladenen Polysacchariden zu belegen (ionische Bindung). Dadurch wird der Stofftransport zwischen wässriger und hydrophober Phase verändert (z. B. geringerer Sauerstoffdurchgang mit verminderter Oxidation der Ölphase, geringere Freisetzung hydrophober Aromastoffe, langsamere Lipidfreisetzung im Verdauungstrakt).
Durch Einbringen der mit einem Polysaccharid zusätzlich beschichteten Öltropfen in eine neutrale Proteinphase ist eine weitere Beschichtung möglich. Nach nochmaliger pH-Absenkung kann eine weitere negativ geladene Polysaccharidschicht angelagert werden. Varianten der Grenzflächenbelegung sind in der folgenden Abbildung für mögliche Grenzflächenstabilisierungen dargestellt.
Zusätzlich zur zweiten Proteinschicht können auch kleinere, mit Protein stabilisierte Öltropfen angelagert werden. Derartige Öltropfen, die mit sehr kleinen Öltropfen umhüllt sind, bezeichnet man als Kolloidosome.[6] Stark denaturierte Proteine, die als sehr kleine Aggregate oder Gelpartikel (Nano oder Mikropartikel) vorliegen, adsorbieren ebenfalls an Grenzflächen und führen zur Stabilisierung. Derartige Tropfenstabilisierung wird als „Pickering-Stabilisierung“, die Emulsionen werden als „Pickering-Emulsionen“ (auch „Pickering-type emulsion“) bezeichnet[7][8] (siehe Feststoffstabilisierung). Mögliche Varianten der Grenzflächenstabilisierung von Öl-in-Wassertropfen sind:[9][10]
- Pickering- oder Partikelstabilisierung,
- Einsatz niedermolekularer oder hochmolekularer Emulgatoren (Proteine),
- Einsatz von Protein-Polysaccharid-Komplexen (lösliche oder unlösliche Komplexe),
- Bildung von Multischichten aus Protein und ionischen Polysacchariden,
- Anlagerung beschichteter Nano-Tropfen (Kolloidosome).
Feststoffstabilisatoren
Eine Emulsion kann z. B. mittels Partikel unterschiedlichster Art stabilisiert werden. Hierzu gehören u. a. starre und nicht quellbare, jedoch unterschiedlich anfeuchtbare, quellbare, synthetisierte ungeladene oder geladen amphiphile starre oder verformbare Partikel (Janus-Partikel). Dies wird allgemein als Partikelstabilisierung oder die Emulsion nach dem Entdecker als Pickering-Emulsion bezeichnet.
Pickering[11] hat 1907 gezeigt, dass kleine Festpartikel (Salze), die von Wasser besser als von Öl benetzt werden, O/W-Emulsionen stabilisieren können. Wichtig für eine ausreichende Stabilisierung ist hierbei, dass sich eine mechanisch stabile Grenzfläche ausbildet.
Partikeleigenschaften
Die Partikel sollten für die Grenzflächenstabilisierung (Luft/Wasser, Öl/Wasser) folgende Eigenschaften aufweisen:
- Nano- oder Mikropartikel, amphiphil oder mit der hydrophilen Phase unterschiedlich benetzbar
- In hydrophiler oder hydrophober Phase unlöslich oder in hydrophiler Phase quellbar
- Bildung eines Kontaktwinkels θ < 90° an der Grenzfläche zur Bildung von Öl-in-Wasser-Emulsionen, θ > 90° zur Bildung einer Wasser-in-Öl-Emulsion
Vorteile einer feststoffstabilisierten Emulsion
- Überwiegend resistenter gegen Änderungen des chemischen Milieus (pH-Wert, Salzkonzentration etc.)
- Erhöhte Langzeitstabilität (hohe Koaleszenzstabilität von Emulsionen mit größeren Öltropfen, z. B. 10 bis 100 µm)
- Koaleszenzstabilisierung von Doppelemulsionen
- Einstellbare Verdaulichkeit im Magendarm-Trakt durch Partikel mit eingestellter Enzymresistenz
- Erhöhung der Gefrier-Tau-Stabilität
- Beeinflussung der rheologischen Eigenschaften (Erhöhung der Viskosität, Fließgrenze und Konsistenz)
Geräte
Um die für die Emulgierung benötigte Arbeit in das Medium einzutragen, gibt es eine ganze Reihe möglicher Methoden. Generell können hierbei jedoch vier unterschiedliche Obergruppen unterschieden werden.
Rotor-Stator-Systeme
Bei diesen wird ein Bauteil bewegt (bzw. gedreht) und ein Bauteil ruht. Beispiele sind:
- Fantaschale und Pistill
- Rührwerke
- Schüttler
- Vibrationsmischer
- Emulgierzentrifugen
- Kolloidmühlen
- Zahnkranzdispergiermaschinen
Strömungsmechanische Mittel
- Prallplatten[12]
- Wirbelkammern
- Hochdruckhomogenisatoren, diese bestehen aus einer Pumpe und Blenden oder Ventilen. Hierfür können z. B. Zerstäuber eingesetzt werden.
Ultraschallgeneratoren
Hier werden mittels eines Ultraschallgebers und einer Sonotrode die Tropfen zerkleinert. Das Prinzip der Ultraschall-Emulgierung basiert auf der Kavitation, welche erzeugt wird, wenn hochintensive Ultraschallwellen in eine Flüssigkeit eingetragen werden. Die Ultraschallkavitation erzeugt hohe Scherkräfte sowie Mikroturbulenzen in der Flüssigkeit, so dass die Tropfen der zwei Phasen (Wasser- und Ölphase) zerkleinert und zu einer Phase vermischt werden.[13]
Mikrostrukturierte Systeme
Mittels Mikroporen in Membranen oder mittels Mikrokanälen (microchannel)[14] können polydisperse oder monodisperse Öltropfen Partikel mit einstellbarem Größenbereich erzeugt werden. Die Architektur der Mikroporen (undefinierte oder definierte Porengestalt, runde oder spaltförmige Austrittsöffnung) ist dabei von Bedeutung.
Wichtige Parameter für die Tropfengröße der Emulsionen sind in der nachfolgenden Abbildung zusammengefasst. Diese Parameter gelten überwiegend auch für die Bildung monodisperser Emulsionen, erzeugt mittels definierter Mikrokanäle.
Rotierende Membranen ermöglichen die Erzeugung sehr kleiner Tropfen insbesondere durch zusätzliche Erhöhung der Wandschubspannung. Über die Rotationsgeschwindigkeit und die Viskosität der kontinuierlichen Phase kann die Wandschubspannung wesentlich erhöht werden.[15]
Zur Herstellung von Membranen mit undefinierter und definierter Porengeometrie werden Kunststoffe, spezielles Glas, Keramik und verschiedenen Metalle (z. B. Nickel, Eisen, Aluminium) eingesetzt. Die Oberflächen werden je nach Dispersphase hydrophiliert oder hydrophobiert. Zur Bildung monodisperser Tropfen werden auch Silicon-Mikroplättchen oder 3-D-Druck-Membranen aus Kunststoff eingesetzt.
Für die Tropfengröße und die Tropfengrößenverteilung sind überwiegend folgende Parameter von Bedeutung:
- Zusammensetzung der kontinuierlichen Phase (Emulgatortyp, Dichte, Viskosität)
- Grenzflächenspannung zwischen den Phasen
- Volumenstrom der kontinuierlichen Phase bzw. Wandschubspannung
- Membranmaterial (Porendurchmesser, Hydrophilie, Porenform)
- Dichte, Viskosität und Flux der Ölphase
Mikroemulsionen
Mikroemulsionen sind Wasser-Öl-Tensid-Gemische, die im Gegensatz zu anderen Emulsionen thermodynamisch stabil sind. Sie sind optisch transparent und bilden sich ohne die für die Herstellung von Emulsionen sonst nötige hohe Energiezufuhr. Meist verwendet man zur Darstellung einer Mikroemulsion Cotenside oder Cosolventien. Mikroemulsionen bilden sich nur in bestimmten Bereichen der Phasendiagramme der ternäre oder auch quaternären Stoffsysteme.
Multiple Emulsion
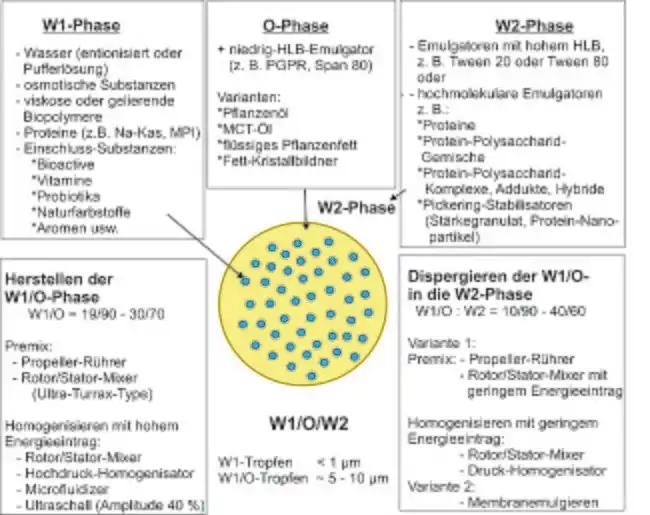
Multiple Emulsionen bestehen aus Tropfen in Tropfen. Während unter multiplen Emulsionen z. B. W1/O1/W2/O2/W3- oder O1/W1/O2/W2-Systeme verstanden werden, bezeichnet man W1/O/W2- und O1/W/O2-Systeme auch als Doppelemulsionen.
Bei der Herstellung derartiger Emulsionen kommt es darauf an, dass für Doppelemulsionen die innere W1- oder O1-Phase mit Tropfengrößen < 1 µm und hoher Koaleszenzstabilität hergestellt wird. Die entstehende W1/O- oder O1/W-Emulsion wird in eine neue äußere Phase unter Bedingungen dispergiert, die die Erhaltung der inneren W1- oder O1-Phase ermöglichen. Es sind deshalb W/O- und O/W-Emulgatoren so auszuwählen, dass beim Emulgierprozess keine negativen Wechselwirkungen stattfinden, die zur Instabilität der inneren Emulsion führen. Weiterhin sind die innere und äußere Wasserphase in der Osmolalität so einzustellen, dass die Tropfen der inneren W1-Phase aufgrund hoher osmotischer Unterschiede nicht quellen oder schrumpfen.[16][17][18]
Doppelemulsionen sind für den Einschluss von Inhaltsstoffen in die innere Phase geeignet. Hiermit können Stoffe verkapselt werden, die empfindlich gegenüber Oxidation sind, aus sensorischen oder anderen Gründen während der Lagerung langsam oder unter Einwirkung von Scherkräften oder osmotischem Schock schnell freigesetzt werden. Es kann sich z. B. um flüchtige Aromastoffe, Geschmacksstoffe (erwünscht oder unerwünscht), Mikronährstoffe, Probiotika, Therapeutika, Enzyme und biologisch aktive Substanzen handeln. Weiterhin sind W1/O/W2-Systeme über die Erhöhung des Anteiles an W1-Phase in O zur Herstellung fettreduzierter Lebensmittelemulsionen geeignet.
Im technischen Bereich können multiple bzw. Doppelemulsionen u. a. zur Flüssigmembran-Permeation (einer Sonderform der Extraktion) genutzt werden, bei der die mittlere Phase (Membranphase) als Filter zwischen innerer und äußerer Phase dient. Die Flüssigmembran-Permeation wird auch zur Extraktion von Schwermetallspuren aus Abwässern genutzt, dabei wird beispielsweise Schwefelsäure in einer Ölphase, die Chelatbildner gelöst enthält, emulgiert und diese Emulsion wiederum im Abwasser emulgiert, die Schwermetalle werden durch Flüssig-Flüssig-Extraktion in der Ölphase gelöst und daraus ebenfalls durch Flüssig-Flüssig-Extraktion in die Schwefelsäure übergeführt. Nach Abtrennung der Ölphase wird die Säure-in-Öl-Emulsion in einem hochfrequenten Wechselstromfeld gespalten.[19]
Fotoemulsion
In der Analogfotografie bezeichnet man die auf einen Schichtträger aufgebrachte lichtempfindliche Schicht gemeinhin als Fotoemulsion. Im oben bezeichneten Sinne handelt es sich dabei aber um keine Emulsion, sondern um eine erstarrte Suspension.
Einteilung im Schema der chemischen Stoffe
| Schematische Einteilung der Stoffe | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Siehe auch
Literatur
- N. I. Kosin: Nahrungsmittelemulsionen. übersetzt aus dem Russischen von Karlwilhelm Horn. Fachbuchverlag Leipzig, 1954, DNB 574438777.
- H. Schubert (Hrsg.): Emulgiertechnik Grundlagen Verfahren und Anwendungen. Behr’s Verlag, Hamburg 2005, ISBN 3-89947-086-9.
- G. Lagaly, O. Schulz, R. Zimehl: Dispersionen und Emulsionen. Steinkopff Verlag, Darmstadt 1997, ISBN 3-7985-1087-3.
- B. Dobiáš: Emulsionen. Teil 1. In: Tenside Detergents. Band 15, Nr. 5, 1978, S. 225-238; Teil 2. In: Tenside Detergents. Band 16, Nr. 6, 1979, S. 289–297.
- H. Asche (Hrsg.): Technologie von Salben, Suspensionen und Emulsionen. Ein Seminar der APV vom 20.–22. September 1982 in Darmstadt. Wissenschaftliche Verlagsgesellschaft, Stuttgart 1984, ISBN 3-8047-0748-3.
- G. Muschiolik, H. Bunjes (Hrsg.): Multiple Emulsionen – Herstellung und Eigenschaften. Behr’s Verlag, 2007, ISBN 978-3-89947-339-1.
Einzelnachweise
- Gerhard Lagaly, Oliver Schulz, Ralf Zimehl: Dispersionen und Emulsionen – Eine Einführung in die Kolloidik feinverteilter Stoffe einschließlich der Tonminerale. Steinkopf-Verlag, Darmstadt, ISBN 3-7985-1087-3, S. 253 (teilweise einsehbar bei Google-Books).
- H. Schubert (Hrsg.): Emulgiertechnik. Grundlagen Verfahren und Abwendungen. ISBN 3-89947-086-9, S. 531.
- Philipp L. Fuhrmann, Guido Sala, Markus Stieger, Elke Scholten: Clustering of oil droplets in o/w emulsions: Controlling cluster size and interaction strength. In: Food Research International. Band 122, August 2019, ISSN 0963-9969, S. 537–547, doi:10.1016/j.foodres.2019.04.027.
- H. Schubert (Hrsg.): Emulgiertechnik. Grundlagen Verfahren und Anwendungen. Behr’s Verlag, ISBN 3-89947-086-9, S. 1 (online in Auszügen einsehbar bei Google-Books), zuletzt abgerufen im Juli 2012.
- G. E. Petrowski: Emulsion Stability and its Relation to Foods. In: Advances in Food Research. Band 22, 1976, S. 309–359.
- Y. S. Gu, E. A. Decker, D. J. McClements: Formation of colloidosomes adsorption of small charged oil droplets onto the surfaces of large oppositely charged oil droplets. In: Food Hydrocolloids. Band 21, 2007, S. 516–526. doi:10.1016/j.foodhyd.2006.05.011
- Y. S. Gu, E. A. Decker, D. J. McClements: Formation of colloidosomes adsorption of small charged oil droplets onto the surfaces of large oppositely charged oil droplets. In: Food Hydrocolloids. Band 21, 2007, S. 516–526. doi:10.1016/j.foodhyd.2006.05.011
- E. Dickinson: Use of nanoparticles and microparticles in the formation and stabilization of food emulsions. In: Trends in Food Science & Technology. Band 24, 2012, S. 4–12. doi:10.1016/j.tifs.2011.09.006
- G. Muschiolik: Grenzflächenaktive Biopolymere - Emulgatoren als green ingredients. In: Deutsche Lebensmittel-Rundschau. Band 114, 2018, S. 434–444.
- G. Muschiolik: Entwicklung neuer Emulsionssysteme. In: Behr´s Jahrbuch 2013. Behr´s Verlag, Hamburg 2013, ISBN 978-3-95468-006-1, S. 117–134.
- S. U. Pickering: Emulsions. In: Journal of the Chemical Society. Band 91, 1907, S. 2001–2021. doi:10.1039/CT9079102001
- Patent EP0674941B1: Vorrichtung zur Bildung einer Öl-Wasser-Emulsion. Angemeldet am 10. März 1995, veröffentlicht am 29. Oktober 1997, Anmelder: MTU friedrichshafen GmbH, Erfinder: Georg Donauer et al.
- Generation of Emulsions by Ultrasonic Cavitation. Abgerufen am 22. Februar 2017 (englisch).
- G. T. Vladisavljević, I. Kobayashi, M. Nakajima: Production of uniform droplets using membrane, microchannel and microfluidic emulsification devices. In: Microfluid Nanofluid. Band 13, 2012, S. 151–178. doi:10.1007/s10404-012-0948-0
- G. Muschiolik, H. Bunjes (Hrsg.): Multiple Emulsionen – Herstellung und Eigenschaften. Behr’s Verlag, 2007, ISBN 978-3-89947-339-1.
- G. Muschiolik, H. Bunjes (Hrsg.): Multiple Emulsionen – Herstellung und Eigenschaften. Behr’s Verlag, 2007, ISBN 978-3-89947-339-1.
- G. Muschiolik: Multiple Emulsionen – Stand und Fortschritte. In: Behr's Jahrbuch 2018 Lebensmittelwirtschaft. Behr´s GmbH, Hamburg 2018, ISBN 978-3-95468-526-4, S. 85–93.
- G. Muschiolik, E. Dickinson: Double Emulsions Relevant to Food Systems: Preparation, Stability, and Applications. In: Comprehensive Reviews in Food Science and Food Safety. Band 16, 2017, S. 532–555. doi:10.1111/1541-4337.12261
- Rolf Marr, Manfred Prötsch, Alexander Bouvier, Josef Draxler, Alois Kriechbaumer: Kontinuierliche Versuche zur Flüssig-Membran-Permeation in einer Pilot-Anlage. In: Chemie Ingenieur Technik. Band 55, Ausgabe 4, 1983, S. 328–329.