Biomineralisation
Biomineralisation ist ein Vorgang, bei dem als Folge der Lebenstätigkeit von Organismen mineralische Produkte (Biominerale) entstehen. Die Fähigkeit zur Biomineralisation ist annähernd so alt wie das Leben auf der Erde (mit den ersten Prokaryoten im Archaikum entstanden) und unterliegt einem ebenso langen Evolutionsprozess. Die damit verbundene laufende Optimierung der Mineralisationsvorgänge hat zu Ergebnissen geführt, die zunehmend auch für die Wissenschaft und Technik interessant werden (Bionik).

Die Biomineralisation kann in die folgenden drei Grundtypen unterteilt werden: Fällungs- und Oxidationsreaktionen, Reaktionen, bei denen perfekt kristallisierte Minerale erzeugt werden sowie Reaktionen, die zu „Verbundwerkstoffen“ führen. Dem zuletzt genannten Reaktionstyp wird allgemein die größte Aufmerksamkeit geschenkt, so dass man ihn als „Biomineralisation im engeren Sinne“ bezeichnen kann.
Fällungs- und Oxidationsreaktionen
Hierbei handelt es sich um vergleichsweise einfache Reaktionen, in denen gelöste Stoffe durch die Stoffwechseltätigkeit von Mikroorganismen in ungelöste Substanzen überführt werden.
Ausfällung von Kalk (Bildung von Stromatolithen)
Die ältesten Stromatolithen sind vor ca. 3,5 Milliarden Jahren von Cyanobakterien gebildet worden und zählen somit zu den ältesten Zeugnissen des Lebens auf der Erde. Als autotrophe Organismen verbrauchen sie Kohlenstoffdioxid und fällen dadurch nach der folgenden Reaktion Calciumcarbonat aus:
Dadurch bilden sich kissen- oder knollenförmige Kalkablagerungen, zu deren Wachstum auch ton- und schluffartige Sedimente beitragen. Für die Organismen liegt der Vorteil dieser Art von Biomineralisation wahrscheinlich darin, dass auf diesem Wege eine feste Grundlage entsteht, auf der sie sich als „Biomatten“ auch unter widrigen Wetterbedingungen halten können.
Ausfällung von Eisen(III)-oxidhydrat (FeO(OH))

In einem Milieu, in dem die Oxidation gelöster Eisen(II)-ionen auf rein chemischem Wege langsam erfolgt, können einige Mikroorganismen die Oxidation der Eisenionen durch Sauerstoff oder Nitrat beschleunigen. Die Oxidation mit Nitrat verläuft nach der folgenden Reaktionsgleichung:
Das Eisen(III)-oxidhydrat lagert sich an den Strukturen der Mikroorganismen ab, ein Vorgang, der „Vererzung“ genannt wird. Als chemoautotrophe Bakterien gewinnen die beteiligten Organismen damit die zur Aufrechterhaltung ihrer Lebensprozesse erforderliche Energie. Ablagerungen von Eisen(III)-oxid und -oxidhydrat sind in der Natur häufig anzutreffen. Dabei kann es sich um Produkte der Biomineralisation handeln. Der Nachweis, dass dies im Einzelfall zutrifft, ist jedoch schwierig zu führen, weil Eisen(II)-ionen unter günstigen Bedingungen auch ohne Mithilfe von Mikroorganismen oxidiert werden können. In Einzelfällen ist jedoch die Struktur der vererzten Mikroorganismen – wie das Bild „Vererzte Exemplare von Gallionella ferruginea…“ zeigt, so deutlich erkennbar, dass an der Biomineralisation in diesem Falle kein Zweifel besteht.
Durch die Tätigkeit Sauerstoff freisetzender Mikroorganismen sind auch die Bändereisenerze entstanden.
Ausfällung von Mangan(IV)-oxid
-oxid_als_Biofilm%252C_2x3_mm.jpg.webp)
Mangan(II)-ionen können nur mit Sauerstoff zu Mangan(IV)-oxid oxidiert werden:
Die Energieausbeute dieser Reaktion ist so niedrig, dass sie zur Aufrechterhaltung der Lebensprozesse nicht ausreicht. Das Mangan(IV)-oxid ist jedoch ein gutes Adsorptionsmittel für Nährstoffe, die sich dadurch in unmittelbarer Nähe der Organismen anreichern. Dadurch entsteht für die Mikroorganismen ein indirekter Nutzen. Spektakuläre Ergebnisse der Biomineralisation von Mangan(IV)-oxid sind die Manganknollen.
Die Ausfällung von Mangan(IV)-oxid durch Mikroorganismen ist die preiswerteste und gleichzeitig effektivste Möglichkeit, im Rahmen der Trinkwasseraufbereitung in Wasserwerken gelöstes Mangan zu eliminieren.
Abscheidung von Pyrit und Markasit

In Grundwasserleitern, die fossile organische Substanz enthalten, können Mikroorganismen Sulfat reduzieren. Bei Gegenwart von Eisen(II)-ionen können dabei Eisendisulfide (Markasit, Pyrit) gebildet werden. Diese Reaktion läuft mit sehr geringer Geschwindigkeit ab (Halbwertszeit: ca. 76 bis 100 Jahre). Die folgende Reaktionsgleichung soll diese Art der Biomineralisation verdeutlichen:
Reduktionsmittel ist der Zellulose-Anteil in der fossilen organischen Substanz, hier vereinfacht als Kohlenstoff (C) wiedergegeben. Bei dieser Reaktion entstehen schlecht kristallisierte Produkte (z. B. „framboidaler Pyrit“). Die beteiligten Mikroorganismen gewinnen mit der Sulfatreduktion die Energie für ihre Lebensprozesse. Die Abscheidung von Markasit bzw. Pyrit ist eine wichtige Teilreaktion bei den Selbstreinigungsprozessen in Grundwasserleitern, die fossile organische Substanz enthalten.
Reaktionen, bei denen perfekt kristallisierte Minerale erzeugt werden
Eis
Eis gilt als Mineral mit vergleichsweise niedrigem Schmelzpunkt. Es kann allen Lebewesen gefährlich werden, wenn sie sich nicht wie die warmblütigen Organismen aktiv gegen das Einfrieren schützen können. Im Laufe der Evolution haben sich zwei Strategien entwickelt, mit denen sich die Organismen wehren können: Manche Fische verhindern das Gefrieren ihrer Körperflüssigkeit mit Frostschutzproteinen. Bestimmte Frosch- und Schildkrötenarten wenden die gegenteilige Taktik an: Sie reichern ihr Blut mit Proteinen („Eisnukleationsproteinen“) an, die das Einfrieren fördern und dabei so steuern, dass ihre Zellen keinen Schaden nehmen. Auch manche Bakterien bilden Proteine, welche die Eisbildung fördern. Suspensionen von Pseudomonas syringae hat man daher schon zur Herstellung künstlichen Schnees verwendet.
Calciumcarbonat
Wasserklare Calcitkristalle haben – je nach optischer Achse – einen Brechungsindex von 1,6584 bzw. 1,4864. Calcit eignet sich daher als Werkstoff für die Herstellung von Linsen. Der Seestern Ophioma wentii besitzt Augen mit optisch korrekt orientierten Mikrolinsen aus Kalzit, die über den gesamten Körper verteilt sind. Optische Kalzitlinsen benutzten bereits vor ca. 350 Millionen Jahren einige Arten der Trilobiten. Ihre Augen bestanden aus bis zu 15.000 Einzellinsen. Auch für das Gehör und den Gleichgewichtssinn kann Calciumcarbonat hilfreich sein: Zebrafische benutzen Gehörsteine aus Aragonit, die sie mit Hilfe von „Starmaker-Proteinen“ so formen, dass sie ihren Zweck optimal erfüllen.
Magnetit
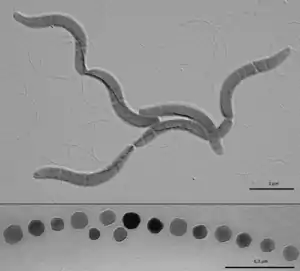
Magnetit, ein schwarzes Eisenoxid mit der Formel Fe3O4 hat, wie der Name andeutet, ferromagnetische Eigenschaften. In lebenden Organismen wurde dieses Mineral zum ersten Mal aufgefunden, als man magnetotaktische Bakterien untersuchte, also Mikroorganismen, die ihre Eigenbewegung an den Feldlinien des Erdmagnetfelds orientieren (z. B. Magnetospirillum gryphiswaldense oder Magnetospirillum magnetotacticum). Die von einer Membran umschlossenen Magnetit-Kristalle, die Magnetosomen, sind in einer kettenförmigen Struktur angeordnet, die durch ein spezielles Protein erzwungen wird. Die Kristalle selbst sind – im Gegensatz zu abiotisch entstandenem Magnetit – völlig frei von Defekten des Kristallgitters. Die definierte Größe der Kristalle von ca. 45 nm bewirkt deren einheitliches magnetisches Moment (Ein-Domänenkristalle).
Die als Magnetotaxis bezeichnete Fähigkeit bietet den Mikroorganismen, die an die Sauerstoffarmut von Gewässersedimenten angepasst sind, den Vorteil, dass sie entlang der Feldlinien den kürzesten Weg in die Sedimente finden können. Auch in höheren Tieren, die bei ihren Wanderungen größere Strecken zurücklegen, hat man Magnetosomen entdeckt, beispielsweise bei Zugvögeln, Forellen und Lachsen.
Erzeugung von „Verbundwerkstoffen“
Mit Verbundwerkstoffen gelingt es dem Menschen schon seit Jahrhunderten, Materialien mit unterschiedlichen Eigenschaften so zu kombinieren, dass neuartige Werkstoffe entstehen. Der bekannteste technische Verbundwerkstoff ist der Stahlbeton, bei dem die Druckfestigkeit des Betons mit der Zugfestigkeit des Stahls kombiniert wird. In der belebten Natur sind Materialien, bei denen es sich prinzipiell um Verbundwerkstoffe handelt, seit mehreren hundert Millionen Jahren weit verbreitet. Die anorganische Komponente dieser Biomaterialien wird meist in sehr geringer Partikelgröße abgeschieden. Daher können sie aus materialwissenschaftlicher Sicht als „Nanokompositwerkstoff“ oder „nanostrukturierter Hybridwerkstoff“ betrachtet werden. Das Material von Knochen und Zahnschmelz sowie die Schalen von Eiern, Muscheln und Kieselalgen sind bekannte Beispiele.
Wissenschaftler versuchen, die Komponenten natürlicher „Verbundwerkstoffe“ schonend zu trennen und getrennt zu analysieren. Aufbau und Funktion der Substanzen können auf diese Weise schrittweise aufgeklärt werden. Von einer Antwort auf die Frage, mit welchen Mitteln Organismen in den Stoffhaushalt ihrer Umgebung eingreifen, um Biomineralisation zu betreiben, ist man jedoch noch weit entfernt.
Calciumcarbonat


Als Komponente biologischer „Verbundwerkstoffe“ spielt Calciumcarbonat („Kalk“) unter anderem eine Rolle bei den Gehäusen einzelliger Organismen (Foraminiferen) und zahlreicher wirbelloser Meerestiere sowie bei den Schalen der Vogeleier. Kein Produkt der Biomineralisation erreicht einen größeren globalen Umsatz als das Calciumcarbonat: Die kalkigen Reste abgestorbener Organismen treten gesteinsbildend auf, in Form feinkörniger Hochseekalksteine (z. B. „Kreide“) oder küstennah entstandener Fossilschuttkalksteine. Wenn Fossilschuttkalksteine verwittern, werden oft die Strukturen der enthaltenen Kalkskelette an der Gesteinsoberfläche herausgearbeitet. Tiere, die sich eine kalkhaltige Hülle zulegen, wie Foraminiferen und andere Einzeller sowie Muscheln, Schnecken und andere Wirbellose, schützen damit ihren empfindlichen Weichkörper.
Es ist davon auszugehen, dass in der Entwicklungsgeschichte die ältesten Schutzhüllen nur aus Proteinen bestanden. Die meisten Schlangen und Eidechsen legen heute noch Eier mit flexibler Protein-Schale. In der Entwicklungslinie, die zu den heutigen Vögeln führt, hat es sich als zweckmäßig erwiesen, in die Schalen Calciumcarbonat einzulagern. Dadurch erhöhte sich die Stabilität der Eihülle. Der Embryo war so besser geschützt, was seine Überlebenschancen bis zum Schlupf erhöhte.
Beispiele:
- Perlmutt ist eine irisierende Form des Aragonits (rhombisch kristallisiertes Calciumcarbonat), die von zahlreichen Meeresschnecken und -muscheln gebildet wird.
- Seeigel nutzen Calciumcarbonat zur Bildung von Schalen, Beißwerkzeugen und Stacheln. Seeigelstachel können über zehn Zentimeter lang werden und dabei eine Festigkeit erreichen, die diejenige von rein anorganischem Calciumcarbonat um mehrere Größenordnungen übertrifft. Auch andere Stachelhäuter besitzen Skelette oder Skelettelemente aus Calciumkarbonat.
- Die Polypen der Steinkorallen scheiden ein Außenskelett auf der Basis von Calciumcarbonat ab. Durch die gemeinsame Abscheidungstätigkeit vieler sehr kleiner Polypen einer Korallenkolonie oder die Kalkabscheidung einzelner größere Polypen (Solitärkorallen) entstehen die typischen kompakten oder verzweigten Strukturen. Die Polypen leben mit bestimmten Photosynthese betreibenden Einzellern (Zooxanthellen) in Symbiose, von denen sie bei der Kalkabscheidung unterstützt werden: die Einzeller konsumieren CO2 und erleichtern dadurch die Kalkausfällung.
Siliziumdioxid
Kieselalgen (Diatomeen) fällen Kieselsäure aus dem Wasser aus und bilden daraus bei Normaltemperatur und Normaldruck wasserhaltiges amorphes Siliziumdioxid (Skelettopal), aus dem sie ihr filigranes Skelett erzeugen. Dieses ist sehr hart und gleichzeitig zäh, so dass es optimalen Schutz bietet.
Die am Aufbau dieses Silikatpanzers beteiligten Proteine können nur durch Flusssäure isoliert werden, mit der der Skelettopal aufgelöst wird. Einige der Aminosäuren, aus denen die Proteine bestehen, gehören nicht zum „Standardrepertoire“ der belebten Natur, sondern wurden nachträglich erheblich verändert. Die ursprüngliche Aminosäuresequenz konnte auf dem Umweg über die genetische Information ermittelt werden. Zwei Typen von Proteinen wurden festgestellt: Das hochmolekulare Protein wird offenbar zur Verstärkung in die Skelettopalstruktur eingebaut. Die niedermolekularen Proteine („Silaffine“) sind in der Lage, aus gewöhnlicher Kieselsäure innerhalb von Minuten einen Festkörper mit komplexer Nanostruktur auszufällen.
Abgestorbene Kieselalgen können Lagerstätten von Kieselgur bilden. Kieselgur ist auf Grund seiner großen inneren Oberfläche ein wichtiges technisches Hilfsmittel, beispielsweise zur Reinigung von Getränken in der Lebensmittelindustrie und zur Herstellung von Dynamit aus Nitroglycerin.
Auch die Pflanzenwelt hat einen großen Umsatz an Siliziumdioxid. Von Reispflanzen ist bekannt, dass sie mit Siliziumdioxid ihre Stängel stabilisieren, die Lichtaufnahme verbessern und die Blätter gegen Wasserverlust durch Verdunstung abdichten.
Hydroxylapatit (Knochen)
Die Knochen der Wirbeltiere (Vertebrata) bestehen zu etwa 65 % aus anorganischen Komponenten, hauptsächlich Hydroxylapatit, einem Calciumphosphat mit der Formel Ca5[OH|(PO4)3] sowie etwa 35 % organischen Komponenten, überwiegend Kollagen. Kollagen ist ein Struktureiweiß sehr hoher Zugfestigkeit. Daneben sind noch Proteine und Fette sowie in frischen Knochen auch noch Wasser vorhanden. Der Hydroxylapatit bewirkt die Druckfestigkeit und Steifigkeit, das Kollagen die Zugfestigkeit der Knochen.

Hydroxylapatit kann in bestimmten Zellen, den Osteoblasten, aus Phosphat- und Calcium-Ionen erzeugt werden. Dazu werden zunächst in einer Kollagen-Matrix aus organischen Phosphaten so lange Phosphationen freigesetzt, bis das Löslichkeitsprodukt für Calciumphosphat überschritten ist. Kollagen wirkt als Kristallisationskeim und es kristallisiert Hydroxylapatit aus. Die hohe Festigkeit kommt dadurch zustande, dass sich die Kristallite des Hydroxylapatits bevorzugt nach Druck- und Zugbeanspruchung in Spannungslinien ausrichten und dabei eine strebenartige Struktur bilden. Diese Architektur des Knochenaufbaus kann mit fossilem Material bis zu den Dinosauriern zurückverfolgt werden.
Die Knochen erlegter Tiere waren für den Menschen durch Jahrtausende hindurch äußerst wertvoll: Als „Verbundwerkstoff“ waren Knochen ein wichtiger Rohstoff zur Herstellung von Werkzeugen. Die organischen Komponenten lieferten Knochenleim und die anorganischen (z. B. als Knochenmehl oder Knochenasche) einen wertvollen Phosphatdünger (bis wegen des BSE-Problems diese Art der Anwendung verboten wurde).
Knochen brauchen nach dem Tod eines Wirbeltieres relativ lange, um zersetzt zu werden. Daher besteht für sie eine höhere Wahrscheinlichkeit, fossil überliefert zu werden, als für die Weichteile. Fossile Knochen sind daher ein wichtiges „Archiv des Lebens“. Was der Mensch heute über die Evolution der Wirbeltiere und damit auch über seine eigene Entwicklungsgeschichte weiß, verdankt er in erster Linie der vergleichsweise hohen fossilem Erhaltungsfähigkeit von Knochen und Zähnen. Auch die Ernährungsweise, Krankheiten und die Folgen kriegerischer Auseinandersetzungen werden in Knochen und Zähnen „archiviert“. In seltenen Fällen konnten in fossilen Knochen noch Reste von Erbsubstanz nachgewiesen werden. Ein eindrucksvolles Beispiel für die Archiv-Funktion von Knochen kann im Dinosaur National Monument in den USA besichtigt werden.
Hydroxylapatit und andere Apatite entstehen auch bei bestimmten biochemischen Bedingungen im Boden (ganze Lagerstätten sind so entstanden) und sind mineralogisch und morphologisch oft von Knochen-Hydroxylapatit nicht zu unterscheiden. Entscheidend ist das durch Tonpartikel, Bakterien (zu etwa 5 % P-haltig) und anderen Mikrowesen (durch Algen erzeugte Monosaccharide zur explosionsartigen Vermehrung der Bakterien) erzeugte Mikroenvironement und die sich ergebenden chemischen Lösungen (siehe Schmittner und Giresse). Das Konzentrationsverhältnis von Ca zu P in der Mikro-Lösung entscheidet über das Entstehen von Hydroxylapatit oder Calcit. 10 Mikrometer große platte Hydroxylapatitkristalle lassen sich so innerhalb von 3 bis 5 Tagen mittels hohen gleichen P- und Ca-Konzentrationen erzeugen. Zur weiteren einfachen Veranschaulichung: eine doppelte Konzentration von Ca zu P ergibt Calcit. Zudem, unsere täglichen Ablagerungen auf den Zähnen bestehen bis zu 60 % aus Hydroxylapatit (entsteht unter Gegenwart von Sauerstoff) und teils auch Calcit (hier aber kein Sauerstoff in der „Mikrowelt“, da von sauerstoffverbrauchenden Bakterien aufgebraucht), besonders nach dem Genuss von süßen Speisen; diese Ablagerungen sind aber nicht erwünscht, da sie mit einer Unzahl von Bakterien versehen sind und Bakterien, wie bekannt, Säuren produzieren, die wiederum den Zahnschmelz angreifen und eine „Mikro- bis Millimeter große Krater-Landschaft“ auf der Zahnoberfläche hinterlassen.
Mit anderen Worten, die rein chemischen Voraussetzungen zur Entstehung von Hydroxylapatit in den Knochen unterscheiden sich nicht von denen, die bei der Entstehung von Hydroxylapatit als Ablagerung auf den Zähnen gegeben sind, oder denen, die die Entstehung von Hydroxylapatit in Gesteinen begünstigen.
Fluorapatit
Zahnschmelz besteht primär aus Hydroxylapatit. Die Härte des Zahnschmelzes ist in erster Linie darauf zurückzuführen, dass er ganz überwiegend (zu ca. 95 Prozent) aus anorganischem Material besteht. Mit fluoridhaltigen Präparaten (Medikamenten, Zahnpflegemittel) gelingt es, im Hydroxylapatit OH-Gruppen teilweise durch Fluorid-Ionen zu ersetzen und so den Hydroxylapatit partiell in Fluorapatit umzuwandeln. Dieser ist widerstandsfähiger gegenüber Säuren und besitzt daher eine bessere Schutzfunktion gegen Karies.
Aktuelle Forschungsarbeiten
Biomineralisation
Das seit Mitte des Jahres 2003 laufende Schwerpunktprogramm der Deutschen Forschungsgemeinschaft (DFG) „Principles of Biomineralisation“ befasst sich unter Federführung der Universität Hannover mit grundlegenden Fragestellungen zum Thema „biologische Verbundwerkstoffe“ mit den anorganischen Komponenten Calciumcarbonat, Siliziumdioxid und Apatit. Das Max-Planck-Institut für Metallforschung in Stuttgart bearbeitet einen Schwerpunkt „Bioinspirierte Synthese keramischer Materialien“. Die Architektur des Knochenaufbaus kann mit fossilem Material bis zu den Dinosauriern zurückverfolgt werden, ein Thema, das bei GKSS, Geesthacht, mit modernster instrumenteller Ausrüstung bearbeitet wird. Forschungen mit überwiegend medizinischer Zielsetzung werden seit rund 15 Jahren in Dresden durchgeführt.
Aus den weltweiten Aktivitäten zum Thema „Biomineralisation“ können nur einige Themen schlaglichtartig herausgegriffen werden:
DNA eignet sich hervorragend als Konstruktionsmaterial im Nanometermaßstab. Möglich wird dies dadurch, dass DNA-Sequenzen so programmiert werden können, dass sie sehr spezifisch an andere Moleküle koppeln, die wiederum mit anorganischen Partikeln in Wechselwirkung treten. Da unterschiedliche DNA-Sequenzen so konstruiert werden können, dass sie sich aneinander anlagern, ergeben sich nahezu unbegrenzte Kombinationsmöglichkeiten.
Eine Forschergruppe an der New York University synthetisiert mit Hilfe gentechnisch veränderten Bakterien der Gattung Escherichia coli ein Peptid, das in der Lage ist, aus einer Lösung von Gold(III)-chlorid Goldpartikel auszufällen und sich an die Goldoberfläche zu heften. Als aktive Stellen des Peptids vermutet man die Aminosäuresequenz Glutamin/Alanin/Threonin. Dieses einfache System dient bisher ausschließlich der Grundlagenforschung.
Am Massachusetts Institute of Technology (MIT) in Cambridge, Massachusetts, züchtet man Bakteriophagen (M13-Viren), die sich in der Lösung eines Kobaltsalzes mit metallischem Cobalt überziehen. Als das Kobalt oxidiert wurde, erhielten die Wissenschaftler Drähte aus Kobaltoxid mit einer Dicke von 6 Nanometer und einer Länge von 900 Nanometer. In einem orientierenden Test konnten sie nachweisen, dass sich dieses Material als Komponente eines Lithiumionen-Akkus eignet.
Ein weiterer Forschungsschwerpunkt ist das folgende Problem: Das CO2, das bei der Verbrennung fossiler Energieträger entsteht und zur globalen Erwärmung beiträgt, wird etwa zur Hälfte von den Ozeanen absorbiert. Dadurch drohen die Ozeane zu versauern, mit der Folge, dass die Bildung kalkhaltiger Strukturen bei der Biomineralisation erschwert wird.
Biomimetische Kristallisation
In den Materialwissenschaften spielt die Biomineralisation – im Labor des Chemikers als „biomimetische Mineralisation“ bezeichnet – eine zunehmende Rolle. Intensiv wird untersucht, nach welchen Gesetzen die Selbstorganisation abläuft, die dazu führt, dass aus den Ausgangssubstanzen Verbundmaterialien aus organischen und anorganischen Komponenten entstehen. Peptide spielen dabei eine Schlüsselrolle.
Auch zur Erzeugung rein anorganischer Kristalle eignen sich bestimmte Peptide. So hat man beispielsweise ein Peptid gefunden, das die Bildung von Powellit (ein Calciummolybdat mit der Formel CaMoO4) in wässriger Lösung ermöglicht. Die technische Herstellung dieses Minerals, das z. B. als Leuchtstoff in LEDs eingesetzt wird, erfordert Temperaturen von 500 bis 1000 °C.
Literatur
- M. Groß: Molekulare Erkennung zwischen Biomolekülen und Kristallen. Spektrum der Wissenschaft, Februar 1995, 25–26
- M. Groß: Das Geheimnis der Nano-Kiesel. Spektrum der Wissenschaft, Januar 2000, 24–26
- M. Groß: Materials at the Interface of biology and chemistry. Nachrichten aus der Chemie 53, November 2005, 1135–1138
- NN: Saurierknochen: Vorbild für neue Strukturwerkstoffe. GKSS-Forschungszentrum Geesthacht GmbH, Jahresbericht 2003/2004, 33–35
- S. C. Doney: Das Meer wird sauer, Spektrum der Wissenschaft, Juni 2006, S. 62–69
- K.-E. Schmittner, P. Giresse, 1999. Micro-environmental controls on biomineralization: superficial processes of apatite and calcite precipitation in Quaternary soils, Roussillon, France. Sedimentology 46/3: 463–476.
- H. Cölfen: Biomineralisation aus dem Reagenzglas, Nachrichten aus der Chemie 56 (Januar 2008), 23–28
- Biomineralization. From Biology to Biotechnology and Medical Application (Wiley-Vch), Edmund Baeuerlein (Ed.), 2001, Wiley & Sons. ISBN 3-527-29987-4
- Handbook of Biomineralization. 3 vols, Edmund Baeuerlein (Ed.), Peter Behrens (Ed.), Matthias Epple (Ed.), 2007, Wiley & Sons, ISBN 3-527-31641-8
- G. C. Schwartze: Mikrobereichsanalytik an marinen Biomineralisationsprodukten: Copepoden des Südpolarmeeres und der Nordsee. Grin Verlag, München, 2011, ISBN 978-3-640-85438-7
Weblinks
- DFG-Schwerpunktprogramm „Principles of Biomineralisation“
- Forschungsgemeinschaft Knochen und Biomineralisation e.V
- Knochen als Archiv des Lebens
- Biomineralisation: die Tricks der Kalk-Produzenten
- Diatomeen
- Projekt „Biologische photonische Kristalle“
- Mikrobenscout – Pyritisierte Fossilien (Memento vom 5. Oktober 2010 im Internet Archive)
- Biomineralization