Schweflige Säure
Die schweflige Säure ist eine unbeständige, nur in wässriger Lösung existierende, zweiprotonige Säure, die beim Lösen von Schwefeldioxid in Wasser entsteht; ihre Salze und Ester heißen Sulfite und Hydrogensulfite.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
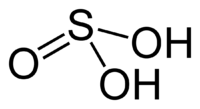 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Schweflige Säure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | H2SO3 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit stechendem Geruch nach Schwefeldioxid[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 82,02 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| pKS-Wert | |||||||||||||||||||
| Löslichkeit |
vollständig mischbar mit Wasser, nur in Lösung beständig[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Eigenschaften
Chemische Eigenschaften
In wässriger Lösung liegt ein Gleichgewicht zwischen Schwefeldioxid und der schwefligen Säure vor:
Das Gleichgewicht der Reaktion liegt weit auf der linken Seite.[2]
Versucht man die Lösung einzudampfen, um wasserfreie schweflige Säure zu erhalten, so zerfällt diese in Umkehrung der Bildungsreaktion. Beim Abkühlen kristallisiert ein Clathrat SO2 · 5,75 H2O aus, das sich bei 7 °C wieder zersetzt. Freie schweflige Säure H2SO3 ist daher nicht isolierbar.
Die Protolyse der schwefligen Säure verläuft in zwei Stufen. In der ersten Stufe bildet sich Hydrogensulfit:
Die Säurekonstante KS1 wird (analog zur Kohlensäure) formal aus der Summe der Konzentrationen des gelösten Schwefeldioxids und der schwefligen Säure bestimmt:
- mit
Die tatsächliche Säurestärke liegt jedoch wesentlich höher, da in wässrigen Lösungen so gut wie keine H2SO3-Moleküle vorliegen.[3] Für die zweite Stufe der Protolyse (KS2) gilt:
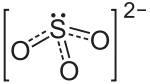
Versetzt man schweflige Säure mit Basen, Metalloxiden oder Carbonaten, so kristallisieren mit dem Eindampfen der Lösungen die Salze der schwefligen Säure, die Sulfite, aus.
Die Hydrogensulfite lassen sich nur mit großen Kationen auskristallisieren, ansonsten entstehen Disulfite. Im Feststoff liegt das Hydrogensulfit-Anion in der Konstitution eines Sulfonats vor, der restliche Wasserstoff ist an den Schwefel gebunden.[2]
Tautomerie
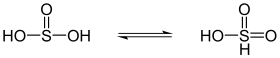
Schweflige Säure bildet in Wasser zwei einwertige tautomere Anionen, das Hydrogensulfit- und das Sulfonat-Ion mit den Strukturen HSO3− und SHO3−, die sich als Deprotonierungsprodukte von der schwefligen Säure bzw. der Sulfonsäure ableiten lassen.
Biologische Bedeutung
Schweflige Säure ist auch Mitverursacher des sauren Regens, da das bei der Verbrennung fossiler Brennstoffe (beispielsweise Kohle, Erdöl, Erdölprodukte) oder Biomasse gebildete Schwefeldioxid vom Regenwasser aus der Erdatmosphäre „ausgewaschen“ wird (siehe auch: Smog). Um zu verhindern, dass Schwefeldioxid in die Umwelt entweicht, gibt es verschiedene Verfahren zur Rauchgasentschwefelung.
Verwendung
Schweflige Säure und ihre Salze sind Reduktionsmittel, da sie durch Aufnahme eines weiteren Sauerstoffatoms zu Schwefelsäure beziehungsweise Sulfat oxidiert werden. In wässriger Lösung wird schweflige Säure durch Luftsauerstoff zu Schwefelsäure oxidiert.[4]
Weblinks
Einzelnachweise
- Eintrag zu Schweflige Säure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2018. (JavaScript erforderlich)
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 101. Auflage. Walter de Gruyter, Berlin 1995, ISBN 3-11-012641-9.
- Arnold Willmes, Taschenbuch Chemische Substanzen, Harri Deutsch, Frankfurt (M.), 2007, S. 775.
- L. Kolditz, Anorganische Chemie, VEB Deutscher Verlag der Wissenschaften, Berlin 1983, S. 476.

