Phosphoroxychlorid
Phosphoroxychlorid ist eine giftige, an der Luft stark rauchende Flüssigkeit, die formal das Trichlorid der Phosphorsäure darstellt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
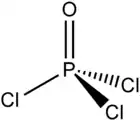 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Phosphoroxychlorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | POCl3 | |||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche viskose Flüssigkeit mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 153,33 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,68 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
105,8 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
heftige Zersetzung mit Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Im Labormaßstab
Im Labormaßstab kann Phosphoroxychlorid durch Einleiten von Schwefeldioxid in Phosphorpentachlorid hergestellt werden.
Das schwach gelbliche Rohprodukt der Umsetzung – eine Mischung aus POCl3 und Thionylchlorid (SOCl2) – wird durch fraktionierte Destillation getrennt.
Weitere Darstellungsmöglichkeiten sind:
- die Umsetzung von Oxalsäure mit Phosphorpentachlorid
- die Oxidation von Phosphortrichlorid mit Kaliumchlorat
- sowie die Umsetzung von Phosphorpentachlorid mit Phosphorpentoxid
- .
Industrielle Verfahren
Die industrielle Herstellung von Phosphoroxychlorid erfolgt auf unterschiedlichen Wegen. Da Phosphoroxychlorid als wichtiger anorganischer Grundstoff in zahlreichen kostenkritischen Herstellungsprozessen eingesetzt wird, spielen bei der Verfahrensauswahl die Produktionskosten eine entscheidende Rolle. Das Augenmerk liegt auf technisch ausgereiften Prozessen, die das Endprodukt in angemessen hoher Qualität bereitstellen und wenig Abfall erzeugen. Bevorzugt sind besonders Verfahren, die den Einsatz kostengünstiger Rohstoffe erlauben bzw. die Nebenprodukte anderer Herstellungsprozesse weiterverwerten können.
Ein Beispiel für diese Strategie ist die Herstellung von Phosphoroxychlorid aus Schwefeldioxid (SO2), das in vielen Prozessen als Abgas anfällt, gasförmigem Chlor (Cl2) und Phosphortrichlorid (PCl3):
Optimale Ergebnisse werden bei kontinuierlicher Prozessführung im kontinuierlichen Rührkesselreaktor oder Schlaufenreaktor (Loop-Reaktor) erzielt.[5]
Auch aus den phosphinhaltigen Abgasen der Hypophosphit-Produktion kann Phosphoroxychlorid gewonnen werden:
Bei dem Verfahren entsteht zunächst Phosphortrichlorid (PCl3), das anschließend mit Sauerstoff zum Endprodukt aufoxidiert wird.[6]
Bei der Herstellung bestimmter heterocyclischer Verbindungen – wichtige Zwischenprodukte u. a. in der Pflanzenschutzmittelproduktion – fällt Phosphoroxychlorid als Nebenprodukt an. Durch Abtrennen des weiterverwertbaren Oxychlorids lassen sich die Produktionskosten der Heterocyclensynthese deutlich senken.[7][8]
Ein besonders reines Phosphoroxychlorid liefert die direkte Oxidation von Phosphortrichlorid (PCl3) mit Sauerstoff (O2) in der Flüssigphase.[9] Das Verfahren wird besonders dann eingesetzt, wenn auch die Herstellung von Phosphortrichlorid, einer weiteren wichtigen Basischemikalie der chemischen Industrie, angestrebt wird.
Für dieses Verfahren gibt es auch eine kontinuierliche Variante.[10] Die Reaktion verläuft mit einer molaren Reaktionswärme von −279,5 kJ·mol−1 stark exotherm.[9]
In der feinchemischen Industrie wird die Phosphortrichlorid-Oxidation meist diskontinuierlich im Rührkesselreaktor durchgeführt. Nachteilig sind bei dieser Prozessführungsvariante aber die ungünstige Volumenausbeute der Reaktion und die relative aufwendige Abtrennung des Oxychlorids vom Startmaterial. Aus der Produktspezifikation, lässt sich oft der Aufwand, der bei der Endproduktabtrennung betrieben wurde und auch die Güte der Produktionsanlage ablesen.
Es gibt ein Verfahren, das den vorstehend beschriebenen Problemen Rechnung trägt.[11] Anstelle von Phosphortrichlorid kommt weißer Phosphor also Ausgangsmaterial der Reaktion zum Einsatz. Der Phosphor wird zunächst mit Sauerstoff oxidiert und das Phosphoroxid anschließend mit elementarem Chlor chloriert. Die Umsetzung wird in der Flüssigphase durchgeführt. Als Reaktionsmedium und Lösungsmittel dient – auch dies ein interessantes Merkmal des Herstellungsprozesses – das ungereinigte Oxychlorid.
Auch durch direktes Verbrennen von Phosphor in einer Sauerstoff-Chlor-Flamme lässt sich Phosphorylchlorid erzeugen.[12] Der Prozess liefert jedoch ein sehr komplexes Produktgemisch und ist technisch nur äußerst schwer zu beherrschen.
Eine Weiterentwicklung der oben von der Knappsack-Griesheim AG beschriebenen Methodik[11] wird in dem 1994 publizierten japanischen Patent der Nippon Sōda vorgestellt.[13] Der japanische Prozess zeichnet sich besonders durch eine verbesserte Prozesskontrolle aus, die eine genaue Steuerung der Chlorierung erlaubt.
In der älteren Patentliteratur werden zahlreiche weitere Verfahren zur Phoshoroxychloridherstellung beschrieben, die jedoch heute nicht mehr eingesetzt werden.
Eigenschaften
Physikalische Eigenschaften
POCl3 schmilzt bei 1,25 °C und ist bei Raumtemperatur eine farblos-klare, sehr giftige, hydrolyseempfindliche und an der Luft stark rauchende, lichtbrechende Flüssigkeit, die bei 105,8 °C siedet. Flüssiges Phosphoroxychlorid hat bei 25 °C eine Dichte von 1,645 g/cm3. Im Gaszustand beläuft sich die Dichte auf 5,3 (Luft=1). Der Dampfdruck über flüssigem Phosphoroxychlorid beträgt bei 20 °C bzw. 50 °C 37 hPa bzw. 139 hPa. Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 4,28166, B = 1445,959 und C = −40.119 im Temperaturbereich von 275 bis 378,3 K.[14] Die spezifische Leitfähigkeit des flüssigem Oxychlorids beträgt 2·10−8 Ohm−1·cm−1 und beruht auf der geringen Eigendissoziation des Oxychlorids in POCl2+, und POCl4 −. In der Praxis trägt zur Leitfähigkeit die selbst in extrem gereinigtem POCl3 stets vorhandene Restfeuchte von 0,0001 mol/l bei, die zur Bildung H3O+Cl− führt.
Flüssiges Phosphoroxychlorid ist ein sehr gutes nicht-wässriges Lösungsmittel, in dem sich Metallchloride – mit Ausnahme der Alkalichloride – unter Bildung gut leitender Lösungen lösen. Über eine Leitfähigkeitsmessung lassen sich somit in reinem Phosphoroxychlorid Verunreinigungen sehr bequem als Summenparameter nachweisen.
Mit Übergangsmetallen wird Komplexbildung beobachtet.
Materialverträglichkeit
Phosphoroxychlorid ist u. a. aufgrund seines Chloridgehalts äußerst korrosiv und materialangreifend. Unter den Edelstählen werden austenitischer Chromnickelstahl bzw. die Edelstahlqualitäten 18-8 und 17-12-3 von Phosphoroxychlorid nur mäßig schnell angegriffen. Die genannten Materialien eignen sich daher für den Bau von Lagerbehältern und Tanks, die der zeitlich begrenzten Zwischenlagerung von Phosphoroxychlorid oder dessen Transport dienen. Eine höhere Widerstandsfähigkeit haben Blei, Nickel und Monel. Aufgrund der Korrosionsgefahr wird für den Leitungsbau und für den Bau von Reaktoren und Langzeitlagerbehältern für Phosphoroxychlorid bevorzugt Glas oder glasarmierter Edelstahl und u. U. kunststoffbeschichteter Edelstahl eingesetzt. Die ausschließliche Verwendung von Kunststoff ist wegen der Feuchte- und Gasdurchlässigkeit praktisch aller Kunststoffe und dem Risiko einer Verunreinigung des Produkts durch Kunststoffbegleitstoffe problematisch. Unter den Kunststoffen sind bei Temperaturen bis ca. 30 °C die folgenden Kunststoffarten begrenzt mit Phosphoroxychlorid kompatibel:
- Hochdichtes Polyethylen (HDPE)
- Polypropylen (PP)
- Polyvinylidenfluorid (PVDF)
- Ethylen-Tetrafluorethylen-Copolymer (ETFE)
Bei höheren Einsatztemperaturen ist ausschließlich ETFE zu empfehlen.
Bei fluorkunststoffbeschichteten Behältern ist zu beachten, dass die Beschichtung aus gesintertem bzw. verschmolzenem Polymerpulver besteht, nicht zwingend porenfrei ist und Bindemittel enthalten kann.
Generell sollte man berücksichtigen, dass Kunststoffe technische Produkte mit nicht einheitlicher Zusammensetzung sind. Auch Kunststoffe mit gleicher Kurzbezeichnung unterscheiden sich oft erheblich in ihren Eigenschaften voneinander. Weiterhin werden manche Kurzbezeichnungen als Handelsnamen verwendet und bezeichnen eine ganze Produktgruppe. In diesem Sinne werden z. B. häufig Bezeichnungen wie Teflon und PTFE verwendet. Bei Fehlen zuverlässiger Materialverträglichkeitsdaten sollte man auf die Verwendung eines bestimmten Werkstoffs verzichten bzw. eine gezielte Gebrauchsprüfung vornehmen. Rückschlüsse aus dem Verhalten des Werkstoffs unter subjektiv ähnlichen erscheinenden Einsatzbedingungen zu ziehen, ist sicherheitstechnisch äußerst riskant.
Chemische Eigenschaften
Phosphoroxychlorid reagiert heftig mit Wasser, Metall, Basen, Aceton (vermutl. allen Ketonen), Alkoholen, Aminen, Phenolen, stark oxidierenden und organischen Substanzen.
Lösungsmittel, die für Reaktionen mit Phosphoroxychlorid verwendet werden sollen, müssen daher wasserfrei sein. Trockene Lösungsmittel lassen sich durch Trocknen z. B. über Molekularsieben leicht und bequem herstellen. Stärker wasserhaltige Lösungsmittel sollten vorher mit Natriumsulfat vorgetrocknet werden. Bei Kontakt mit den Lösungsmitteln Dimethylformamid oder Dimethylsulfoxid kann eine explosionsartige Reaktion erfolgen.[1]
Verwendung
Phosphoroxychlorid ist wichtiger Grundstoff zur Herstellung von Phosphorsäureester (Alkyl- und Aryl-Phosphiten). Die Synthese erfolgt durch Reaktion von Phosphoroxychlorid mit Alkoholen, Phenolen oder Epoxiden und liefert wirtschaftlich bedeutsame Produkte wie
- Weichmacher für PVC und andere Kunststoffe
- Flammschutzmittel
- Kraftstoffadditive
- Hydrauliköle und Hydrauliköladditive
- Extraktionsmittel für die Uranaufbereitung und Metallgewinnung
- Insektizide
Der Verwendung von Phosphoroxychlorid zur Herstellung phosphororganischer Insektizide ist dessen Einsatz in der Produktion der zur gleichen Substanzfamilie gehörenden phosphororganischen Nervengase eng verwandt.
Phosphoroxychlorid wird weiterhin als
- Chlorierungsmittel zur Herstellung von Carbonsäurechloriden und Säureanhydriden
- Katalysator bei der Herstellung von Triphenylmethanfarbstoffen
- Reagenz zur Bildung des Vilsmeier-Haack-Komplexes
- nicht-wässriges Lösungsmittel
sowie als
- Hilfsstoff in der Herstellung optischer Glasfasern
- n-Dotierungsmittel in der Halbleiter- und Solarzellenproduktion
eingesetzt.
Produktionsmengen und Hersteller
Phosphoroxychlorid zählt zu den unverzichtbaren anorganischen Grundchemikalien der chemischen Industrie. Die weltweite Jahresproduktion belief sich 2002 auf geschätzte 200.000 t. Etwa 150.000 Tonnen/Jahr der Produktionskapazität befinden sich in den OECD-Ländern und 50 000 Tonnen/Jahr in Drittländern. 1995 betrugen die Produktionskapazitäten etwa 39.900 Tonnen in den USA, 100.000 Tonnen in Westeuropa und 30.000 Tonnen in Japan. In Westeuropa gab es 2004 vier Hersteller von Phosphoryltrichlorid. Drei von ihnen hatten Produktionsstätten in Deutschland.[15] Produktionsschwerpunkte sind Europa, die USA und Japan. Wichtige Erzeugerländer sind außerdem China, Indien und Australien. Typische Produktionsanlagen haben Jahresproduktionskapazitäten im Bereich von 5.000 bis 10.000 Tonnen.
Ein Großteil des Phosphoroxychlorids wird unmittelbar zu Folgeprodukten weiterverarbeitet. Die Phosphoroxychlorid-Produktion ist daher oft mit der Herstellung wichtiger Folgeprodukte, z. B. mit der Herstellung von Kunststoffadditiven, Flammschutzmitteln, Pestiziden, Schmierstoffen und sogenannten funktionalen Flüssigkeiten, vernetzt.
Wichtige Phosphoroxychloridhersteller sind die Firmen Lanxess (D), BASF, Akzo Nobel, Monsanto, Rhodia, Syngenta, Taixing Shenlong Chemical, Fu Tong Chemical, Jiangsu Jibao Technology, Wynca, Xuzhou JianPing Chemical und andere.[16]
Qualität und Lieferform
Das Phosphoroxychlorid, das nach einem der oben beschriebenen Syntheseverfahren hergestellt wird, fällt zunächst als mehr oder weniger stark verunreinigtes Rohprodukt an. Das Verunreinigungsprofil des Rohprodukts wird von der Herstellungsmethode, vom Verunreinigungsprofil der Ausgangsmaterialien und nicht zuletzt vom Zustand der Produktionsanlage bestimmt. Moderne Produktionsanlagen liefern durchgängig ein bereits sehr hochwertiges und reines Rohprodukt. Die weitere Aufreinigung des Rohprodukts erfolgt durch fraktionierte Destillation die ggf. durch eine Festphasenabsorption ergänzt wird. In der Destillation werden flüssige und gasförmige Reaktionsnebenprodukte sowie Rohmaterialienrestanteile – z. B. Phosphortrichlorid (PCl3) – abgetrennt. Der Aufwand, der bei der Rohproduktaufreinigung betrieben wird, unterliegt naturgemäß einer strengen Wirtschaftlichkeitskontrolle.
Weitere Faktoren, die die Produktreinheit entscheidend beeinflussen, sind die Handhabung des Produkts nach der Aufreinigung, die Produktverpackung, die Lagerung des Produkts am Herstellungsort und der Transport und die Lagerung und Handhabung des Oxychlorids beim Zwischenhandel und Endverbraucher.
Ein Großteil des industriell erzeugten Phosphoroxychlorids wird unmittelbar nach der Herstellung in Folgeprozessen verbraucht. In den Handel gelangt Phosphoroxychlorid mit spezifizierten Reinheiten von 98–99,9999 %. Für Phosphoroxychlorid, das modernen Großproduktionsanlagen entstammt, sind Basisproduktreinheiten >99,9 % typisch. Als Hauptverunreinigung wird meist Phosphortrichlorid (PCl3) genannt. Das für einige Anwendungen wichtige Metallverunreinigungsniveau liegt bei produktionsfrischem Phosphoroxychlorid meist sehr niedrig, da Übergangsmetalle bereits in Spurenkonzentrationen den POCl3-Herstellungsprozess inhibieren und daher von vornherein sorgfältig vermieden werden. Die in der Produktspezifikation genannte Gesamtreinheit bezieht sich, wie bei Chemieprodukten üblich, meist auf die Gesamtmenge der in der Produktanalyse erfassten Verunreinigungen. Weiterhin spielen beim Aufstellen von Produktspezifikationen vermarktungstechnische Gesichtspunkte eine wichtige Rolle. So ist es z. B. üblich, Produkte hoher Reinheit unterschiedlichen Zielmärkten mit jeweils angepasster Spezifikation anzubieten.
Ein Großteil des handelsüblichen Phosphoroxychlorids besitzt eine spezifizierte Mindestreinheit von >98,5 % bis >99,9 % und gelangt auf direktem Weg oder über den Chemiezwischenhandel zum Endverbraucher. Die Packungsgröße ist vom Verwendungszweck abhängig. Kleinmengen werden vom Laborhandel in Kunststoffflaschen mit bis zu 0,6 kg Inhalt angeboten. Größere Produktmengen werden in Kunststoffkanistern mit 50 kg Inhalt oder in Fässern aus Kunststoff oder kunststoffbeschichtetem Stahl mit bis zu 300 kg Fassungsvermögen an den Käufer geliefert. Für noch größere Produktmengen kommen Tank- und Kesselwagen zu Einsatz.
Für spezielle Anwendungen, z. B. für die Produktion von Glasfaser, Halbleitern oder Solarzellen, wird Phosphoroxychlorid mit einer Gesamtreinheit >99,999 % angeboten. Das sogenannte hochreine und höchstreine Phosphoroxychlorid ist meist mit dem Standardprodukt ausgewählter Großhersteller identisch. Da die Analyse von Phosphoroxychlorid außerordentlich fehleranfällig ist, wird meist auf Batchanalyse der Originalhersteller zurückgegriffen.
Mit dem von der Mykrolis Corporation beschriebenen Festphasenabsorptionsverfahren lässt sich hochreines Phosphoroxychlorid in eleganter Weise quasi am ‚Point-of-use‘ erzeugen.[18] Besonders vorteilhaft ist hier, dass zumindest ein Teil der während der Lagerung in das Produkt gelangten Verunreinigungen erfasst und beseitigt wird.
Die Belieferung der Endabnehmer von hochreinem Phosphoroxychlorid erfolgt über den Laborfachhandel bzw. über spezialisierte Zwischenhändler. Als Verpackung eignen sich ausschließlich Glasampullen, Glasflaschen oder glasarmierte Edelstahlbehälter. Kunststoffbehälter und kunststoffbeschichtete Behälter sind nicht geeignet (siehe unten).
Handelsbeschränkungen
Phosphoroxychlorid kann zur Herstellung von Giftstoffen verwendet werden, die in Massenvernichtungswaffen eingesetzt werden können. Der Export von Phosphoroxychlorid unterliegt daher in allen Industrieländern einer strikten Kontrolle und Genehmigungspflicht.
Sicherheitshinweise
Mit feuchter Luft oder mit Wasser reagiert Phosphoroxychlorid unmittelbar und stark exotherm. Die Hydrolysereaktion führt zur Bildung stark ätzender, phosphor- und salzsäurehaltiger Nebel, die auch dampfförmiges Phosphoroxychlorid enthalten können. Einen gewissen Schutz vor Vergiftung und Verätzung ergibt sich beim Auslaufen oder Verschütten kleiner Phosphoroxychloridmengen aus der Tatsache, dass Phosphoroxychlorid wegen seines niedrigen Dampfdrucks nur langsam verdampft, die Dämpfe deutlich schwerer als Luft sind und verdampftes Phosphoroxychlorid an feuchter Luft sehr schnell hydrolysiert wird. Beim Verschütten oder Auslaufen in geschlossenen Räumen ist dagegen das sofortige Verlassen des Raums unumgänglich.
Siehe auch
Literatur
- A. D. F. Toy: Phosphorus Chemistry in Every Day Living. American Chemical Society, Washington 1976
- E. Fluck, K. Maas (Hersg): Themen zur Chemie des Phosphors. Dr. Alfred Hüttig Verlag GmbH, Heidelberg 1973
- Ullmann’s Encyclopedia of Technical Chemistry. 6. Auflage. Vol 26, S. 193, Phosphorous Compound, Inorganic, Verlag Wiley – VCH, Weinheim, 2002
Weblinks
- Sicherheitsdatenblatt (engl.)
Einzelnachweise
- Eintrag zu Phosphoryltrichlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- Eintrag zu Phosphoryl trichloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Phosphorylchlorid (PDF) bei Merck, abgerufen am 3. Februar 2017.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 10025-87-3 bzw. Phosphoroxychlorid), abgerufen am 2. November 2015.
- US-Patent US5498400, Great Lakes Chemical Corp.
- US-Patent US6685904, Occicdental Chemical Corp.
- Patent EP0900762, DSM Fine Chemicals Austria GmbH.
- DE19730224, Bayer AG.
- G. Bettermann, W. Krause, G. Ries, T. Hofmann: Phosphorus Compounds, Inorganic. In: Ullmanns Enzyklopädie der Technischen Chemie, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2012; doi:10.1002/14356007.a19_527.
- US-Patent US4183905, Mobil Oil Corp.
- Patentanmeldung DE1194382: Verfahren zur Herstellung von Phosphoroxy-chlorid und/oder hoeheren Phosphor-Chlor-Sauerstoffverbindungen der allgemeinen Formel POCl. Angemeldet am 12. Juli 1962, veröffentlicht am 10. Juni 1965, Anmelder: Knapsack-Griesheim AG, Erfinder: Mueller-Schiedmayer, Heinz Harnisch, Joseph Cremer.
- Patent DE801513: Verfahren zur Herstellung von Phosphoroxychlorid. Angemeldet am 2. Oktober 1948, veröffentlicht am 11. Januar 1951, Anmelder: BASF, Erfinder: Alfons Janson.
- JP6122509, Nippon Soda Corp.
- D. R. Stull: Vapor Pressure of Pure Substances Organic Compounds in Ind. Eng. Chem. 39 (1947) 517–540.
- OECD: Screening Information Dataset (SIDS) Initial Assessment Report (SIAR) für Phosphoryl trichloride, abgerufen am 23. September 2015.
- 360 Market Updates: Global Phosphorus Trichloride Industry Production Sales And Consumption Status And Prospects Professional Market Research Report 2017 2022 – 360 Market Updates, abgerufen am 12. Oktober 2017.
- Patent WO2005092790, Mykrolis Corporation.


