Antoine-Gleichung
Die Antoine-Gleichung beschreibt den funktionalen Zusammenhang zwischen der Temperatur und dem Sättigungsdampfdruck für reine Stoffe und ist von der Clausius-Clapeyron-Gleichung abgeleitet.
Die Gleichung
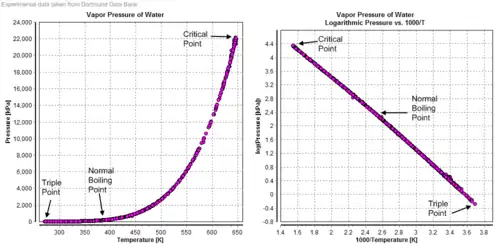
links: p vs. T, rechts: log(p) vs. 1/T
Die vereinfachte Form mit
heißt August-Gleichung nach dem deutschen Physiker Ernst Ferdinand August (1795–1870). Sie leitet sich direkt von der Clausius-Clapeyron-Beziehung ab und beschreibt eine rein lineare Beziehung zwischen dem Logarithmus des Drucks und dem Kehrwert der Temperatur. Der Faktor B (Steigung der Geraden) korrespondiert mit der Verdampfungsenthalpie.
Die Krümmung der Geraden wird durch die Antoine-Gleichung von Louis Charles Antoine (1825–1897) präzisiert.
Originalgleichung
Antoine verwendete die Form
Es zeigt sich, dass mit den Umrechnungen
die heutzutage verwendete Form der Originalgleichung entspricht.
Mit den von Antoine für Benzol gegebenen Werten Aorig = 1,1650, D = 5,8524 und C = 216 ergibt sich für 80 °C (entspricht dem Siedepunkt von Benzol) ein Dampfdruck von Benzol zu
und damit annähernd Atmosphärendruck.
Heute gebräuchliche Form
mit
- p: Druck, meist in mmHg gegeben
- T: Temperatur, in °C gegeben
- A, B, C empirische, stoffspezifische Parameter, wobei aus B einfach die molare Verdampfungsenthalpie abgeleitet werden kann.
Temperatur-explizite Form (Umkehrfunktion)
Die Antoine-Gleichung kann umgestellt werden, so dass die Temperatur als Funktion des Drucks berechnet werden kann:
Geltungsbereich
Die Antoine-Gleichung kann mit ihren drei Parametern nicht die gesamte Sättigungsdampfdruckkurve zwischen dem Tripelpunkt und dem kritischen Punkt korrekt beschreiben. Daher werden zumeist 2 Parametersätze für eine Komponente verwendet. In der Regel ist dabei ein Parametersatz unterhalb des Normalsiedepunkts gültig und ein zweiter für den Bereich vom Normalsiedepunkt bis zum kritischen Punkt. Da sich an der Übergangsstelle dann Inkonsistenzen ergeben, ist die Anwendung der Antoine-Gleichung heute nicht mehr zeitgemäß.
- Typische Abweichungen einer Parameteranpassung über den gesamten Bereich (experimentelle Daten für Benzol)
 Abweichung einer Anpassung der August-Gleichung (2 Parameter)
Abweichung einer Anpassung der August-Gleichung (2 Parameter) Abweichung einer Anpassung der Antoine-Gleichung (3 Parameter)
Abweichung einer Anpassung der Antoine-Gleichung (3 Parameter) Abweichung einer Anpassung der DIPPR 101-Gleichung (4 Parameter)
Abweichung einer Anpassung der DIPPR 101-Gleichung (4 Parameter)
Beispiele
| A | B | C | Tmin (°C) |
Tmax (°C) | |
|---|---|---|---|---|---|
| Wasser | 8,07131 | 1730,63 | 233,426 | 1 | 100 |
| Wasser (unter Druck, p>760 mmHg) | 8,14019 | 1810,94 | 244,485 | 99 | 374 |
| Ethanol | 8,20417 | 1642,89 | 230,300 | −57 | 80 |
| Ethanol (unter Druck, p>760 mmHg) | 7,68117 | 1332,04 | 199,200 | 77 | 243 |
[p] = mmHg
Beispielrechnung
Für Ethanol beträgt der Normalsiedepunkt TB=78,32 °C. Damit ergibt sich folgende Rechnung:
(760 mmHg = 101,325 kPa = 1,000 atm = Normaldruck)
Einheiten
Die Koeffizienten der Antoine-Gleichung werden üblicherweise in mmHg und °C gegeben – auch heute noch, wo das Einheitensystem SI bevorzugt wird und damit die Druckeinheit Pascal und die Temperatureinheit Kelvin. Der Gebrauch der Vor-SI-Einheiten hat ausschließlich historische Gründe und stammt direkt aus Antoines Originalveröffentlichung.
Es ist allerdings einfach, die Antoine-Parameter in andere Druck- und Temperatureinheiten zu konvertieren. Um von Grad Celsius nach Kelvin zu wechseln, werden 273,15 vom C-Parameter subtrahiert. Um von Millimeter-Quecksilber zu Pascal zu wechseln, genügt es, den dekadischen Logarithmus des Faktors zwischen den Einheiten zum A-Parameter hinzuzuaddieren:
(101325 Pa sind 760 mmHg)
Die Parameter in °C und mmHg für Ethanol
A B C 8,20417 1642,89 230,300
werden für K and Pa konvertiert zu
A B C 10,32907 1642,89 −42,85
Die erste Beispielrechnung bei TB = 351,47 K wird zu
Eine ähnliche einfache Transformation kann benutzt werden, wenn der dekadische gegen den natürlichen Logarithmus ausgetauscht werden soll. Es ist ausreichend, die Parameter A und B mit ln(10) = 2,302585 zu multiplizieren.
Die Beispielrechnung mit den konvertierten Parametern (für K and Pa)
A B C 23,7836 3782,89 −42,85
wird zu
(Die kleinen Differenzen in den Resultaten entstehen ausschließlich durch die benutzte begrenzte Genauigkeit der Koeffizienten.)
Erweiterungen der Gleichung
Um die Limitierungen der Antoine-Gleichung zu umgehen, gibt es einfache Erweiterungen um weitere Terme.
Die weiteren Parameter erhöhen die Flexibilität der Gleichungen und erlauben damit die Beschreibung der gesamten Dampfdruckkurve vom Tripelpunkt bis zum kritischen Punkt. Außerdem lassen sich die erweiterten Gleichungen auf die ursprüngliche Antoine-Gleichung durch Setzen der weiteren Parameter D, E und F auf 0 reduzieren.
Ein Unterschied zur Originalform ist außerdem, dass die erweiterten Gleichungen die e-Funktion und den natürlichen Logarithmus verwenden. Dies hat jedoch keinen Einfluss auf die Gleichungsform.
Quellen
- NIST Chemistry WebBook
- Dortmunder Datenbank
- Diverse Nachschlagewerke und Veröffentlichungen, bspw.
- Lange's Handbook of Chemistry. McGraw-Hill Professional
- Ivan Wichterle, Jan Linek: Antoine Vapor Pressure Constants of pure compounds. Academia, Prag 1971
- Carl L. Yaws, Haur-Chung Yang: To Estimate Vapor Pressure Easily. Antoine Coefficients Relate Vapor Pressure to Temperature for Almost 700 Major Organic Compounds. In: Hydrocarbon Processing. Bd. 68, Nr. 10, 1989, ISSN 0018-8190, S. 65–68.