Kalorimeter
Ein Kalorimeter (lat. calor ,Wärme‘, altgr. μέτρον ‚Maß‘) ist ein Messgerät (oder eine Apparatur) zur Bestimmung der Wärmemenge, die bei physikalischen, chemischen oder biologischen Prozessen freigesetzt oder aufgenommen wird. Mit Hilfe eines Kalorimeters kann zudem die spezifische Wärmekapazität eines Stoffes ermittelt werden. Man unterscheidet Kalorimeter nach Betriebsarten wie zum Beispiel adiabatisch oder isotherm, oder nach dem Messprinzip wie zum Beispiel Leistungskompensations- oder Wärmeleitungsprinzip. Das Messverfahren selbst bezeichnet man als Kalorimetrie.[1][2][3]
Kalorimeter für die Messung der bei einer chemischen Reaktion entstehenden Reaktionswärme werden als Reaktionskalorimeter bezeichnet.
Allgemein
Unterschieden werden:
- Wärmeflusskalorimeter,
- Wärmebilanzkalorimeter und
- adiabatische Kalorimeter
Wärmefluss- und Wärmebilanzkalorimeter werden meist isotherm gefahren, d. h. mit einem Regler wird die Innentemperatur konstant gehalten. Dann ist die abgeführte Wärmeleistung identisch mit der von der Probe erzeugten Leistung.
Im Wärmeflusskalorimeter wird die Wärme durch Wärmeleitung transportiert und die dazu nötige Temperaturdifferenz gemessen. Der Wärmewiderstand der Wand muss bekannt bzw. das Kalorimeter kalibriert sein. Kleine Wärmeströme leitet man vorteilhaft möglichst vollständig durch eine Thermosäule in der ansonsten gut isolierten Wand.
Im Wärmebilanzkalorimeter werden die Temperaturdifferenz zwischen Vor- und Rücklauf des Temperiermantels, sowie der Massenfluss des Temperiermediums gemessen und daraus die über die Wand transportierte Wärmeleistung berechnet.
Beim adiabatischen (genauer: anisothermen) Kalorimeter befindet sich die Probe in einem gedämmten Gefäß oder im Vakuum. Die durch die Reaktion erzeugte Wärmeenergie wird aus der gemessenen Temperaturerhöhung berechnet. Die Wärmekapazität der Probe muss bekannt sein. Bei der dynamischen Differenzkalorimetrie wird parallel einer gleichartigen, aber nicht reagierenden Probe durch Energiezufuhr der gleiche Temperaturverlauf aufgezwungen. Die elektrisch zugeführte Leistung ist leicht zu messen.
Anisotherme Kalorimeter
Das Kalorimeter ist gegenüber der Umgebung wärmegedämmt. Der Wärmeaustausch erfolgt mit einer Flüssigkeit (Flüssigkeitskalorimeter) oder mit einem Metall (Metallblockkalorimeter). Dieser Gerätetyp ist in der Kalorimetrie der häufigste. Bei sauberem Arbeiten sind mit ihm Genauigkeiten von bis zu 0,01 % möglich. Man wendet dieses Verfahren an, wenn der Wärmeaustausch maximal 20 min dauert.[4]
Flüssigkeitskalorimeter
Es besteht aus einem doppelwandigen Kupferbehälter, dessen Zwischenraum mit Wasser gefüllt ist und für eine temperaturkonstante Umgebung im inneren Kalorimeter sorgen soll. Das Kalorimetergefäß aus dünnem Blech wird auf einer wärmegedämmten Unterlage aufgestellt. Als Kalorimeterflüssigkeit dient gewöhnliches Wasser, doch können auch andere Flüssigkeiten verwendet werden. Durch ein Rührwerk, dessen Umdrehungszahl konstant bleiben muss, wird ein besserer Wärmeaustausch gewährleistet. Die Temperaturänderung wird mit einem Thermometer gemessen. siehe auch: Bombenkalorimeter zur Brennwertbestimmung.
Adiabatische Kalorimeter
Die Temperaturdifferenz zwischen der Kalorimeterflüssigkeit und dem Gefäßmantel wird bei diesen Geräten ständig durch Erwärmen oder Abkühlen ausgeglichen. Beide Vorgänge müssen mit der gleichen Geschwindigkeit ablaufen. Dies ist umso leichter zu erreichen, je langsamer die Wärmeabgabe an das Kalorimeter erfolgt (20 bis 60 Minuten).[5][6][7][8]
Isotherme Kalorimeter
Bei diesen Geräten wird die Wärmemenge von bestimmten Substanzen abgenommen, die dabei eine Phasenänderung erleiden. Die Temperaturen bleiben also während des Versuches konstant. Man bezeichnet diese Geräte auch als Phasenumwandlungskalorimeter. Sie werden bei langsam ablaufenden Reaktionen eingesetzt, die über mehrere Stunden dauern.
Eiskalorimeter
Für Messungen von Wärmemengen bei 0 °C gehört dieses Kalorimeter zu den genauesten. Mit der zu messenden Wärmemenge wird Eis zum Schmelzen gebracht. Da die Schmelzwärme des Wassers bekannt ist, kann aus der Menge des Schmelzwassers die Wärmemenge bestimmt werden.

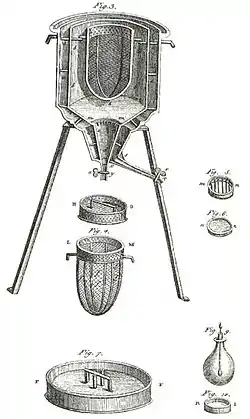
Ein klassisches Eiskalorimeter besteht aus einem trichterförmigen Innenbehälter, der von einem Außenbehälter umgeben ist. Zur Vorbereitung wird der Innenbehälter mit destilliertem Wasser, und der Außenbehälter mit einer Kältemischung befüllt, so dass sich auf der Innenwand des Innenbehälters eine Eisschicht bildet. Danach werden die Kältemischung und das restliche, nicht gefrorene Wasser abgelassen und das gesamte Kalorimeter auf die Schmelztemperatur des Wassers temperiert. Das Experimentiergut wird in den Innenbehälter eingebracht und das Kalorimeter mit einem Deckel verschlossen. Das sich bildende Schmelzwasser läuft aus einem Auslass des Innenbehälters zur Vermessung heraus.
Kondensationskalorimeter
Dieses Kalorimeter, häufig auch Dampfkalorimeter genannt, wird hauptsächlich zur Bestimmung der spezifischen Wärmekapazität eines Stoffes zwischen 100 °C und 20 °C verwendet. Dabei wird als kondensierendes Gas Wasserdampf benutzt. Der zu untersuchende Körper K wird mittels eines feinen Drahtes an einer empfindlichen Waage aufgehängt und befindet sich im Inneren des Kalorimeters. Leitet man plötzlich gesättigten Wasserdampf, der von tropfbarer Flüssigkeit befreit ist, in diesen Raum ein, so wird eine bestimmte Dampfmenge auf den anfangs kalten Körper kondensieren, bis der Körper die Temperatur des Dampfes angenommen hat. Dabei geht eine Wärmemenge von auf den Körper über (mit : Wärmemenge; : Kondensationswärme; Masse an kondensiertem Dampf).
Gegen Abtropfen von Wasser schützt ein unten am Körper befestigtes dünnwandiges Platinschälchen. Der Auftrieb, der wegen der Dampfströmung auftritt, muss berücksichtigt werden. Die Methode kann sehr genaue Werte liefern.
Wärmeaustauschkalorimeter
Bei Reaktionen, die sich über mehrere Stunden bis zu einigen Monaten erstrecken, sorgt man für einen schnellen und vollständigen Wärmeaustausch mit der Umgebung. Es wird dabei die Geschwindigkeit in Abhängigkeit von der Zeit gemessen.
Reaktionskalorimeter
Reaktionskalorimeter sind für Chemieanwendungen optimierte Kalorimeter. Sie werden in der chemischen Verfahrensentwicklung verwendet, um die bei einer Reaktion entstehende Wärme und den zeitlichen Verlauf der Leistung (Wärmestrom) zu messen. Die dabei gewonnenen wärmetechnischen Daten werden für die sicherheitstechnische Beurteilung des Prozesses und die Auslegung der Reaktor-Kühlsysteme benötigt. Besonders empfindliche kalorische Messungen können durch Chip-Kalorimeter realisiert werden, wobei der Wärmestrom vorzugsweise durch Serien von Thermoelementpaaren bestimmt wird. Mikrodurchfluss-Kalorimeter ermöglichen mit diesem Messprinzip auch rasche serielle Messungen.
Teilchenphysik
In der Teilchenphysik versteht man unter einem Kalorimeter ein Instrument zur Bestimmung der Energie eines einzelnen Teilchens, siehe Kalorimeter (Teilchenphysik).
Literatur
- Franz Xaver Eder: Thermische und kalorische Stoffeigenschaften. In: Arbeitsmethoden der Thermodynamik. Band 2. Springer Verlag, Berlin/Heidelberg 1983, ISBN 3-540-11727-X, 5.1 Kalorimetrische Messverfahren, S. 125–261, doi:10.1007/978-3-642-93226-7.
- Dieter Meschede: Gerthsen Physik. 24. Auflage. Springer, Heidelberg, Dordrecht, London, New York 2010, ISBN 978-3-642-12893-6, S. 260.
- S. M. Sarge: Kalorische Zustandsgrößen. In: Friedrich Kohlrausch (Hrsg.): Praktische Physik. Band 1. Teubner-Verlag, Stuttgart 1996, ISBN 3-519-23001-1, S. 411–493 (ptb.de [PDF; 6,9 MB; abgerufen am 10. Juni 2017]).
Weblinks
Belege
- Kalorimeter. In: Brockhaus-Enzyklopädie. Band 14. Leipzig ; Mannheim : Brockhaus, 2006, ISBN 3-7653-4114-2.
- Kalorimetrie. In: Jürgen Falbe, Manfred Regitz (Hrsg.): Römpp Lexikon Chemie. Band 3. Georg Thieme Verlag, Stuttgart 1997, ISBN 3-13-734810-2.
- S. M. Sarge: Kalorische Zustandsgrößen. In: Friedrich Kohlrausch (Hrsg.): Praktische Physik. Band 1. Teubner-Verlag, Stuttgart 1996, ISBN 3-519-23001-1, 3.3.2 Charakterisierung von Kalorimetern, S. 412–428 (ptb.de [PDF; 6,9 MB; abgerufen am 10. Juni 2017]).
- Erich Meister: Grundpraktikum der Physikalischen Chemie. vdf Hochschulverlag AG an der ETH Zürich, Zürich 2006, 9 Verbrennungswärme, Bombenkalorimeter, S. 156–171.
- Erich Meister: Grundpraktikum der Physikalischen Chemie. vdf Hochschulverlag AG an der ETH Zürich, Zürich 2006, 10 Kalorimetrie, Das Lösungsmittelkalorimeter, Thermometrische Titration, S. 173–187.
- Thermische Sicherheit. Adiabatische Kalorimetrie. TÜV SÜD in der Schweiz, abgerufen am 9. Juni 2017.
- Adiabatische Reaktionskalorimetrie. (pdf) Safety first! In: Fokus Analytik - Newsletter der Product Line Analytik. Evonik Technology & Infrastructure GmbH, März 2016, abgerufen am 9. Mai 2019 (Firmenmitteilung Beschreibung eines adiabatischen Kalorimeter und Beschreibung einer Anwendung).
- Phi-TEC II // Precise Stability & Reaction Safety Calorimetry. (pdf) In: Website der Firma. HEL Inc, 2019, abgerufen am 9. Mai 2019 (Produktdaten zu Phi-TEC II – ein PC-gesteuertes adiabatisches Kalorimeter).