Henry Cavendish
Henry Cavendish (* 10. Oktober 1731 in Nizza; † 24. Februar 1810 in London) war ein britischer Naturwissenschaftler. Seine bekanntesten Leistungen sind die Entdeckung des Elements Wasserstoff und die erste experimentelle Bestimmung der mittleren Dichte der Erde („Wiegen der Erde“), die in weiterer Folge die Bestimmung der Gravitationskonstanten ermöglichte.

Leben

Henry Cavendish war der Sohn von Lord Charles Cavendish (ein Sohn von William Cavendish, 2. Duke of Devonshire, 1704–1783), und Lady Anne Grey, Tochter von Henry Grey, 1. Duke of Kent. Die Familie Cavendish gehörte zum alteingesessenen Adel und war mit vielen anderen bedeutenden Adelsfamilien in Großbritannien eng verbunden. Henry wurde 1731 in Nizza geboren, wo sich – nach George Cavendish, 1. Earl of Burlington – seine Mutter aufgrund ihres schlechten Gesundheitszustandes aufhielt. Seine Mutter starb 1733 nach der Geburt seines Bruders Frederick (1733–1812).
Im Alter von elf Jahren war Cavendish ein Schüler der Newcome’s School in Hackney, einer der größten und anerkanntesten Privatschulen des 18. Jahrhunderts. Am 18. Dezember 1749 wurde er Student im Peterhouse College der University of Cambridge, das er am 23. Februar 1753 ohne Abschluss verließ. Seine erste wissenschaftliche Arbeit erschien im Jahre 1766 und trug den Titel Experiments on Factitious Airs („künstliche Luftarten“, d. h. durch chemische Reaktionen dargestellte Gase). Nach einer Reise mit seinem Bruder Frederick durch Europa lebte er zusammen mit seinem Vater bis zu dessen Tod 1783 in Soho (London). Während dieser Zeit führte er seine elektrischen und die meisten chemischen Forschungen durch. Er begann dabei als Assistent seines Vaters, der selbst wissenschaftliche Experimente durchführte. Mit 40 Jahren erbte Henry Cavendish ein großes Vermögen, das es ihm ermöglichte, seine wissenschaftlichen Studien weiterzuführen. Nach dem Tod seines Vaters zog er in eine Villa nach Clapham Common,[1] wo er ein großes Experimentierlabor einrichtete. Er besaß aber auch ein Stadthaus im Londoner Stadtteil Bloomsbury und ein weiteres Haus für seine Bibliothek in der Dean Street, Soho. Er besuchte die Zusammenkünfte der Royal Society, deren Fellow er 1760 wurde und mit deren Mitgliedern er donnerstags dinierte. Ansonsten mied er gesellschaftliche Ereignisse und sogar Lord George Cavendish, den er später zu seinem Haupterben machte, sah er nur einmal jährlich für wenige Minuten. Abgesehen davon änderte sich durch die Erbschaft kaum etwas an seinem bescheidenen Lebensstil.
Cavendish legte ein exzentrisches Verhalten an den Tag. Sein Abendessen bestellte er täglich durch eine Notiz, die er auf dem Flurtisch hinterlegte, und seine weiblichen Angestellten waren angewiesen, außer Sichtweite zu bleiben, wenn sie nicht ihre Entlassung riskieren wollten. Frauen und Fremden gegenüber war er äußerst schüchtern und er vermied es, mit ihnen überhaupt zu sprechen. Er war ein großgewachsener Mann mit einer schrillen, dünnen Stimme und trug als Kleidung einen abgetragenen, verblassten, violetten Samtanzug und einen Dreispitz aus dem vorherigen Jahrhundert. Er war ein wortkarger Einzelgänger.
Einer seiner wichtigsten Mitarbeiter war Charles Blagden, der an einer Vielzahl seiner Experimente beteiligt war. Auch existiert eine intensive Korrespondenz zwischen den beiden Wissenschaftlern.[2] 1790 lernte Cavendish auch Alexander von Humboldt kennen, der seine chemischen Erkenntnisse bald akzeptierte.[3] 1803 wurde er Mitglied der Académie des sciences in Paris.[4]
Cavendish führte unzählige wissenschaftliche Studien und Experimente durch, von denen allerdings die meisten zu seinen Lebzeiten unveröffentlicht blieben. Während seines ganzen Lebens hat er nur 20 Artikel und kein einziges Buch veröffentlicht. Erst lange nach seinem Tod, gegen Ende des 19. Jahrhunderts, beschäftigte sich James Clerk Maxwell mit den Forschungen Cavendishs und erkannte, dass viele wissenschaftliche Errungenschaften von ihm bereits vorweggenommen worden waren, so zum Beispiel das ohmsche Gesetz, das Dalton-Gesetz, das Gesetz von Gay-Lussac und die Prinzipien der elektrischen Leitfähigkeit. Er gab 1879 die Experimental Researches von Cavendish heraus.[5][6] Dabei gab er auch seine Verwunderung darüber kund, dass dieser ein ausführliches Manuskript über seine Forschungen anlegte und aufwändig in seinen Experimenten selbst Spezialfragen nachging, die damals nur er selbst zu würdigen wusste, er aber seine ausgearbeiteten Manuskripte nie veröffentlichte.
Cavendish starb am 24. Februar 1810 und wurde in der All Saints Church in Derby begraben (heute Derby Cathedral). Er hinterließ Lord George Cavendish ein bedeutendes Vermögen, dem Urenkel von William Cavendish, 2. Duke of Devonshire. Henry Cavendish war Enkel des Letzteren. Sein nachgelassenes Vermögen betrug £700.000 mit Einkünften aus Liegenschaften von £8000 pro Jahr sowie £50.000 bei seiner Bank. 1871 stiftete William Cavendish, 7. Duke of Devonshire und Prinzipal der University of Cambridge, das Geld zum Aufbau des Cavendish-Laboratorium genannten Physik-Fachbereichs der University of Cambridge.[7] Erster Direktor und erster Cavendish-Professor war James Clerk Maxwell.
Der Mondkrater Cavendish und der Asteroid (12727) Cavendish sind nach ihm benannt.
Werk
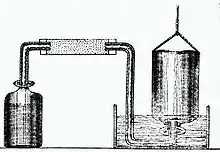
Entdeckung des Wasserstoffs und Verwerfung der Phlogistontheorie
1766 entdeckte Cavendish ein Gas, das durch Einwirken von Säure auf Metalle entstand, erkannte aber nicht, dass es sich um ein chemisches Element handelt. Er nannte das Gas inflammable air (brennbare Luft) und interpretierte das so, dass die brennbare Luft aus dem Metall entwichen war. Da sie sich in gleicher Weise bei verschiedenen Säuren bildete, identifizierte er sie mit der lang gesuchten hypothetischen Substanz Phlogiston, die beim Brennen aus den Körpern freigesetzt wird. Das testete er dadurch, dass er auch die Kalke, die bei der Verbrennung von Metallen übrigblieben und also kein Phlogiston mehr enthalten sollten, mit Säure behandelte. Dabei bildete sich keine entflammbare Luft. Joseph Priestley stellte außerdem 1782 fest, dass sich Metallkalke durch die brennbare Luft wieder in Metalle zurückverwandelten und die brennbare Luft dabei verschwand. Der nächste Schritt erfolgte, nachdem Cavendish 1781 Priestleys Knallgasversuche wiederholte, bei denen sich ein „Tau“ gebildet hatte. Er fand, dass der „Tau“ reines Wasser war. Somit war Wasser nicht elementar, sondern das langgesuchte zusammengesetzte Oxyd der entzündlichen Luft. Es besteht aus der von Cavendish entdeckten brennbaren Luft, die bald Wasserstoff genannt wurde, und dem 1774 von Priestley entdeckten Sauerstoff. Inzwischen hatte auch Lavoisier 1783 von den Experimenten von Cavendish erfahren, diese schnell aufgegriffen und teilweise vor Publikum so spektakulär vorgeführt, dass die Versuche von Cavendish dadurch überschattet wurden. Cavendishs Versuchsreihen zur Deutung der Synthese des Wassers zeigten, ebenso wie die Experimente von Lavoisier, welch große Bedeutung quantitative Messungen in der Chemie haben.[8][9]
Cavendish selbst blieb auch nach seinen Experimenten zur Synthese des Wassers bei der Phlogistonlehre, die er nur neu interpretierte.[10] Nach ihm war das, was Lavoisier für das Element Wasserstoff hielt, an Phlogiston gebundenes Wasser, während er Lavoisiers Sauerstoff für das Wasser hielt, dem Phlogiston entzogen wurde. Bei der Bildung von Wasser aus Wasserstoff und Sauerstoff wäre somit lediglich Phlogiston ausgetauscht worden.
Bestimmung der Gravitationskraft und der Masse der Erde
Cavendish gelang es 1797 als erstem, in einem Experiment mit zwei Körpern bekannter Masse ihre gegenseitige Anziehung zu beobachten.[11] Dieses Phänomen war ein Jahrhundert zuvor von Isaac Newton in seinem Gravitationsgesetz zur Erklärung der Planetenbewegung und des Gewichts der Körper auf der Erde postuliert worden. Mittels einer empfindlichen Drehwaage konnte Cavendish nach Abschirmung aller bekannten Störeinflüsse die Kraft nachweisen und vermessen, mit der sich der schwerere Probekörper mit der Masse m1 = 158 kg und der leichtere Probekörper mit der Masse m2 = 0,73 kg anziehen. Das Experiment bestimmte unter Annahme der Richtigkeit des von Newton postulierten Gravitationsgesetzes indirekt die Masse MErde der Erde und damit auch ihre mittlere Dichte. Das Experiment wurde daher populär als Wiegen der Erde bezeichnet.[Anm. 1] Dazu genügt es anzunehmen, dass die Anziehungskraft zweier kugelförmiger Körper proportional zum Produkt ihrer Massen und umgekehrt proportional zum Quadrat des Abstands ihrer Mittelpunkte ist, so dass das Verhältnis zweier Gravitationskräfte ausschließlich vom Verhältnis der Massen und Abstände abhängt. Im Einzelnen gilt für das Verhältnis der Kraft FProbe, mit der der leichte Probekörper vom schweren angezogen wird, und der Kraft FErde, mit der der leichte Probekörper von der Erde angezogen wird (also seinem Gewicht):
R12, RErde sind die jeweiligen Abstände. Die Masse m2 des leichten Probekörpers muss dazu gar nicht bekannt sein, denn sie hebt sich heraus. Nach der Messung von FProbe ist MErde die letzte verbleibende Unbekannte und kann einfach bestimmt werden.
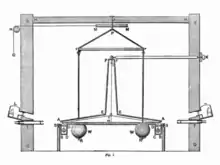
Der Messapparat – eine Torsionswaage – stammte ursprünglich von dem Geologen John Michell, der ihn kurz vor seinem Tod 1793 fertigstellte, selbst aber keine Messungen mehr durchführte. Cavendish betonte, dass Michell die Idee schon vor Coulomb hatte, der 1785 auf die gleiche Weise die elektrostatische Anziehung und Abstoßung untersucht hatte. Für den Nachweis der viel schwächeren Gravitation musste Cavendish die Waage teilweise umbauen, um Störfaktoren auszuschalten, insbesondere den Einfluss geringster Temperaturschwankungen. Er bediente deshalb sein Experiment aus einem anderen Raum und las die Messwerte mit einem Fernrohr ab. Gemessen wurde die Winkel-Auslenkung einer an einem Torsionsfaden aufgehängten Hantel mit zwei Bleikugeln, wenn sie von zwei in unmittelbare Nähe gebrachten größeren Bleikugeln angezogen wurden. Die Rückstellkraft wurde nach dem hookeschen Gesetz proportional zum Auslenkungswinkel angenommen. Cavendish führte während eines ganzen Jahres sein Experiment 17 mal mit 29 Messungen durch und berücksichtigte auch kleinste denkbare Störungen. Seine Endergebnisse für G weichen um 1,2 Prozent und für die Dichte der Erde um 0,6 Prozent vom heutigen Wert ab. Mit Kenntnis der absoluten Erdmasse konnten aus dem Gravitationsgesetz nun auch die Massen anderer Körper des Sonnensystems bestimmt werden, die wie die Erde von beobachtbaren Begleitern umrundet werden.
Das Experiment von Cavendish gilt heute als Klassiker in der Geschichte der Physik. Es wird als erste Bestimmung der Gravitationskonstante G gewertet, die eine der drei fundamentalen Naturkonstanten ist. Cavendish selbst lag diese Betrachtungsweise noch fern, selbst der Begriff „Gravitationskonstante“ konnte erst in der zweiten Hälfte des 19. Jahrhunderts auftauchen, nachdem 1873 mit der ersten allgemeinen Definition einer Krafteinheit (Dyn) die begriffliche Voraussetzung dafür geschaffen worden war.[12]
Werke (Auswahl)
- Henry Cavendish: An Attempt to Explain Some of the Principal Phaenomena of Electricity, by means of an Elastic Fluid: By the Honourable Henry Cavendish, F. R. S. Phil. Trans. January 1, 1771 61:584–677; doi:10.1098/rstl.1771.0056 (Volltext)
- Henry Cavendish: Experiments to determine the Density of the Earth. Philosophical Transactions of the Royal Society of London, Vol. 88 (1798), 469–526 (Volltext)
- Henry Cavendish in: Philosophical Transactions of the Royal Society of London (1776–1886). Internet-Archive online
- James Clerk Maxwell (Hrsg.): The electrical researches of the Honourable Henry Cavendish; edited by J. Clerk Maxwell. Written between 1771 and 1781. Edited from the original Manuscripts in the Possession of the Duke of Devonshire. Cambridge University, Press 1879, archive.org
Literatur
- Russell McCormmach, Christa Jungnickel: Cavendish: The experimental life. Bucknell, Cranbury N.J. 1999, ISBN 0-8387-5445-7. Edition Open Access
- Russell McCormmach: Speculative truth: Henry Cavendish, Natural philosophy and the rise of modern theoretical science. Oxford University Press, Oxford 2004, ISBN 0-19-516004-5.
- Russell McCormmach: Cavendish, Henry. In: Charles Coulston Gillispie (Hrsg.): Dictionary of Scientific Biography. Band 3: Pierre Cabanis – Heinrich von Dechen. Charles Scribner’s Sons, New York 1971, S. 155–159.
- George Wilson: The Life of the Hon. Henry Cavendish: Including Abstracts of His More Important Scientific Papers. Printed for the Cavendish Society, London 1851, Textarchiv – Internet Archive
- Cavendish, Henry (1732–1804). In: Leslie Stephen (Hrsg.): Dictionary of National Biography. Band 9: Canute – Chaloner. MacMillan & Co, Smith, Elder & Co., New York City / London 1887, S. 348–353 (englisch, Volltext [Wikisource]). Textarchiv – Internet Archive
- Cavendish, Henry. In: Encyclopædia Britannica. 11. Auflage. Band 5: Calhoun – Chatelaine. London 1910, S. 580 (englisch, Volltext [Wikisource]).
Weblinks
- Eintrag zu Cavendish; Henry (1731–1810); Natural Philosopher im Archiv der Royal Society, London
- Henry Cavendish. Famous Chemists
Anmerkungen
- Da mit Wiegen die Bestimmung des Gewichts gemeint ist, das die Erde hätte, wenn sie an ihrer eigenen Oberfläche auf eine Waage gelegt würde, ist diese Umschreibung in sich unlogisch.
Einzelnachweise
- Clapham in the 18th century.
- Blagdens Korrespondenzliste In: Archives associated with this Fellow beim Eintrag zu Cavendish; Henry (1731–1810); Natural Philosopher im Archiv der Royal Society, London (englisch).
- Hanno Beck: Alexander von Humboldt. Band 1. Steiner, Wiesbaden 1959, S. 26, 39–40.
- Verzeichnis der Mitglieder seit 1666: Buchstabe C. Académie des sciences, abgerufen am 28. Oktober 2019 (französisch).
- Maxwell (Hrsg.): The Experimental Researches of the Honorouble Henry Cavendish. Cambridge University Press, 1879
- Isobel Falconer: arxiv:1504.07437 Editing Cavendish: Maxwell and The Electrical Researches of Henry Cavendish. (Arxiv), Proceedings of the International Conference on the History of Physics 2014
- The History of the Cavendish Laboratory.
- Richard E. Dickerson, Harry B. Gray, Marcetta Y. Darensbourg: Prinzipien der Chemie. Walter de Gruyter & Co, Berlin 1988. S. 28.
- Martin Carrier: Cavendishs Version der Phlogistonchemie. S. 41.
- Martin Carrier: Cavendishs Version der Phlogistonchemie. uni-bielefeld.de (Memento vom 29. November 2014 im Internet Archive)
- Henry Cavendish: Experiments to determine the Density of the Earth (PDF) 1798 (englisch).
- B. E. Clotfelter: The Cavendish experiment as Cavendish knew it. Am. J. Phys. 55, 210 (1987); doi:10.1119/1.15214