Theophyllin
Theophyllin (von lateinisch thea ‚Tee‘ und altgriechisch φύλλον phýllon, deutsch ‚Blatt‘) ist ein vom Xanthin abgeleiteter Naturstoff aus der Gruppe der Purinalkaloide. Der Name leitet sich von Teeblättern ab, aus denen Albrecht Kossel 1888 als Erster kleine Mengen dieser Substanz isolieren konnte. In geringer Menge kommt Theophyllin auch in Kaffeebohnen,[3] Kolanüssen und Guaraná vor und ist ein Abbauprodukt des Coffeins im Stoffwechsel des Menschen. Theophyllin wird therapeutisch als Arzneistoff gegen Bronchialasthma und andere Bronchialerkrankungen eingesetzt. Ferner steigert Theophyllin auch die Leistung des Herzens und wirkt harntreibend.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
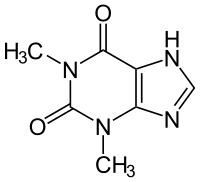 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Theophyllin | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C7H8N4O2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 180,16 g·mol−1 | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
8,6[3] | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Geschichte
.jpg.webp)
Bereits Mitte des 19. Jahrhunderts wies der Londoner Arzt Henry Salter darauf hin, dass Kaffeegenuss bei Asthmaanfällen zur Besserung führe.[7] Albrecht Kossel gelang 1888 erstmals die Isolierung von Theophyllin und er gab der Substanz auch ihren heutigen Namen.[8][9] Bereits sieben Jahre nach seiner Entdeckung gelang Emil Fischer und Lorenz Ach die synthetische Herstellung, ausgehend von 1,3-Dimethylharnsäure.[10] Theophyllin war somit das erste Purinalkaloid, das künstlich hergestellt werden konnte. Im Jahr 1900 beschrieb Wilhelm Traube mit der Traube-Synthese einen chemischen Syntheseweg, der bis heute Anwendung findet.[11][12]
Nach der Entdeckung der Reinsubstanz und der Erstbeschreibung seines als Aminophyllin bezeichneten Ethylendiaminsalzes wurde es zunächst als harntreibendes Mittel (Diuretikum) eingesetzt.[13] 1912 wiesen Jakob Pál und Paul Trendelenburg unabhängig voneinander nach, dass Xanthine wie Coffein und Theophyllin auf die glatte Muskulatur erschlaffend wirken. Hans Guggenheimer führte 1921 Theophyllin in die Therapie der Angina Pectoris ein.[14] 1922 etablierte S. R. Hirsch Methylxanthine wie Theophyllin in der Asthmatherapie.[15] Als ein wichtiges Element seines Wirkmechanismus entdeckten 1957 Mitarbeiter der Firma Hoechst die antagonistische Wirkung an Adenosinrezeptoren.[16][17] Die Entwicklung von Theophyllinpräparaten mit verzögerter Wirkstofffreisetzung ermöglichte in den 1970er Jahren eine zufriedenstellende Dauerbehandlung von Asthmatikern. Mit der Einführung von Glucocorticoiden und Beta-Sympathomimetika zur Inhalation verlor Theophyllin wenig später wieder an Bedeutung.
Vorkommen

Theophyllin ist ein Alkaloid, das in der Natur immer zusammen mit anderen Purinalkaloiden wie Coffein und Theobromin vorkommt. Im Vergleich zu den Hauptalkaloiden Coffein und Theobromin, die in purinalkaloidreichen Pflanzenteilen einen Gehalt von bis zu 6 % erreichen können, ist der Gehalt des Nebenalkaloids Theophyllin sehr gering. Der höchste Theophyllingehalt kann in Guaraná (bis 0,25 %), Pflanzenteilen von Theobroma-Arten (z. B. Kakao, 0,05 %), Mate-Blättern (0,05 %) und Teeblättern (0,03 %) nachgewiesen werden. Darüber hinaus kommt Theophyllin in Spuren in Kaffeebohnen und Kolanüssen vor.[18][19][20] Diese natürlichen Quellen haben jedoch für die Gewinnung von Theophyllin als Reinsubstanz keine wirtschaftliche Bedeutung.
Biosynthese
In Pflanzen kann Theophyllin über zwei verschiedene Biosynthesewege, ausgehend von Inosinmonophosphat (IMP) und Xanthosinmonophosphat (XMP), die auch Schlüsselpositionen in der Biosynthese der zellulären Energieträger Adenosintriphosphat (ATP) und Guanosintriphosphat (GTP) einnehmen, und anschließender Dephosphorylierung zu Xanthosin gebildet werden. Eine direkte N-3- und N-1-Methylierung von Xanthin, die zu Theophyllin führt, wurde postuliert.[21] Alternativ dazu wurde beschrieben, dass das in Kaffee, Tee, Kolanüssen und Guarana enthaltene Theophyllin ein Abbauprodukt des Coffeins sei.[22][23]
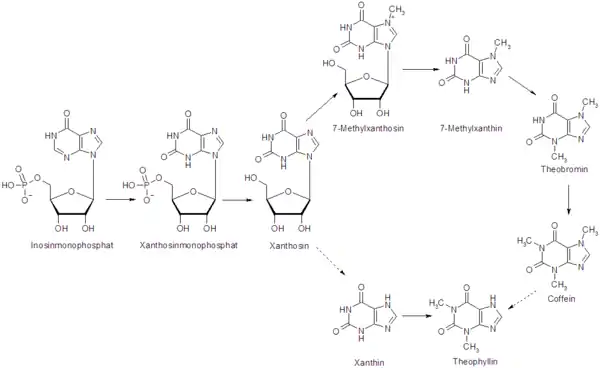
Auch im menschlichen Körper kann Theophyllin zu einem geringen Prozentsatz durch Abbau von Coffein in der Leber mit Hilfe des Cytochrom-P450-Isoenzyms CYP1A2 gebildet werden.
Klinische Angaben
Anwendungsgebiete (Indikationen)
Theophyllin findet in der Akutbehandlung von Atemnotzuständen aufgrund einer Verengung der Atemwege beim Asthma bronchiale und anderer obstruktiver Atemwegserkrankungen Anwendung.[24] Dabei wird Theophyllin auch in der Akutbehandlung des therapieresistenten Status asthmaticus und des schweren akuten Bronchospasmus eingesetzt. Zu diesem Zweck steht Theophyllin als Infusion zur Verfügung.[25] In Arzneiformen zur oralen Anwendung mit verzögerter Freisetzung (Retardtabletten oder -kapseln) ist Theophyllin zur Dauerbehandlung und Vorbeugung gegen asthmatische Anfälle und andere obstruktive Atemwegserkrankungen zugelassen.[26] Es gilt bei der Behandlung von Asthma sowohl als Dauertherapie wie in der Notfallbehandlung auf Grund seiner geringen therapeutischen Breite als Reservemittel bei schweren Fällen.[27][28] Eine auch als Drug Monitoring bezeichnete Beobachtung des Serumwirkspiegels zur Sicherung des therapeutischen Erfolgs und zur Vermeidung von unerwünschten Arzneimittelwirkungen wegen der engen therapeutischen Breite wird auch aufgrund von bevölkerungsrepräsentativen pharmakoepidemiologischen Studien dringend empfohlen.[29]
In der Kinderheilkunde kann Theophyllin zur Behandlung des idiopathischen Atemstillstands bei Früh- und Neugeborenen in Begleitung mit anderen geeigneten therapeutischen Maßnahmen zur Atemstimulation eingesetzt werden. Ebenso ist Theophyllin zur Sekundärprophylaxe der anscheinend lebensbedrohlichen Ereignisse bei Säuglingen (ALTE) zugelassen, wenngleich keine ausreichenden Daten über eine Minderung der Sterblichkeit vorliegen.[24]
Der Einsatz von Theophyllin – außerhalb seiner Zulassung – zur Vorbeugung gegen einen durch Kontrastmittel ausgelösten Nierenschaden ist umstritten.[30] Seine Verwendung als Diuretikum und sein früherer Einsatz in der Behandlung der Angina Pectoris gelten als überholt.
Theophyllin kann möglicherweise helfen, die Defekte, die bei Erkrankungen wie Multiple Sklerose in Gehirn und peripherem Nervensystem durch Schädigung der Myelinscheiden entstehen, zu reparieren[31]
Anwendung in der Tierheilkunde
In der Tiermedizin findet Theophyllin vor allem bei Asthma bronchiale Anwendung; allerdings ist derzeit in Deutschland kein tiermedizinisches Präparat zugelassen.
Die EU-Rückstandshöchstmengen-Verordnung für Lebensmittel tierischen Ursprungs erlaubt die Anwendung von Theophyllin bei allen zur Lebensmittelerzeugung genutzten Tierarten.[32]
Gegenanzeigen (Kontraindikationen)
Theophyllin darf nicht bei bekannter Überempfindlichkeit gegen diesen Wirkstoff, nach einem frischen Herzinfarkt oder bei akuten tachykarden Herzrhythmusstörungen angewendet werden. Nur mit größter Vorsicht und strenger Indikationsstellung darf Theophyllin bei Patienten mit instabiler Angina Pectoris, Neigung zu tachykarden Herzrhythmusstörungen, schwerem Bluthochdruck, hypertropher obstruktiver Kardiomyopathie, Schilddrüsenüberfunktion, Epilepsie, Magen- oder Zwölffingerdarmgeschwür oder der Stoffwechselerkrankung Porphyrie angewendet werden. Leber- und Nierenfunktionsstörungen stellen keine Kontraindikation dar, erfordern aber, wie auch die Anwendung bei alten, multimorbiden, schwerkranken oder intensivtherapierten Patienten, eine Anpassung und Kontrolle der Dosierung mit Hilfe des Drug Monitorings.[26]
Anwendung während Schwangerschaft und Stillzeit
Die Anwendung von Theophyllin während des ersten Schwangerschaftsdrittels (Trimenon) sollte gemieden werden, da keine ausreichenden Daten zur Anwendung des Wirkstoffs in dieser Schwangerschaftsphase vorliegen. Während des zweiten und dritten Trimenons kann eine Anwendung von Theophyllin unter strenger Nutzen-Risiko-Abwägung erfolgen. Dabei sind insbesondere die Plazentagängigkeit von Theophyllin und seine sympathomimetischen Eigenschaften auf das Kind zu berücksichtigen. Bei Anwendung kurz vor Ende der Schwangerschaft können sympathomimetische Wirkungen auf die Mutter zu einer Hemmung der Wehentätigkeit führen.
Theophyllin geht in die Muttermilch über und kann beim gestillten Säugling therapeutisch wirksame Serumspiegel erreichen. Daher sollte ebenfalls eine Nutzen-Risiko-Abwägung vorgenommen werden, die Dosierung bei der Mutter möglichst niedrig gewählt werden oder gegebenenfalls abgestillt werden.[26]
Wechselwirkungen mit anderen Medikamenten
Arzneistoffe und andere körperfremde Stoffe (Xenobiotika), die zu einer Verringerung oder Erhöhung der Theophyllinkonzentration im Organismus führen, können auf Grund der geringen therapeutischen Breite leicht entweder zur Unwirksamkeit des verabreichten Theophyllins oder zu toxischen Reaktionen führen. Enzyminduktoren, wie Barbiturate, Carbamazepin, Phenytoin, Primidon, Rifampicin und Sulfinpyrazon, aber auch Rauchen führen zu einem beschleunigten Abbau von Theophyllin. Die damit verbundenen erniedrigten Plasmaspiegel können durch eine überwachte Dosiserhöhung angepasst werden.
Demgegenüber führen Inhibitoren des Cytochrom-P450-Enzymsystems, insbesondere CYP-1A2-Inhibitoren, zu einem verminderten Abbau von Theophyllin, was eine Anreicherung zur Folge haben kann. Bedeutsame Wechselwirkungen in diesem Zusammenhang konnten mit Makroliden (z. B. Erythromycin, Clarithromycin), Fluorchinolonen (z. B. Ciprofloxacin, Enoxacin), Thiabendazol, Cimetidin und Allopurinol beobachtet werden. Auch Antibabypillen, Imipenem, Isoniazid, Calciumantagonisten (z. B. Verapamil, Diltiazem), Propranolol, Mexiletin, Propafenon, Ticlopidin, Alpha-Interferon und Influenzaimpfstoffe können zu einer Erhöhung der Plasmakonzentration von Theophyllin führen und eine kontrollierte Dosisreduktion erfordern. Eine Interaktion mit Ranitidin ist ebenfalls möglich, jedoch nicht gesichert.
Über einen Synergismus ist Theophyllin in der Lage, die Wirkung von anderen Xanthinen, einschließlich Coffein, zu verstärken. Ebenso wird die Wirkung von β2-Sympathomimetika und Diuretika verstärkt. Die Wirkung von Betablockern und Lithium kann hingegen durch gleichzeitige Einnahme von Theophyllin abgeschwächt werden. Bei gleichzeitiger Anwendung mit Halothan konnte eine Verstärkung der kardialen Nebenwirkungen des Inhalationsanästhetikums beobachtet werden.[26]
Nebenwirkungen
Mit einer Häufigkeit von über 10 Prozent können unerwünschte Arzneimittelwirkungen auf das Nervensystem, wie Kopfschmerzen, Tremor, Unruhe, Erregung und Schlaflosigkeit sowie den Stoffwechsel und Elektrolythaushalt wie Kaliummangel (Hypokaliämie), Überzuckerung (Hyperglykämie), Erhöhung des Harnsäurespiegels (Hyperurikämie), Anstieg des Serum-Calciums (Hyperkalzämie) und des Serum-Kreatinins auftreten. Die ebenfalls sehr häufigen Nebenwirkungen im Harnapparat äußern sich in einer verstärkten Diurese. Diese Nebenwirkung wurde früher bei der Anwendung von Theophyllin als Diuretikum ausgenutzt.[33] Gelegentlich (0,1–1 %) treten Überempfindlichkeitsreaktionen gegen den Wirkstoff auf, die einen Wechsel des Therapeutikums erfordern. Die Häufigkeit von Krampfanfällen bei bestimmungsgemäßer Anwendung von Theophyllin ist nicht quantifiziert.[26]
Überdosierung
| Serumspiegel | Nebenwirkung | Häufigkeit der Nebenwirkungen |
|---|---|---|
| 8–20 µg/ml | Zittern, Schlafstörungen, Übelkeit, Sodbrennen |
5–10 % |
| 20–25 µg/ml | Unruhe, Erregbarkeit, Erhöhung der Herzfrequenz |
25 % |
| >35 µg/ml | Herzrhythmusstörungen, Erniedrigung des Kaliumspiegels, Krampfanfälle |
75 % |
Abhängig von der Dosis treten verschiedene charakteristische, in der nebenstehenden Tabelle aufgeführte Nebenwirkungen auf. Auf Grund der geringen therapeutischen Breite von Theophyllin kann eine Überdosierung schnell zu toxischen Reaktionen bis hin zum Tod führen. Die Sicherheit der Therapie kann durch Bestimmung des Theophyllinspiegels aus Serum oder Speichel erhöht werden (therapeutisches Drug Monitoring). Während im therapeutischen Bereich von 8 bis 20 µg/ml i.S. Zittern, Schlaflosigkeit, Übelkeit und Unruhe beobachtet werden können, treten bei Serumkonzentrationen von über 25 µg/ml Krampfanfälle, plötzlicher Blutdruckabfall, Herzrhythmusstörungen, Rhabdomyolyse und schwerwiegende Magen-Darm-Störungen in den Vordergrund.[26] Zur Vermeidung schwerer Nebenwirkungen wie Herzfrequenzanstieg, Atemnot und Krampfanfälle sollte Theophyllin bei intravenöser Gabe nur sehr langsam und nicht als Bolus gegeben werden.[34] Besonders schwere Theophyllinintoxikationen können tödlich enden.
Bei leichten Intoxikationserscheinungen sollte der Wirkstoff abgesetzt und sein Serumspiegel bestimmt werden. Anhand dieser Daten kann eine Fortsetzung der Therapie mit einer angepassten (verringerten) Dosis erfolgen. Treten zentralnervöse Symptome wie Unruhe und Krämpfe auf, können diese mit Diazepam oder Phenobarbital behandelt werden. Theophyllin antagonisiert die Wirkung von Benzodiazepinen, welche gegen Krampfanfälle unterschiedlicher Ursache angewendet werden. Infolgedessen muss bei Krampfanfällen, die durch Theophyllin hervorgerufen werden, mit einem höheren Bedarf an Benzodiazepinen gerechnet werden. In einer retrospektiven Studie über Theophyllin-induzierte Anfälle von Kindern musste rund ein Viertel der Patienten zudem intubiert werden.[35] Beim Auftreten bedrohlicher Herzrhythmusstörungen ist die intravenöse Gabe von Betablockern bei Nicht-Asthmatikern oder Verapamil bei Asthmatikern angezeigt. Bei Bedrohung der Vitalfunktion stehen die Überwachung lebenswichtiger Funktionen, das Freihalten der Atemwege und die Versorgung mit Sauerstoff, das Entfernen von Theophyllinresten aus dem Magen-Darm-Trakt durch Magenspülung und Gabe von Aktivkohle, die Kontrolle des Wasser- und Elektrolythaushalts sowie gegebenenfalls die Volumensubstitution mit Plasmaexpandern im Vordergrund. Mit Hilfe der Hämodialyse und der Hämoperfusion kann zudem bei besonders schweren Intoxikationen eine schnelle und vollständige Entgiftung erreicht werden.[26]
Pharmakologische Eigenschaften
Wirkungsweise (Pharmakodynamik)
Theophyllin führt primär zu einer Erschlaffung der glatten Muskulatur der Atemwege und somit zu einer Erweiterung der Bronchien. Zusätzlich steigert dieser Arzneistoff den Abtransport von Fremdstoffen und Schleim durch die Zilien der Lunge, senkt den Druck in den Lungengefäßen und steigert den Atemantrieb sowie die Kontraktionsfähigkeit der Atemmuskulatur. Entzündungshemmende Effekte von Theophyllin können bei Dauerbehandlung ebenso zu dessen Asthmawirksamkeit beitragen.[25]
Auf molekularer Ebene werden verschiedene Mechanismen für die anti-asthmatische Wirksamkeit von Theophyllin verantwortlich gemacht. Als nichtselektiver Hemmstoff (Inhibitor) der Phosphodiesterasen führt Theophyllin zu einem Anstieg des in der Zelle vorliegenden cAMP. Zusätzlich wirkt Theophyllin antagonistisch an A1- und A2-Adenosinrezeptoren. Auf diese Weise wird einerseits die Ausschüttung von Entzündungsmediatoren, wie Histamin und Leukotrienen, gehemmt und andererseits die Konzentration des zellulären cAMPs weiter erhöht. Auf den cAMP-Anstieg können die Erschlaffung der glatten Muskulatur, aber möglicherweise auch sekundäre Effekte, wie die Freisetzung von Interleukin-10, die Hemmung des entzündungsfördernden Transkriptionsfaktors NF-κB und Wirkungen auf den gesteuerten Zelltod (Apoptose) von Granulozyten und T-Lymphozyten zurückgeführt werden. Bei sehr hohen Theophyllinkonzentrationen, die keine therapeutische Relevanz besitzen, führt Theophyllin zu einer Hemmung von Calciumkanälen.[36]
Die antientzündliche Wirkkomponente von Theophyllin wird zusätzlich mit einer Steigerung der Aktivität von Histon-Deacetylasen an Genen in Verbindung gebracht, die für Entzündungsmediatoren kodieren.[37]
Pharmakokinetik
Nach Infusion von Theophyllin setzt die bronchienerweiternde Wirkung innerhalb weniger Minuten ein, sobald ein Plasmaspiegel von 5 µg/ml erreicht ist. Die bronchienerweiternde Wirkung hält in etwa sechs bis acht Stunden an. Nach oraler Gabe einer Theophyllinlösung wird der Wirkstoff rasch und vollständig aufgenommen. Die bronchienerweiternde Wirkung tritt ebenfalls innerhalb weniger Minuten ein. Zur Dauerbehandlung werden Retardpräparate eingesetzt, die ihr Wirkmaximum nach rund sechs bis acht Stunden erreichen.[25][26]
Im therapeutischen Konzentrationsbereich liegt Theophyllin zu 60 % an Plasmaproteine gebunden vor. Die Plasmaproteinbindung bei Neugeborenen sowie bei Patienten mit einer Leberzirrhose ist erniedrigt und liegt bei etwa 40 %.[26]
Theophyllin wird fast vollständig durch das Cytochrom-P450-Enzymsystem in der Leber abgebaut. Die Geschwindigkeit der Verstoffwechselung schwankt jedoch individuell sehr stark und ist unter anderem von der Lebenssituation (insbesondere Alter, körperlicher Belastung und Körpergewicht), den Ernährungsgewohnheiten und den Rauchgewohnheiten des Patienten abhängig. Verminderte Abbauraten können bei Patienten mit fieberhaften Infekten, Leberschädigungen und Rechtsherzinsuffizienz beobachtet werden. Die Plasmahalbwertszeit liegt beim gesunden Erwachsenen üblicherweise zwischen 7 und 9 Stunden. Bei Rauchern ist diese auf 4 bis 5 Stunden und bei Kindern auf 3 bis 4 Stunden deutlich reduziert. Bei Hunden liegt die Plasmahalbwertszeit bei 6 Stunden, bei Katzen bei 8 Stunden, bei Schweinen bei 11 Stunden und bei Pferden bei 10 bis 17 Stunden.[32]
Einen wesentlichen Einfluss auf die Plasmahalbwertszeit von Theophyllin haben insbesondere Arzneistoffe, die den Abbau über das Cytochrom-System hemmen oder induzieren. So führen unter anderem die Cytochrom-P450-Hemmer Cimetidin, Allopurinol, orale Kontrazeptiva, Makrolide und Fluorchinolone zu einem verlangsamten Abbau und somit zu einer Anhäufung (Kumulation) von Theophyllin. Enzyminduktoren, wie Phenytoin, Carbamazepin, Rifampicin, Isoniazid und Barbiturate, aber auch das Rauchen von Tabak oder Marihuana senken hingegen den Spiegel von Theophyllin. Ebenso kann der Genuss von Koffein zu einem verminderten Abbau von Theophyllin führen.[26][27][38][39] Es ist ein genetischer Polymorphismus des CYP1A2-Gens beschrieben, der zu einem verminderten Abbau von Theophyllin führt.[40]
Chemie
Eigenschaften

Theophyllin ist ein weißes, geruchloses, amorphes oder kristallines Pulver bitteren Geschmacks. Es kann in zwei polymorphen Formen und als Monohydrat auftreten.[2] Die Form II ist die bei Raumtemperatur stabile Form. Sie schmilzt bei 271 °C mit einer Schmelzwärme von 167,1 J·g−1.[2] Die Form I besitzt einen Schmelzpunkt von 275 °C mit einer Schmelzwärme von 155,5 J·g−1.[2] Beide Formen stehen enantiotrop zueinander. Die beiden Polymorphe und das Monohydrat zeigen unterschiedliche Lösungsenthalpien. Diese betragen für die Form I 19,64 kJ·mol−1 bzw. 109 kJ·mol−1, für die Form II 21,44 kJ·mol−1 bzw. 119 kJ·mol−1 und für das Monohydrat 29,34 kJ·mol−1 bzw. 163 kJ·mol−1.[41] Als Salz (Monohydrat, Lysinsalz oder Magnesiumacetat) ist es an der Luft stabil, die freie Base zersetzt sich unter Luft- und Lichteinwirkung. Das Alkaloid ist amphoter und kann als schwache Säure mit einer Säurekonstanten pKs2 von 8,6 (Deprotonierung des Imidazol-Stickstoffs in Position 7) oder als schwache Base mit einem pKs1-Wert von 0,3 (Protonierungsgleichgewicht des Imidazol-Stickstoffs in Position 9) reagieren.[42] In wässriger Lösung liegt Theophyllin, wie auch das Purin, in einem tautomeren Gleichgewicht vor, wobei das 9H-Tautomer überwiegt. Auf Grund seiner Amphoterie löst sich Theophyllin gut in verdünnten Säuren oder basischen Lösungen. Demgegenüber ist die Substanz in Wasser, Ethanol oder Diethylether wenig löslich.[3] Mit dem Ziel der Verbesserung der Löslichkeit wurden Theophyllinsalze, wie beispielsweise Theophyllindiethanolamin, Theophyllinethanolamin, Theophyllinisopropanolamin, Theophyllinnatriumacetat und Theophyllinnatriumglycinat entwickelt. Pharmazeutisch verwendet werden neben dem wasserfreien Theophyllin auch sein Monohydrat sowie Theophyllinnatriumglycinat und Theophyllinethylendiamin (Aminophyllin).
Synthese
Theophyllin ist ein Derivat des Xanthins. Seine Herstellung kann durch Umsetzung der Ausgangsstoffe N,N′-Dimethylharnstoff und Cyanessigsäureethylester mit Hilfe der Traube-Synthese erfolgen.[3] Der Syntheseweg wurde bereits 1900 in der Zeitschrift Chemische Berichte von Wilhelm Traube aus der Chemischen Abtheilung des pharmakologischen Instituts zu Berlin veröffentlicht.[11][12]
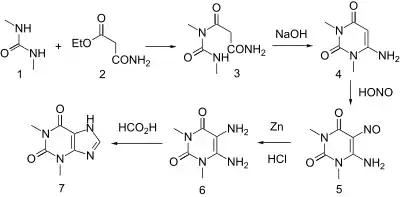
Derivate
Auf Grund seiner pharmakologischen Eigenschaften war Theophyllin in der medizinischen Chemie ein beliebtes Objekt für Strukturmodifikationen. Insbesondere Veränderungen der Substituenten in den Positionen 7 und 8 führten zu neuen Arzneistoffen. Zu den Derivaten, die eine therapeutische Relevanz errangen, zählen 8-Chlortheophyllin, Fenetyllin, Etofyllin, Cafedrin und Reproterol.
Analytik
Zur Identifizierung von Theophyllin kann die klassische Murexid-Reaktion verwendet werden, die für Theophyllin, wie auch für andere Methylxanthine, eine positive Reaktion ergibt. Zusätzlich kann die Theophyllidin-Reaktion, die auf einer alkalischen Hydrolyse des Theophyllins und einer Kupplung mit diazotierter Sulfanilsäure beruht, zum Nachweis von Theophyllin genutzt werden. Ein positiver Nachweis gelingt auch mit Hilfe von Gibbs-Reagenz. Zur Unterscheidung zwischen Theophyllin und anderen Methylxanthinen eignet sich die Zwikker-Reaktion. Darüber hinaus bildet Theophyllin im Gegensatz zu Coffein und Theobromin im ammoniakalischen Milieu mit Silbernitrat einen weißen Niederschlag.[3]
Die Gehaltsbestimmung von Theophyllin erfolgt nach dem europäischen Arzneibuch als Titration mit Hilfe der Alkalimetrie.[43] Da der Gehalt auf Grund der vergleichsweise niedrigen Säurestärke des Theophyllins nicht direkt im wässrigen Milieu bestimmbar ist, erfolgt die Titration mit Natriumhydroxidlösung nach Fällung und Deprotonierung mit Silbernitrat unter Verwendung des Indikators Bromthymolblau. Alternative Gehaltsbestimmungsmethoden schließen instrumentelle Verfahren, wie beispielsweise HPLC, ein.
Die Bestimmung von Theophyllin in biologischen Proben wird durch deren Beschaffenheit bestimmt. Bei relativ einfachen Analysenproben kommen Methoden wie die Dünnschichtchromatografie, auch in Kombination mit der UV- beziehungsweise IR-Spektroskopie, zur Anwendung. Komplexere Proben, wie z. B. Blut, Serum und Urin, erfordern jedoch zur qualitativen und quantitativen Bestimmung aufwändigere Verfahren wie z. B. Enzymimmunoassays, Gaschromatographie mit Massenspektrometrie-Kopplung (GC/MS) oder Flüssigchromatographie mit Massenspektrometrie-Kopplung (HPLC/MS).[44][45]
Handelsnamen
Theophyllin wird als Monopräparat unter anderem unter den Handelsnamen Aerobin (D), Afonilum (D), Bronchoretard (D), Euphyllin retard (A, CH), Euphylong (D), Respicur retard (A), Solosin retard (D), Theolair (CH), Theospirex retard (A), Tromphyllin (D), Unifyl (A, CH) und Uniphyllin (D) sowie unter generischer Bezeichnung in Form von Tabletten oder Kapseln mit einer verzögerten Freisetzung (Retardierung) in Einzeldosen zwischen 100 und 600 mg vertrieben. Als nichtretardierte Präparate werden Solosin Tropfen (D) und Euphylong quick (D) für den Akutfall angeboten. Ebenfalls für den Akutfall stehen afpred forte-THEO (D), Bronchoparat (D), Euphyllin (A, CH), Euphylong i.v. (D), Respicur Ampullen (A), Solosin Infusionslösung (D) und Theospirex-Ampullen (A) zur Infusion zur Verfügung. Als Kombinationspräparat mit Ambroxol ist Broncho-Euphyllin (D) im Handel.[46][47][48]
Weblinks
Einzelnachweise
- Eintrag zu THEOPHYLLINE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Dezember 2020.
- P. Szerner, B. Legendre, M. Sghaier: Thermodynamic properties of polymorphic forms of theophylline. Part I: DSC, TG, X-ray study. In: J. Therm. Anal. Calorim. Band 99, 2010, S. 325–335, doi:10.1007/s10973-009-0186-1 (englisch).
- F. von Bruchhausen, Hermann Hager: Hagers Handbuch der pharmazeutischen Praxis. Band 9: Stoffe P–Z. 5. Auflage. Birkhäuser, 1999, ISBN 3-540-52688-9, S. 853–855.
- Eintrag zu Theophyllin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. März 2011.
- Eintrag zu Theophyllin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Datenblatt Theophylline bei Sigma-Aldrich, abgerufen am 24. April 2011 (PDF).
- H. Salter: On some points in the treatment and clinical history of asthma. In: Edinb. Med. J. Band 4, 1859, S. 1109–1115 (englisch).
- A. Kossel: Über eine neue Base aus dem Pflanzenreich. In: Ber. Dtsch. Chem. Ges. Band 21, 1888, S. 2164–2167, doi:10.1002/cber.188802101422.
- A. Kossel: Über das Theophyllin, einen neuen Bestandtheil des Thees. In: Hoppe Seylers Z Physiol Chem. Band 13, 1889, S. 298–308.
- E. Fischer, L. Ach: Synthese des Caffeins. In: Ber. Dtsch. Chem. Ges. Band 28, 1895, S. 3135–3143, hier 3139, doi:10.1002/cber.189502803156.
- Wilhelm Traube: Ueber eine neue Synthese des Guanins und Xanthins. In: Chem. Ber. Band 33, Nr. 1, 1900, S. 1371–1383, doi:10.1002/cber.190003301236.
- Wilhelm Traube: Der synthetische Aufbau der Harnsäure, des Xanthins, Theobromins, Theophyllins und Caffeïns aus der Cyanessigsäure. In: Chem. Ber. Band 33, Nr. 3, Oktober 1900, S. 3035–3056, doi:10.1002/cber.19000330352.
- O. Minkowski: Über Theocin (Theophyllin) als Diureticum. In: Ther. Gegenwart. Band 43, 1902, S. 490–493.
- H. Guggenheimer: Euphyllin intravenös als Herzmittel. In: Ther. Monatshefte. Band 35, 1921, S. 566–572.
- G. Schultze-Werninghaus, J. Meier-Sydow: The clinical and pharmacological history of theophylline: first report on the bronchospasmolytic action in man by S. R. Hirsch in Frankfurt (Main) 1922. In: Clin. Allergy. Band 12, 1982, S. 211–215, PMID 7042115 (englisch).
- Klaus Aktorius (Hrsg.): Allgemeine und spezielle Pharmakologie und Toxikologie. 10. Auflage. München 2009, ISBN 978-3-437-42522-6, S. 188–189.
- B. B. Fredholm, C. G. Persson: Xanthine derivatives as adenosine receptor antagonists. In: European Journal of Pharmacology. Band 81, Nr. 4, 1982, S. 673–676, PMID 6288418 (englisch).
- M. A. Jalal, H. A. Collin: Estimation of caffeine, theophylline and theobromine in plant material. In: New Phytol. Band 76, 1976, S. 277–281, doi:10.1111/j.1469-8137.1976.tb01461.x (englisch).
- Rudolf Hänsel, Otto Sticher: Pharmakognosie, Phytopharmazie. 8. Auflage. Springer-Verlag, 2007, ISBN 978-3-540-26508-5, S. 1455.
- James A. Duke: Handbook of phytochemical constituents of GRAS herbs and other economic plants. CRC Press, Boca Raton FL 1992, ISBN 0-8493-3672-4.
- T. Suzuki, E. Takahashi: Biosynthesis of caffeine by tea-leaf extracts. Enzymic formation of theobromine from 7-methylxanthine and of caffeine from theobromine. In: Biochem. J. 146, 1975, S. 87–96. PMID 238504.
- Biosynthesis of alkaloids derived from histidine and purine. Kyoto Encyclopedia of Genes, Genomes
- T. Suzuki, G. R. Waller: Biosynthesis and biodegradation of caffeine, theobromine, and theophylline in Coffea arabica L. fruits. In: J. Agric. Food Chem., 32 (4), 1984, S. 845–848. doi:10.1021/jf00124a038.
- BfArM Mustertext für Fachinformationen 8000368: Theophyllin – Konzentrat zur Herstellung einer Infusionslösung (Stand 17. Juni 2008; RTF; 117 kB).
- B. Lemmer, R. Wettengel: Erkrankungen der Atemwege. In: Björn Lemmer, Kay Brune: Pharmakotherapie – Klinische Pharmakologie. 13. Auflage. Heidelberg 2007, ISBN 978-3-540-34180-2, S. 343–344, S. 349–350.
- BfArM Mustertext für Fachinformationen 8000370: Theophyllin – Retardtablette, Retardkapsel, Retardgranulat (Stand 17. Juni 2008; RTF; 120 kB).
- Gerd Herold: Innere Medizin. Köln 2009, ISBN 978-1-111-15195-9, S. 343–346.
- D. Ukena, L. T. Fishman, W. B. Niebling: Asthma bronchiale – Diagnostik und Therapie im Erwachsenenalter. In: Deutsches Ärzteblatt. 105(21), 2008, S. 385–394.
- U. Langen, H. Knopf, H. U. Melchert: Arzneimitteltherapie des Asthma bronchiale. Ergebnisse des Bundes-Gesundheitssurveys 1998. In: Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 49 (9), Sep 2006, S. 903–910. PMID 16927032.
- S. M. Bagshaw, W. A. Ghali: Theophylline for prevention of contrast-induced nephropathy: a systematic review and meta-analysis. In: Arch Intern Med. 165, 2005, S. 1087–1093. PMID 15911721.
- Theophyllin unterstützt Remyelinisierung von Nervenfasern. In: Deutsches Ärzteblatt. 14. September 2020, abgerufen am 1. Dezember 2020.
- Wolfgang Löscher: Theophyllin. In: Wolfgang Löscher u. a. (Hrsg.): Pharmakotherapie bei Haus- und Nutztieren. 7. Auflage. Paul Parey Verlag, 2006, ISBN 3-8304-4160-6, S. 115.
- S. Rau: Die Geschichte der Diuretika: Vom Coffein zum Furosemid. In: Pharmazie in unserer Zeit. Band 35, Nr. 4, 2006, S. 286–292, PMID 16886504.
- Heinz Lüllmann, Klaus Mohr, Lutz Hein: Pharmakologie und Toxikologie. 16. Auflage. Stuttgart 2006, ISBN 3-13-368516-3, S. 176.
- H. Yoshikawa: First-line therapy for theophylline-associated seizures. In: Acta Neurol Scand. 115 (4), Apr 2007, S. 57–61. PMID 17362277.
- P. J. Barnes: Theophylline: new perspectives for an old drug. In: Am J Respir Crit Care Med. 167, 2003, S. 813–818. PMID 12623857.
- K. Ito, S. Lim, G. Caramori, B. Cosio, K. F. Chung, I. M. Adcock, P. J. Barnes: A molecular mechanism of action of theophylline: Induction of histone deacetylase activity to decrease inflammatory gene expression. In: Proc Natl Acad Sci U S A. 99 (13), 25 Jun 2002, S. 8921–8926. PMID 12070353.
- J. H. Jonkman, R. A. Upton: Pharmacokinetic drug interactions with theophylline. In: Clinical Pharmacokinetics. Band 9, Nr. 4 (Jul–Aug), August 1984, S. 309–334, PMID 6147220.
- P. Kozak: Factors that influence theophylline metabolism. In: Western Journal of Medicine. Band 131, Nr. 4, Oktober 1979, S. 319–320, PMC 1271836 (freier Volltext).
- Yasushi Obase, Terufumi Shimoda, Tetsuya Kawano, Sachiko Saeki, Shin-ya Tomari, Kazuko Mitsuta-Izaki, Hiroto Matsuse, Moritoshi Kinoshita, Shigeru Kohno: Polymorphisms in the CYP1A2 gene and theophylline metabolism in patients with asthma. In: Clin Pharmacol Ther. Band 73, Nr. 5, 2003, S. 468–474, PMID 12732846.
- Vesa-Pekka Lehto; Mikko Tenho; Olli-Pekka Hämäläinen; Jarno Salonen; Calorimetric determination of dissolution enthalpy with a novel flow-through method. In: J. Pharm. Biomed. Anal. 53 (2010) 821–825, doi:10.1016/j.jpba.2010.06.029.
- Theophyllin. In: Kommentar zur Ph. Eur.
- Europäisches Arzneibuch 6.0. Band 3: Monographie Theophyllin. Deutscher Apotheker Verlag, Stuttgart 2008, ISBN 978-3-7692-3962-1, S. 4116–4117.
- H. Juárez-Olguín, J. Flores-Pérez, I. Lares-Asseff: Plasmatic levels of theophylline in asthmatic patients. Comparative evaluations of two different methods. In: Arch Med Res. 29 (1), 1998, S. 45–50. PMID 9556922.
- M. Kress, D. Meissner, P. Kaiser, R. Hanke, W. G. Wood: Determination of theophylline by HPLC and GC-IDMS, the effect of chemically similar xanthine derivatives on the specificity of the method and the possibility of paracetamol as interfering substance. In: Clin Lab. 48 (9–10), 2002, S. 541–551. PMID 12389716.
- Rote Liste online, Stand: Oktober 2009.
- AM-Komp. d. Schweiz, Stand: Oktober 2009.
- AGES-PharmMed, Stand: Oktober 2009.