Ranitidin
Ranitidin ist ein Arzneistoff aus der Gruppe der H2-Antihistaminika, der zur Unterdrückung der Magensäureproduktion bei Sodbrennen, zur Behandlung der Refluxkrankheiten und zur Magengeschwür-Prophylaxe sowohl in der Humanmedizin als auch in der Veterinärmedizin angewendet werden kann.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-Ranitidine_Structural_Formulae_V.1.png.webp) | ||||||||||||||||||||||
| (E,Z)-Isomerengemisch: (E)-Form (oben) und (Z)-Form (unten) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Ranitidin | |||||||||||||||||||||
| Andere Namen |
N-{2-[({5-[(Dimethylamino)methyl]furan-2-yl}methyl)sulfanyl]ethyl}-N′-methyl-2-nitroethen-1,1-diamin | |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A02BA02 | |||||||||||||||||||||
| Wirkstoffklasse |
Ulkustherapeutika | |||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
löslich in Essigsäure und Wasser, löslich in Methanol (Ranitidin·Hydrochlorid)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Im April 2020 hat die Food and Drug Administration (FDA) alle ranitidinhaltigen Arzneimittel vom US-Markt zurückgerufen, in der EU empfahl die europäische Arzneimittelagentur im gleichen Monat das Ruhen der Zulassung für solche Arzneimittel. Vorangegangen war die Feststellung, dass ranitidinhaltige Arzneimittel geringe Mengen des als möglicherweise krebserregend eingestuften N-Nitrosodimethylamin (NDMA) als Verunreinigung enthielten.
Verkaufsabgrenzung
In Deutschland sind Ranitidin-Präparate verschreibungspflichtig, ausgenommen sind jedoch Zubereitungen zur Einnahme in Stärken bis zu 75 mg und Packungsgrößen bis zu 1050 mg, sofern die Anwendung auf Patienten ab 16 Jahre, auf die Anwendungsgebiete „Bei Sodbrennen und/oder saurem Aufstoßen“ und auf eine maximale Therapiedauer von 14 Tagen beschränkt ist.
Gewinnung und Darstellung
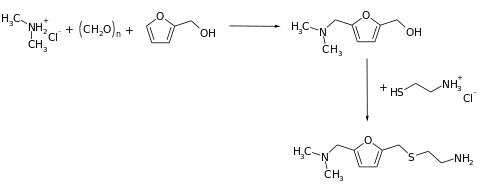
Die Synthese von Ranitidin erfolgt über die Herstellung von zwei Hauptvorprodukten, deren Umsetzung dann zum Zielmolekül führt. Die Synthese des einen Vorprodukts beginnt mit der parallelen Alkylierung und Aminierung von Furfurylalkohol zum 5-Dimethylaminomethylfurfurylalkohol,[6] der dann mit Cysteaminhydrochlorid zum Dimethylaminomethylfurfurylthioether umgesetzt wird.
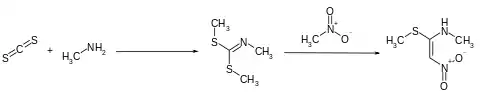
Die Synthese des zweiten Vorprodukts beginnt mit der Umsetzung von Schwefelkohlenstoff und Methylamin in Benzol mittels Natronlauge in Gegenwart von Tetrabutylammoniumbromid zum Dimethyl-N-methylcarboimidodithionat. Die Reaktion mit Nitromethan führt dann zum N-Methyl-1-methylthio-2-nitroethenamin.[7][8]
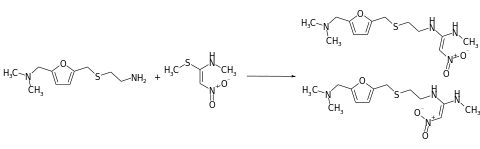
Das Zielmolekül erhält man durch die Umsetzung der Thioetherverbindung mit dem Nitroethenamin.[9]
Isomerie
Auf Grund der Wechselwirkung zwischen den Aminfunktionen und der Nitrogruppe über einen Sechsring ist die Rotationsbarriere der Kohlenstoff-Kohlenstoff-Doppelbindung nur sehr niedrig. Im NMR-Spektrum werden nur gemittelte Signale aus (E)- und (Z)-Isomer gefunden. Das System lässt sich bei 271 K einfrieren, wo dann separate Signale für (E)- und (Z)-Isomer gefunden werden. Bei Raumtemperatur liegen also beide Isomere das Ranitidins gleichzeitig vor.[2]
Wirkung
Ranitidin ist ein reversibler, kompetitiver Antagonist des Histamin-H2-Rezeptors (H2-Antihistaminikum). Durch diese Rezeptorblockade wird die histaminabhängige Produktion der Salzsäure und Freisetzung des Verdauungsenzyms Pepsin im Magen vermindert. Ranitidin ist etwa zehnmal stärker in dieser Wirkung als Cimetidin, hat aber dennoch deutlich weniger Nebenwirkungen.
Ranitidin wird nach oraler Aufnahme schnell im Darm resorbiert. Es verteilt sich im Körper, passiert auch die Plazenta und wird auch über die Milch ausgeschieden. Ranitidin wird in der Leber abgebaut und über die Nieren ausgeschieden. Die Wirkungsdauer beträgt etwa 8 bis 12 Stunden.
Anwendung
Ranitidin wird bei Geschwüren und Entzündungen des Magens, Labmagens, des Zwölffingerdarms (Duodenum), bei Gastritis, Ösophagitis und Refluxerkrankungen eingesetzt. Neuere Leitlinien ziehen allerdings Protonenpumpenhemmer den H2-Blockern in der Therapie der Gastritis, Ösophagitis und der Refluxerkrankungen vor. Ranitidin wird zum Beispiel auch zum Magenschutz während einer Cortison-Therapie verwendet sowie auch gelegentlich als Magenschutzmittel bei der Schmerztherapie mit nichtsteroidalen Antirheumatika, da diese häufig – insbesondere bei hohen Dosierungen und/oder bei der Langzeitanwendung – zu Magenschmerzen, Magenblutungen und Sodbrennen (saurem Aufstoßen) führen.
Beim Haushund kann Ranitidin auch zur Behandlung des Gastrinoms (canines Zollinger-Ellison-Syndrom), der Mastozytose und von Mastzell-Tumoren verwendet werden. Bei Katzen hat Ranitidin keinen signifikanten Effekt auf den pH-Wert des Magens.[11]
Kontraindikationen und Nebenwirkungen
Das Mittel darf nicht bei bekannter Unverträglichkeit eingesetzt werden. Bei Funktionsstörungen der Nieren sollte Ranitidin mit Vorsicht angewendet werden.
Obwohl nahezu alle Organe H2-Rezeptoren besitzen, sind die Wirkungen auf andere Organe kaum nachweisbar. Seltene Nebenwirkungen sind beim Menschen psychische Verwirrung und Kopfschmerzen, Agranulozytose, vorübergehende Herzrhythmusstörungen (Bradykardie), Hautausschlag, Übelkeit mit Erbrechen, Durchfall, Stuhlverstopfung und Libidoverlust.
Ranitidin sollte nicht mit Alkohol eingenommen werden, da Ranitidin die Bioverfügbarkeit von Ethanol signifikant erhöht und somit zu einer erheblich höheren Ethanolkonzentration führt. Dies ist auf die Verminderung seiner First-pass Extraktion zurückzuführen.
Nitrosamin-Verunreinigungen
Im September 2019 informierten Arzneimittelbehörden über das Auftreten von N-Nitrosodimethylamin (NDMA) in einigen Arzneimittelchargen mit dem Wirkstoff Ranitidin.[12] Diese als potentiell krebserregend eingestufte Substanz war bereits 2018 im Zusammenhang mit dem „Valsartan-Skandal“ in die Schlagzeilen geraten. Aus Gründen des vorbeugenden Gesundheitsschutzes veranlasste die EMA am 17. September 2019 Rückrufe von allen Ranitidin-haltigen Arzneimitteln, die den Wirkstoff des Herstellers Saraca Laboratories Limited enthielten. Es gab ferner Hinweise, dass auch Wirkstoffe weiterer Hersteller betroffen sein könnten.[13] Die europäische Arzneimittelbehörde EMA leitete daraufhin im September 2019 ein Verfahren ein zur Bewertung der potenziellen Gefährdung von Patienten, die längere Zeit verunreinigte Ranitidin-Präparate eingenommen haben.[14] Im April 2020 empfahl der Ausschuss für Humanarzneimittel (CHMP) der EMA dann das Ruhen aller Zulassungen ranitidinhaltiger Arzneimittel in der EU.[15]
Im eigenen Labor durchgeführten Untersuchungen der US-amerikanischen Versandapotheke Valisure zufolge soll NDMA durch Abbau von Ranitidin unter bestimmten Bedingungen entstehen. Solche könnten etwa die Gegenwart von Luft und Licht während der Lagerung darstellen. Insbesondere soll es in vivo unter Bedingungen, wie sie im menschlichen Magen oder sogar außerhalb des menschlichen Magens bestehen, zur Bildung hoher Mengen von NDMA kommen können. Dabei könnte zusätzlich zu strukturellen Komponenten des Ranitidins (Nitrogruppe, Dimethylaminogruppe) das Enzym DDAH-1 eine Rolle spielen. Eine in den USA gegen die Zulassungsinhaber des ranitidinhaltigen Medikaments Zantac erhobene Sammelklage erhärte die These, dass die potentiellen Risiken von Ranitidin schon seit mindestens 40 Jahren bekannt sein könnten.[16][17][18] Im April 2020 rief in den USA die Zulassungsbehörde Food and Drug Administration (FDA) alle verschreibungspflichtigen und verschreibungsfreien Ranitidin-Arzneimittel vom Markt zurück.[19] Sie sei zu der Einschätzung gelangt, dass die Konzentration des potenziell krebserregenden Stoffs in einigen Präparaten bei Lagerung über Raumtemperatur mit der Zeit steige, was dazu führen könne, dass Verbraucher „unakzeptablen Mengen“ dieser Verunreinigung ausgesetzt seien.[20]
Handelsnamen
Junizac (D, außer Handel), Pylorisin (A), Ranic (A), Ranicux (D), Ranimed (CH), Raniprotect (D), Ranitic (D), Sostril (D), Ulcidin (CH), Ulsal (A), Zantac (A), Zantic (D, CH), zahlreiche Generika (D, A, CH)
Weblinks
- Eintrag zu Ranitidin bei Vetpharm, abgerufen am 11. August 2012.
Einzelnachweise
- H. N. de Armas, Os. M. Peeters, N. Blaton, E. Van Gyseghem, J. Martens, G. Van Haele, G. Van Den Mooter: Solid state characterization and crystal structure from X-ray powder diffraction of two polymorphic forms of ranitidine base. In: J Pharm Sci. 98, 2009, S. 146–158, doi:10.1002/jps.21395.
- T. J. Cholerton, J. H. Hunt, G. Klinkert, M. Martin-Smith: Spectroscopic studies on ranitidine – its structure and the influence of temperature and pH. In: J. Chem. Soc. Perkin Trans. 2, 1984, S. 1761–1766, doi:10.1039/P29840001761.
- The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals. 14. Auflage. Merck & Co., Whitehouse Station, NJ, USA, 2006, ISBN 0-911910-00-X, S. 1396–1397.
- Datenblatt Ranitidine hydrochloride bei Sigma-Aldrich, abgerufen am 29. Mai 2011 (PDF).
- Eintrag zu Ranitidine in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- E. W. Gill, H. R. Ing: 953. Furan and tetrahydrofuran compounds analogous to ganglion-blocking agents of the 3-oxapentane-1 : 5-bistrialkylammonium series. In: J. Chem. Soc. 1958, S. 4728–4731, doi:10.1039/JR9580004728.
- A. R. A. S. Deshmukh, T. I. Reddy, B. M. Bhawal, V. P. Shiralkar, S. Rajappa: Zeolites in organic syntheses: a novel route to functionalised ketene S,N-acetals. In: J. Chem. Soc. Perkin Trans. 1, 1990, S. 1217–1218, doi:10.1039/P19900001217.
- K. Mohanalingam, M. Nethaji, P. K. Das: Second harmonic generation in push-pull ethylenes: Influence of chirality and hydrogen bonding. In: J. Mol. Struct. 378, 1996, S. 177–188, doi:10.1016/0022-2860(95)09180-7.
- Patent US5696275: Process for the manufacture of pharmaceutical grade ranitidine base. Veröffentlicht am 9. Dezember 1997, Erfinder: JAG MOHAN KHANNA, NARESH KUMAR, BRIJ KHERA, PURNA CHANDRA RAY.
- Siegfried Hauptmann: Organische Chemie. 2. Auflage. Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 516.
- S. Šutalo, M. Ruetten, S. Hartnack, C. E. Reusch, P. H. Kook: The effect of orally administered ranitidine and once-daily or twice-daily orally administered omeprazole on intragastric pH in cats. In: Journal of veterinary internal medicine / American College of Veterinary Internal Medicine. Band 29, Nummer 3, Mai-Jun 2015, S. 840–846, doi:10.1111/jvim.12580. PMID 25966746.
- https://www.deutsche-apotheker-zeitung.de/news/artikel/2019/09/13-09-2019/nitrosaminverunireinigungen-ndma-in-ranitidin-gefunden/
- https://www.deutsche-apotheker-zeitung.de/news/artikel/2019/09/17-09-2019/ranitidin-rueckrufe-betapharm-hexal-1-a-pharma-abz-ratiopharm
- https://www.ema.europa.eu/en/news/ema-review-ranitidine-medicines-following-detection-ndma
- Suspension of ranitidine medicines in the EU, EMA, 30. April 2020.
- https://www.deutsche-apotheker-zeitung.de/news/artikel/2019/09/19-09-2019/ranitidin-bildet-tausende-von-nanogramm-ndma-im-magen
- https://www.deutsche-apotheker-zeitung.de/news/artikel/2019/09/17-09-2019/ranitidin-online-apotheke-gab-entscheidenden-nitrosamin-hinweis
- https://www.biospace.com/article/national-class-action-lawsuit-accuses-sanofi-of-concealing-zantac-cancer-risk/
- FDA Requests Removal of All Ranitidine Products (Zantac) from the Market, FDA NEWS RELEASE, 1. April 2020
- A. Mende: Rückruf aller Ranitidin-Präparate, Pharmazeutische Zeitung, 2. April 2020
-Ranitidine_Equilibria_V.2.png.webp)