Migräne
Die Migräne (wie französisch migraine über mittellateinisch hemigrania, einseitiger Kopfschmerz, von altgriechisch ἡμικρανία hēmikranía, deutsch ‚Kopfschmerz auf der einen Seite, Migräne‘,[1] dieses von altgriechisch ἡμι hēmi, deutsch ‚halb‘ sowie altgriechisch κρανίον kraníon, deutsch ‚Hirnschale‘)[2] ist eine neurologische Erkrankung, unter der rund 10 % der Bevölkerung leiden. Sie tritt bei Frauen etwa dreimal so häufig auf wie bei Männern, ist vor der Pubertät aber zwischen den Geschlechtern gleich verteilt[3] und hat ein vielgestaltiges Krankheitsbild. Es ist bei Erwachsenen typischerweise gekennzeichnet durch einen periodisch wiederkehrenden, anfallartigen, pulsierenden und halbseitigen Kopfschmerz, der von zusätzlichen Symptomen wie Übelkeit, Erbrechen, Lichtempfindlichkeit (Photophobie) oder Geräuschempfindlichkeit (Phonophobie) begleitet sein kann. Bei manchen Patienten geht einem Migräneanfall eine Migräneaura voraus, während der insbesondere optische oder sensible Wahrnehmungsstörungen auftreten. Es sind aber auch motorische Störungen möglich. Die Diagnose wird nach Ausschluss anderer Erkrankungen als Ursachen üblicherweise mit Hilfe einer Anamnese gestellt.
| Klassifikation nach ICD-10 | |
|---|---|
| G43.0 | Migräne ohne Aura (Gewöhnliche Migräne) |
| G43.1 | Migräne mit Aura (Klassische Migräne) |
| G43.2 | Status migraenosus |
| G43.3 | Komplizierte Migräne |
| G43.8 | Sonstige Migräne |
| G43.9 | Migräne, nicht näher bezeichnet |
| ICD-10 online (WHO-Version 2019) | |
Epidemiologie
|
|
|
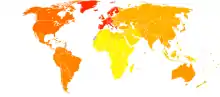
In Deutschland leiden etwa acht Millionen Menschen an einer Migräne.[4] In anderen westlichen Staaten wie beispielsweise anderen europäischen Staaten und den USA wird von einer vergleichbaren Migränehäufigkeit berichtet,[5][6] während in Südamerika, Asien und Afrika geringfügig weniger Menschen unter Migräne leiden.[7]
Statistisch gesehen sind Frauen (Prävalenz 18 %) häufiger als Männer (Prävalenz 6 %) betroffen.
Eine Migräne wird vor allem bei Personen im Alter zwischen 25 und 45 Jahren festgestellt. Die Einjahres-Prävalenz ist in der Altersgruppe zwischen 35 und 39 Jahren am höchsten, und bei 75 % aller Betroffenen liegt der Krankheitsbeginn vor 35 Jahren. Im Alter nimmt die Prävalenz ab. Bei erstmals auftretenden Migränesymptomen bei über 50-Jährigen besteht eine hohe Wahrscheinlichkeit für eine andere Grunderkrankung.[8]
Die Krankheit kann schon im Kindesalter beginnen, neue Studien bringen die Migräne mit der kindlichen Kolik im Säuglingsalter in Verbindung, die auch eine Art der Migräne darstellen könnte.[9] Im letzten Grundschuljahr klagen bis zu 80 % aller Kinder über Kopfschmerzen. Etwa 12 % von ihnen berichten über Beschwerden, die mit der Diagnose einer Migräne vereinbar sind.[10] Bis zur Pubertät erhöht sich der Anteil auf 20 %. Vor der Geschlechtsreife besteht statistisch gesehen kein Unterschied zwischen den Geschlechtern in Bezug auf das Erkrankungsrisiko.[3] Erst mit der Pubertät und synchron zur Entwicklung der Sexualfunktion steigt die Prävalenz beim weiblichen Geschlecht an. Allerdings wird insbesondere bei Männern, die häufiger an nichtklassischen Migräneformen leiden, eine höhere Dunkelziffer angenommen.[11][12]
Auf Grund ihrer Häufigkeit besitzt die Migräne eine volkswirtschaftliche Bedeutung. Jährlich werden in Deutschland etwa 500 Mio. Euro als direkte Kosten von Patienten und Krankenversicherungen für die ärztliche und medikamentöse Behandlung der Migräne ausgegeben. Die durch Arbeitsausfall und Produktivitätseinschränkungen zusätzlich entstehenden indirekten Kosten werden auf über das Zehnfache dieser Summe geschätzt.[13]
Symptome
Während eines Migräneanfalls können verschiedene Phasen mit unterschiedlichen charakteristischen Symptomen durchlaufen werden. Oft kündigt sich ein Anfall durch eine Vorboten- oder Prodromalphase mit Vorbotensymptomen an. Ihr kann eine Phase mit Wahrnehmungsstörungen, die sogenannte Migräneaura, folgen, die insbesondere das Sehen betreffen. In der Kopfschmerzphase bestehen neben den Kopfschmerzen unterschiedliche weitere Symptome wie Übelkeit, Erbrechen, Licht-, Lärm- und Geruchsempfindlichkeit. Bei manchen Patienten überdauert der Migräneanfall das Abklingen der Kopfschmerzen. Diese Phase wird als Rückbildungsphase bezeichnet.
Vorbotenphase
Bei mindestens 30 % der Migränepatienten kündigt sich eine Migräneattacke bereits frühzeitig in Form von Vorbotensymptomen an. Die Vorbotenphase kann wenige Stunden bis zwei Tage einer Migräneattacke vorausgehen und dauert bei den meisten Patienten ein bis zwei Stunden an.[14] Während der Vorbotenphase treten insbesondere psychische, neurologische und vegetative Symptome auf, die sich von denen der Auraphase unterscheiden. Am häufigsten sind Müdigkeit, Geräuschempfindlichkeit und häufiges Gähnen.[15] Vielfach zeigen sich auch Störungen im Magen-Darm-Trakt, die Verstopfungen einschließen können. Charakteristisch ist bei vielen Patienten ein Heißhunger auf bestimmte Nahrungsmittel, der meist als Migräneauslöser fehlinterpretiert wird. Viele Patienten erkennen keinen Zusammenhang zwischen diesen Symptomen und einer deutlich später folgenden Migräneattacke. Daher wird die Häufigkeit dieser Symptome als Vorboten einer Migräneattacke möglicherweise deutlich unterschätzt.[15]
Auraphase
- Visuelle Symptome einer Migräneaura
.jpg.webp) Fortifikation mit an ein Fort erinnernden Zickzack-Strukturen
Fortifikation mit an ein Fort erinnernden Zickzack-Strukturen_1.jpg.webp) Negatives Skotom, lokaler Verlust der Wahrnehmung von Strukturen
Negatives Skotom, lokaler Verlust der Wahrnehmung von Strukturen_1.jpg.webp) Positives Skotom, lokale Wahrnehmung zusätzlicher Strukturen
Positives Skotom, lokale Wahrnehmung zusätzlicher Strukturen_1.jpg.webp) Meist einseitiger Verlust der Wahrnehmung
Meist einseitiger Verlust der Wahrnehmung
Migräne geht in ca. 15 % bis 20 % der Fälle mit einer Aura einher. Es werden in der Auraphase meist visuelle Störungen wie Skotome, Fortifikationen, Verlust des räumlichen Sehens und Unschärfe oder Sensibilitätsstörungen wie der Verlust der Berührungsempfindung oder Kribbeln in den Armen, Beinen und im Gesicht empfunden, die langsam einsetzen und wieder vollständig abklingen. Zusätzlich können Störungen des Geruchsempfindens, Gleichgewichtsstörungen, Sprachstörungen oder andere neurologische Ausfälle auftreten. Die Aura wird von Patient zu Patient anders wahrgenommen und beschrieben. Auren mit stark visueller Ausprägung, wie sie im Rahmen einer Migräne auftreten können, werden auch als Alice-im-Wunderland-Syndrom bezeichnet.[16] Einige berühmte Migränepatienten ließen sich von visuellen Erscheinungen während der Auraphase für ihr künstlerisches Werk inspirieren.[17]
Charakteristisch für Migräneauren ist die Dynamik des Prozesses, beispielsweise das „Wandern“ des Flimmerskotoms im Gesichtsfeld oder Wandern des Kribbelgefühls im Arm oder durch die einzelnen Finger. Auch eine Verschiebung der Aurasymptome, beispielsweise von Seh- über Sensibilitäts- bis hin zu Sprachstörungen und Lähmungserscheinungen, kann beobachtet werden. Diese Dynamik zeigt sich bei Messungen im Gehirn in Form einer wandernden Störungsfront (Streudepolarisierung). Die Dynamik der Symptome sowie deren langsames Einsetzen und Abklingen sind ein wichtiges Unterscheidungsmerkmal zu anderen neurologischen Erkrankungen, insbesondere gegenüber dem Schlaganfall. Die Aura hat keinerlei schädigende Auswirkungen auf das Hirngewebe, ihre Anzeichen sind lediglich vorübergehend und dauern in der Regel bis zu 60 Minuten.
Auren können in Einzelfällen auch ohne eine nachfolgende Kopfschmerzphase auftreten.
Kopfschmerzphase
Der Kopfschmerz tritt in der Kopfschmerzphase meistens halbseitig (etwa 70 % der Fälle) insbesondere im Bereich von Stirn, Schläfe und Auge auf. Er ist meist pulsierend und nimmt bei körperlicher Betätigung an Intensität zu, während Ruhe und Dunkelheit zur Linderung der Kopfschmerzen beitragen. Die Kopfschmerzen des Migräneanfalls werden oft von zusätzlichen Symptomen wie Appetitlosigkeit (> 80 %), Übelkeit (80 %), Erbrechen (40 % bis 50 %) sowie Photophobie (60 %), Phonophobie (50 %) und seltener Osmophobie (Geruchsempfindlichkeit, < 10 % bis 30 %) begleitet.[18] Der Kranke ist blass und erträgt äußere Einflüsse wie Licht und Lärm schlecht, da diese seine Beschwerden noch verstärken. Die Dauer der Kopfschmerzphase variiert zwischen 60 Minuten und bis zu drei Tagen in Abhängigkeit von Patient und Migräneform. Dauert der Anfall länger, wird dies als Status migraenosus bezeichnet. Kinder haben kürzere Migräneattacken mit eher beidseitiger Lokalisation in der Stirn-Schläfenregion. Als Begleitsymptom treten bei Kindern und Jugendlichen häufiger Geruchsempfindlichkeit, Schwindel und Gleichgewichtsstörungen auf.[10] Einige Sonderformen der Migräne können ohne Kopfschmerz auftreten.
Rückbildungsphase
In der Rückbildungsphase nehmen der Migränekopfschmerz und die Begleitsymptome bis zur vollständigen Erholung langsam ab. Der Patient fühlt sich müde und abgespannt. Diese Phase kann bis zu 24 Stunden dauern.
Auslösende Faktoren
Da die Prävalenz der Migräne in den Industrieländern in den letzten 40 Jahren um den Faktor zwei bis drei zugenommen hat, kann angenommen werden, dass Umweltfaktoren und Lebensstil eine wesentliche Rolle bei der Entstehung der Migräne spielen. Migräne kann bei empfindlichen Personen durch spezielle Situationen oder Substanzen, sogenannte Trigger (Schlüsselreize), ausgelöst werden. Dazu zählen insbesondere hormonelle Faktoren, Schlaf, Stress, Lebensmittel und Umweltfaktoren.[19] Diese Auslösefaktoren sind jedoch individuell sehr unterschiedlich und können mit Hilfe eines Kopfschmerztagebuchs in Erfahrung gebracht werden.
Zu den häufigsten Auslösern einer Migräne zählen Stress, unregelmäßiger Biorhythmus mit Schlafmangel oder zu viel Schlaf und Umweltfaktoren.[19] Bei einigen Migränepatienten folgt ein Migräneanfall erst in der Poststress-Entspannungsphase („Wochenendmigräne“). Neben Geruchsreizen werden oft Wetterschwankungen als äußere Faktoren genannt, die eine Migräneattacke auslösen können. Dabei ist weniger der Thermometerwert relevant, als die gefühlte Temperatur. Diese setzt sich aus Luftfeuchte, Lufttemperatur, Strahlungswärme, Wärmereflexion und Wind zusammen.[20]
Einer der wichtigsten Triggerfaktoren bei Frauen sind hormonelle Schwankungen. Über die Hälfte aller weiblichen Migränepatienten gibt den Menstruationszyklus als Auslöser einer Migräne an. Ein Migräneanfall kann insbesondere während der späten lutealen Phase des Zyklus oder während der einnahmefreien Zeit bei der Empfängnisverhütung mit oralen Kontrazeptiva auftreten.[21]
Etwa zwei Drittel aller Migränepatienten sehen einen Zusammenhang zwischen dem Konsum bestimmter Lebens- und Genussmittel und dem Auslösen eines Migräneanfalls. Als wichtigster Migränetrigger dieser Gruppe gilt Alkohol. Darüber hinaus werden insbesondere glutamat-, tyramin-, histamin- und serotoninhaltige Lebens- und Genussmittel wie Rotwein, Schokolade und Käse als Auslösefaktoren genannt. Auch Kaffee wird häufig als ein Auslösefaktor empfunden.[19] Von vielen Patienten wird jedoch ein gesteigerter Appetit auf bestimmte Lebensmittel, der ein bekannter Vorbote einer bereits sich anbahnenden Migräneattacke ist, als Auslösefaktor fehlinterpretiert. Somit werden viele der ernährungsbedingten Faktoren als Ursache überbewertet. Wichtiger erscheint eine regelmäßige Ernährung ohne Auslassen von Mahlzeiten.
Auch einige Arzneimittel, insbesondere Stickstoffmonoxid freisetzende, gefäßerweiternde Substanzen (Vasodilatatoren), können einen Migräneanfall induzieren.[22]
Andererseits besteht durch die retrospektive Suche nach Triggern die Möglichkeit einer kognitiven Verzerrung, vor allem kommt es oft zu einem Recall Bias und einem Attributionsfehler. Falsche Zuordnungen von vermeintlichen Triggern sind häufig, und in einer Studie wurde bei 27 Probanden nur bei dreien durch eine Exposition des vermeintlichen Triggers tatsächlich eine Migräneattacke ausgelöst.[8]
Einteilung und Klassifikation
| Klassifikation der Migräne gemäß der Richtlinie der IHS[23] | |
|---|---|
| 1. | Migräne ohne Aura (Gewöhnliche Migräne) |
| 2. | Migräne mit Aura (Klassische Migräne) |
| 2.1. | Typische Aura mit Migränekopfschmerz |
| 2.2. | Typische Aura mit Nicht-Migränekopfschmerz |
| 2.3. | Typische Aura ohne Kopfschmerz |
| 2.4. | Familiäre hemiplegische Migräne |
| 2.5. | Sporadische hemiplegische Migräne |
| 2.6. | Migräne vom Basilaristyp |
| 3. | Periodische Syndrome in der Kindheit, die im Allgemeinen Vorläufer einer Migräne sind |
| 3.1. | Zyklisches Erbrechen |
| 3.2. | Abdominelle Migräne |
| 3.3. | Gutartiger paroxysmaler Schwindel in der Kindheit |
| 4. | Retinale Migräne |
| 5. | Migränekomplikationen |
| 5.1. | Chronische Migräne |
| 5.2. | Status migränosus |
| 5.3. | Persistierende Aura ohne Hirninfarkt |
| 5.4. | Migränöser Infarkt |
| 5.5. | Zerebrale Krampfanfälle, durch Migräne getriggert |
| 6. | Wahrscheinliche Migräne (migräneartige Störung) |
| 6.1. | Wahrscheinliche Migräne ohne Aura |
| 6.2. | Wahrscheinliche Migräne mit Aura |
| 6.3. | Wahrscheinliche chronische Migräne |
Die Migräne ist wie der Spannungskopfschmerz und der Cluster-Kopfschmerz eine primäre Kopfschmerzerkrankung. Das heißt, sie ist nicht die offensichtliche Folge anderer Erkrankungen wie Hirntumoren, Hirntraumata, Hirnblutungen oder Entzündungen.
Bereits Galen von Pergamon unterschied mindestens 4 verschiedene Kopfschmerzarten, eine davon bezeichnete er als "Hemikrania" (pulsierend, einseitig, paroxysmal), aus dem sich der Begriff Migräne ableitet. Jason Pratensis (1486–1558) unterschied in seinem Buch "De cerebri morbis" 9 unterschiedliche Kopfschmerzen, u. a. auch die Hemikrania. Thomas Willis (1621–1675) unterschied die Kopfschmerzen nach Lokalisation und Zeitmuster. 1962 wurde von einem ad-hoc Komitee des NINDS auf Betreiben von Harold Wolff (1898–1962) in den USA die erste systematische Klassifikation herausgegeben mit 15 Kopfschmerzformen.[24] Seit 1988 erfolgt die Klassifikation der Migräne und migräneartiger Erkrankungen rein phänomenologisch gemäß den Richtlinien der International Headache Society (IHS) primär anhand des Auftretens oder der Abwesenheit einer Migräneaura. Edition 1 der ICHD erschien 1988; Edition 2 in 2004, Edition 3 in 2018. e[23][25]
Migräne ohne Aura (Gewöhnliche Migräne)
Die Migräne ohne Aura ist mit etwa 80 % bis 85 % der Migräneanfälle die häufigste Form der Migräne. Von einer Migräne ohne Aura kann gesprochen werden, wenn in der Krankengeschichte mindestens fünf Migräneattacken auftraten, bei denen mindestens zwei der vier Hauptkriterien erfüllt sind und der Kopfschmerzphase keine Aura vorausging:
- Hemikranie (einseitiger Kopfschmerz), Seitenwechsel ist möglich
- mittlere bis starke Schmerzintensität
- pulsierender oder pochender Schmerzcharakter
- Verstärkung durch körperliche Aktivität
Zusätzlich muss mindestens ein vegetatives Symptom, also Übelkeit und optional Erbrechen oder Phono- und Photophobie, vorhanden sein.[23] Wenngleich eine Auraphase fehlt, können Vorboten wie Unruhe, Erregungszustände und Stimmungsveränderungen auftreten. Diese zeigen sich einige Stunden bis zwei Tage vor der eigentlichen Attacke. Der Kopfschmerz ist in 2/3 der Fälle halbseitig und pulsierend, verstärkt sich bei körperlicher Aktivität und kann unbehandelt zwischen 4 Stunden und 3 Tagen andauern. Begleitsymptome wie Übelkeit oder Erbrechen (80 %), Lichtempfindlichkeit (60 %), Geräuschempfindlichkeit (50 %) und Geruchsempfindlichkeit (< 30 %) können auftreten.[26] Bei Kindern kann die Migränedauer verkürzt sein. Dafür ist bei ihnen der Kopfschmerz meist beidseitig lokalisiert. Bei Frauen weist die Migräne ohne Aura oft eine strenge Beziehung zur Menstruation auf. Leitlinien seit 2000 unterscheiden daher zwischen einer nicht-menstruellen, einer menstruationsassoziierten und einer rein menstruellen Migräne ohne Aura.[27]
Migräne mit Aura (Klassische Migräne)
Eine Migräne mit Aura ist geprägt durch reversible neurologische Symptome, die Sehstörungen mit Skotomen (Gesichtsfeldausfällen), Lichtblitzen oder Wahrnehmen von bunten, schillernden, gezackten Linien oder Flimmern, Gefühlsstörungen mit Kribbeln oder Taubheitsgefühl und Sprachstörungen einschließen. Gelegentlich (6 %) kommt es auch zu motorischen Störungen bis hin zu Lähmungserscheinungen. Diese Aurasymptome halten im Durchschnitt 20 bis 30 Minuten, selten länger als eine Stunde an. Während der Aura bis spätestens 60 Minuten danach tritt zumeist eine Kopfschmerzphase ein, die der Migräne ohne Aura entspricht und von Symptomen wie Übelkeit, Erbrechen, Lichtempfindlichkeit und Geräuschempfindlichkeit begleitet sein kann. Diese Kopfschmerzphase kann wie im Falle der typischen Aura ohne Kopfschmerz vollständig fehlen.
Nach den Kriterien der IHS wird von einer Migräne mit Aura gesprochen, wenn die folgenden Kriterien erfüllt sind:[23]
- vollständig reversible Sehstörungen, Gefühlsstörungen oder Sprachstörungen
- sich langsam entwickelnde oder ablösende Aurasymptome mit einer Dauer von 5 bis 60 Minuten
Typische Aura mit Migränekopfschmerz
Die typische Aura mit Migränekopfschmerz ist die häufigste Form der Migräne mit Aura. Daneben folgt bei vielen Patienten der Aura ein Kopfschmerz, der nicht den Kriterien eines Migränekopfschmerzes entspricht. Die Kopfschmerzen sind dann nicht pulsierend, halbseitig und begleitet von zusätzlichen Symptomen wie Übelkeit, Erbrechen, Licht- und Geräuschempfindlichkeit.[23]
Typische Aura ohne Kopfschmerz
Während den meisten Migräneauren ein Kopfschmerz folgt, tritt bei einer Minderheit von Patienten eine Aura, die oben genannten Kriterien entspricht, ohne Kopfschmerz auf. Dieser Migränetyp ist besonders bei Männern verbreitet. Darüber hinaus kann bei Migränepatienten mit zunehmendem Alter eine typische Aura mit Migränekopfschmerz in eine typische Aura ohne Migränekopfschmerz übergehen.[23]
Familiäre hemiplegische Migräne
Neben den oben genannten typischen Symptomen einer Migräne mit Aura sind bei der seltenen, aber familiär gehäuft auftretenden familiären hemiplegischen Migräne oft motorische Störungen zu beobachten. Auch können Symptome, die charakteristisch für eine Migräne vom Basilaristyp sind, sowie Bewusstseinsstörungen bis hin zum Koma, Fieber und Verwirrtheitszuständen auftreten. Das wichtigste Kriterium für die Diagnose ist, dass wenigstens ein Verwandter ersten oder zweiten Grades ebenfalls Migräneattacken mit den Symptomen einer familiären hemiplegischen Migräne hat.[23] Als eine Ursache für die familiäre hemiplegische Migräne konnten bisher drei Gendefekte mit Lokalisation auf den Chromosomen 1, 2 und 19 gefunden werden. Anhand der Lage der Gendefekte kann unterschieden werden zwischen den Typen I (FMH1), II (FMH2) und III (FMH3) der familiären hemiplegischen Migräne.[28]
Sporadische hemiplegische Migräne
Die sporadische hemiplegische Migräne gleicht in ihren Symptomen der familiären hemiplegischen Migräne. Das wichtigste Unterscheidungskriterium gegenüber der familiären hemiplegischen Migräne ist das Fehlen von vergleichbaren Fällen in der Verwandtschaft ersten und zweiten Grades. Auch können der sporadischen hemiplegische Migräne keine Gendefekte als Ursache zugeordnet werden. Von einer sporadischen hemiplegischen Migräne sind insbesondere Männer betroffen. Ihre Häufigkeit ist mit der der familiären hemiplegischen Migräne vergleichbar.[23]
Migräne vom Basilaristyp
Die Migräne vom Basilaristyp, auch Basilarismigräne genannt, tritt gehäuft bei jungen Erwachsenen auf. Die neurologischen Symptome einer Migräne vom Basilaristyp können von den zuvor genannten Aurasymptomen abweichen. Charakteristische Symptome sind Sprachstörungen, Schwindel, Tinnitus, Hörminderung, Doppelbilder, Sehstörungen gleichzeitig sowohl im temporalen als auch im nasalen Gesichtsfeld beider Augen, Ataxie, Bewusstseinsstörung oder gleichzeitige beidseitige Parästhesien.[23] In Einzelfällen kommt es zu einem locked-in-Syndrom: vollständige Bewegungslosigkeit bei wachem Bewusstsein für die Dauer von 2 bis 30 Minuten, gelegentlich sind noch vertikale Augenbewegungen möglich (Bickerstaff-Syndrom). Weiterhin zählt das Alice-im-Wunderland-Syndrom zu den möglichen Symptomen. Sowohl die Aurasymptome als auch der Migränekopfschmerz werden meist beidseitig wahrgenommen. Eine Beteiligung der namensgebenden Arteria basilaris wird zwar vermutet, ist aber nicht gesichert.
Retinale Migräne
Charakteristisch für eine retinale Migräne sind obligatorisch einseitige auraähnliche visuelle Phänomene wie Skotome, Flimmern oder Blindheit, die sich auf die Zeit der Migräneattacke beschränken. Während dieser Sehstörungen oder bis zu 60 Minuten danach setzt die Migränekopfschmerzphase ein.[23]
Wahrscheinliche Migräne
Von einer wahrscheinlichen Migräne wird gemäß IHS gesprochen, wenn mit Ausnahme eines Kriteriums alle Kriterien für die Diagnose einer Migräne ohne Aura oder einer Migräne mit Aura erfüllt sind. Eine Einstufung als eine wahrscheinliche Migräne sollte auch erfolgen, wenn die zuvor genannten Kriterien einer Migräne mit oder ohne Aura erfüllt wurden, aber auch akut Medikamente in einer Menge eingenommen wurden, die einen medikamenteninduzierten Kopfschmerz nicht ausschließen.[23]
Chronische Migräne
Leidet ein Patient an mehr als 15 Tagen im Monat über mehrere Monate (≥ 3) hinweg unter einer Migräne, so spricht man von einer chronischen Migräne. Die chronische Migräne ist oft eine Komplikation der Migräne ohne Aura und wird in zunehmenden Fällen beobachtet. Von einer chronischen Migräne abzugrenzen ist der ebenfalls chronische Kopfschmerz bei Medikamenteneinnahme, der beispielsweise durch einen Übergebrauch von Analgetika induziert wird.[23]
Status migraenosus
Bei einem Status migraenosus geht ein Migräneanfall unmittelbar in den nächsten über oder die Migränesymptome nehmen nach 72 Stunden nicht ab.[23] Dem Patienten bleibt kaum Erholungszeit, und der Leidensdruck ist dementsprechend hoch.
Migränöser Infarkt
Der migränöse Infarkt ist ein Hirninfarkt im Ablauf einer typischen Migräneattacke mit Aura. Charakteristischerweise treten ein oder mehrere Aurasymptome auf, die länger als 60 Minuten andauern. Mit Hilfe bildgebender Verfahren ist ein ischämischer Schlaganfall in relevanten Gehirnteilen nachweisbar. Abzugrenzen von einem migränösen Infarkt sind Hirninfarkte aus anderen Gründen bei gleichzeitig bestehender Migräne und Hirninfarkte aus anderen Gründen mit migräneähnlichen Symptomen. Betroffen von einem migränösen Infarkt sind vor allem Frauen unter 45 Jahren.[23]
Persistierende Aura ohne Infarkt
Die seltene persistierende Aura ohne Infarkt ist gekennzeichnet durch Aurasymptome, die länger als eine Woche anhalten, ohne dass ein Hirninfarkt radiologisch nachgewiesen werden kann. Die Aurasymptome werden meist beidseitig wahrgenommen.[23] Im Gegensatz zum migränösen Infarkt wird das Gehirn nicht dauerhaft geschädigt.
Migralepsie
Unter Migralepsie werden zerebrale Krampfanfälle verstanden, die durch eine Migräne getriggert werden. Sie ist eine Komplikation einer Migräne mit Aura, bei der die komplexen Verbindungen zwischen Migräne und Epilepsie deutlich werden. Ein epileptischer Anfall wird während oder innerhalb von 60 Minuten nach einer Auraphase ausgelöst.[23]
Visual Snow
Visual Snow ist ein Beschwerdekomplex, welcher epidemiologisch assoziiert zur Migräne mit Aura scheint. Das Krankheitsbild geht mit einem anhaltenden Bildrauschen im gesamten Gesichtsfeld, ähnlich einer persistierenden Migräneaura, einher, weshalb es häufig als solche fehlinterpretiert wird.[29]
Diagnose
Die Migräne ist eine Erkrankung, die auf Basis der Beschwerden diagnostiziert wird. Die Diagnose einer Migräne erfolgt durch eine Befragung des Patienten mit Erhebung der Krankengeschichte (Anamnese). Zu diesem Zweck können auch ein Kopfschmerztagebuch geführt und der Grad der Beeinträchtigung (Migraine Disability Assessment Score) dokumentiert werden. Eine allgemeine körperliche Untersuchung trägt über den Ausschluss anderer Erkrankungen als Kopfschmerzursache ebenfalls der Diagnosefindung bei und spielt eine wichtige Rolle bei der Auswahl der Medikation. Laboruntersuchungen und apparative Untersuchungsmethoden tragen in der Praxis nicht zur direkten Migränediagnose bei, sondern sind nur dann erforderlich, wenn eine andere Erkrankung zweifelsfrei ausgeschlossen werden soll.
In erster Linie muss zwischen der Diagnose eines sekundären Kopfschmerzes und einer primären Kopfschmerzerkrankung unterschieden werden. Ein sekundärer Kopfschmerz, der Folge anderer Erkrankungen ist und häufig im Zusammenhang mit Tumoren, Traumata, Blutungen und Entzündungen beobachtet werden kann, muss auf jeden Fall dann in Betracht gezogen werden, wenn Alarmzeichen auftreten. Dazu zählen beispielsweise erstmaliges und plötzliches Auftreten, insbesondere bei kleinen Kindern oder bei Patienten im fortgeschrittenen Alter, kontinuierliche Zunahme der Beschwerden oder Fieber, Hypertonie oder Krampfanfälle als Begleitsymptome. Zu diesem Zweck können neben allgemeinen körperlichen Untersuchungen auch Laboruntersuchungen und apparative Untersuchungen durchgeführt werden. Ist eine sekundäre Ursache ausgeschlossen, kann im Anschluss mit Hilfe der Anamnese zwischen einer Migräne und anderen primären Kopfschmerzformen wie Spannungskopfschmerz und Cluster-Kopfschmerz unterschieden werden. Beispielsweise ist eine Verstärkung der Symptome durch körperliche Aktivität ein wichtiges Unterscheidungsmerkmal zwischen einer Migräne und einem Cluster-Kopfschmerz.
Pathophysiologie
Migräneanfall
Der Pathomechanismus des Migräneanfalls ist nicht aufgeklärt. Mit Hilfe von verschiedenen sich ergänzenden Hypothesen wird versucht, die Entstehung einer Migräne zu beschreiben. Die Neurotransmitter Serotonin (5-HT) und Glutamat, das Calcitonin Gene-Related Peptide (CGRP) und Stickstoffmonoxid (NO) nehmen in diesen Theorien eine wichtige Rolle ein.
Vaskuläre Hypothese
Die vaskuläre Hypothese beruht auf der klassischen Beobachtung, dass Blutgefäße des Kopfes während eines Migräneanfalls erweitert sind.[30] Die beobachtete Erweiterung der Blutgefäße wird als ein Bestandteil eines Reflexes angesehen (trigeminovaskulärer Reflex).[31] In den Wänden dieser Blutgefäße befinden sich Schmerz- und Dehnungsrezeptoren (freie Nervenendigungen) des Nervus trigeminus, die im Falle eines Migräneanfalles aktiviert werden. Eine Projektion der Reizung des Nervus trigeminus über Dehnungsrezeptoren oder Chemorezeptoren der Blutgefäße im unteren Abschnitt des Nucleus spinalis nervi trigemini und darüber hinaus in die Großhirnrinde wird für das Schmerzempfinden verantwortlich gemacht. Für die beobachteten Begleitsymptome der Migräne wird eine Projektion in den Hypothalamus (Photophobie, Phonophobie) und in die Chemorezeptoren-Triggerzone (Übelkeit, Erbrechen) diskutiert.
Der pulsierende Charakter des Migränekopfschmerzes lässt sich am besten mit der vaskulären Hypothese erklären. Gestützt wird sie auch durch die Beobachtung, dass sich je nach Prädisposition durch Blutgefäße erweiternde Substanzen (Vasodilatatoren) wie Nitroglycerin eine Migräne oder ein migräneartiger Kopfschmerz auslösen lässt.[32] Eine mechanische Kompression der Blutgefäße hingegen führt zu einer Reduktion der Migränesymptome.[30] Auch die Migränewirksamkeit aller spezifischen Migränetherapeutika einschließlich der Mutterkornalkaloide, Triptane und CGRP-Rezeptorantagonisten wird zumindest zum Teil mit einer Kontraktion der Blutgefäße des Kopfes erklärt. Mutterkornalkaloide und Triptane führen über eine Aktivierung von Serotonin-Rezeptoren des Typs 5-HT1B an der Oberfläche der Blutgefäße direkt zu einer Gefäßkontraktion. CGRP-Antagonisten hemmen über eine Kompetition an CGRP-Rezeptoren die blutgefäßerweiternden Eigenschaften des Calcitonin Gene-Related Peptides.
Da die Aurasymptome und die Begleitsymptome der Migräne durch die vaskuläre Hypothese nicht oder nur unzureichend erklärt werden können, wird die Migräne heute nicht mehr als eine ursächlich vaskuläre Erkrankung angesehen.
Übererregbarkeitshypothese
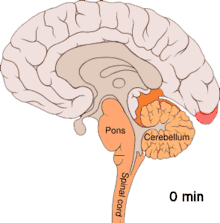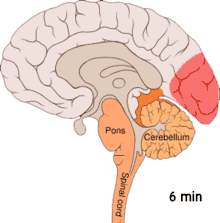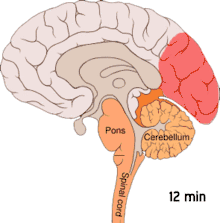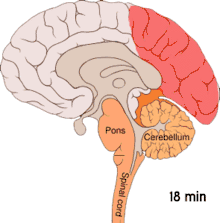
Die Beobachtung, dass Patienten, die regelmäßig an Migräne leiden, eine erhöhte Erregbarkeit der Hirnrinde des Hinterhauptslappens (occipitaler Cortex) zeigen, führte zur Postulierung einer weiteren Hypothese (Übererregbarkeitshypothese). Diese Übererregbarkeit ist an eine Freisetzung von Kaliumionen in den Extrazellularraum gekoppelt. Kaliumionen führen zu einer Depolarisation, die sich über einen Bereich der Hirnrinde ausbreitet (Streudepolarisierung oder Cortical spreading depression). Eine Ausbreitung dieser Depolarisation in das Sehzentrum wird mit der Entstehung einer visuellen Migräneaura in Verbindung gebracht. Der Migränekopfschmerz wird nach dieser Hypothese im einfachsten Fall mit einer Projektion in bestimmte Anteile des sogenannten sensorischen Trigeminuskerns erklärt.[33] Alternativ dazu können hohe Konzentrationen freigesetzter Kaliumionen sowie Glutamat und Stickstoffmonoxid direkt einen Migränekopfschmerz auslösen.
Die auffälligen Parallelen zwischen der Entstehung und Ausbreitung einer Migräne und der Pathophysiologie eines epileptischen Anfalls werden am besten durch die Übererregbarkeitshypothese beschrieben.
Hypothese der neurogenen Entzündung
Die Hypothese der neurogenen Entzündung beruht auf der während eines Migräneanfalls nachgewiesenen Freisetzung von entzündungsvermittelnden Botenstoffen (Entzündungsmediatoren) wie Calcitonin Gene-Related Peptide (CGRP), Substanz P und Neurokinin A aus Nervenendigungen des fünften Hirnnerves (Nervus trigeminus).[34] Insbesondere das CGRP, das während einer Migräneattacke vermehrt im Blutplasma nachgewiesen werden kann,[35] spielt eine zentrale Rolle und bewirkt eine sogenannte „sterile neurogene Entzündung“ mit einer Aktivierung von Mastzellen. Als Folge können eine Erweiterung der Blutgefäße (Vasodilatation), eine Rekrutierung von Leukozyten und eine Gefäßpermeabilitätserhöhung mit Ödembildung beobachtet werden.[36] Eine Aktivierung von Matrixmetalloproteasen kann zusätzlich die Durchlässigkeit der Blut-Hirn-Schranke für Proteine und Peptide steigern.[37] Sowohl die Vasodilatation als auch die Permeabilitätserhöhung mit Ödembildung werden als Ursachen des Migränekopfschmerzes diskutiert.
Trigemino-vaskuläres System
Bei der Genese von Migräne-Attacken sind mehrere Signalmoleküle beteiligt, die erstens starke Vasodilatatoren sind, also die Gefäße erweitern, und zweitens im trigemino-vaskulären System weitverbreitet sind:
- CGRP (Calcitonin gene-related peptide)
- PACAP-38 (Pituitary adenylate cyclase-activating peptide 38)
- Stickstoffmonoxid (NO, nitric oxide)
In Expositionsversuchen konnte mit diesen drei Vasodilatatoren bei Migräne-Patienten sehr häufig eine Migräneattacke bei intravenöser Gabe ausgelöst werden, während Probanden ohne Migräne keine oder allenfalls leichte Kopfschmerzen beklagten. Nitroglycerin als NO-Träger löste in 80 %, CGRP in 57 % und PACAP-38 in 58 % eine Migräne bei Migränepatienten aus. Diese Signalmoleküle aktivieren intrazellulär Signalwege über Cyclisches Adenosinmonophosphat (cAMP) für Stickstoffmonoxid und Cyclisches Guanosinmonophosphat (cGMP) für CGRP und PACAP-38 als Second Messenger.[8]
Darüber hinaus konnten Medikamente, die den Abbau der Second Messenger cAMP und cGMP blockierten, in über 80 % eine Migräne-Attacke bei Migräne-Patienten auslösen. Möglicherweise sind Aktivierungen dieser cAMP- und cGMP-Signalwege im trigemino-vaskulären System der gemeinsame neurochemische Mechanismus einer Migräne-Attacke. Beide Botenstoffe führen zu einer vermehrten Öffnung ATP-sensitiver Kaliumkanäle. Dies führte zu der Hypothese, dass die Modulation nozizeptiver Übertragung durch Ionenkanäle, vor allem durch Kaliumkanäle, die gemeinsame Endstrecke der Auslösung einer Migräne-Attacke darstellen könnte. So löst die intravenöse Gabe des Kaliumkanalöffners Levcromakalim bei allen Migräne-Patienten eine Migräne-Attacke aus.[8]
Demnach wäre es plausibel, dass durch Trigger ATP-sensitive Kaliumkanäle auf den Zellen der glatten Gefäßmuskulatur der intrakraniellen Arterien geöffnet werden, dies eine Vasodilatation auslöst, davon die perivaskulären trigeminalen Afferenzen aktiviert werden und nozizeptive Impulse übermitteln. Diese könnten durch weitere sekundäre und tertiäre trigeminale Afferenzen in kortikalen und subkortikalen Hirnbereichen dann die Schmerzwahrnehmung der Migräne-Attacke auslösen. Dies würde auch die Beobachtung einer Erhöhung der extrazelluläre Konzentration positiv geladener Ionen, nicht nur von Kaliumionen erklären, die die trigeminalen Rezeptoren aktivierten. Dass Ionenkanäle an der Modulation phasenweiser Schmerzsyndrome beteiligt sind, ist bereits bei anderen episodischer Schmerzsyndrome, so beim familiären episodischen Schmerzsyndrom (familial episodic pain syndrome) gezeigt worden.[8]
Bei einer Aura kommt es zu einer wellenförmigen Ausbreitung einer Depolarisationsbewegung (Übererregbarkeitshypothese), die mit einer Öffnung neuronaler Pannexin-1-Kanäle verbunden ist. Dies wiederum führt zur Freisetzung von Entzündungsmediatoren, wie Stickstoffmonoxid und Prostanoide, die die intrakraniellen Gefäße dilatieren (weiten) und dadurch wiederum Kaliumkanäle öffnen könnten (Hypothese der neurogenen Entzündung).[8]
Genetische Ursachen
Eine familiäre Häufung besteht oft, und Schätzungen führen 42 % auf ein erbliches Risiko zurück. Es gibt seltene monogenetische familiäre Migräne-Syndrome, vor allem die familiäre hemiplegische Migräne, aber in der Regel liegt ein polygenetisches Risikoprofil vor, es sind also mehrere Genvarianten involviert. Genomweite Assoziationsstudien haben 38 Suszeptibilitätsgene identifiziert, die mit einem erhöhten Migränerisiko einhergehen. Vor allem waren Gene involviert, die die Glatte Muskulatur an Gefäßen und Eingeweiden ("viszeral") steuern, in einer weiteren Arbeit zeigte sich eine Anreicherung der genetischen Marker in Nervengeweben.[8]
Für ein gehäuftes Auftreten der Migräne mit Aura bei Patienten mit einem persistierenden Foramen ovale werden ebenfalls genetische Defekte als Ursachen beider Krankheiten diskutiert. Gendefekte werden auch als Ursachen für eine Komorbidität von Migräne und Depression vermutet.[38]
Familiäre hemiplegische Migräne
Dies ist eine seltene monogenetische Erbkrankheit, die mit Migränesymptomen einhergeht. Es wurden mindestens drei verschiedene Gendefekte als mögliche Ursachen identifiziert.[39][40] Beim Typ I der familiären hemiplegischen Migräne (FHM1) finden sich Mutationen im CACNA1A Gen auf dem Chromosom 19. Dieses Gen codiert eine Untereinheit des spannungsabhängigen L-Typ-Calciumkanals. Mutationen im ATP1A2 Gen auf dem Chromosom 1, welches eine Untereinheit der Natrium-Kalium-ATPase, eine Ionenpumpe, codiert, sind die genetische Ursache für den Typ II (FHM2). Die Ursache für den Typ III der familiären hemiplegischen Migräne (FHM3) ist ein durch Mutationen im SCN1A-Gen auf dem Chromosom 2 verursachter Defekt eines spannungsabhängigen Natriumkanals.[28] Alle drei beschriebenen Gendefekte werden auch mit dem Auftreten einer Epilepsie assoziiert.[41]
Behandlung und Vorbeugung
Die Deutsche Gesellschaft für Neurologie (DGN) und die Deutsche Migräne- und Kopfschmerzgesellschaft (DMKG) haben im Mai 2018 neue Empfehlungen für die Migräne-Therapie und Prophylaxe vorgelegt. Die S1-Leitlinie Therapie der Migräneattacke und Prophylaxe der Migräne ist online aufrufbar.[42]
Die Migräne ist eine Erkrankung, die derzeit durch medizinische Maßnahmen nicht heilbar ist. Die Intensität der Migräneanfälle und die Anfallshäufigkeit kann durch geeignete Maßnahmen reduziert werden.
Akuttherapie
Nach Empfehlung der Deutschen Migräne- und Kopfschmerz-Gesellschaft (DMKG) können zur Akutbehandlung des Migränekopfschmerzes einerseits unspezifisch Schmerz- und Entzündungsprozesse hemmende Schmerzmittel aus der Gruppe der Nichtopioid-Analgetika (zum Beispiel Acetylsalicylsäure, Paracetamol und Ibuprofen) und andererseits spezifische Migränetherapeutika aus den Gruppen der Triptane (zum Beispiel Sumatriptan, Naratriptan und Zolmitriptan) als Mittel der ersten Wahl eingesetzt werden.
Nichtopioid-Analgetika
Die Nichtopioid-Analgetika Acetylsalicylsäure, Ibuprofen, Naproxen, Diclofenac und Paracetamol sind insbesondere bei einem leichten bis mittelschweren Migräneanfall indiziert. Auch eine Kombination aus Acetylsalicylsäure, Paracetamol und Coffein, die wirksamer ist als die Einzelsubstanzen[43] oder Ibuprofen,[44] wird von der DMKG empfohlen.[18][45] Bei mittleren bis schweren Anfällen zeigen Triptane eine hohe Wirksamkeit.[46] Die Migränewirksamkeit von Phenazon und Metamizol gilt hingegen als weniger gut dokumentiert. In klinischen Studien haben sich darüber hinaus die COX-2-Hemmer Valdecoxib und das auf Grund seiner Herz-Kreislauf-Nebenwirkungen vom Markt genommene Rofecoxib als effektiv zur Behandlung akuter Migräneattacken erwiesen.[47][48] Eine arzneimittelrechtliche Zulassung für die Verwendung als Migränetherapeutika besteht jedoch nicht. Generell besteht bei länger andauernder oder gar dauerhafter Anwendung von Nichtopioid-Analgetika die Gefahr eines medikamenteninduzierten Kopfschmerzes.
Um schnell zu wirken und die ohnehin bei Migräne oft bestehende Übelkeit nicht zusätzlich zu verstärken, werden viele Nichtopioid-Analgetika in einer schnell verfügbaren und als magenfreundlich geltenden Darreichungsform angeboten. Dazu zählen beispielsweise gepufferte Brausetabletten. Ist eine orale Anwendung eines Nichtopioid-Analgetikums nicht möglich, so steht beispielsweise Paracetamol als Zäpfchen (Suppositorium) zur rektalen Anwendung zur Verfügung. Metamizol, Acetylsalicylsäure sowie Paracetamol sind darüber hinaus auch als intravenöse Infusion erhältlich.
Triptane
Seit den 1990er Jahren stehen 5-HT1B/1D-Rezeptoragonisten aus der Gruppe der Triptane zum Kupieren von Migräneanfällen zur Verfügung.[49] Deren Vertreter unterscheiden sich voneinander in ihrer Pharmakokinetik, insbesondere in ihrer Bioverfügbarkeit, ihrer ZNS-Gängigkeit und ihrer Halbwertzeit. Darüber hinaus werden Triptane in unterschiedlichen Darreichungsformen wie beispielsweise als Schmelztabletten, Suppositorien, Nasensprays und Injektionen zur subkutanen Anwendung angeboten. Triptane sollten rechtzeitig während eines Migräneanfalls eingenommen (und gegebenenfalls nachdosiert) werden, da sich sonst ihre Wirksamkeit verringert. Bei Daueranwendung hingegen besteht die Gefahr der Entwicklung eines arzneimittelinduzierten Kopfschmerzes. Bei Nichtansprechen auf ein Triptan kann ein anderer Vertreter dieser Gruppe dennoch wirksam sein.[18]
Triptane (auf dem deutschen Markt derzeit:[50] Sumatriptan, Rizatriptan, Zolmitriptan, Almotriptan, Naratriptan, Eletriptan) sind Serotoninagonisten, die durch Stimulation von 5-HT1B/1D-Rezeptoren zu einer Vasokonstriktion führen.[51]
Triptane sind im Allgemeinen sehr gut verträglich, es bestehen jedoch folgende Kontraindikationen,[52] die teilweise in ihrer gefäßverengenden Wirkung begründet sind:
- Koronare Herzkrankheit
- Herzinfarkt, Schlaganfall oder andere Gefäßerkrankungen
- Hypertonie verschiedenen Ausmaßes
- Leberinsuffizienz, Niereninsuffizienz
- gleichzeitige Anwendung von Ergotamin oder anderen Triptanen
Ditane
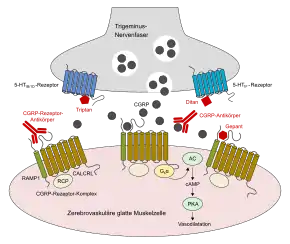
AC = Adenylatcyclase, CALCRL = Calcitonin receptor-like receptor (Calcitonin-Rezeptor-ähnlicher Rezeptor), cAMP = Cyclisches Adenosinmonophosphat, CGRP = Calcitonin Gene-Related Peptide, Gsα = α-Untereinheit des heterotrimeren Gs-Proteins, PKA = Proteinkinase A, RAMP1 = Receptor activity modifying protein 1, RCP = Receptor component protein, 5-HT = 5-Hydroxytryptamin (Serotonin)
Während die Triptane agonistisch am 5-HT1B/1D-Rezeptor wirken, binden Ditane hoch selektiv an die 5-HT1F-Rezeptoren. Als Vertreter ist bislang einzig Lasmiditan (Reyvow) seit 2019 in den USA[53] zugelassen. Es gibt Hinweise darauf, dass der Wirkungsmechanismus darauf beruht, dass Lasmiditan die Freisetzung von Neuropeptiden verringert und dadurch die Schmerzleitung hemmt, auch derjenigen im Trigeminusnerv und in den Ganglien. Ditane können eine therapeutische Alternative darstellen für Patienten, bei denen Triptane nicht ausreichend wirksam oder kontraindiziert sind.[54][55]
Niedermolekulare CGRP-Rezeptorantagonisten
Niedermolekulare Calcitonin-Gene-Related-Peptide-Rezeptorantagonisten (Gepante) blockieren antagonistisch die Rezeptoren für CGRP (Calcitonin-Gene-Related-Peptide-Rezeptor, CGRP-Rezeptor). Anders als die monoklonalen Antikörper können sie oral gegeben werden und werden für die Akuttherapie der Migräne entwickelt. Die zunächst erprobten Gepante Olcegepant und Telcacepant zeigten zwar gute Migränewirksamkeit, scheiterten aber in der weiteren klinischen Entwicklung aufgrund mangelnder Bioverfügbarkeit bzw. lebertoxischer Nebenwirkungen.[56][57] Die Wirkstoffe der zweiten Generation, Ubrogepant und Rimegepant[58] sind seit 2019[59] bzw. 2020[60] in den USA zugelassen. 2021 folgte die Zulassung von Atogepant in den USA zur vorbeugenden Behandlung der episodischen Migräne.[61] In der klinischen Prüfung ist ferner das nasal angewendete Zavegepant, das sich in Zwischenergebnissen gegenüber Placebo überlegen zeigte.[62]
Mutterkornalkaloide
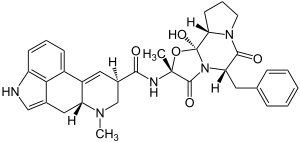
Mutterkornalkaloide wie Ergotamin, die mit der Einführung der Triptane ihre frühere Bedeutung verloren haben, können ebenfalls in der Akuttherapie der Migräne eingesetzt werden. Die Migränewirkung der Mutterkornalkaloide wird wie im Falle der Triptane über einen Agonismus am 5-HT1B/1D-Rezeptor erklärt. Ihre Migränewirksamkeit ist zwar seit über einem Jahrhundert dokumentiert, jedoch lässt sie sich auf Grund eines weitgehenden Mangels moderner prospektiver klinischer Studien schlecht einschätzen.[63] Im Vergleich zu Triptanen sind Mutterkornalkaloide weniger wirksam.[64] Darüber hinaus besitzen sie ein deutlich breiteres Nebenwirkungsspektrum, das insbesondere vaskuläre Ereignisse wie Durchblutungsstörungen, aber auch Muskelkrämpfe und arzneimittelinduzierten Kopfschmerz umfasst. Daher gelten Mutterkornalkaloide als Mittel der zweiten Wahl, deren Anwendung bei länger andauernden Migräneattacken und bei bereits erfolgreicher Anwendung von Mutterkornalkaloiden in der Krankengeschichte angezeigt sein kann.[18]
Antiemetika
Eine Kombination von Analgetika oder spezifischen Migränetherapeutika mit einem Antiemetikum oder Prokinetikum wie Metoclopramid oder Domperidon kann sinnvoll sein, da durch diese nicht nur die gastrointestinalen Begleitsymptome der Migräne (Übelkeit, Erbrechen) beseitigt werden, sondern auch die Aufnahme des Analgetikums gefördert wird. Die Wirksamkeit von Metoclopramid ist in diesem Zusammenhang besser belegt als die von Domperidon.[18]
Sonstige Therapeutika
Erfolgreiche Therapieversuche und Hinweise auf eine Wirksamkeit in kleineren klinischen Studien wurden auch für andere Therapeutika dokumentiert. Eine Wirksamkeit bei akuten Migräneattacken konnte auch für das Antiepileptikum Valproinsäure gezeigt werden.[65][66] Eine arzneimittelrechtliche Zulassung von Valproinsäure zur Akutbehandlung der Migräne besteht jedoch nicht.
Berichte über eine erfolgreiche Akutbehandlung einer ansonsten therapieresistenten Migräne schließen Kortikoide wie Dexamethason ein. Wenngleich kein gesicherter Hinweis auf eine direkte Wirkung von Kortikoiden auf den Migräneschmerz besteht, sollen diese die Wirksamkeit von Triptanen erhöhen[67] und können zudem die Rekurrenzrate von Migräneattacken reduzieren.[68]
Die in der Schmerztherapie etablierten Opioide gelten bei der Behandlung der Migräne als nur beschränkt wirksam. Eine Kombination aus Tramadol und Paracetamol zeigte sich in einer klinischen Studie als wirksam zur Behandlung des Migränekopfschmerzes, der Phonophobie und der Photophobie.[69] Dennoch gilt auf Grund des Übelkeit und Erbrechen einschließenden Nebenwirkungsspektrums, das die Symptomatik der Migräne noch verstärkt, und der verstärkten Gefahr eines medikamenteninduzierten Kopfschmerzes die Anwendung als nicht empfehlenswert.[18]
Eine Studie von 2017 wies darauf hin, dass Cannabisextrakte (bestehend aus den Hauptwirkstoffen THC und CBD) bei akuten Anfällen die Schmerzintensität um etwa die Hälfte senken könnten.[70]
Nichtmedikamentöse Methoden
Als nichtmedikamentöse Methoden gelten Reizabschirmung durch Ruhe in einem geräuscharmen, abgedunkelten Raum, Aromatherapie, Pfefferminzöleinreibungen auf die Stirn, Akupressurmatten, autogenes Training und Psychophonie. Diese Verfahren sind jedoch nicht ausreichend evaluiert.
Prophylaxe
Das Ziel der Migräneprophylaxe ist, die Häufigkeit oder die Schwere von Migräneattacken bereits vor ihrer Entstehung zu senken. Diese ist insbesondere dann angezeigt, wenn der Patient einen starken Leidensdruck oder starke Einschränkungen der Lebensqualität durch die Migräne erfährt. Eine Nutzen-Risiko-Abwägung sollte durchgeführt werden. Ein positives Nutzen-Risiko-Verhältnis kann insbesondere dann vorliegen, wenn der Patient besonders häufig unter Migräne leidet (mehr als drei Attacken pro Monat), Migräneattacken regelmäßig länger andauern (drei Tage oder länger), die Migräne nicht zufriedenstellend mit Standardtherapeutika behandelt werden kann oder schwer zu behandelnde Sonderformen und Komplikationen der Migräne vorliegen.[18]
Zur Migräneprophylaxe stehen insbesondere Arzneistoffe zur Verfügung, die nicht gezielt als Migräneprophylaktika, sondern für verschiedene andere Anwendungsgebiete wie beispielsweise die Behandlung des Bluthochdrucks oder der Epilepsie entwickelt wurden. Für diese Arzneistoffe konnte nachträglich eine migräneprophylaktische Wirkung belegt werden.
Betablocker
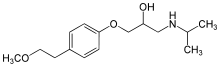
Leitlinienübergreifend gelten Betablocker als Mittel der ersten Wahl für die Migräneprophylaxe. Am besten ist die prophylaktische Wirkung für Metoprolol und Propranolol belegt. Diese Wirksamkeit wird direkt auf eine Hemmung von β-Adrenozeptoren des Zentralnervensystems zurückgeführt[71] und nicht, wie ursprünglich angenommen, auf eine von einigen Betablockern vermittelte zusätzliche Hemmung von Serotonin-Rezeptoren.[72] Somit kann eine Wirksamkeit auch für andere Betablocker angenommen werden. In kleineren oder älteren klinischen Studien haben sich beispielsweise auch Bisoprolol,[73] Atenolol[74] oder Timolol[75] als wirksame Migräneprophylaktika erwiesen. Betablocker sind insbesondere dann angezeigt, wenn der Patient zusätzlich unter Bluthochdruck, einem primären Anwendungsgebiet der Betablocker, leidet.
Calciumantagonisten
Eine migräneprophylaktische Wirkung des nicht selektiven Calciumantagonisten Flunarizin gilt ebenfalls als sehr gut belegt. Daher wird auch dieser Arzneistoff von internationalen Gremien als Mittel der ersten Wahl eingestuft.[76][77] Für andere Calciumkanalblocker wie Verapamil oder Cyclandelat liegen keine konsistenten Daten über eine migräneprophylaktische Wirksamkeit vor. Ein Klasseneffekt kann daher nicht angenommen werden.
Antiepileptika
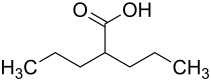
Viele Antiepileptika sind nicht nur in der Lage die Häufigkeit epileptischer Anfälle zu reduzieren, sondern führen zusätzlich zu einem Rückgang der Frequenz von Migräneanfällen. Am besten von diesen Substanzen ist die migräneprophylaktische Wirkung für Valproinsäure und Topiramat dokumentiert. Unter Berücksichtigung des Nebenwirkungsspektrums gelten diese Substanzen ebenfalls als Mittel der ersten Wahl, wenn keine Betablocker eingesetzt werden können.[18] Die Anwendung von Valproinsäure in der Migräneprophylaxe entspricht in Deutschland, nicht aber in vielen anderen Staaten, einem Off-Label-Use, da kein valproinsäurehaltiges Präparat für diese Indikation zugelassen ist. Basierend auf Daten aus einer einzelnen klinischen Studie mit Gabapentin, in der eine leichte Reduktion der Migränehäufigkeit beobachtet wurde,[78] gilt dieser Arzneistoff als Mittel der dritten Wahl.[77] Für das Antiepileptikum Lamotrigin hingegen konnte keine migräneprophylaktische Wirkung, jedoch eine Reduktion des Auftretens einer Aura beobachtet werden.[79] Für andere Antiepileptika liegen keine ausreichenden Daten über ihre migräneprophylaktische Wirksamkeit vor oder sie haben sich, wie im Fall von Oxcarbazepin,[80] als unwirksam erwiesen.
Monoklonale Antikörper im CGRP-Signalweg
CGRP ist als wichtiger Faktor in der Entstehung von Migräne gut charakterisiert. Eine periphere Freisetzung ruft im Körper eine starke Vasodilatation hervor. Außerdem gilt das Peptid als Entzündungsmediator. Im Zentralnervensystem ist CGRP an der Regulation der Körpertemperatur beteiligt und moduliert die Schmerzübertragung.[81] Im Mai 2018 erteilte die US-amerikanische Zulassungsbehörde (FDA) die Zulassung für einen monoklonalen Antikörper (Erenumab, Aimovig) als erstem Medikament, das den Calcitonin Gene-Related-Peptide-Rezeptor (CGRP-R) blockiert.[82][83][84] Im Juli des gleichen Jahres folgte die Zulassung in der EU.[85]
In der Folge wurden drei weitere monoklonale Antikörper zur Migräneprophylaxe zugelassen, die anders als Erenumab, nicht den CGRP-Rezeptor hemmen, sondern sich direkt gegen das Calcitonin Gene-Related Peptide (CGRP) richten: Galcanezumab (Emgality, 2018 USA,[86] 2018 EU[87]) Fremanezumab (Ajovy, 2018 USA,[88] 2019 EU[89]); Eptinezumab (Vyepti, Lundbeck), wurde 2020 in den USA zugelassen[90] und im November 2021 in der EU zur Zulassung empfohlen.[91]
Erenumab, Fremanezumab und Galcanezumab werden subkutan, Eptinezumab intravenös verabreicht.
Sonstige Therapeutika

Für das Antidepressivum Amitriptylin konnte in einer Vielzahl klinischer Studien eine migräneprophylaktische Wirkung gezeigt werden. Daher wird Amitriptylin in der Migräneprophylaxe als Mittel der ersten oder zweiten Wahl eingestuft.[18][76] Die für Amitriptylin beobachtete prophylaktische Migränewirksamkeit lässt sich jedoch nicht auf andere Antidepressiva übertragen.[77] Eine Studie belegt, dass sich die Anzahl der Anfälle mit der regelmäßigen Einnahme von Cannabisextrakt (THC und CBD) ähnlich wirkungsvoll reduzieren lassen wie mit Amitriptylin.[70]
Eine migräneprophylaktische Wirkung konnte auch für das langwirksame Nichtopioid-Analgetikum Naproxen gezeigt werden.[92] Demgegenüber liegen für andere Nichtopioid-Analgetika keine konsistenten Daten über eine Migräne vorbeugende Wirkung vor. Hinzu kommt die bei Daueranwendung bestehende Gefahr der Entwicklung eines medikamenteninduzierten Kopfschmerzes. Nichtopioid-Analgetika gelten daher in der Migräneprophylaxe als Mittel der zweiten oder dritten Wahl.[76][77]
Als Mittel der dritten Wahl gelten die Antihypertensiva Lisinopril und Candesartan, die sich in Pilotstudien als wirksam erwiesen.[77] Gleichfalls kann möglicherweise eine prophylaktische Anwendung mit Botulinumtoxin die Häufigkeit von Migräneattacken reduzieren. Der Wert von Mutterkornalkaloiden wie beispielsweise Dihydroergotamin ist trotz einer arzneimittelrechtlichen Zulassung zur Migräneprophylaxe strittig. Als unwirksam hat sich der für diese Indikation entwickelte Neurokininrezeptor-Antagonist Lanepitant erwiesen.[93] Die über eine Hemmung von Serotoninrezeptoren wirkenden Arzneistoffe Methysergid und Pizotifen sind hingegen migräneprophylaktisch wirksam. Auf Grund ihrer schweren Nebenwirkungen haben sie jedoch keine therapeutische Relevanz mehr.
Die migräneprophylaktische Wirksamkeit des traditionell angewendeten Phytopharmakons Pestwurz konnte mit Hilfe klinischer Studien belegt werden und wird als Mittel der zweiten Wahl eingestuft.[94][95] Eine marginale Wirksamkeit konnte ebenfalls für einen CO2-Extrakt aus Mutterkraut belegt werden. Inwieweit diese Wirksamkeit auf andere Extrakte übertragen werden kann, ist fraglich.[96] Schlechter belegt ist eine mögliche Wirksamkeit von Coenzym Q10, hochdosiertem Magnesium (580 mg) und hochdosiertem Riboflavin (400 mg). Homöopathische Migräneprophylaxen zeigen keine über einen Placeboeffekt hinausgehende Wirkungen.[97][98]
Akupunktur
Die Wirksamkeit der Akupunktur zur Behandlung der Migräne wurde in zahlreichen Studien untersucht. Sie ist bei der Migräneprophylaxe mit weniger Nebenwirkungen mindestens so wirksam wie konventionelle medikamentöse Prophylaxe. Daher wird die Akupunktur oft als zusätzliche Therapiemöglichkeit empfohlen. Die „korrekte“ Platzierung der Akupunkturnadeln spielt keine Rolle, ein Unterschied zwischen chinesischen und nichtchinesischen oder Scheinpunkten ist nicht belegbar.[99]
Sonstige nichtmedikamentöse Prophylaxe
Die Progressive Muskelentspannung nach Jacobson und das Biofeedback können ebenso eine wirksame Möglichkeit der Migräneprophylaxe sein.[100][101] Daneben stehen verschiedene andere Methoden wie zum Beispiel Ernährungsmaßnahmen, Entspannungstechniken, Yoga, autogenes Training und leichter Ausdauersport als Alternativen zur Verfügung. Ihre migräneprophylaktische Wirksamkeit ist jedoch nicht ausreichend evaluiert.
Eine randomisierte klinische Studie zeigte eine Senkung der monatlichen Kopfschmerzattacken durch supraorbitale transkutane elektrische Nervenstimulation (TENS).[102] Diese führt wahrscheinlich indirekt durch wiederholte elektrische Reizung von Hautnerven im Zentralnervensystem zur Bildung von Endorphinen, welche Schmerzen lindern. Dies ist jedoch nicht belegt, weswegen die TENS zu den „Naturheilverfahren“ zählt, welche von den Krankenkassen in der Regel nicht übernommen werden.
Ob Migräne mit einer Biofeedback-Therapie seltener auftritt oder weniger stark ausfällt, hat der IGeL-Monitor des MDS (Medizinischer Dienst des Spitzenverbandes Bund der Krankenkassen) untersucht. Dabei werden Vorgänge im Körper zum Beispiel mit Licht- oder Geräuschsignalen wahrnehmbar gemacht, um diese Körpervorgänge bewusst steuern zu können. Nach einer systematischen Literaturrecherche bewertet der IGeL-Monitor die Biofeedback-Therapie als „unklar“. Denn den gefundenen Studien zufolge sei es zwar besser, Migräne mit Biofeedback zu behandeln als nichts zu tun. Dabei sei jedoch ein Placebo-Effekt nicht auszuschließen. Beim Vergleich gegen eine Scheinbehandlung zeige sich Biofeedback nicht überlegen. Es gebe somit keine belastbaren Hinweise auf einen Nutzen – allerdings auch keine Hinweise auf mögliche Schäden.[103]
Therapie und Prophylaxe in der Schwangerschaft
Die Entscheidung für einen Einsatz von migränewirksamen Arzneimitteln in der Schwangerschaft ist eine Nutzen-Risiko-Abwägung, bei der auch eine mögliche Schädigung durch mütterliche Migräneattacken auf das ungeborene Kind zu berücksichtigen ist. Paracetamol gilt in allen Phasen der Schwangerschaft als verträglich. Im zweiten Trimenon können zusätzlich andere Nichtopioid-Analgetika wie beispielsweise Acetylsalicylsäure, Ibuprofen und Naproxen eingesetzt werden. Triptane sind nicht für den Einsatz in der Schwangerschaft zugelassen, retrospektive Analysen lassen jedoch nicht auf eine schädigende Wirkung von Sumatriptan, Naratriptan und Rizatriptan schließen. Mutterkornalkaloide sind wegen ihrer teratogenen Wirkung kontraindiziert. Ist eine migräneprophylaktische Behandlung während der Schwangerschaft nötig, gilt abgesehen von nichtmedikamentösen Verfahren wie Entspannungsübungen, Biofeedback und Akupunktur nur der Beta-Blocker Metoprolol als vertretbar.[18]
Therapie und Prophylaxe im Kindesalter
Für die Behandlung akuter Migräneattacken bei Kindern gelten die Nichtopioid-Analgetika Ibuprofen und Paracetamol, gegebenenfalls ergänzt durch die Anwendung des Prokinetikums Domperidon, als Mittel der ersten Wahl. Die Wirksamkeit von Triptanen ist hingegen nicht gesichert. Neuere Studien mit Sumatriptan, Zolmitriptan und Rizatriptan deuten jedoch auf eine migränehemmende Wirkung bei Kindern.[104][105][106]---_> Triptane sind nicht für Kinder unter einem Alter von 12 Jahren zu Migränetherapie zugelassen. Alternativ können bei Kindern Allgemeinmaßnahmen in Form von Reizabschirmung mit Entspannen im abgedunkelten Raum, Kühlen des Kopfes und Pfefferminzöleinreibungen auf die Stirn unternommen werden.
Für eine migräneprophylaktische Daueranwendung ist die Wirksamkeit für Flunarizin am besten belegt. Widersprüchliche Daten existieren für das bei Erwachsenen als Standardprophylaktikum eingesetzte Propranolol. Für alle anderen in der Migräneprophylaxe eingesetzten Arzneistoffe liegen keine ausreichenden Erkenntnisse über die Wirksamkeit bei Kindern vor.[107] Auch Entspannungsübungen, verhaltenstherapeutische Maßnahmen und Biofeedback zeigen eine mögliche Wirksamkeit, während diätische Maßnahmen in kontrollierten klinischen Studien ohne Erfolg waren.[108]
Therapie und Prophylaxe der Aura
Eine spezifische Behandlung der Migräneaura ist in der Regel nicht erforderlich. Zudem stehen keine ausreichend wirksamen Arzneistoffe zur Akuttherapie der Migräneaura zur Verfügung. Bei einem entsprechenden Leidensdruck kann eine Migräneprophylaxe erwogen werden. Eine spezifische Prophylaxe der migränösen Aura, jedoch nicht der Kopfschmerzen, ist für das Antiepileptikum Lamotrigin beschrieben worden.[79]
Komorbidität
Menschen mit Migräne haben ein höheres Risiko für kardiovaskuläre und zerebrovaskuläre Erkrankungen.[109] Bei einer Metaanalyse, die 394.942 Patienten mit Migräne und 757.465 Vergleichspersonen ohne Migräne umfasste, fand man ein Schlaganfallrisiko von 1,42 und ein Herzinfarktrisiko von 1,23. Die Steigerung betraf sowohl ischämische (durch Gefäßverschluss) als auch haemorrhagische (durch Hirnblutung) Schlaganfälle. Bei Migräne mit Aura war das Schlaganfallrisiko mit 1,56 höher als ohne Aura (1,11). Auch das Gesamtsterberisiko war mit Aura höher (1,2) als ohne Aura (0,96).
Geschichte der Migränetherapie
Erste Versuche der Behandlung migräneartiger Kopfschmerzen lassen sich spekulativ bis in die Mittelsteinzeit (ca. 8500–7000 v. Chr.) zurückverfolgen. In dieser Zeit wurden vielleicht Dämonen und böse Geister im Kopf der Patienten als Ursache der Migräne und anderer neurologischer Erkrankungen angesehen. Funde aus dem Neolithikum belegen, dass bereits zu dieser Zeit Trepanationen (chirurgische Eröffnungen der Schädeldecke) mit Hilfe von Steinwerkzeugen durchgeführt wurden. Wenngleich kontrovers diskutiert wird, ob diese Behandlungen vorrangig aus mystischen, kultischen oder medizinischen Gründen erfolgten, sollen sie angewendet worden sein, um Dämonen aus dem Schädel entweichen zu lassen. Auch wenn die Erfolgsquote der Trepanation undokumentiert blieb, konnten zumindest archäologische Funde belegen, dass über 50 % der Patienten diese Maßnahme überlebten. Dieses Verfahren wurde bis in das 17. Jahrhundert angewendet.[110]
Auch aus dem Alten Ägypten während der Pharaonenzeit sind Behandlungsmethoden von Kopfschmerzen dokumentiert. So nennt der auf ca. 1550 v. Chr. datierte Papyrus Ebers verschiedene Heilmethoden für Kopfschmerzen, vielleicht auch Migränekopfschmerzen, einschließlich der Verwendung der Asche des Skeletts eines Welses als Einreibung.[111]
Typische Migränekopfschmerzen finden sich erstmals in einem Text einer mittelbabylonischen Keilschrifttafel aus der Bibliothek von Tukulti-apil-Ešarra I. (1115–1077 v. Chr.) beschrieben.[112]
Der berühmte griechische Arzt Hippokrates erkannte ca. 400 v. Chr. erstmals die Aura als einen möglichen Vorboten eines Kopfschmerzes. Er sah als Ursache „Dämpfe, die vom Magen in den Kopf aufsteigen“. Die erste umfassende Beschreibung der Symptome einer Migräne mit einem halbseitigen Kopfschmerz sowie Schwitzen, Übelkeit und Erbrechen wurde im zweiten Jahrhundert von Aretaios unter der Bezeichnung heterocrania dokumentiert. Er grenzte somit gleichzeitig die Migräne von anderen Kopfschmerzformen ab. Auf der Suche nach Krankheitsursachen wurden die Theorien von Hippokrates durch Galenos aufgegriffen, der auch dessen Humoralpathologie weiterentwickelte. Für die Entstehung einer hemicrania machte er eine „übermäßige, aggressive gelbe Galle“ verantwortlich.[113] Der von ihm verwendete Begriff hemicrania (in alten Texten auch emigranea geschrieben[114]) gilt als Vorläufer der heutigen Bezeichnung „Migräne“.[111]
Eine zentralnervöse Ursache der Migräne unter Beteiligung einer Dilatation zerebraler Arterien wurde erstmals 1664 von Thomas Willis erwähnt. Zu dieser Zeit wurden Kaliumcyanid, Brechnuss, Tollkirsche, Fingerhut und Quecksilberverbindungen zur Therapie der Migräne eingesetzt.[111]
Die moderne Migränetherapie begründete 1884 William H. Thompson, der einen Extrakt aus dem Mutterkorn als migränewirksam erkannte. Arthur Stoll gelang 1920 daraus die Isolierung des Wirkstoffs Ergotamin, der bis heute in der Migränetherapie eingesetzt wird. Die Entdeckung des Wirkmechanismus des Ergotamins, der Stimulation der Serotoninrezeptoren 5-HT1B/1D, führte schließlich seit den 1980er Jahren zur Entwicklung moderner Migränetherapeutika, der Gruppe der Triptane.
Literatur
- Hartmut Göbel: Erfolgreich gegen Kopfschmerzen und Migräne. 7. Auflage. Springer, Berlin 2014, ISBN 978-3-642-54725-6.
- Stefan Evers: Fakten. Migräne. Thieme, Stuttgart 2006, ISBN 3-13-143631-X.
- Julia Holzhammer, Christian Wöber: Alimentäre Triggerfaktoren bei Migräne und Kopfschmerz vom Spannungstyp. In: Der Schmerz. 20, 2006, ISSN 0932-433X, S. 151–159.
- Julia Holzhammer, Christian Wöber: Nichtalimentäre Triggerfaktoren bei Migräne und Kopfschmerz vom Spannungstyp. In: Der Schmerz. 20, 2006, ISSN 0932-433X, S. 226–237.
- P. J. Goadsby: Recent advances in the diagnosis and management of migraine. In: BMJ. 332(7532), 7. Jan 2006, S. 25–29. Review. PMID 16399733 (Text ist frei zugänglich).
- Dietrich von Engelhardt: Migräne in Medizin- und Kulturgeschichte. In: Pharmazie in unserer Zeit. 31, 5, 2002, ISSN 0048-3664, S. 444–451.
- Katrin Janhsen, Wolfgang Hoffmann: Pharmazeutische Betreuung von Kopfschmerzpatienten. In: Pharmazie in unserer Zeit. 31, 5, 2002, ISSN 0048-3664, S. 480–485.
- Günter Neubauer, Raphael Ujlaky: Migräne – eine Volkskrankheit und ihre Kosten. In: Pharmazie in unserer Zeit. 31, 5, 2002, ISSN 0048-3664, S. 494–497.
- Jan Brand: Migräne – Krankheit oder Ausrede. Die verschwiegene Krankheit. Arcis, München 2000, ISBN 3-89075-145-8.
- Oliver Sacks: Migräne. Rowohlt, Reinbek bei Hamburg 1998, ISBN 3-499-19963-7.
- Manfred Wenzel: Migräne. Insel-Verlag, Frankfurt am Main 1995, ISBN 3-458-33389-4.
Weblinks
- Schmerzklinik Kiel: Migränewissen
- Migräne – Informationen bei Gesundheitsinformation.de (Online-Angebot des Instituts für Qualität und Wirtschaftlichkeit im Gesundheitswesen)
- S1-Leitlinie Therapie der Migräneattacke und Prophylaxe der Migräne der Deutschen Gesellschaft für Neurologie. In: AWMF online (Stand 2008)
- S1-Leitlinie Kopfschmerz bei Übergebrauch von Schmerz- oder Migränemitteln der Deutschen Gesellschaft für Neurologie. In: AWMF online (Stand Mai 2018)
- Aspirin with or without an antiemetic for acute migraine headaches in adults. In: V Kirthi, S Derry, RA Moore, HJ McQuay: Cochrane Database of Systematic Reviews 2010, Issue 4. Art. No.: CD008041. doi:10.1002/14651858.CD008041.pub2. Cochrane Pain, Palliative and Supportive Care Group, 9. März 2010, abgerufen am 19. August 2010 (englisch).
- Deutsche Migräne- und Kopfschmerzgesellschaft (DMKG)
- Informationen der Internationalen Kopfschmerzgesellschaft IHS über Migräne
- Migräne im Open Directory Project
Einzelnachweise
- Wilhelm Pape, Max Sengebusch (Bearb.): Handwörterbuch der griechischen Sprache. 3. Auflage, 6. Abdruck. Vieweg & Sohn, Braunschweig 1914 (zeno.org [abgerufen am 12. September 2019]).
- Friedrich Kluge, Alfred Götze: Etymologisches Wörterbuch der deutschen Sprache. 20. Auflage. Hrsg. von Walther Mitzka. De Gruyter, Berlin / New York 1967; Neudruck („21. unveränderte Auflage“) ebenda 1975, ISBN 3-11-005709-3, S. 478.
- Deutsche Gesellschaft für Neurologie, federführend HC Diener: S1-Leitlinie Therapie der Migräne, Abschnitt Epidemiologie. In: Leitlinien für Diagnostik und Therapie in der Neurologie. Kapitel Kopfschmerzen und andere Schmerzen. Stand September 2012 in der Fassung vom 21. März 2013, AWMF-Registriernummer 030 - 057
- M. Obermann, Z. Katsarava: Epidemiology of unilateral headaches. In: Expert Rev Neurother. 8(9), Sep 2008, S. 1313–1320. PMID 18759543.
- L. J. Stovner, J. A. Zwart, K. Hagen, G. M. Terwindt, J. Pascual: Epidemiology of headache in Europe. In: Eur. J. Neurol. Band 13, Nr. 4, April 2006, S. 333–345, doi:10.1111/j.1468-1331.2006.01184.x, PMID 16643310.
- J. D. Bartleson, F. M. Cutrer: Migraine update. Diagnosis and treatment. In: Minn Med. Band 93, Nr. 5, Mai 2010, S. 36–41, PMID 20572569.
- L. J. Stovner, K. Hagen, R. Jensen u. a.: The global burden of headache: a documentation of headache prevalence and disability worldwide. In: Cephalalgia. Band 27, Nr. 3, März 2007, S. 193–210, doi:10.1111/j.1468-2982.2007.01288.x, PMID 17381554.
- Messoud Ashina: Migraine. New England Journal of Medicine 2020, Band 383, Seiten 1866–1876, doi:10.1056/NEJMra1915327
- Silvia Romanello: Association Between Childhood Migraine and History of Infantile Colic. In: JAMA. 309, 2013, S. 1607, doi:10.1001/jama.2013.747.
- S.-H. Lee, C. von Stülpnagel, F. Heinen: Therapie der Migräne im Kindesalter. Update. In: Monatsschrift Kinderheilkunde. 154, 2006, S. 764–772.
- W. F. Stewart, M. S. Linet, D. D. Celentano, M. Van Natta, D. Ziegler: Age- and sex-specific incidence rates of migraine with and without visual aura. In: Am. J. Epidemiol. Band 134, Nr. 10, November 1991, S. 1111–1120, PMID 1746521.
- R. B. Lipton, W. F. Stewart, D. D. Celentano, M. L. Reed: Undiagnosed migraine headaches. A comparison of symptom-based and reported physician diagnosis. In: Arch Intern Med. Band 152, Nr. 6, Juni 1992, S. 1273–1278, PMID 1599358.
- G. Neubauer, R. Ujlaky: Migräne – eine Volkskrankheit und ihre Kosten. In: Pharm. in unserer Zeit. Band 31, Nr. 5, 2002, S. 494–497, doi:10.1002/1615-1003(200209)31:5<494::AID-PAUZ494>3.0.CO;2-G, PMID 12369168.
- L. Kelman: The premonitory symptoms (prodrome): a tertiary care study of 893 migraineurs. In: Headache. Band 44, Nr. 9, Oktober 2004, S. 865–872, doi:10.1111/j.1526-4610.2004.04168.x, PMID 15447695.
- G. G. Schoonman, D. J. Evers, G. M. Terwindt, J. G. van Dijk, M. D. Ferrari: The prevalence of premonitory symptoms in migraine: a questionnaire study in 461 patients. In: Cephalalgia. Band 26, Nr. 10, Oktober 2006, S. 1209–1213, doi:10.1111/j.1468-2982.2006.01195.x, PMID 16961788.
- J. Todd: The syndrome of Alice in Wonderland. In: Can Med Assoc J. Band 73, Nr. 9, November 1955, S. 701–704, PMID 13304769, PMC 1826192 (freier Volltext).
- Richard Grossinger: Migraine Auras: When the Visual World Fails. North Atlantic Books, 2006, ISBN 1-55643-619-X, The Nature and Experience of Migraina Auras, S. 1–96.
- S. Evers, A. May, G. Fritsche, P. Kropp, C. Lampl, V. Limmroth, V. Malzacher, S. Sandor, A. Straube, H. C. Diener: Akuttherapie und Prophylaxe der Migräne – Leitlinie der Deutschen Migräne- und Kopfschmerzgesellschaft und der Deutschen Gesellschaft für Neurologie. In: Nervenheilkunde. Band 27, Nr. 10, 2008, S. 933–949 (dmkg.de [PDF]).
- P. T. Fukui, T. R. Gonçalves, C. G. Strabelli u. a.: Trigger factors in migraine patients. In: Arq Neuropsiquiatr. Band 66, 3A, September 2008, S. 494–499, PMID 18813707 (scielo.br).
- Migräne. Abgerufen am 30. Juni 2020.
- U. Bingel: Migräne und Hormone: Was ist gesichert? In: Schmerz. 22 Suppl 1, Februar 2008, S. 31–36, doi:10.1007/s00482-007-0613-9, PMID 18256855.
- J. Olesen: The role of nitric oxide (NO) in migraine, tension-type headache and cluster headache. In: Pharmacol Ther. Band 120, Nr. 2, November 2008, S. 157–171, doi:10.1016/j.pharmthera.2008.08.003, PMID 18789357.
- J. Olesen, G. M. Bousser, H. C. Diener u. a.: The international classification of headache disorders - The primary headaches. In: Cephalalgia. Band 24, Suppl. 1, 2004, S. 24–136.
- Kopfschmerzklassifikation in der Medizingeschichte. Stefan Evers. Nervenheilkunde 2019; 38; 714-721
- Website The International Headache Classification (ICHD-3 Beta). Abgerufen am 29. August 2016.
- A. May: Diagnostik und moderne Therapie der Migräne. In: Dtsch. Ärztebl. 103(17), 2003, s. A 1157–A 1166.
- J. Olesen, G. M. Bousser, H. C. Diener u. a.: The international classification of headache disorders - Appendix. In: Cephalalgia. Band 24, Suppl. 1, 2004, S. 138–149.
- A. H. Stam, A. M. van den Maagdenberg, J. Haan, G. M. Terwindt, M. D. Ferrari: Genetics of migraine: an update with special attention to genetic comorbidity. In: Curr. Opin. Neurol. Band 21, Nr. 3, Juni 2008, S. 288–293, doi:10.1097/WCO.0b013e3282fd171a, PMID 18451712 (wkhealth.com).
- Headache Classification Committee of the International Headache Society (IHS) The International Classification of Headache Disorders, 3rd edition. In: Cephalalgia. Band 38, Nr. 1, Januar 2018, S. 1–211, doi:10.1177/0333102417738202.
- J. R. Graham, H. G. Wolff: Mechanism of migraine headache and action of ergotamine tartrate. In: Arch Neurol Psychiatry. Band 39, 1938, S. 737–763.
- A. May, P. J. Goadsby: The trigeminovascular system in humans: pathophysiologic implications for primary headache syndromes of the neural influences on the cerebral circulation. In: J. Cereb. Blood Flow Metab. Band 19, Nr. 2, Februar 1999, S. 115–127, doi:10.1097/00004647-199902000-00001, PMID 10027765.
- L. L. Thomsen, J. Olesen: Nitric oxide theory of migraine. In: Clin. Neurosci. Band 5, Nr. 1, 1998, S. 28–33, PMID 9523055.
- M. A. Moskowitz, K. Nozaki, R. P. Kraig: Neocortical spreading depression provokes the expression of c-fos protein-like immunoreactivity within trigeminal nucleus caudalis via trigeminovascular mechanisms. In: J. Neurosci. Band 13, Nr. 3, März 1993, S. 1167–1177, PMID 8382735.
- M. A. Moskowitz: Neurogenic inflammation in the pathophysiology and treatment of migraine. In: Neurology. Band 43, 6 Suppl 3, Juni 1993, S. S16–S20, PMID 8389008.
- P. J. Goadsby, L. Edvinsson, R. Ekman: Vasoactive peptide release in the extracerebral circulation of humans during migraine headache. In: Ann. Neurol. Band 28, Nr. 2, August 1990, S. 183–187, doi:10.1002/ana.410280213.
- P. Geppetti, J. G. Capone, M. Trevisani, P. Nicoletti, G. Zagli, M. R. Tola: CGRP and migraine: neurogenic inflammation revisited. In: J Headache Pain. Band 6, Nr. 2, April 2005, S. 61–70, doi:10.1007/s10194-005-0153-6, PMID 16362644.
- Y. Gursoy-Ozdemir, J. Qiu, N. Matsuoka u. a.: Cortical spreading depression activates and upregulates MMP-9. In: J. Clin. Invest. Band 113, Nr. 10, Mai 2004, S. 1447–1455, doi:10.1172/JCI21227, PMID 15146242, PMC 406541 (freier Volltext).
- H. C. Diener, M. Küper, T. Kurth: Migraine-associated risks and comorbidity. In: J. Neurol. Band 255, Nr. 9, September 2008, S. 1290–1301, doi:10.1007/s00415-008-0984-6, PMID 18958572.
- nature.com
- nature.com
- J. Haan, A. M. van den Maagdenberg, O. F. Brouwer, M. D. Ferrari: Migraine and epilepsy: genetically linked? In: Expert Rev Neurother. Band 8, Nr. 9, September 2008, S. 1307–11, doi:10.1586/14737175.8.9.1307, PMID 18759542.
- Leitlinie der Deutschen Gesellschaft für Neurologie (DGN) in Zusammenarbeit mit der Deutschen Migräne- und Kopfschmerzgesellschaft (DMKG), Website der DGN, abgerufen am 25. Juni 2018
- H. C. Diener, V. Pfaffenrath, L. Pageler, H. Peil, B. Aicher: The fixed combination of acetylsalicylic acid, paracetamol and caffeine is more effective than single substances and dual combination for the treatment of headache: a multicentre, randomized, double-blind, single-dose, placebo-controlled parallel group study. In: Cephalalgia. Band 25, Nr. 10, Oktober 2005, S. 776–787, doi:10.1111/j.1468-2982.2005.00948.x, PMID 16162254.
- J. Goldstein u. a.: Acetaminophen, aspirin, and caffeine in combination versus ibuprofen for acute migraine: results from a multicenter, double-blind, randomized, parallel-group, single-dose, placebo-controlled study. In: Headache. 46, 2006, S. 444–453. PMID 16618262
- Es gibt derzeit (Stand 22. Oktober 2020) nur ein einziges in dieser Indikation zugelassenes Kombinationspräparat auf dem deutschen Pharmamarkt. Mischanalgetika dieses Typs werden, da sie nicht rezeptpflichtig sind, wegen ihrer Nebenwirkungen kritisch gesehen.
- Hartmut Göbel Schmerzklinik Kiel: Mirgänewissen - Anfallsbehandlung.
- D. Kudrow, H. M. Thomas, G. Ruoff u. a.: Valdecoxib for treatment of a single, acute, moderate to severe migraine headache. In: Headache. Band 45, Nr. 9, Oktober 2005, S. 1151–1162, doi:10.1111/j.1526-4610.2005.00238.x, PMID 16178945.
- S. Silberstein, S. Tepper, J. Brandes u. a.: Randomized, placebo-controlled trial of rofecoxib in the acute treatment of migraine. In: Neurology. Band 62, Nr. 9, Mai 2004, S. 1552–1557, PMID 15136680.
- Schmerzklinik Kiel: Migränewissen - Anfallsbehandlung.
- Rote Liste, Fachinfo-Service, abgerufen am 9. November 2020
- Checkliste Neurologie. 6. Auflage. Georg Thieme Verlag, Stuttgart 2016, ISBN 978-3-13-126276-9, doi:10.1055/b-003-129347 (thieme.de [abgerufen am 7. November 2020]).
- Hauke Basedau, Arne May: Steckbrief Migräne. In: Hamburger Ärzteblatt 74, 11 (10. November 2020), S. 12.
- FDA approves new treatment for patients with migraine, PM FDA vom 11. Oktober 2019, abgerufen am 6. November 2019
- C. Müller: Lasmiditan bei akuter Migräne – eine Alternative zu Triptanen, Deutsche Apothekerzeitung, 17. Oktober 2019.
- K. Gräfe: Neue Option bei Migräne-Attacken, Pharmazeutische Zeitung, 15. Oktober 2019.
- S. J. Tepper, M. J. Stillman: Clinical and preclinical rationale for CGRP-receptor antagonists in the treatment of migraine. In: Headache. Band 48, Nr. 8, Dezember 2008, S. 1259–1268, doi:10.1111/j.1526-4610.2008.01214.x.
- Lanfranco Pellesi, Simona Guerzoni, Luigi Alberto Pini: Spotlight on Anti-CGRP Monoclonal Antibodies in Migraine: The Clinical Evidence to Date. In: Clinical Pharmacology in Drug Development. Band 6, Nr. 6, 2017, S. 534–547, doi:10.1002/cpdd.345, PMID 28409893, PMC 5697612 (freier Volltext).
- Philip R. Holland, Peter J. Goadsby: Targeted CGRP Small Molecule Antagonists for Acute Migraine Therapy. In: Neurotherapeutics. Band 15, Nr. 2, April 2018, S. 304–312, doi:10.1007/s13311-018-0617-4, PMID 29556965, PMC 5935646 (freier Volltext).
- UBRELVY- ubrogepant tablet (en) DailyMed.
- NURTEC ODT- rimegepant sulfate tablet, orally disintegrating (en) DailyMed.
- FDA Approves QULIPTA™ (atogepant), the First and Only Oral CGRP Receptor Antagonist Specifically Developed for the Preventive Treatment of Migraine. Pressemitteilung Abbvie, 28. September 2021.
- BBiohaven Achieves Positive Topline Results in Pivotal Phase 2/3 Study of Vazegepant, The First and Only Intranasal CGRP Receptor Antagonist in Clinical Development for the Acute Treatment of Migraine, Pressemitteilung Biohaven Pharmaceuticals, 17. Dezember 1019.
- P. Tfelt-Hansen, P. R. Saxena, C. Dahlöf u. a.: Ergotamine in the acute treatment of migraine: a review and European consensus. In: Brain. 123 ( Pt 1), Januar 2000, S. 9–18, PMID 10611116.
- H. C. Diener, J. P. Jansen, A. Reches, J. Pascual, D. Pitei, T. J. Steiner: Efficacy, tolerability and safety of oral eletriptan and ergotamine plus caffeine (Cafergot) in the acute treatment of migraine: a multicentre, randomised, double-blind, placebo-controlled comparison. In: Eur. Neurol. Band 47, Nr. 2, 2002, S. 99–107, PMID 11844898 (karger.com).
- K. R. Edwards, J. Norton, M. Behnke: Comparison of intravenous valproate versus intramuscular dihydroergotamine and metoclopramide for acute treatment of migraine headache. In: Headache. Band 41, Nr. 10, 2001, S. 976–980, doi:10.1046/j.1526-4610.2001.01191.x, PMID 11903525.
- T. Leniger, L. Pageler, P. Stude, H. C. Diener, V. Limmroth: Comparison of intravenous valproate with intravenous lysine-acetylsalicylic acid in acute migraine attacks. In: Headache. Band 45, Nr. 1, Januar 2005, S. 42–46, doi:10.1111/j.1526-4610.2005.05009.x, PMID 15663612.
- M. Bigal, F. Sheftell, S. Tepper, D. Tepper, T. W. Ho, A. Rapoport: A randomized double-blind study comparing rizatriptan, dexamethasone, and the combination of both in the acute treatment of menstrually related migraine. In: Headache. Band 48, Nr. 9, Oktober 2008, S. 1286–1293, doi:10.1111/j.1526-4610.2008.01092.x, PMID 19031496.
- I. Colman, B. W. Friedman, M. D. Brown u. a.: Parenteral dexamethasone for acute severe migraine headache: meta-analysis of randomised controlled trials for preventing recurrence. In: BMJ. Band 336, Nr. 7657, Juni 2008, S. 1359–1361, doi:10.1136/bmj.39566.806725.BE, PMID 18541610, PMC 2427093 (freier Volltext).
- S. D. Silberstein, F. G. Freitag, T. D. Rozen u. a.: Tramadol/acetaminophen for the treatment of acute migraine pain: findings of a randomized, placebo-controlled trial. In: Headache. Band 45, Nr. 10, 2005, S. 1317–1327, doi:10.1111/j.1526-4610.2005.00264.x, PMID 16324164.
- Interactive Programme Planner – EAN Congress 2017 in Amsterdam. (Nicht mehr online verfügbar.) Ehemals im Original; abgerufen am 30. November 2017 (englisch). (Seite nicht mehr abrufbar, Suche in Webarchiven) Info: Der Link wurde automatisch als defekt markiert. Bitte prüfe den Link gemäß Anleitung und entferne dann diesen Hinweis.
- K. G. Shields, P. J. Goadsby: Propranolol modulates trigeminovascular responses in thalamic ventroposteromedial nucleus: a role in migraine? In: Brain. Band 128, Pt 1, Januar 2005, S. 86–97, doi:10.1093/brain/awh298, PMID 15574468.
- H. Nishio, Y. Nagakura, T. Segawa: Interactions of carteolol and other beta-adrenoceptor blocking agents with serotonin receptor subtypes. In: Arch Int Pharmacodyn Ther. Band 302, 1989, S. 96–106, PMID 2576893.
- R. Wörz, B. Reinhardt-Benmalek, K. H. Grotemeyer: Bisoprolol and metoprolol in the prophylactic treatment of migraine with and without aura - a randomized double-blind cross-over multicenter study. In: Cephalalgia. Band 11, Suppl. 11, 1991, S. 152–153.
- V. Johannsson, L. R. Nilsson, T. Widelius u. a.: Atenolol in migraine prophylaxis a double-blind cross-over multicentre study. In: Headache. Band 27, Nr. 7, Juli 1987, S. 372–374, PMID 3308768.
- R. M. Gallagher, R. A. Stagliano, C. Sporazza: Timolol maleate, a beta blocker, in the treatment of common migraine headache. In: Headache. Band 27, Nr. 2, Februar 1987, S. 84–86, PMID 3553070.
- S. D. Silberstein: Practice parameter: evidence-based guidelines for migraine headache (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. In: Neurology. Band 55, Nr. 6, September 2000, S. 754–762, PMID 10993991.
- S. Evers, J. Afra, A. Frese u. a.: EFNS guideline on the drug treatment of migraine - report of an EFNS task force. In: Eur. J. Neurol. Band 13, Nr. 6, Juni 2006, S. 560–572, doi:10.1111/j.1468-1331.2006.01411.x, PMID 16796580.
- N. T. Mathew, A. Rapoport, J. Saper u. a.: Efficacy of gabapentin in migraine prophylaxis. In: Headache. Band 41, Nr. 2, Februar 2001, S. 119–128, doi:10.1046/j.1526-4610.2001.111006119.x, PMID 11251695.
- J. Pascual, A. B. Caminero, V. Mateos u. a.: Preventing disturbing migraine aura with lamotrigine: an open study. In: Headache. Band 44, Nr. 10, 2004, S. 1024–1028, doi:10.1111/j.1526-4610.2004.04198.x, PMID 15546267.
- S. Silberstein, J. Saper, F. Berenson, M. Somogyi, K. McCague, J. D'Souza: Oxcarbazepine in migraine headache: a double-blind, randomized, placebo-controlled study. In: Neurology. Band 70, Nr. 7, Februar 2008, S. 548–555, doi:10.1212/01.wnl.0000297551.27191.70, PMID 18268247.
- Monoklonale Antikörper zur Prophylaxe von Migräne – Erenumab (Aimovig®), Galcanezumab (Emgality®) und Fremanezumab (Ajovy®) – Wechsel bei Nichtansprechen? (PDF; 165 kB) Arzneiverordnung in der Praxis, AKDAE vom 30. Januar 2020, abgerufen am 31. Januar 2020
- FDA approves novel preventive treatment for migraine, PM FDA vom 17. Mai 2018, abgerufen am 20. Mai 2018
- FDA Approves Aimovig™ (erenumab-aooe), A Novel Treatment Developed Specifically For Migraine Prevention,PM Amgen vom 17. Mai 2018, abgerufen am 19. Mai 2018
- Aimovig (Memento vom 18. Mai 2018 im Internet Archive) Multimedia News Release, abgerufen am 19. Mai 2018
- https://ec.europa.eu/health/documents/community-register/html/h1293.htm
- https://www.fda.gov/drugs/drug-approvals-and-databases/drug-trials-snapshots-emgality
- https://ec.europa.eu/health/documents/community-register/html/h1330.htm
- https://www.fda.gov/drugs/drug-trials-snapshot-ajovy
- https://ec.europa.eu/health/documents/community-register/html/h1358.htm
- https://www.fda.gov/drugs/drug-approvals-and-databases/drug-trials-snapshots-vyepti
- https://www.ema.europa.eu/en/medicines/human/summaries-opinion/vyepti
- K. M. Welch, D. J. Ellis, P. A. Keenan: Successful migraine prophylaxis with naproxen sodium. In: Neurology. Band 35, Nr. 9, September 1985, S. 1304–1310, PMID 4022376.
- D. J. Goldstein, W. W. Offen, E. G. Klein u. a.: Lanepitant, an NK-1 antagonist, in migraine prevention. In: Cephalalgia. Band 21, Nr. 2, März 2001, S. 102–106, doi:10.1046/j.1468-2982.2001.00161.x, PMID 11422091.
- H. C. Diener, V. W. Rahlfs, U. Danesch: The first placebo-controlled trial of a special butterbur root extract for the prevention of migraine: reanalysis of efficacy criteria. In: Eur. Neurol. Band 51, Nr. 2, 2004, S. 89–97, doi:10.1159/000076535, PMID 14752215 (karger.com).
- R. B. Lipton, H. Göbel, K. M. Einhäupl, K. Wilks, A. Mauskop: Petasites hybridus root (butterbur) is an effective preventive treatment for migraine. In: Neurology. Band 63, Nr. 12, Dezember 2004, S. 2240–2244, PMID 15623680.
- M. H. Pittler, E. Ernst: Feverfew for preventing migraine. In: Cochrane database of systematic reviews. 2004, CD002286.
- H. Walach, W. Haeusler, T. Lowes u. a.: Classical homeopathic treatment of chronic headaches. In: Cephalalgia. Band 17, Nr. 2, April 1997, S. 119–126; discussion 101, doi:10.1046/j.1468-2982.1997.1702119.x, PMID 9137850.
- T. E. Whitmarsh, D. M. Coleston-Shields, T. J. Steiner: Double-blind randomized placebo-controlled study of homoeopathic prophylaxis of migraine. In: Cephalalgia. Band 17, Nr. 5, August 1997, S. 600–604, doi:10.1046/j.1468-2982.1997.1705600.x, PMID 9251877.
- K. Linde, G. Allais, B. Brinkhaus, E. Manheimer, A. Vickers, A. R. White: Acupuncture for migraine prophylaxis. In: Cochrane Database Syst Rev. Nr. 1, 2009, S. CD001218 (cochrane.org).
- D. B. Penzien, F. Andrasik, B. M. Freidenberg u. a.: Guidelines for trials of behavioral treatments for recurrent headache, first edition: American Headache Society Behavioral Clinical Trials Workgroup. In: Headache. 45 Suppl 2, Mai 2005, S. S110–S132, doi:10.1111/j.1526-4610.2005.4502004.x, PMID 15921503.
- Y. Nestoriuc, A. Martin: Efficacy of biofeedback for migraine: a meta-analysis. In: Pain. Band 128, Nr. 1-2, März 2007, S. 111–127, doi:10.1016/j.pain.2006.09.007, PMID 17084028.
- J. Schoenen, B. Vandersmissen, S. Jeangette, L. Herroelen, M. Vandenheede, P. Gérard, D. Magis: Migraine prevention with a supraorbital transcutaneous stimulator: a randomized controlled trial. In: Neurology. Band 80, Nr. 8, Februar 2013, S. 697–704, doi:10.1212/WNL.0b013e3182825055, PMID 23390177.
- IGeL-Monitor: Biofeedback bei Migräne. abgerufen am 14. Januar 2019. Mehr zur Begründung der Bewertung im Ergebnisbericht. (PDF; 113 kB) abgerufen am 14. Januar 2019.
- L. Damen, J. K. Bruijn, A. P. Verhagen, M. Y. Berger, J. Passchier, B. W. Koes: Symptomatic treatment of migraine in children: a systematic review of medication trials. In: Pediatrics. Band 116, Nr. 2, August 2005, S. e295–e302, doi:10.1542/peds.2004-2742, PMID 16061583.
- K. Ahonen, M. L. Hämäläinen, M. Eerola, K. Hoppu: A randomized trial of rizatriptan in migraine attacks in children. In: Neurology. Band 67, Nr. 7, Oktober 2006, S. 1135–1140, doi:10.1212/01.wnl.0000238179.79888.44, PMID 16943370.
- D. W. Lewis, P. Winner, A. D. Hershey, W. W. Wasiewski: Efficacy of zolmitriptan nasal spray in adolescent migraine. In: Pediatrics. Band 120, Nr. 2, August 2007, S. 390–396, doi:10.1542/peds.2007-0085, PMID 17671066.
- L. Damen, J. Bruijn, A. P. Verhagen, M. Y. Berger, J. Passchier, B. W. Koes: Prophylactic treatment of migraine in children. Part 2. A systematic review of pharmacological trials. In: Cephalalgia. Band 26, Nr. 5, Mai 2006, S. 497–505, doi:10.1111/j.1468-2982.2005.01047.x, PMID 16674757.
- L. Damen, J. Bruijn, B. W. Koes, M. Y. Berger, J. Passchier, A. P. Verhagen: Prophylactic treatment of migraine in children. Part 1. A systematic review of non-pharmacological trials. In: Cephalalgia. Band 26, Nr. 4, April 2006, S. 373–383, doi:10.1111/j.1468-2982.2005.01046.x, PMID 16556238.
- Ahmed N Mahmoud, Amgad Mentias, Akram Y Elgendy, Abdul Qazi, Amr F Barakat: Migraine and the risk of cardiovascular and cerebrovascular events: a meta-analysis of 16 cohort studies including 1 152 407 subjects. In: BMJ Open. Band 8, Nr. 3, 2018, ISSN 2044-6055, S. e020498, doi:10.1136/bmjopen-2017-020498, PMID 29593023, PMC 5875642 (freier Volltext) – (bmj.com [abgerufen am 24. November 2019]).
- Carlos M. Villalón u. a.: An Introduction to Migraine: from Ancient Treatment to Functional Pharmacology and Antimigraine Therapy. In: Proc. West. Pharmacol. Soc. 45, 2002, S. 199–210.
- Christian Waeber, Michael A. Moskowitz: Therapeutic implications of central and peripheral neuroligic mechanisms in migraine. In: Neurology. 61 (Suppl. 4), 2003, S. S9–S20.
- Manfred Wenzel: Migräne. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. de Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 987.
- Hartmut Göbel: Die Kopfschmerzen. 2. Auflage. Springer, 2004, ISBN 3-540-03080-8, Migräne, S. 141–368.
- Wouter S. van den Berg (Hrsg.): Eene Middelnederlandsche vertaling van het Antidotarium Nicolaï (Ms. 15624–15641, Kon. Bibl. te Brussel) met den latijnschen tekst der eerste gedrukte uitgave van het Antidotarium Nicolaï. Hrsg. von Sophie J. van den Berg, N. V. Boekhandel en Drukkerij E. J. Brill, Leiden 1917, S. 209.