Lasmiditan
Lasmiditan ist ein Arzneistoff zur Akutbehandlung eines Migräneanfalls mit oder ohne Aura. Für die Migränevorbeugung ist es ist nicht geeignet. Die Substanz aus der Gruppe der Ditane wirkt als Agonist am Serotoninrezeptor und ist oral anwendbar. Im Unterschied zu den ebenfalls in der Migränebehandlung verwendeten Triptanen wirkt Lasmiditan jedoch nicht gefäßverengend.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
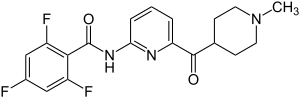 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Lasmiditan | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C19H18F3N3O2 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse |
Ditane | |||||||||||||||
| Wirkmechanismus |
Selektiver Agonismus am 5-HT1F-Rezeptor | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 377,36 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Chemische Eigenschaften
Lasmiditan ist der erste therapeutisch verwendete Wirkstoff aus der Gruppe der Ditane und besitzt, anders als die ebenfalls in der Migränebehandlung verwendeten Triptane, keine Tryptophan-Partialstruktur. Lasmiditan besteht aus drei Ringsystemen (Trifluorbenzoesäure, Pyridin-2-Amin und N-Methylpiperidin), die über funktionelle Gruppen miteinander verbunden sind.
Pharmazeutisch verwendet wird der Wirkstoff als Lasmiditanhemisuccinat,[2] also dem Salz der Bernsteinsäure. Lasmitditanhemisuccinat ist ein weißes, kristallines Pulver, schwer löslich in Wasser, wenig löslich in Ethanol und löslich im Methanol.[3] Als ein weiteres Salz ist das Lasmiditanhydrochlorid[4] beschrieben.
Pharmakologische Eigenschaften
Lasmiditan wirkt agonistisch und selektiv an den 5-HT1F-Rezeptoren. Es gibt Hinweise darauf, dass der Wirkungsmechanismus darauf beruht, dass es die Freisetzung von Neuropeptiden verringert und dadurch die Schmerzleitung hemmt, auch derjenigen im Trigeminusnerv und in den Ganglien. Die Selektivität von Lasmiditan für den 5-HT1F-Rezeptor ist 440-fach größer als gegenüber dem 5-HT1B-Rezeptor, von dem angenommen wird, dass er für vasokonstriktive Effekte verantwortlich ist. Die gefäßverengende Wirkung an den peripheren Gefäßen entfällt und Lasmiditan darf auch bei Patienten mit Herz-Kreislauf-Erkrankungen eingesetzt werden.[5][6][7]
Lasmiditan ist oral wirksam, als häufigste unerwünschten Wirkungen wurden Schwindel, Müdigkeit, Empfindungsstörungen und eine Dämpfung beobachtet.
Zulassung
Unter dem Namen Reyvow wurde Lasmiditan im Oktober 2019 von der FDA in den USA für die Akutbehandlung der Migräne zugelassen.[8] Das Arzneimittel ist eine Entwicklung der Lilly-Tochter CoLucid Pharmaceuticals.[9] Ein Zulassungsantrag für die EU ist gestellt, aber die Zulassung steht noch aus.
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Externe Identifikatoren von bzw. Datenbank-Links zu Lasmiditanhemisuccinat: CAS-Nummer: 439239-92-6, EG-Nummer: 815-300-4, ECHA-InfoCard: 100.249.353, PubChem: 46927777, ChemSpider: 30790735, Wikidata: Q27292373.
- Prescribing Information Reyvow Tablets 50 mg, 100 mg, Eli Lilly and Company, September 2019.
- Externe Identifikatoren von bzw. Datenbank-Links zu Lasmiditanhydrochlorid: CAS-Nummer: 613677-28-4, EG-Nummer: 947-092-7, ECHA-InfoCard: 100.256.790, PubChem: 17980336, ChemSpider: 16472699, Wikidata: Q90415167.
- C. Müller: Lasmiditan bei akuter Migräne – eine Alternative zu Triptanen, Deutsche Apothekerzeitung, 17. Oktober 2019.
- K. Gräfe: Neue Option bei Migräne-Attacken, Pharmazeutische Zeitung, 15. Oktober 2019.
- K. Gräfe: Ditane und Gepante gegen Migräne-Attacken, Pharmazeutische Zeitung, 14. Oktober 2019.
- FDA approves new treatment for patients with migraine, PM FDA vom 11. Oktober 2019, abgerufen am 6. November 2019
- Lilly holt sich Lasmiditan zurück Ärzte Zeitung online, 27. Januar 2017.