Metoclopramid
Metoclopramid (MCP) ist ein Arzneistoff aus der Gruppe der Antiemetika. Es regt die Peristaltik im oberen Magen-Darm-Trakt an und lindert damit Übelkeit und Erbrechen. Die Wirkung bei postoperativer Übelkeit ist nicht gesichert.[5] Außerdem fördert es indirekt, durch Beschleunigung der Peristaltik des Magens und Erhöhung der Öffnungsfrequenz des Pylorus, die Aufnahme anderer Medikamente bzw. Wirkstoffe und wird aus diesem Grund vor allem in Migräne-Präparaten in Kombination mit einem Schmerzmittel (z. B. ASS, Paracetamol) eingesetzt. Es steht auf der Liste der unentbehrlichen Arzneimittel der WHO.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Metoclopramid | |||||||||||||||||||||
| Andere Namen |
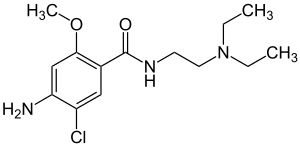
4-Amino-5-chlor-N-[2-(diethylamino)ethyl]-2-methoxybenzamid (IUPAC) | |||||||||||||||||||||
| Summenformel | C14H22ClN3O2 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis fast weißes, feines polymorphes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A03FA01 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 299,80 g·mol−1 | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
9,27 (25 °C)[3] | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Pharmakologische Eigenschaften
Wirkungsmechanismus (Pharmakodynamik)
Metoclopramid bindet an Dopaminrezeptoren und ist ein Dopamin-Antagonist (Typ D2). Dopamin, als körpereigener Botenstoff, hat einen emetischen Effekt, d. h., es kann Erbrechen auslösen. Dopamin-Antagonisten können ebenfalls an den Dopaminrezeptoren binden und diese somit für Dopamin und agonistisch wirkende Substanzen blockieren. Man unterscheidet zwischen zentralen und peripheren Dopaminantagonisten. Periphere Antagonisten können die Blut-Hirn-Schranke nicht überwinden und haben folglich keine oder sehr wenig Wirkung auf das zentrale Nervensystem, im Gegensatz zu zentralen Antagonisten, die als Psychopharmaka eingesetzt werden. MCP überwindet die Blut-Hirn-Schranke in gewissem Maß und führt daher möglicherweise im zentralen Nervensystem zu neuroleptischen Nebenwirkungen.
Metoclopramid bindet auch an Serotonin-Rezeptoren und beeinflusst zusätzlich: es wirkt (partiell) antagonistisch auf 5-HT3-, aber agonistisch auf 5-HT4-Rezeptoren, die Einfluss auf die Peristaltik des Magen-Darm-Trakts haben und die intestinale Sekretion von Wasser und Elektrolyten fördern.
Zudem bindet Metoclopramid an Histaminrezeptoren.[6]
Therapeutische Verwendung
Aufgrund möglicher zentraler Nebenwirkungen ist MCP in Deutschland verschreibungspflichtig.
Humanmedizin
Metoclopramid ist angezeigt zur Vorbeugung von Übelkeit und Erbrechen nach Chemo- und Strahlentherapie (oral, rektal) sowie nach Operationen (parenteral zur PONV-Prophylaxe[7]); ferner zur symptomatischen Behandlung von (etwa durch Migräne ausgelöst) Übelkeit und Erbrechen und in der Behandlung der Migräne in Kombination mit oralen Schmerzmitteln zur Verbesserung deren Resorption. Nach einem 2011 durch die europäische Arzneimittelagentur aufgrund des Auftretens von unerwünschten schweren neurologischen und seltenen, aber ernsten kardiovaskulären Wirkungen eingeleiteten Risikobewertungsverfahren, beschied die EU-Kommission im Dezember 2013 die Einschränkung von Indikation, Therapiedauer und Konzentration von Metoclopramid in Lösungs- oder Tropfenform.[8] So soll die maximale Verordnungsdauer nur noch 5 Tage betragen während sowohl die empfohlene Einzeldosis für erwachsene Menschen weiterhin 10 mg und die empfohlene Tagesdosis ebenfalls unverändert bis zu 30 mg für Erwachsene beträgt.[8] Säuglinge sollten das Mittel gar nicht mehr erhalten.[9] Ausgeschlossen werden sollen Anwendungsgebiete wie Verdauungsstörungen (Dyspepsie, gastrointestinale Motilitätsstörungen) und Refluxösophagitis, für welche keine ausreichenden Belege für eine klinisch relevante Wirksamkeit vorlagen. Laut Bernd Mühlbauer von der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) hätten die Ärzte MCP zu häufig als Allheilmittel verordnet.[10] Ferner soll Metoclopramid bei akutem Erbrechen nach Chemotherapie nicht mehr angewendet werden, da eine Wirksamkeit in der empfohlenen Dosierung als nicht ausreichend angesehen wird, sondern nur noch bei verzögerter chemotherapieinduzierter Übelkeit und Erbrechen.
Das Pharmakovigilanz- und Beratungszentrum für Embryonaltoxikologie empfiehlt Metoclopramid als Mittel der Wahl zur Behandlung von Übelkeit und Erbrechen in der Schwangerschaft.[11]
Tiermedizin
In der Tiermedizin ist Metoclopramid zugelassen zur symptomatischen Behandlung von Erbrechen, reduzierter Magen-Darm-Motilität bei Magenschleimhautentzündung (Gastritis), Magenpförtnerkrampf (Pylorusspasmus), chronischer Nierenentzündung (Nephritis) und Verdauungsintoleranz gegenüber manchen Tierarzneimitteln bei Hunden und Katzen.[8][12]
Nebenwirkungen
Sehr häufig tritt ein Gefühl von Schläfrigkeit ein. Häufige Nebenwirkungen sind Depression, unkontrollierbare Bewegungsstörungen (Dyskinesien) wie Muskelkrämpfe oder Zittern, Ruhelosigkeit, Schwindelgefühl, Durchfall und eine Abnahme des Blutdrucks. Gelegentlich können Halluzinationen, Allergien, Bewusstseinsstörungen, Störung der Regelblutung oder ein erhöhter Spiegel von Prolaktin, welcher bei Männern und bei nicht stillenden Frauen milchige Absonderungen aus der Brustdrüse hervorrufen kann. Zudem ist Mundtrockenheit eine potenzielle Nebenwirkung.[13] Selten treten Krampfanfälle (besonders bei epileptischen Patienten) oder Zustände der Verwirrtheit auf.[8][14]
Möglicherweise ist MCP der häufigste Auslöser für medikamentöse Bewegungsstörungen. Ein erhöhtes Risiko besteht bei jungen Patienten, hoher Dosis und langer Anwendung. Aufgrund möglicher Spätdyskinesien verpflichtete die US-Arzneimittelzulassungsbehörde die Hersteller, eine Black-Box-Warnung anzubringen.[15] Das Auftreten von unerwünschten schweren neurologischen und kardiovaskulären Wirkungen war Anlass für ein im Dezember 2011 durch die europäische Arzneimittelagentur eingeleitetes Risikobewertungsverfahren. In Deutschland ist MCP seit dem 9. April 2014 in Humanarzneimitteln (Monopräparaten) in flüssiger Form zur oralen Anwendung mit einer Konzentration von mehr als 1 mg/ml, als Formulierung zur parenteralen Anwendung mit einer Konzentration von mehr als 5 mg/ml und bei rektaler Anwendung von mehr als 20 mg aufgrund eines Zulassungswiderrufs nicht mehr verkehrsfähig.[16] Das BfArM setzt damit die Empfehlungen zur Risikominimierung MCP-haltiger Arzneimittel um, die die europäische Arzneimittelbehörde EMA anhand einer Neubewertung zum Nutzen-Risiko-Verhältnis aussprach.[17] Das Risiko für schwere unerwünschte neurologische Ereignisse könne laut EMA durch die Anwendung von niedrigeren Dosen von Metoclopramid minimiert werden.[9]
Eine weitere relevante Nebenwirkung von Metoclopramid ist eine Erhöhung des Prolaktinspiegels, die zu nachlassender Libido, Menstruationsstörungen und Impotenz führen kann.
Gegenanzeigen und Anwendungsbeschränkungen
Metoclopramid ist bei Malariapatienten unter Malaronetherapie oder Patienten, die eine Malarone-Prophylaxe einnehmen, kontraindiziert. Morbus Parkinson ist eine neurodegenerative Erkrankung. Im Laufe der Zeit sterben in der Substantia nigra die dopaminergen Neuronen ab. Der Mangel an Dopamin führt dann schließlich zu den Symptomen dieser Krankheit, welche auch unter dem Namen „Schüttellähmung“ bekannt ist. Metoclopramid ist ein Dopamin-Antagonist mit der Fähigkeit, die Blut-Hirn-Schranke zu passieren, und darf deshalb nicht bei Morbus Parkinson eingesetzt werden. Bei Übelkeit kann man alternativ Domperidon einsetzen. Domperidon überwindet im Gegensatz zu Metoclopramid die Blut-Hirn-Schranke kaum.
Stillzeit
Die pharmazeutischen Unternehmen raten von der Verwendung von Metoclopramid und gleichzeitigem Stillen ab, da Metoclopramid in die Muttermilch übertritt und die Wirkung von Dopamin-Antagonisten auf das kindliche Nervensystem nicht ausreichend erforscht sei.[18] Studien des Pharmakovigilanz- und Beratungszentrums für Embryonaltoxikologie der Charité zeigten, dass MCP nur in geringen Mengen über die Muttermilch abgegeben wird und lediglich in Einzelfällen Blähungen und andere Nebenwirkungen beim Kind hervorrufen kann. Das Zentrum empfiehlt, MCP gegebenenfalls indikationsgerecht über kurze Zeit einzusetzen. Teilweise wird MCP als Dopaminantagonist auch dazu eingesetzt, die Bildung der Muttermilch anzuregen.[11]
Chemie
Chemisch gesehen handelt es sich bei MCP um 4-Amino-5-chlor-N-(2-diethylaminoethyl)-2-methoxybenzamid (auch Methoxychloroprocainamid). Es ist ein Procainamid-Derivat, gehört also zu den Benzamiden, besitzt jedoch keine lokalanästhetische, sondern eine dopaminantagonistische Wirkung.
Synthese
Als Substanzklasse kann Metoclopramid den aromatischen Aminosäureamiden zugeordnet werden. Somit steht die ganze Palette der Peptid-Synthesen zur Verfügung. Zur Knüpfung der Amid-Bindung kann entweder die Carbonsäure aktiviert werden, wobei Schutzgruppen der Aminogruppe eingesetzt werden, oder das aliphatische Amin wird aktiviert.
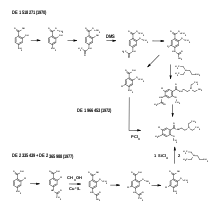
- Aktivierung der Aminobenzoesäure: MCP wurde 1964 neben mehreren Benzamiden bei der Firma Delagrange, heute Sanofi-Gruppe, entwickelt[19] und als Ausscheidung daraus als Patent angemeldet.[20] Ausgehend von 4-Aminosalicylsäure wird diese verestert, die Aminogruppe acetyliert, mit Dimethylsulfat alkyliert, der Aromat chloriert und der Ester einer Aminolyse mit Diethylaminoethylamin unterworfen. Die Umsetzung des relativ trägen Esters wird durch Aluminiumtriisopropylat katalysiert. Die Schutzgruppe wird schließlich mit Salzsäure abgespalten (siehe Reaktionsschema). Relativ spät wird die Methode der gemischten Anhydride für MCP geschützt.[21]
- Aktivierung von Diethylaminoethylamin: Schon lange ist bekannt, dass durch Acidolyse von Phosphorigsäureamiden Amide dargestellt werden können.[22] Dieses Verfahren wird auch zur Synthese von MCP herangezogen,[23] wobei man auch ohne Schutzgruppentechnik direkt 4-Amino-5-chlor-2-methoxybenzoesäure einsetzen kann.[24] Allerdings ist das Produkt gelb verfärbt. Phosphazene werden mit Phosphoroxychlorid erhalten, die als Base ebenfalls zu MCP umgesetzt werden können.[25] Ebenfalls ohne Schutzgruppe gelingt die Synthese von MCP durch direkte Acylierung von Silazanen.[26] Besonders gute Umsätze liefert diese Methode, wenn ein Molverhältnis Amin zu Siliciumtetrachlorid von 2 zu 1 gewählt wird.[27] Die vorangehende Anmeldung[28] zeigt auch einen Weg auf, wie der Einsatz von toxischem Dimethylsulfat zur Bildung des Ethers umgangen werden kann. Die in Gegenwart eines Liganden durch Kupfer(I)-katalysierte Solvolyse von 2-Chlorbenzoesäurederivaten in Methanol führt zu entsprechenden 2-Methoxybenzoesäuren (siehe Reaktionsschema).
Polymorphie
Metoclopramid kann als freie Base, wasserfreies Monohydrochlorid, Dihydrochlorid, Dihydrochlorid-Hydrat und Hydrochlorid-Hydrat isoliert werden. Für feste galenische Zubereitungen ist die polymorphe Form des Wirkstoffes von entscheidender Bedeutung für die Freisetzungsrate.[29] Die Form I des wasserfreien Metoclopramidhydrochlorids zeigt einen Schmelzpunkt von 187 °C, während die metastabile Form II bereits bei 155 °C schmilzt.[30] Im Diagramm der Differenzial-Thermoanalyse (DSC) der Form I sind bei einer Heizrate von 2 °C pro Minute zwei Maxima bei 97 °C und 190 °C erkennbar, resultierend aus Wasserverlust und Schmelzvorgang. Auch MCP-Base zeigt das Phänomen der Polymorphie.[30]
Handelsformen und -namen
Metoclopramid kann oral, intravenös oder rektal verabreicht werden. In Zäpfchen wird vor allem die freie Base, in Tabletten, Tropfen und Injektionslösung das Hydrochlorid-Monohydrat („Metoclopramidhydrochlorid (Ph. Eur.)“) eingesetzt. Lösungen zum Einnehmen waren in Deutschland als Fertigarzneimittel lediglich in Konzentrationen mit 4 bis 5 mg/ml im Handel. Nachdem diese mit Wirkung ab 9. April 2014 nicht mehr verkehrsfähig waren, haben pharmazeutische Unternehmen neue Zulassungen für entsprechend niedrig dosierte Präparate beantragt.[31] Diese sind seit August 2015 in einer Dosierung von 1 mg/ml erhältlich.[32]
Ceolat (A), Cerucal (D), Gastronerton (D), Gastrosil (A), Metogastron (A), Paspertin (D, A, CH), Primperan (CH), Geffer (ITA), zahlreiche Generika (D)
Migpriv (CH), Migraeflux (D), Migräne-Neuridal (D), Migraenerton (D), Migralave (D)
Emeprid, Vomend
Einzelnachweise
- Europäische Arzneibuch-Kommission (Hrsg.): Europäische Pharmakopöe 5. Ausgabe. Band 5.0–5.8, 2006.
- The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals, 14. Auflage (Merck & Co., Inc.), Whitehouse Station, NJ, USA, 2006, ISBN 978-0-911910-00-1; S. 1058–1059.
- Eintrag zu Metoclopramide in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
- Datenblatt Metoclopramide hydrochloride bei Sigma-Aldrich, abgerufen am 10. April 2011 (PDF).
- J. Wallenborn, L. Eberhart, Peter Kranke: Postoperative Übelkeit und Erbrechen – Alles beim Alten in der Pharmakotherapie von PONV? In: Anästhesiologie, Intensivmedizin, Notfallmedizin, Schmerztherapie. Band 44, 2009, S. 296–305; PMID 19367534.
- J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704, hier: S. 695 f. und 701.
- Vgl. J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704.
- MCP-ratiopharm® 1 mg/ml Lösung zum Einnehmen – ratiopharm GmbH. Abgerufen am 14. Januar 2018.
- European Medicines Agency recommends changes to the use of metoclopramide, Pressemitteilung der EMA vom 26. Juli 2013.
- APOTHEKE ADHOC: „Ärzte hätten stringenter sein müssen“.
- Embryotox.de: Arzneimittelsicherheit in Schwangerschaft und Stillzeit: Datenbank Medikamente und Wirkstoffe: Metoclopramid (Memento vom 9. September 2013 im Internet Archive).
- Fachinformation Emeprid, Stand Mai 2010.
- J. Wallenborn und andere: Metoclopramid und Dexamethason zur Prophylaxe von postoperativer Übelkeit und Erbrechen nach balancierter Anästhesie. In: AINS. Band 38, Nr. 11, November 2003, S. 695–704, hier: S. 702.
- Gebrauchsinformation MCP-AbZ 1mg/ml Lösung. AbZ-Pharma, abgerufen am 19. Oktober 2019.
- U.S. Food and Drug Administration: FDA Requires Boxed Warning and Risk Mitigation Strategy for Metoclopramide-Containing Drugs. In: Press Announcements. U.S. Food and Drug Administration. 26. Februar 2009. Abgerufen am 16. Juli 2011.
- BfArM: Metoclopramidhaltige Arzneimittel: Umsetzung des Durchführungsbeschlusses der EU-Kommission, 23. April 2014.
- Pharmazeutische Zeitung online: BfArM ruft MCP zurück, 16. April 2014.
- Rote Liste
- Patent BE648164: Nouveux procédé de préparation de benzamides substitués.. Veröffentlicht am 20. November 1964, Erfinder: Leon Thominet Michel (Ile de France).
- Patent DE1518271: Verfahren zur Herstellung von substituierten Benzamiden.. Veröffentlicht am 17. Dezember 1970, Erfinder: Leon Thominet Michel (Societe d'Etudes Scientifiques et Industrielles de l'Ile-de-France ).
- Patent DE2327192: Verfahren zur Herstellung von 2-Alkoxy-4,5-disubstituierten Benzamiden.. Veröffentlicht am 13. Dezember 1973, Erfinder: Bulteau Gerard, Acher Jaques (Societe d'Etudes Scientifiques et Industrielles de l'Ile-de-France).
- Goldschmidt Stefan, Krauss, H. L.: N-substituierte Amide der Phosphorigen und der Phosphor-Säure und ihre Verwendung zum Aufbau von Peptid-Bindungen. In: Angew. Chem. Band 57, Nr. 17-18, 1955, S. 471–475, doi:10.1002/ange.19550671705.
- Patent DE1932512: Verfahren zur Herstellung son therapeutisch aktivem N Diäthyl-aminoäthyl-2-methoxy-4-amino-5-chlorbenzamid und dessen physiologisch wirksamen Salzen.. Veröffentlicht am 19. Oktober 1972, Erfinder: Murakami Masuo, Inukai Norioshi, Koda Akio. Nakano Koji (YAMANOUCHI PHARMA CO LTD).
- Patent DE1966453: Neue Verfahren zur Herstellung von N-(Diäthylaminoäthyl) 4-amino-2-methoxybenzamiden.. Veröffentlicht am 8. Januar 1970, Erfinder: Meri Broms (HUHTAMAEKI YHTYMAE OY LAEAEKET).
- Patent DE2162947: Neue Verfahren zur Herstellung von Benzamidderivaten.. Veröffentlicht am 7. September 1972, Erfinder: Nakajima I., Tsuijkawa K., Kato Yukuru, Shinuchi Tadami (TEIKOKU CHEMICAL IND.).
- Patent DE2342934: Verfahren zur Herstellung von Benzamidverbindugen.. Veröffentlicht am 28. März 1974, Erfinder: Podesva, Ctirad; Scott, William Thomas; Navratil, Milada M.; Kishner, Lynda D.; (Delmar Chemicals Ltd.).
- Patent DE2365988: Verfahren zur Herstellung von N-Dialkylaminoäthyl-2-alkoxy-4-aminobenzoesäureamiden.. Veröffentlicht am 17. März 1977, Erfinder: Liebenow Walter, Grafe Ingomar (LUDWIG HEUMANN & Co GmbH).
- Patent DE2335439: Verfahren zur Herstellung von N-Dialkylaminoäthyl-2-alkoxy-4-amino-benzoesäuren.. Veröffentlicht am 6. Februar 1975, Erfinder: Antrag auf Nichtnennung (LUDWIG HEUMANN & Co GmbH).
- Maria Esther Dias Reis, Jennifer Tavares Jacon, Mônica Esselin, de Sousa Lino, Juliana Savioli Simões et al.: Polymorphism: an evaluation of the potential risk to the quality of drug products from the Farmácia Popular Rede Própria. In: Brazilian Journal of Pharmaceutical Sciences. Band 50, 2014, S. 1, doi:10.1590/S1984-82502011000100002 (englisch).
- A. G. Mitchell: Polymorphism in metoclopramide hydrochloride and metoclopramide. In: Journal of Pharmacy and Pharmacology. Band 37, Nr. 9, 1985, S. 601–604, doi:10.1111/j.2042-7158.1985.tb05093.x (englisch).
- APOTHEKE ADHOC: MCP-Rückruf reißt Lücke, 16. April 2014.
- MCP-Tropfen sind zurück (Memento vom 9. Dezember 2015 im Internet Archive), 30. Juli 2015.
Siehe auch
Weblinks
- Eintrag zu Metoclopramid bei Vetpharm, abgerufen am 5. August 2012.