Assimilation (Biologie)
Assimilation (lateinisch assimilatio ‚Angleichung, Eingliederung‘) ist der anabole Stoff- und Energiewechsel von Lebewesen, bei dem aufgenommene, fremde anorganische und organische Stoffe aus der Umwelt in Bestandteile des Organismus umgewandelt werden, meistens unter Energiezufuhr. Dabei wird je nach Betrachtungsweise zwischen Kohlenstoff-, Stickstoff-, Schwefel-, Phosphat- und Mineralstoff-Assimilation unterschieden. Dissimilation bezeichnet den umgekehrten Stoff- und Energiewechsel.
Kohlenstoff-Assimilation
Die Kohlenstoff-Assimilation (oder auch C-Assimilation) ist der wichtigste Assimilationsprozess.[1]
Heterotrophe Organismen (Tiere, Pilze, Protisten, die meisten Bakterien) bauen körpereigene Stoffe aus organischen Stoffen auf, die sie der Umgebung entnehmen und die somit unter anderem als Kohlenstoffquelle dienen.[1]
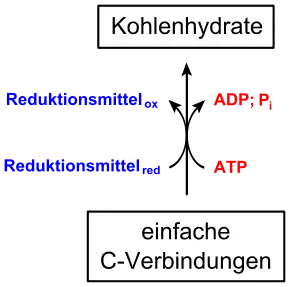
Autotrophe Organismen (Pflanzen, einige Bakterien) stellen aus Kohlenstoffdioxid (CO2) bei der Kohlenstoffdioxid-Assimilation durch Zufuhr von Energie und mit Hilfe eines Reduktionsmittels energiereiche, einfache organische Stoffe her, die im weiteren Stoffwechsel zu komplexeren Molekülen umgewandelt werden.[1]
Photoautotrophe Organismen (Pflanzen, einige Bakterien) nutzen Licht als Energiequelle. Diese Form der Assimilation wird deshalb Photosynthese genannt. Ein Beispiel dafür ist die Bildung von D-Glucose (C6H12O6) aus Kohlenstoffdioxid (CO2) und Wasser mithilfe von Lichtenergie:
- 6 H2O + 6 CO2→ C6H12O6 + 6 O2
Die benötigte Lichtenergie beträgt unter thermodynamischen Standardbedingungen 2872 kJ/mol.
- Alle grünen Pflanzen und einige Bakterien (Cyanobakterien) nutzen bei der Photosynthese Wasser als Reduktionsmittel bzw. Elektronenquelle. Dabei wird auch Sauerstoff erzeugt, sodass eine oxygene Photosynthese vorliegt.
- Andere Bakterien nutzen Wasserstoff (H2), Schwefelwasserstoff (H2S), Schwefel oder Eisen(II)-Ionen als Reduktionsmittel. Da hierbei kein Sauerstoff frei wird, bezeichnet man dies als eine anoxygene Photosynthese.
Chemoautotrophe Organismen (einige Bakterien) nutzen chemische Energie, die sie aus exergonen chemischen Stoffumsetzungen gewinnen. Diese Form der Assimilation wird deshalb Chemosynthese oder Chemotrophie genannt.[1]
Phosphat-Assimilation bei Pflanzen
Die Wurzeln der Pflanzen importieren Phosphat-Ionen (HPO42−) aus dem Boden über H+/PO43−-Symporter in der Zellmembran von Rhizodermis-Zellen. Phosphat dient u. a. als Substrat für die Phosphorylierung von Adenosindiphosphat (ADP) zu Adenosintriphosphat (ATP) im Zytosol (Glycolyse), in den Mitochondrien (Citrat-Zyklus) und in den Chloroplasten (Photosynthese). Die hinzugefügte Phosphat-Gruppe kann in weiteren Reaktionen für die Synthese von Zuckerphosphaten, Phospholipiden oder Nukleotiden eingesetzt werden.
Schwefel-Assimilation bei Pflanzen
Schwefel wird hauptsächlich in Form von Sulfat (SO42−) aus verwitterndem Gestein über H+/SO42−-Symporter aufgenommen (vgl. Phosphat-Assimilation) und vor allem in Blättern über mehrere Schritte unter Reduktion bei der Synthese der Aminosäure Cystein verwendet. Glutathion, Ferredoxin, NADH, NADPH und O-Acetylserin wirken hierbei als Elektronen-Donatoren. Cystein liefert in den Plastiden Schwefel, gebunden in einer Sulfhydrylgruppe, für die Synthese von Methionin, einer weiteren schwefelhaltigen Aminosäure. Der Schwefel dieser beiden Aminosäuren kann nachfolgend in Proteine, Acetyl-CoA oder S-Adenosylmethionin eingebaut werden und in Form von Glutathion über das Phloem in den Spross, in die Wurzelspitzen und in Früchte transportiert werden, wo keine Schwefel-Assimilation stattfindet.[2]
Stickstoff-Assimilation bei Pflanzen
Pflanzen und viele Bakterien verwenden den Stickstoff aus Nitrat (NO3−) oder Ammonium (NH4+) für die Herstellung stickstoffhaltiger organischer Verbindungen.
Nitrat-Assimilation
Die Assimilation von Stickstoff aus Nitrat erfolgt bei Pflanzen artabhängig vorwiegend in der Wurzel oder im Spross. Über die Reduktion von Nitrat zu Nitrit und Ammonium mündet sie in die Synthese von Asparagin und Glutamin.
Nitrat (NO3−) wird wie Sulfat und Phosphat über einen H+-Symport in die Wurzeln aufgenommen. Im Zytosol wird Nitrat von der Nitratreduktase zu Nitrit (NO2−) reduziert. Als Reduktionsmittel dient hauptsächlich NADH, daneben in nicht-grünen Geweben auch NADPH. Die durch Licht bedingte Dephosphorylierung eines bestimmten Serin-Rests der Nitratreduktase führt zur Aktivierung dieses Enzyms, während Dunkelheit zur Phosphorylierung und somit Enzym-Inaktivierung führt. Daher wird Nitrat vor allem am Tag (während der Photosynthese) assimiliert. Nitrit wird in die Plastiden transportiert und dort durch die Nitritreduktase zu Ammonium reduziert. Die für die Reduktion benötigten Elektronen liefert Ferredoxin, das in Wurzeln Elektronen aus dem im oxidativen Pentosephosphatweg gebildeten NADPH erhält. In grünen Geweben stammen die Elektronen aus der photosynthetischen Elektronentransportkette. Die Expression der Nitritreduktase-Gene wird durch Licht und erhöhte Nitrat-Konzentration erhöht, während Asparagin und Glutamin als Endprodukte der Nitrat-Assimilation die Enzymbildung hemmen.[2]
Zusammengefasst in Formeln:
1. Schritt (Nitratreduktase): NO3− + NADH + H+ → NO2− + NAD+ + H2O
2. Schritt (Nitritreduktase): NO2− + 6 Fdred + 8 H+ → NH4+ + 6 Fdox + 2 H2O
Ammonium-Assimilation
In den Plastiden katalysiert die Glutamat-Ammonium-Ligase den Einbau von Ammonium-Stickstoff in Form einer Amidogruppe in die Aminosäure Glutaminsäure (Glutamat), wodurch Glutamin entsteht. In einem zweiten Schritt überträgt die Glutamat-Synthase diese Amidogruppe als Aminogruppe auf 2-Oxoglutarat, wodurch zwei Moleküle Glutaminsäure entstehen:
- Glutamat + NH4+ + ATP → Glutamin + ADP + Pi (Glutamat-Ammonium-Ligase)
- Glutamin + 2-Oxoglutarat + e− → 2 Glutamat (Glutamat-Synthase)
Als Elektronen-Donator für die Glutaminsäure-Synthese wird in den Wurzel-Plastiden NADH und in den Chloroplasten der Blätter Ferredoxin verwendet. Ammonium kann gleichzeitig über die Glutamat-Dehydrogenase assimiliert werden:
- 2-Oxoglutarat + NH4+ + e− → Glutamat + H2O (Glutamatdehydrogenase)
Elektronen-Donator für diese Reaktion ist in den Mitochondrien NADH, in den Chloroplasten NADPH.
Der in Glutamin und Glutamat eingebaute Stickstoff wird durch Transaminierung zur Synthese anderer Aminosäuren verwendet. Diese durch Aminotransferasen katalysierten Reaktionen entsprechen der Bindung der Aminogruppe einer Aminosäure an die Carbonylgruppe eines Intermediats aus der Glycolyse (3-Phosphoglycerat, Phosphoenolpyruvat und Pyruvat) oder aus dem Citrat-Zyklus (α-Ketoglutarat und Oxalacetat).
Ein Beispiel für Transaminierungsreaktionen liefert die Aspartat-Aminotransferase:
- Glutamat + Oxalacetat → Aspartat + 2-Oxoglutarat
Das hier gebildete Aspartat (eine Aminosäure) ist ein Substrat für die Asparaginsynthetase:
- Aspartat + Glutamin + ATP → Asparagin + Glutamat + AMP + PPi
Asparagin ist als Aminosäure nicht nur ein Substrat für die Proteinbiosynthese, sondern dient auch basierend auf dem hohen N:C-Verhältnis der Speicherung und dem Transport von Stickstoff.
Die Expression der Asparagin-Synthetase-Gene wird durch Licht und Kohlenhydrate verringert. Daher geschieht die Regulation dieses Enzyms komplementär zur Regulation der Enzyme für die Glutamin- und Glutamatsynthese (Glutamin- bzw. Glutamat-Synthase). Folgerichtig wird bei ausreichender Energie-Verfügbarkeit (viel Licht, hohe Kohlenhydrat-Konzentrationen) die Synthese der relativ kohlenstoffreichen Stoffe Glutamin und Glutamat begünstigt; bei Energie-Knappheit (wenig Licht, geringe Kohlenhydrat-Konzentrationen) überwiegt die Synthese von kohlenstoffarmem Asparagin zwecks Speicherung und Transport von Stickstoff.
Nitrat- und Ammonium-Assimilation ermöglichen Pflanzen, alle für ihren Metabolismus notwendigen Aminosäuren herzustellen. Menschen und Tiere können bestimmte Aminosäuren nicht selbst synthetisieren und müssen diese als essentielle Aminosäuren aus ihrer Nahrung beziehen, die direkt oder indirekt aus Pflanzen stammen. Zu den essentiellen Aminosäuren gehören Histidin, Isoleucin, Lysin, Methionin, Phenylalanin, Threonin, Tryptophan und Valin.
Viele Leguminosen-Arten beziehen im Rahmen der Stickstoff-Assimilation Ammoniak (NH3) aus der Symbiose mit Bakterien der Gattung Rhizobium („Knöllchenbakterien“), die elementaren Stickstoff (N2) zu Ammoniak reduzieren, während Algenfarne Ammoniak aus der Symbiose mit N2-reduzierenden Cyanobakterien erhalten.[3]
Literatur
- Gerhard Richter: Stoffwechselphysiologie der Pflanzen. Stuttgart: Thieme 1998, ISBN 978-3-134420067.
Einzelnachweise
- Horst Bannwarth, Bruno P. Kremer, Andreas Schulz: Basiswissen Physik, Chemie und Biochemie, S. 381; ISBN 978-3642107665.
- Peter Karlson, Detlef Doenecke, Jan Koolman, Georg Fuchs, Wolfgang Gerok: Karlsons Biochemie und Pathobiochemie, S. 443.
- Jan Koolman, Klaus-Heinrich Röhm: Taschenatlas Biochemie des Menschen, S. 164.