Dimethylformamid-dimethylacetal
Dimethylformamid-dimethylacetal ist das durch Acetalisierung von Dimethylformamid mit Methanol gebildete und zwei Alkoxygruppen an der Carbonylgruppe tragende Amid-Acetal. Die Verbindung hat als Formylierungsreagenz und Methylierungsmittel für Carbonsäuren, Phenole, Amine, Thiole und Aminosäuren[5][6][7] sowie als Molekülbaustein (building block), insbesondere für Heterocyclen,[8] größere Verbreitung gefunden.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
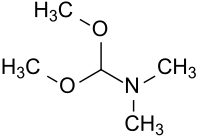 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Dimethylformamid-dimethylacetal | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C5H13NO2 | ||||||||||||||||||
| Kurzbeschreibung | |||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 119,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt |
−85 °C bei 1,013 hPa[4] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,3972 (20 °C, 589 nm)[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Vorkommen und Darstellung
Analog der ersten Veröffentlichung über Dimethylformamid-diethylacetal aus dem Arbeitskreis von Hellmut Bredereck[9] wird das Dimethylformamid-dimethylacetal des durch Umsetzung (O-Methylierung) von Dimethylformamid mit Dimethylsulfat erhaltenen Addukts mit Natriummethanolat in Methanol bei 0 °C in Ausbeuten von 72 bis 87 % erhalten.[10][11]
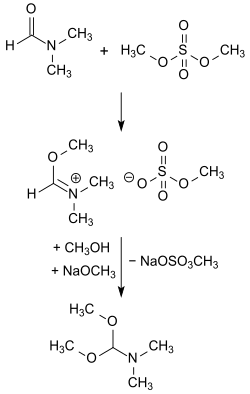
Wegen der Zersetzung des DMF-DMA bei der Destillation unter Normaldruck wird die schnelle Destillation des Reaktionsgemischs unter Zugabe von Methanol als Schleppmittel und anschließende fraktionierte Destillation des erhaltenen Methanol/DMF-DMA-Gemischs empfohlen. Dadurch werden Reinausbeuten von Dimethylformamid-dimethylacetal von 85 bis 90 % erreicht.[12]
Die Reaktion des Vilsmeier-Reagenz' N,N-Dimethyl(chlormethylen)iminiumchlorid in Chloroform mit Natriummethanolat in Methanol liefert DMF-DMA in 55%iger Ausbeute.[13][14]
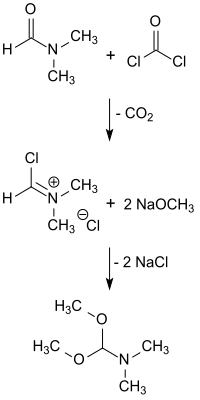
Dimethylformamid-dimethylacetal entsteht auch bei Umsetzung der Reaktanden Methanolat, DMF und CHCl3.[15] Dabei reagiert Chloroform mit festem Natriummethanolat oder Natriummethanolat in Methanol vermutlich über das intermediär gebildete Dichlorcarben :CCl2, das Dimethylformamid unter CO-Abspaltung zu DMF-DMA umsetzt.[16]
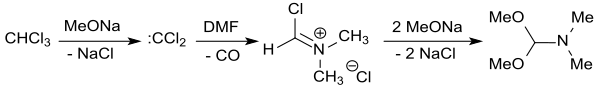
In millimolaren Ansätzen werden Rohausbeuten bis 91 % erzielt.
Eigenschaften
Dimethylformamid-dimethylacetal ist eine klare, farblose, aminartig riechende Flüssigkeit, die sich mit Wasser und vielen organischen Lösungsmitteln mischt. In Wasser zersetzt sich das Acetal allmählich.[6]
Anwendungen
DMF-DMA als Methylierungsmittel
Acide Verbindungen[17], wie z. B. Carbonsäuren[18][19], Phenole[18], Thiole[20] werden von Dimethylformamid-dimethylacetal in glatter Reaktion methyliert,
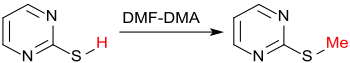
ebenso wie NH-Heterocyclen, wie z. B. Triazole.[21]
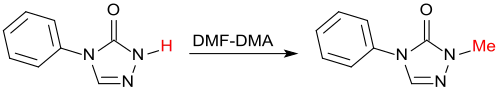
DMF-DMA als Formylierungsmittel
Dimethylformamid-dimethylacetal reagiert mit primären Aminen zu N,N-Dimethylformamidinen[22] und mit α-Aminosäuren zu den entsprechenden relativ stabilen α-Formamidinomethylestern.[23]
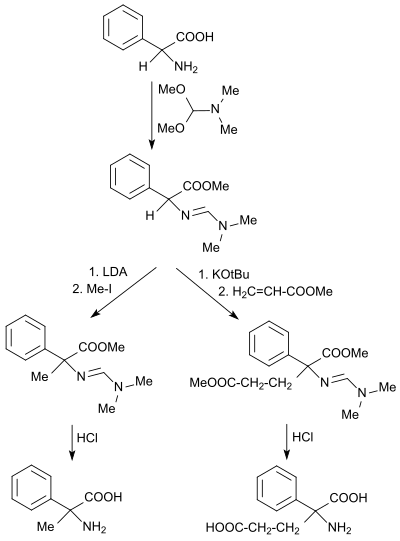
Die α-Formamidinomethylester können mit guten Ausbeuten nach Deprotonierung mit starken Basen, wie z. B. Lithiumdiisopropylamid LDA oder Kalium-tert-butanolat KOtBu mit Alkylhalogeniden, wie z. B. Iodmethan alkyliert oder in einer Michael-Addition mit z. B. Acrylsäuremethylester umgesetzt werden.
Als Alternative zur eher als Laborverfahren geeigneten Synthese des cyclischen Polyamins Cyclen nach Reed und Weisman[24] eignet sich die Umsetzung von Triethylentetramin TETA mit DMF-DMA unter Bildung des Bis-Amidins 1,1'-Ethylendi-2-imidazolin in 85%iger Ausbeute (1. Stufe). Dessen Makrocyclisierung unter Verdünnungsbedingungen mit 1,2-Dibromethan liefert eine Monoimidazolium-Verbindung mit 70%iger Ausbeute, die anschließend mit kochender Kalilauge in einer Ausbeute von 88 % zum Cyclen gespalten wird.[25][26]
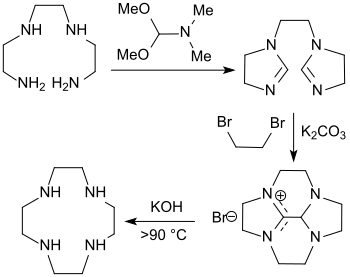
Durch Reaktion von Dimethylformamid-dimethylacetal mit sekundären Aminen werden die entsprechenden N-Formyl-N,N-dialkylamine gebildet.[27]
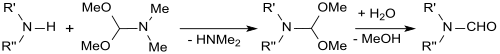
Mit CH-aciden Verbindungen mit aktivierten Methylengruppen, wie z. B. Ketonen, reagiert DMF-DMA glatt zu vinylogen Amiden, den so genannten Enaminonen.[28]
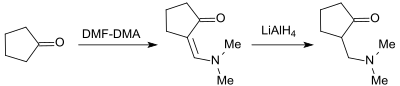
So bildet Cyclopentanon mit DMF-DMA in 86%iger Ausbeute das entsprechende Enaminon, das mit Lithiumaluminiumhydrid LiAlH4 in 88%iger Ausbeute die entsprechende Mannich-Base ergibt.[29]
Mit Diketonen werden analog Bis-Enaminone gebildet, aus denen eine Vielzahl von Heterocyclen zugänglich sind.[30]
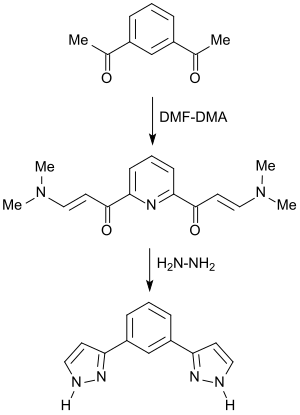
Das bei der Reaktion von 2,6-Diacetylpyridin mit DMF-DMA praktisch quantitativ entstehende Bis-Enaminon reagiert mit Hydrazin zum 3-Arylpyrazol.[31]
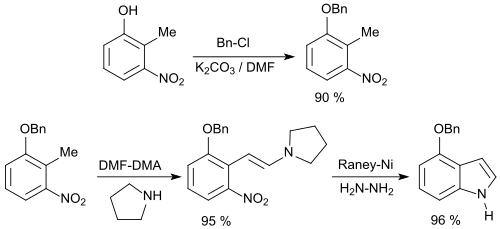
Eine effektive Methode zur Herstellung substituierter Indole ist die in der englischen Literatur so genannte "Leimgruber-Batcho indole synthesis" aus 2-Nitrotoluolen und Dimethylformamid-dimethylacetal, wobei zur Reaktionsbeschleunigung Pyrrolidin zugesetzt wird.[32]
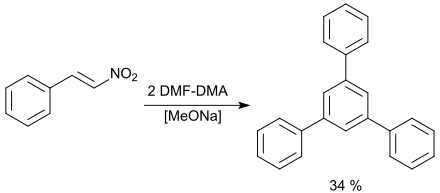
In Gegenwart von Natriummethanolat-Spuren bildet sich aus β-Nitrostyrolen und zwei Äquivalenten DMF-DMA in DMF in mäßigen Ausbeuten (bis 40 %) 1,3,5-Triphenylbenzole.[33]
Andere Reaktionen mit DMF-DMA
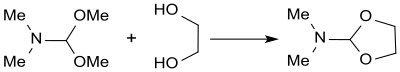
Wie das homologe Dimethylformamid-diethylacetal kann DMF-DMA mit überschüssigen höheren Alkoholen zu den entsprechenden Dimethylformamid-dialkylacetalen umacetalisiert werden (Umacetalisierung).[34]
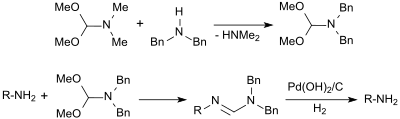
Die Umamidierung von DMF-DMA mit Dibenzylamin liefert N,N-Dibenzylformamid-dimethylacetal, das sich als Schutzgruppe für primären Amine eignet, mit denen es glatt zu Amidinen reagiert. Diese Schutzgruppe ist gegenüber Säuren, Basen und Nukleophilen stabil und kann durch katalytische Hydrierung mit Palladium(II)-oxid auf Aktivkohle wieder abgespalten werden.[35]
Dimethylformamid-dimethylacetal kann als Scavenger für Schwefelwasserstoff H2S und Mercaptane in Erdgas und kohlenwasserstoffbasierten Treibstoffen, wie z. B. Benzin, Diesel oder Kerosin eingesetzt werden.[36]
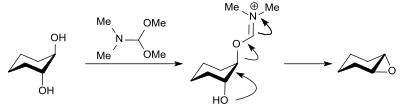
Mit 1,2-Diolen, wie z. B. trans-Cyclohexan-1,2-diol, reagiert DMF-DMA in hoher Ausbeute (88 %) unter Konfigurationsumkehr zum Epoxid Cyclohexenoxid.[6][5]
Einzelnachweise
- Eintrag zu N,N-Dimethylformamide Dimethyl Acetal for Esterification bei TCI Europe, abgerufen am 25. September 2017.
- Datenblatt N,N-Dimethylformamid-dimethylacetal bei Sigma-Aldrich, abgerufen am 25. September 2017 (PDF).
- Datenblatt N,N-Dimethylformamid dimethyl acetal, 97% bei AlfaAesar, abgerufen am 25. September 2017 (PDF) (JavaScript erforderlich).
- Datenblatt N,N-Dimethylformamiddimethylacetal zur Synthese (PDF) bei Merck, abgerufen am 3. November 2021.
- R.F. Abdulla, R.S. Brinkmeyer: The chemistry of formamide acetals. In: Tetrahedron. Band 35, Nr. 14, 1979, S. 1675–1735, doi:10.1016/0040-4020(79)88001-1.
- U. Pindur: N,N-Dimethylformamide Diethyl Acetal. In: e-EROS Encyclopedia of Reagents for Organic Synthesis. 2001, doi:10.1002/047084289X.rd336.
- D. Kidjemet: N,N-Dimethylformamide Dimethyl Acetal. In: Synlett. Band 10, 2002, S. 1741–1742, doi:10.1055/s-2002-34251.
- F.A. Abu-Shabab, S.M. Sherif, S.A.S. Mousa: Dimethylformamide dimethyl acetal as a building block in heterocyclic synthesis. In: J. Heterocyclic Chem. Band 46, Nr. 5, 2009, S. 801–827, doi:10.1002/jhet.69.
- H. Bredereck, F. Effenberger, G. Simchen: Reaktionsfähige Säureamid-Dimethylsulfat-Komplexe. In: Angew. Chem. Band 73, Nr. 14, 1961, S. 493, doi:10.1002/ange.19610731407.
- H. Bredereck, G. Simchen, S. Rebsdat, W. Kantlehner, P. Horn, R. Wahl, H. Hoffmann, P. Grieshaber: Säureamid-Reaktionen, L; Orthoamide, I Darstellung und Eigenschaften der Amidacetale und Aminalester. In: Chem. Ber. Band 101, Nr. 1, 1964, S. 41–50, doi:10.1002/cber.19681010108.
- D. Mesnard, L. Miginiac: Synthèse régiospécifique d’amines tertiaries à groupe secondaires bi-insaturé. In: J. Organometallic Chem. Band 373, Nr. 1, 1989, S. 1–10, doi:10.1016/0022-328X(89)85018-1.
- Patent DE2215954: Verfahren zur destillativen Aufbereitung von Dimethylformamiddimethylacetal. Angemeldet am 1. April 1972, veröffentlicht am 23. November 1972, Anmelder: Deutsche Akademie der Wissenschaften zu Berlin, Erfinder: H. Groß, L. Haase, I. Keitel.
- H. Eilingsfeld, M. Seefelder, H. Weidinger: Amidchloride und Carbamidchloride. In: Angew. Chem. Band 72, Nr. 22, 1960, S. 836–845, doi:10.1002/ange.19600722208.
- H. Eilingsfeld, M. Seefelder, H. Weidinger: Synthesen mit Amidchloriden, I. Reaktionen an der funktionellen Gruppe N,N-disubstituierter Carbonsäureamidchloride. In: Chem. Ber. Band 96, Nr. 10, 1963, S. 2671–2690, doi:10.1002/cber.19630961023.
- J.W. Scheeren, R.J.F. Nivard: Synthesis and stability of tri-sec-aminomethanes. In: Recl. Trav. Chim. Pays-Bas. Band 88, Nr. 3, 1969, S. 289–300, doi:10.1002/recl.19690880306.
- P.L. Anelli, M. Brocchetta, D. Copez, D. Palano, M.V.P. Paoli: Unexpected formation of acylformamidines by reaction of primary carboxamides with MeONa in DMF in the presence of CHCl3. In: Tetrahedron. Band 53, Nr. 46, 1997, S. 15827–15832, doi:10.1016/0040-4020(97)10041-2.
- J. Gloede, B. Costisella: Zur Reaktion von Dimethylformamid-dimethylacetal mit aciden Verbindungen. In: J. Prakt. Chem. Band 313, Nr. 2, 1971, S. 277–286, doi:10.1002/prac.19713130212.
- H. Vorbrüggen: Die Reaktion von Carbonsäuren und Phenolen mit Amidacetalen. In: Angew. Chem. Band 75, Nr. 6, 1963, S. 296–297, doi:10.1002/ange.19630750612.
- J.-P. Thenot, E.C. Horning, M. Stafford: Fatty acid esterification with N,N-dimethylformamide dialkyl acetals for GC analysis. In: Analyt. Lett. Band 5, Nr. 4, 1972, S. 217–2223, doi:10.1080/00032717208069552.
- A. Holý: Transformation of nucleosides into their 5'-deoxy derivatives. In: Tetrahedron Lett. Band 13, Nr. 7, 1972, S. 585–588, doi:10.1016/S0040-4039(01)84384-7.
- G. Fairley, C. Hall, R. Greenwood: Selective Methylation of NH-Containing Heterocycles and Sulfonamides Using N,N-Dimethylformamide Dimethylacetal Based on Calculated pKa Measurements. In: Synlett. Band 24, Nr. 5, 2013, S. 570–574, doi:10.1055/s-0032-1318315.
- D.A. Dickman, M. Boes, A.I. Meyers: (S)-N,N-Dimethyl-N-(1-tert-butoxy-3-methyl-2-butyl)formamidine In: Organic Syntheses. 67, 1989, S. 52, doi:10.15227/orgsyn.067.0052; Coll. Vol. 8, 1993, S. 204 (PDF).
- J.J. Fitt, H.W. Gschwend: α-alkylation and Michael addition of amino acids: a practical method. In: J. Org. Chem. Band 42, Nr. 15, 1977, S. 2639–2641, doi:10.1021/jo00435a027.
- D.P. Reed, G.R. Weisman: 1,4,7,10-Tetraazacyclododecane In: Organic Syntheses. 78, 2002, S. 73, doi:10.15227/orgsyn.078.0073; Coll. Vol. 10, 2004, S. 667 (PDF).
- P.S. Athey, G.E. Kiefer: A new, facile synthesis of 1,4,7,10-tetraazacyclododecane: Cyclen. In: J. Org. Chem. Band 67, Nr. 12, 2002, S. 4081–4085, doi:10.1021/jo016111d.
- Patent US5587451A: Process for preparing polyazamacrocycles. Angemeldet am 1. Oktober 1994, veröffentlicht am 24. Dezember 1996, Anmelder: The Dow Chemical Co., Erfinder: P.S. Athey, G.E. Kiefer.
- J.-P. Thenot, T.I. Ruo, O.J. Bouwsma: Formylation of secondary amines with dimethylformamide dimethylacetal. In: Analyt. Lett. Band 13, Nr. 9, 1980, S. 759–769, doi:10.1080/00032718008077997.
- A.-Z.A. Elassar, A.A. El-Khair: Recent developments in the chemistry of enaminones. In: Tetrahedron. Band 59, Nr. 43, 2003, S. 8463–8480, doi:10.1016/S0040-4020(03)01201-8.
- P.F. Schuda, C.B. Ebner, T.M. Morgan: The synthesis of Mannich bases from ketones and esters via enaminones. In: Tetrahedron Lett. Band 27, Nr. 23, 1986, S. 2567–2570, doi:10.1016/S0040-4039(00)84586-4.
- Bis-enaminones as versatile precursors for terheterocycles: synthesis and reactions; A.S. Shawali, Arkivoc, 2012(i), 383–431 (PDF).
- A.-K. Pleier, H. Glas, M. Grosche P. Sirsch, W.R. Thiel: Microwave-assisted synthesis of 1-aryl-3-dimethylaminoprop-2-enones: A simple and rapid access to 3(5)-aryl pyrazoles. In: Synthesis. Band 1, 2001, S. 55–62, doi:10.1055/s-2001-9761.
- A.D. Batcho, W. Leimgruber: Indoles from 2-methylnitrobenzenes by condensation with formamide acetals followed by reduction: 4-benzyloxyindole In: Organic Syntheses. 63, 1985, S. 214, doi:10.15227/orgsyn.063.0214; Coll. Vol. 7, 1990, S. 34 (PDF).
- T.Y. Kim, H.S. Kim, K.Y. Lee, J.N. Kim: N,N-Dimethylformamide dimethylacetal (DMF-DMA) catalyzed formation of 1,3,5-trisubstituted benzene derivatives from α, β-unsaturated nitro compounds. In: Bull. Korean Chem. Soc. Band 20, Nr. 11, 1999, S. 1255–1256 (easechem.com [PDF]). N,N-Dimethylformamide dimethylacetal (DMF-DMA) catalyzed formation of 1,3,5-trisubstituted benzene derivatives from α, β-unsaturated nitro compounds (Memento vom 26. Oktober 2017 im Internet Archive)
- H. Meerwein, W. Florian, N. Schön, G. Stopp: Über Säureamidacetale, Harnstoffacetale und Lactamacetale. In: Justus Liebigs Ann. Chem. Band 641, Nr. 1, 1961, S. 1–39, doi:10.1002/cber.19616410102.
- S. Vincent, S. Mons, L. Lebeau, C. Mioskowski: N,N-Dibenzyl formamidine as a new protective group for primary amines. In: Tetrahedron Lett. Band 38, Nr. 43, 1997, S. 7527–7530, doi:10.1016/S0040-4039(97)10023-5.
- Patent US9273254B2: Amino acetals and ketals as hydrogen sulfide and mercaptan scavengers. Angemeldet am 20. Dezember 2013, veröffentlicht am 1. März 2016, Anmelder: Ecolab USA Inc., Erfinder: D.R. Compton, K. Ekoue-Kovi.



