Thiole
Thioalkohole sind organisch-chemische Verbindungen, die eine oder mehrere aliphatisch oder aromatisch gebundene Thiolgruppen (auch Mercaptogruppen) (–SH) als funktionelle Gruppen tragen. Thioalkohole entsprechen Alkoholen, deren Sauerstoffatom durch ein Schwefelatom ersetzt ist. Wie sich Alkohole und Phenole formal vom Wasser (H2O) ableiten, sind die Thioalkohole und Thiophenole Abkömmlinge des Schwefelwasserstoffs (H2S). Alkanthiole leiten sich direkt von den Alkanen mit Thiolgruppe ab. Thioalkohole bilden zusammen mit den Thiophenolen die Gruppe der Thiole.
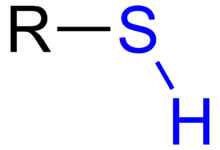
Nomenklatur
Thioalkohole nennt man aufgrund ihrer Fähigkeit, Quecksilber(II)-Ionen zu binden, auch Mercaptane (von lat. Mercurium captans: Quecksilber fangend). Die Namen einzelner Alkanthiole werden aus dem entsprechenden Namen des Alkans und der Endsilbe -thiol gebildet, beispielsweise Methanthiol, Ethanthiol usw. Bei Molekülen mit einer funktionellen Gruppe höherer Priorität wird die Vorsilbe Mercapto- (oder Sulfanyl-, veraltet auch Sulfhydryl-[1]) verwendet. Darüber hinaus haben viele Alkanthiole Trivialnamen, z. B. Ethylmercaptan für Ethanthiol.
Herstellung
Durch nukleophile Substitution an Alkylhalogeniden, Alkylsulfonaten oder Alkylsulfaten mit Hydrogensulfiden:[2]
Als Nebenprodukte entstehen hier Thioether:
Die Bildung von Thioethern kann durch einen Überschuss von Schwefelwasserstoff unterdrückt werden.
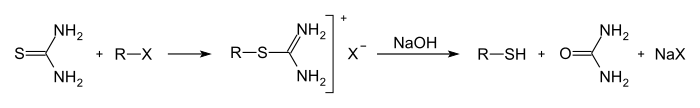
Frei von Thioethern erhält man Thioalkohole durch Alkylierung von Thioharnstoff mit Alkylhalogeniden und anschließendes Erhitzen mit Natronlauge.[2] Als Intermediat bildet sich hier ein Isothioronium-Salz:
Die Synthese kann auch durch Umsetzung von Alkoholen mit Schwefelwasserstoff an Aluminiumoxid als Katalysator erfolgen:[2]
Durch Sulfhydrierung von endständigen Olefinen mit Schwefelwasserstoff entstehen ebenfalls Thiole:[3]
Eigenschaften
Chemische Eigenschaften
Als Homologe der Alkohole – Schwefel steht in der gleichen Hauptgruppe wie Sauerstoff – gehen Thioalkohole ähnliche Reaktionen ein. Ihre Salze heißen Thiolate; die Anionen sind gute Nukleophile. Weiterhin sind sie Reduktionsmittel, die beispielsweise vielfach in der Proteinchemie eingesetzt werden.
Da die S–H-Bindung schwächer ist als die O–H-Bindung, sind Thioalkohole stärker sauer als die analogen Alkohole und bilden bereits in wässriger NaOH-Lösung Thiolate. Ferner lassen sich Thiole im Gegensatz zu Alkoholen oxidativ zu Disulfiden dimerisieren; dies ist wichtig bei Proteinen, in denen zwei Aminosäure-Ketten über Cystein-Einheiten verknüpft sein können, wobei Cystin-Derivate entstehen.
Physikalische Eigenschaften
Thioalkohole sieden niedriger als die analogen Alkohole, da Schwefel aufgrund der geringeren Elektronegativität zum Wasserstoff schwächere Wasserstoffbrückenbindungen bildet.
Toxizität
Flüchtige Thiole, vor allem die kurzkettigen Homologe, riechen besonders widerwärtig. Sie wirken toxisch auf das Zentralnervensystem.
Vorkommen

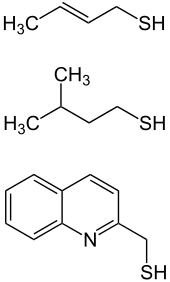
Als Aromastoffe findet man Thioalkohole u. a. in Milch, Käse, Zwiebeln und Knoblauch. Sie werden bei Abbau- und Fäulnisprozessen von organischem Material frei, z. B. in Biogasanlagen. Mehrere Thioalkohole kommen im Drüsensekret des Stinktiers vor.[4] Weitere Beispiele für das Vorkommen von Thiolen sind Rohöl und das Kondensat aus der Erdgasgewinnung. Das Erdgaskondensat aus dem von Katar und dem Iran erschlossenen Gasfeld South Pars kann bis zu 3000 ppm Mercaptane enthalten.
Beispiele für Thioalkohole
- Acetylcystein
- Dimercaptobernsteinsäure
- Dimercaptopropansulfonsäure
- Ethanthiol (Ethylmercaptan)
- Dithiothreitol (DTT)
- Dithioerythritol (DTE)
- Captopril
- Coenzym A
- Cystein
- Penicillamin
- 1-Propanthiol
- 2-Propanthiol
- Glutathion
- Homocystein
- Mesna
- Methanthiol (Methylmercaptan)
- Thiophenol
Anwendung
Besonders lineare Thiole wie Hexadecanthiol finden in neuerer Zeit verstärkt Anwendung beim Aufbau selbstorganisierender Monoschichten (Self Assembling Monolayers, SAM). Die hohe Affinität der Thiolgruppe zu Münzmetallen, insbesondere Gold, führt dazu, dass sich die Thiole spontan in einer hochgeordneten Schicht zusammenlagern, wenn ein Goldsubstrat einer Thiollösung exponiert wird. Sind die Thiole geeignet funktionalisiert, wie zum Beispiel mit ssDNA oder Proteinen, bildet dieses System die Grundlage für Biosensoren (Biacore). Die metallkomplexierende Eigenschaft wird in verschiedenen Antidoten gegen Schwermetallvergiftungen (z. B. Blei, Quecksilber oder Cadmium) genutzt. Ein weiterer antidotischer Effekt liegt in der reduzierenden Eigenschaft der Sulfhydrylgruppe.
Darüber hinaus werden Brenngasen wie Erdgas oder Campinggas Gemische aus Methanthiol, Ethanthiol, Propan-1-thiol und 2-Methyl-2-propanthiol (tert-Butylmercaptan, TBM) als Odorierungsmittel beigemengt. Sie erzeugen den „Gasgeruch“, da Erdgas bzw. Methan selbst geruchlos sind, und tragen zur sicheren Verwendung dieser Brennstoffe bei. Ein Beispiel dafür ist die unbeabsichtigte Freisetzung des Odorierungsmittels am 16. Januar 2001 im Stadtlabor Berns, wonach die Altstadt wegen Gasgeruchs für den Verkehr gesperrt wurde.[5]
Weblinks
Einzelnachweise
- Eintrag zu Thiole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 7. Juni 2014.
- Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. 23. Auflage. S. Hirzel, Stuttgart 1998, ISBN 3-7776-0808-4.
- Patent DE6031183: Katalytisches Verfahren zur Herstellung von Alkylmercaptanen durch Additionsreaktion von Wasserstoffsulfid an ein Olefin. Veröffentlicht am 23. September 2003, Erfinder: Georges Fremy, Nadina Essayem, Michael Lacroix, Elodie Zausa.
- Wolfgang Legrum: Riechstoffe, zwischen Gestank und Duft. Vieweg + Teubner, 2011, ISBN 978-3-8348-1245-2, S. 55.
- Gasgeruch in Berner Altstadt. In: new.ch. 16. Januar 2001, abgerufen am 3. Februar 2019.