Dimethylsulfat
Dimethylsulfat ist eine farblose, süßlich riechende sehr giftige Flüssigkeit. Sie ist der Dimethylester der Schwefelsäure und in mäßiger Ausbeute aus Methanol und H2SO4 erhältlich. In chemischen Synthesen ist es ein äußerst potentes Alkylierungsmittel. Seine Giftigkeit beruht auf der Alkylierung von DNA und Proteinen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
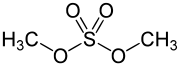 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Dimethylsulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C2H6O4S | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit süßlichem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 126,13 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
1,33 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
188,5 °C (Zersetzung)[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (28 g·l−1 bei 18 °C)[1] | |||||||||||||||
| Brechungsindex |
1,3874 (20 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR)[4] | |||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−735,5 kJ/mol[6] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
In Europa wird die größte Produktionsanlage von der Grillo-Werke AG im Industriepark Höchst am Standort Frankfurt betrieben.[7]
Die häufig verwendete Abkürzung DMS ist nicht eindeutig, da sie ebenso für Dimethylsulfid, Dimethylsulfon und Dimethylsulfit verwendet wird. Eine Verwechslung der Stoffe ist wegen ihrer unterschiedlichen Eigenschaften gefährlich.
Synthese
Die Synthese erfolgt durch die Umsetzung von Dimethylether mit Schwefeltrioxid (SO3). Bis in die 1980er Jahre war dies die Hauptverwendung von Dimethylether, 1998 wurden von den in Mitteleuropa produzierten 50.000 t etwa 15.000 t zu Dimethylsulfat umgesetzt.[8]
Reaktionsverhalten
Das Sulfation ist ein sehr schwaches Nucleophil und damit eine hervorragende Abgangsgruppe in einer SN-Reaktion. Darauf beruht die kräftige Methylierungsfähigkeit des Dimethylsulfats. Bei Raumtemperatur reagiert zunächst nur eine Methylgruppe, bei Erwärmung können beide Methylgruppen ausgenutzt werden. Als Beispiel für eine solche Methylierung sei hier die Reaktion mit einer Carbonsäure erwähnt:
- Herstellung eines Carbonsäuremethylesters
Verwendung
Dimethylsulfat wird in Labor und Technik zur Methylierung von Carbonsäuren, Aminen, Phenolen und anderen Verbindungen verwendet. Es ist ein Rohstoff für die Herstellung von Kosmetika, Weichspüler für Textilien, Farben, Arzneimitteln und Agrarprodukten. In der Molekularbiologie wurde es als Reagenz für die Methylierung der Base Guanin (G) eingesetzt, die einem spezifischen Strangbruch bei der Sequenzierung nach Maxam und Gilbert vorausgeht.
Sicherheitshinweise
Dimethylsulfat ist beim Menschen als eindeutig karzinogen und mutmaßlich mutagen eingestuft. Es kann schnell durch intakte Haut diffundieren. Aufgrund der alkylierenden Wirkung ist Dimethylsulfat ein starkes Schleimhaut- und Lungengift. Darauf beruht auch die karzinogene Wirkung von Dimethylsulfat: Die DNA wird methyliert und kann dadurch nicht mehr gelesen werden, die vergiftete Zelle stirbt ab oder mutiert.[9] Auch Leber, Nieren, Herz und das Nervensystem werden angegriffen. Durch die bei der Hydrolyse entstehende Schwefelsäure wirkt Dimethylsulfat außerdem stark ätzend. Die Substanz ist nach Anhang II, Nr. 6 der deutschen Gefahrstoffverordnung (GefStoffV) als besonders gefährlicher krebserzeugender Stoff eingestuft und darf nur in geschlossenen Anlagen hergestellt oder verwendet werden.[10]
Bei der Arbeit mit der Substanz ist äußerste Vorsicht geboten. Da eine Warnwirkung fehlt (geruchsneutral, keine akute Reizwirkung), kann es leicht unbemerkt zur Aufnahme gefährlicher Mengen kommen. Nach einer ca. sechs- bis zwölfstündigen Latenzzeit folgen schwere Verätzungen der Atemwege. Das Tragen von speziellen Schutzhandschuhen und das Arbeiten in einem gut ziehenden Abzug sind unerlässlich. Reste von Dimethylsulfat sind in einer Mischung aus 10 % Monoethanolamin, 30 % Butyldiglycol und 60 % Wasser zu vernichten.[11]
Einzelnachweise
- Eintrag zu Dimethylsulfat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2017. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-210.
- Eintrag zu Dimethyl sulphate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 16. Juli 2014.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 77-78-1 bzw. Dimethylsulfat), abgerufen am 2. November 2015.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-23.
- Grillo-Werke AG | DIMETHYLSULFAT (DMS). (grillo.de [abgerufen am 8. November 2018]).
- Manfred Müller, Ute Hübsch: Dimethyl Ether. In: Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim 2006, doi:10.1002/14356007.a08_541.
- Carsten Schmuck, Bernd Engels, Tanja Schirmeister, Reinhold Fink: Chemie für Mediziner, Pearson Studium, ISBN 978-3-8273-7286-4, S. 457.
- Gefahrstoffverordnung (GefStoffV) - Stand: April 2017.
- BG RCI - GisChem Gefahrstoffinformationssystem Chemikalien. In: www.gischem.de. Abgerufen am 22. Oktober 2016.
Weblinks
Sicherheitsdatenblätter
Sicherheitsdatenblätter verschiedener Hersteller in alphabetischer Reihenfolge für Dimethylsulfat:
- Datenblatt Dimethylsulfat bei Acros, abgerufen am 26. Februar 2010..
- Datenblatt Dimethylsulfat (PDF) bei Merck, abgerufen am 26. Februar 2010..


