Nervengift
Nervengifte oder Neurotoxine sind Stoffe, die bereits in einer geringen Dosis eine schädigende Wirkung auf Nervenzellen bzw. Nervengewebe erzielen. Nervengifte sind eine heterogene Gruppe von Stoffen mit einer Vielzahl an Wirkmechanismen. Die Mehrheit der Nervengifte sind exogene, natürlich vorkommende Toxine, die von Organismen stammen. Einige chemische Elemente sind Nervengifte, darunter Schwermetalle wie Blei, Cadmium, Quecksilber und Thallium. Die Bezeichnung „Nervengas“ – insbesondere für Nervenkampfstoffe – ist irreführend, da alle hier aufgeführten Nervenkampfstoffe teilweise hochviskose Flüssigkeiten sind und nur wenige Gase zu den Nervengiften zählen. Der Begriff stammt daher, dass die ersten chemischen Kampfstoffe – wie etwa Chlor – Gase waren und zum Schutz dagegen Gasmasken eingesetzt wurden, welche auch einen geringen Schutz gegen Nervenkampfstoffe bieten. Eine endogene Vergiftung von Nervenzellen kann durch Reizüberflutung und darauf folgende übermäßige Ausschüttung von Neurotransmittern auftreten (Excitotoxizität).
Neurotoxine
Die meisten Nervengifte sind Toxine, das heißt, von Lebewesen synthetisierte Nervengifte, und andere organische Stoffe. Sie werden im Tierreich häufig zur Verteidigung oder als Beutegift zur Jagd anderer Tiere oder von Pflanzen und Pilzen als Fraßschutz eingesetzt. Die Wirkung dieser Stoffe beruht meist auf der Interaktion der Stoffe mit bestimmten Rezeptoren der Nervenzellen, indem sie als Agonisten (z. B. Nicotin an nicotinischen Acetylcholinrezeptoren) diese auslösen oder als Antagonisten (z. B. Atropin an muskarinischen Acetylcholinrezeptoren) diese blockieren, wodurch die Erregungsweiterleitung und damit die Funktion von Organen gestört wird. Ein weiterer, häufiger Wirkmechanismus beruht auf der Öffnung oder dem Blockieren von Ionenkanälen, wie der Öffnung von Calciumkanälen durch Alpha-Latrotoxin, dem Gift der Europäischen Schwarzen Witwe oder der Blockade von Natriumkanälen durch Saxitoxin, welches vorwiegend von Dinoflagellaten produziert wird. Die Herkunft solcher Toxine sind beispielsweise
- Spinnentiere
- Schlangen
- Pilze
- Mutterkornalkaloide aus Mutterkorn
- Ibotensäureverbindungen aus Wulstlingen
- Psilocybin aus Psilocybe-Arten
- Pflanzen
- Bakterien
- Botulinumtoxin aus Clostridium botulinum
- Tetanospasmin aus Clostridium tetani, dem Erreger von Tetanus
- Sonstige Lebewesen
- Saxitoxin aus Dinoflagellaten
- Conotoxine aus der Kegelschnecken-Gattung Conus
Nervenkampfstoffe
Als Nervenkampfstoffe wird eine Klasse von chemischen Waffen bezeichnet, welche auf die Weiterleitung von Signalen in den Nerven und zwischen den Nerven einwirken. Diese Nervengifte können über die Haut, Atmung und über Körperöffnungen in den Körper eindringen und führen zu schweren, systemischen Symptomen, welche schließlich zum Tod führen können. Solche Symptome können starke Muskelkrämpfe und Krampfanfälle, Zittern, Zucken der Muskulatur, Kopfschmerzen, Augenschmerzen, Müdigkeit, Verwirrtheit, Angstzustände, Spannungen, Übelkeit mit Erbrechen und Durchfällen, unkontrollierter Harn- und Stuhlabgang, Appetitlosigkeit, Atemnot, Bewusstlosigkeit und Atemlähmung sein.
Reihen
Nervenkampfstoffe werden nach dem Ursprung ihrer Entwicklung in Gruppen eingeteilt, die als Reihe bezeichnet werden. Man unterscheidet dabei die G-Reihe, V-Reihe und die Nowitschok-Reihe. Zur analytischen Charakterisierung der Stoffe und ihrer Abbauprodukte finden Methoden der Kopplung der HPLC mit der Massenspektrometrie Verwendung.[1][2]
G-Reihe
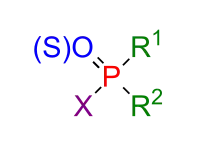
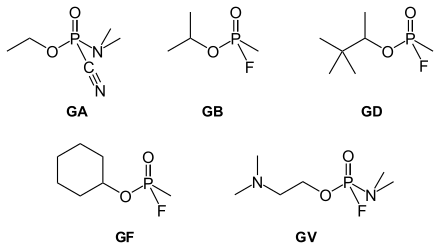
Die G-Reihe wurde während des Zweiten Weltkrieges vom deutschen Chemiker Gerhard Schrader synthetisiert, das G steht hierbei für Germany[3]
Es handelt sich um nicht persistente phosphororganische Verbindungen, welche als Phosphorsäureester angesehen werden können und einen ähnlichen Aufbau, wie in der nebenstehenden Abbildung zu entnehmen ist, aufweisen. So enthalten alle bis auf Tabun anstatt einer OH-Gruppe der Phosphorsäure ein Fluoratom; Tabun enthält stattdessen eine Nitril-Gruppe. Zu dieser Stoffreihe zählen Tabun (GA, 1936), Sarin (GB, 1939), Soman (GD, 1944), Cyclosarin (GF, 1949) und GV (in Klammern jeweils G-Reihen-Bezeichnung und das Jahr der Erstherstellung).
Die Wirkung dieser Nervenkampfstoffe beruht auf der Hemmung der Acetylcholinesterase. Die Gifte besetzen das aktive Zentrum des Enzyms und reagieren dort mit einem nukleophilen Serin-Rest unter Bildung einer kovalenten Bindung.[4] Der durch die Enzymblockade gehemmte Abbau des Acetylcholins führt zu einem drastischen Konzentrationsanstieg dieses Neurotransmitters im cholinergen System und äußert sich im sogenannten akuten cholinergen Toxidrom mit Übererregung der Nerven und schließlich Blockade der Erregungsübertragung. Es kommt je nach Stärke der Vergiftung zu folgenden Symptomen: Kopfschmerzen, Übelkeit mit Erbrechen und Durchfällen, Augenschmerzen, Müdigkeit, Krampfanfälle, Zittern, Zucken der Muskulatur, unkontrollierter Harn- und Stuhlabgang, Atemnot, Appetitlosigkeit, Angstzustände, Spannungen, Verwirrtheit, Bewusstlosigkeit. Der Tod tritt schließlich durch Atemlähmung ein. Die Antidote der medizinischen Notfallausrüstung von NATO-Soldaten enthalten als Anticholinergikum Atropin und Enzymreaktivatoren wie Trimedoximbromid und Obidoximchlorid. Letztere gehören zur Stoffgruppe der Oxime.
Im Gegensatz zu den Vertretern der V-Reihe sind die Vertreter der G-Reihe und DFP durch eine Phosphotriesterase in Tieren und manchen Mikroorganismen spaltbar, ebenso durch die Organophosphorsäure-Hydrolase aus Flavobakterien und Pseudomonas diminuta und durch das Calamari-Enzym.[5]
V-Reihe
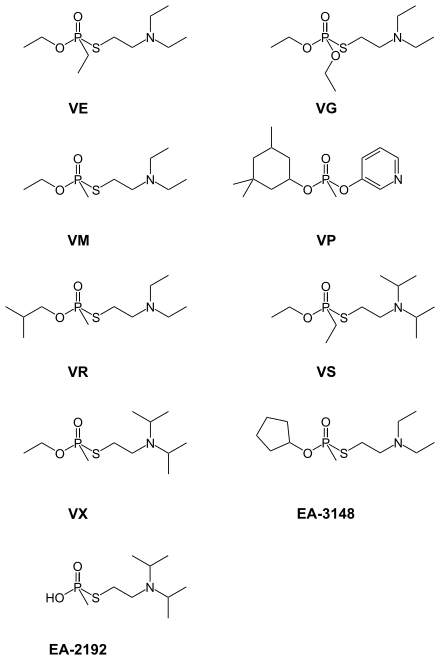
Diese Reihe hatte ihren Ursprung bei dem Chemiker Ranajit Ghosh, welcher für das britische Unternehmen Imperial Chemical Industries Pflanzenschutzmittel erforscht hatte. ICI brachte 1954 unter dem Namen Amiton das waffenfähige VG auf den Markt. Es galt jedoch als zu gefährlich für den Einsatz als Pflanzenschutzmittel, fand aber schnell Verwendung bei den Streitkräften des Vereinigten Königreiches und der USA,[6] auch wenn es aufgrund von erheblichen Problemen bei der Produktion, Lagerung und Munitionierung nie großtechnisch hergestellt oder gelagert wurde.
Der Name leitet sich je nach Quelle von „Victory“ („Sieg“),[7] „Venomous“ („giftig“)[8] oder „Viscous“ („viskos“) ab. Die Stoffe dieser Reihe werden gelegentlich auch „Tammelin’s esters“ genannt. Lars-Erik Tammelin hatte sich für das schwedische Forschungsinstitut der Verteidigung mit den chemischen Kampfstoffen des Ersten Weltkrieges und Zweiten Weltkrieges beschäftigt und war seit 1952 ebenfalls an der Erforschung der V-Reihe beteiligt.
Es handelt sich ebenfalls um phosphororganische, den Phosphorsäurestern ähnliche Kampfstoffe, welche im Gegensatz zur G-Reihe stabiler und etwa 5-mal so giftig sind (vgl. LD50 7 µg·kg−1 für VX (Ratte, i.v.) und 39 μg·kg−1 für Sarin (Ratte i.v.)). Sie verbleiben länger auf dem Schlachtfeld, in der Kleidung sowie anderen Gegenständen und können auch länger gelagert und beispielsweise in Granaten, Raketen und auch Landminen eingesetzt werden. Die Konsistenz ist zähflüssig und ölartig, weshalb die häufige Bezeichnung Nervengas irreführend ist. Neben den bekannten hier abgebildeten Beispielen, von denen jedoch nur VX und VR[9] militärisch verwendet wurden, gibt es noch weitere Derivate mit ähnlichen Eigenschaften. Die Wirkung und entsprechenden Gegenmaßnahmen sind denen der G-Reihe gleich. Zu dieser Reihe zählen die Stoffe VE, VG, VM, VP, VR, VS und VX, sowie EA-2192 und EA-3148, wobei VX als der bekannteste und am besten erforschte Kampfstoff dieser Reihe gilt.
Der Kontakt mit Giften aus der V-Reihe kann, nach adäquater Probenvorbereitung, durch Identifizieren des Stoffwechselprodukts Methylphosphonsäure mit Hilfe der Kopplung der Massenspektrometrie mit der Ionenchromatographie nachgewiesen werden.[10] Eine relativ schnelle Nachweismethode für Gifte, auch der VR-Klasse, verwendet die Kopplung der HPLC mit der Tandem-Massenspektrometrie. Die Nachweisgrenze für die Gifte in Urinproben wird hierbei mit 5 μg/ml angegeben.[11]
Nowitschok-Reihe
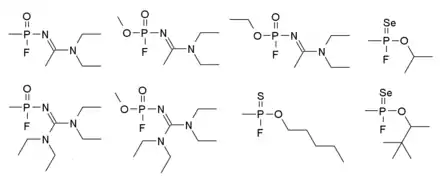
Nowitschok (russisch новичок, so viel wie Neuling oder Anfänger) bezeichnet eine Reihe neuartiger sowjetischer Nervenkampfstoffe, welche etwa zwischen 1970 und 1990 entwickelt wurden. Sie zählen zu den tödlichsten Nervenkampfstoffen, die jemals hergestellt worden sind, von denen einige etwa 5- bis 8-mal so stark wie VX sein sollen. Es gibt über hundert Varianten in dieser Serie, von denen einige in der Darstellung rechts gezeigt werden. Die Wirkung und entsprechende Gegenmaßnahmen sind denen der G-Reihe gleich.[12]
Sonstige Nervenkampfstoffe
Diisopropylfluorphosphat, kurz DFP, wurde erstmals im Zweiten Weltkrieg von englischer Seite entwickelt und produziert. Es war gedacht, DFP als taktisches Gemisch mit Senfgas einzusetzen. So wäre es zu einem Kontaktgift geworden. Die tatsächliche Verwendung von DFP als Kampfstoff ist nicht bekannt geworden.
Antidote
In vitro konnte gezeigt werden, dass 1,1’-(Propan-1,3-diyl)bis(4-tert-butylpyridinium)diiodid in der Lage ist, durch allosterische Modulation von nikotinischer Acetylcholinrezeptoren der Wirkung von Soman entgegenzuwirken.[13]
Sonstige Nervengifte
Auch einige Medikamente und Alkaloide wirken schädigend auf Nervenzellen und zählen damit zu den Nervengiften. Edelgase zählen nicht zu den Giften und sind gegenüber Biomolekülen chemisch inert. Jedoch über induzierte Dipole können Atome des Gases mit biologischen Systemen wechselwirken. So wirkt Xenon beispielsweise durch einen noch nicht vollständig geklärten Mechanismus unter Beteiligung von Glutamat-Rezeptoren narkotisierend.[14]
Literatur
Einzelnachweise
- V. Tak, A. Purohit, D. Pardasani, D. R. Goud, R. Jain, D. K. Dubey: Simultaneous detection and identification of precursors, degradation and co-products of chemical warfare agents in drinking water by ultra-high performance liquid chromatography-quadrupole time-of-flight mass spectrometry. In: J Chromatogr A. Band 1370, 28. Nov 2014, S. 80–92. PMID 25454132
- S. A. Willison: Investigation of the persistence of nerve agent degradation analytes on surfaces through wipe sampling and detection with ultrahigh performance liquid chromatography-tandem mass spectrometry. In: Anal Chem. Band 87, Nr. 2, 20. Jan 2015, S. 1034–1041. PMID 25495198
- Frederick R. Sidell, Jonathan Newmark, John McDonough: Nerve Agents. In: Medical Aspects of Chemical Warfare. Kapitel 5, S. 155–219. ke.army.mil (PDF; 902 kB)
- Fredrik Ekström, Andreas Hörnberg, Elisabet Artursson, Lars-Gunnar Hammarström, Gunter Schneider, Yuan-Ping Pang, Joel L. Sussman: Structure of HI-6•Sarin-Acetylcholinesterase Determined by X-Ray Crystallography and Molecular Dynamics Simulation: Reactivator Mechanism and Design. In: PLoS ONE. Band 4, Nr. 6, 18. Juni 2009, S. e5957, doi:10.1371/journal.pone.0005957 (englisch).
- Karlheinz Lohs: Fachlexikon Toxikologie. Springer-Verlag, 2008, ISBN 978-3-540-27337-0, S. 129 (eingeschränkte Vorschau in der Google-Buchsuche).
- J. P. Robinson: the rise of CB weapons. In: The Problem of Chemical and Biological Warfare. Band 1, New York 1971, ISBN 0-391-00200-7, S. 71.
- Mohammd Moshiri, Emadodin Darchini-Maragheh, Mahdi Balali-Mood: Advances in toxicology and medical treatment of chemical warfare nerve agents. In: DARU Journal of Pharmaceutical Sciences 2012. Band 20, Nr. 81, 28. November 2012, doi:10.1186/2008-2231-20-81, PMC 3470074 (freier Volltext) – (amerikanisches Englisch).
- Detoxifying VX. In: Chemical & Engineering News. Band 94, Nr. 38, 26. September 2016, S. 10–11, doi:10.1021/cen-09438-scicon001.
- A. Radilov u. a.: Russian VX. In: R. C. Gupta (Hrsg.): Handbook of Toxicology of Chemical Warfare Agents. Elsevier, 2009, ISBN 978-0-12-374484-5, Chap. 7, S. 69 ff.
- T. Baygildiev, A. Zatirakha, I. Rodin, A. Braun, A. Stavrianidi, N. Koryagina, I. Rybalchenko, O. Shpigun: Rapid IC-MS/MS determination of methylphosphonic acid in urine of rats exposed to organophosphorus nerve agents. In: J Chromatogr B Analyt Technol Biomed Life Sci. Band 1058, 15. Jul 2017, S. 32–39. PMID 28531843
- I. Rodin, A. Braun, A. Stavrianidi, T. Baygildiev, O. Shpigun, D. Oreshkin, I. Rybalchenko: ‘Dilute-and-shoot‘ RSLC-MS-MS method for fast detection of nerve and vesicant chemical warfare agent metabolites in urine. In: J Anal Toxicol. Band 39, Nr. 1, Jan-Feb 2015, S. 69–74. PMID 25326204
- The (agent) fate of Novichok. (PDF) In: CBRNe World. cbrneworld.com, abgerufen am 12. März 2018 (englisch).
- Allosterische Modulation nikotinischer Acetylcholinrezeptoren – eine neue Therapieoption für die Behandlung von Nervenkampfstoffvergiftungen? In: Wehrmedizinische Monatsschrift. Nr. 5, 2017.
- B. Preckel, N. C. Weber, R. D. Sanders, M. Maze, W. Schlack: Molecular Mechanisms Transducing the Anesthetic, Analgesic, and Organ-protective Actions of Xenon. In: Anesthesiology, Vol. 105, Nr. 1, 2006, S. 187–197.