Pharmazeutische Biotechnologie
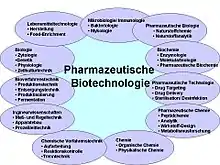
Die Pharmazeutische Biotechnologie ist eine anwendungsorientierte Wissenschaft, die wissenschaftliche Methoden und Techniken zur Entwicklung, Prüfung, Herstellung und Zulassung von Arzneistoffen umfasst. Es handelt sich somit um ein Teilgebiet der Roten Biotechnologie. Die Pharmazeutische Biotechnologie steht in enger Verbindung mit Bioprozesstechnik, Gentechnik, Analytik, pharmazeutischer Technologie und Arzneimittelzulassung.
Herstellung biotechnologischer Arzneimittel
Die biotechnologische Herstellung rekombinanter Arzneimittel (Biopharmazeutika) hat in der modernen Pharmazie einen breiten Stellenwert eingenommen. Neben der Schaffung gentechnisch veränderter Organismen (GVO) zur Produktion rekombinanter therapeutischer Proteine, ist die historische Fermentation von Bakterien und Pilzen zu nennen, die die industrielle Herstellung von niedermolekularen Arzneistoffen wie beispielsweise Antibiotika, HMG-CoA-Reduktase-Inhibitoren und Immunsuppressiva erlaubte. Wesentlicher Unterschied zu GVO ist, dass die natürliche biochemische Stoffwechselleistung des Produktionsorganismus ausgenutzt wird. Züchterische Verbesserungen der Produktausbeute, wie für Penicillium eindrucksvoll seit dem Zweiten Weltkrieg gezeigt, sind zu unterscheiden von der bewussten Isolierung und Veränderung genomischer DNA des Produzenten, der über neue nicht artspezifische Biosyntheseleistungen verfügt.
30 Jahre nach den ersten erfolgreichen Klonierungsversuchen zur Einführung nicht artspezifischer genetischer Informationen in Escherichia coli ist die genetische Veränderung unterschiedlicher Produktionsorganismen und die Gewinnung beliebiger rekombinanter Proteine einschließlich physiologischer Glykosylierungsvarianten Routine geworden. Heute sind 115 Medikamente mit 84 therapeutischen Proteinen in Arzneimitteln zur Anwendung am Menschen zugelassen (Stand Februar 2006). Optimistische Schätzungen geben an, dass bis 2015 die Hälfte der neuen innovativen Arzneimittel Proteine oder Oligopeptide sein werden, und eine Steigerung der Apothekenumsätze von € 220 Mio. (1996) auf über € 1 Mrd. Ende des Jahrzehntes zu erwarten ist. Parallel ist auch die Vermarktung von Arzneimitteln als Biosimilars (auch gelegentlich als Biogenerika bezeichnet) zu erwarten.
Alle rekombinant hergestellten therapeutischen Produkten müssen der Monographie „DNA-rekombinationstechnisch hergestellte Produkte“ des Europäischen Arzneibuches genügen. Folgende Definition des Europäischen Arzneibuches ist gegeben, die sich mit den Leitlinien der Europäischen Arzneimittelagentur und der Food and Drug Administration (FDA) inhaltlich decken: „DNA-rekombinationstechnisch hergestellte Produkte werden durch genetische Modifikation hergestellt, bei der die für das benötigte Produkt codierende DNA mit Hilfe eines Plasmids oder viralen Vektors in einen geeigneten Mikroorganismus oder eine geeignete Zelllinie eingeführt wird, in denen diese DNA exprimiert und translatiert wird. Das gewünschte Produkt wird dann durch Extraktion und Reinigung gewonnen. Die vor der Aufnahme des Vektors vorliegende Zelle oder der Mikroorganismus wird als Wirtszelle bezeichnet, die im Herstellungsprozess verwendete stabile Verbindung der beiden als Wirt-Vektor-System.“
Aus der Monographie ergibt sich, dass das biotechnologisch erzeugte Produkt durch den gesamten Herstellungsprozess charakterisiert sein muss. Nicht nur die Frage nach der chemischen Identität und Reinheit ist entscheidend, sondern auch die des biologischen Produktionssystems sind relevant für die Identität des therapeutischen Proteins. Im Gegensatz zu nicht rekombinant produzierten klassischen Stoffen ist die Erweiterung der Definition um Fragen des Vektors, der Produzentenlinie und der Extraktion und Reinigung ein zusätzlicher Sicherheitsaspekt, da durch Wechsel der Produktionslinie und Abänderungen der Arbeitsmethodik Endprodukte mit nicht bekannten oder unterschiedlichen Metaboliten entstehen können, die toxikologisch und pharmakokinetisch für den Patienten von Bedeutung sind.
Wie alle Produktionsprozesse in der Pharmazie muss auch die Herstellung biotechnologischer Arzneimittel nach den Regeln der Good Manufacturing Practice (GMP) durchgeführt werden.
Produktion biotechnologischer Produkte
Die Herstellung biotechnologischer Therapeutika lässt sich in einen Herstellungs- oder Upstream-Prozess und einem Aufreinigungs- oder Downstream-Prozess unterscheiden. Im Rahmen des Upstream-Prozesses erfolgt die Anzucht des Produktionsstammes aus Zellbanken und die sukzessive Kultivierung und Biomassevermehrung über Erlenmeyerkolben oder Laborfermenter zum industriellen Produktionsfermenter. Ist das gewünschte Protein in ausreichender Menge produziert, erfolgt im Downstream-Prozess die Abreicherung, Inaktivierung, Extraktion und Aufreinigung des gewünschten Produktes sowie die bioanalytischen Prüfungen und galenische Formulierung des Produktes.

Produktionslinien und Vektorsysteme
Mikroorganismen
Der überwiegende Teil der rekombinanten Wirkstoffe wird in Mikroorganismen produziert, wobei Escherichia coli als wichtigster Produzent zu nennen ist. Der Einsatz von Mikroorganismen ist wegen der einfachen und anspruchslosen Kultivierung von Vorteil. Weitere Vorteile sind die im Vergleich zu Säugerzellen meist kürzeren Fermentationszeiten und die höhere chemische und physikalische Proteinstabilität bei der Aufarbeitung. Mikroorganismen sind häufig einfacher zugänglich für genetische Manipulationen als tierische oder pflanzliche Zellen.
Industriell eingesetzte Produktionsorganismen müssen den Status GRAS („Generally recognized as safe“ oder im Deutschen „Generell als sicher angesehen“) aufweisen, d. h. sie dürfen nicht pathogen sein und keine toxischen oder antibiotischen Stoffe bilden. Typische Beispiele sind E. coli K12, Bacillus subtillis, Lactobacillen und einige Streptomyces-Arten als Vertreter für Bakterien, und Aspergillus, Penicillium, Pichia, Mucor, Rhizopus und besonders Saccharomyces cerevisae als typische Vertreter für filamentöse Pilze. Zu beachten ist, dass in der Regel niedermolekulare Naturstoffe in das Medium abgegeben werden. Hochmolekulare Stoffe wie hier diskutierte rekombinante Proteine (Bsp. Insulin, Interferone) werden intrazellulär akkumuliert und können als sogenannte Einschlusskörperchen ausfallen.
Säugerzellen
Die Produktion von Proteinen durch Säugerzellen findet bevorzugt statt, wenn ein glykosyliertes Produkt gewünscht ist (Bsp. Follitropin, Erythropoietin) oder ein Therapeutikum gefordert ist, das der humanen Konformation entsprechen muss. Tierische Zellen und Mikroorganismen unterscheiden sich in diesen Anforderungen deutlich voneinander. So sind Bakterien nicht zur posttranslationalen Glykosylierung befähigt und sind nur bedingt zur korrekten Proteinfaltung humaner Proteine in der Lage. Bei der therapeutischen Anwendung dieser Produkte werden hohe Anforderungen an die Qualität hinsichtlich Reinheit und ihrer Struktureigenschaften gestellt. Korrekte Faltung und Glykosylierung sind entscheidende Faktoren für die biologische und pharmakologische Aktivität der Zielproteine.
Bei Einsatz von Säugerzellen ist eine technisch höherwertige Ausstattung der Produktionsstätte erforderlich. Von den in der pharmazeutischen Biotechnologie eingesetzten Zelllinien aus der molekularbiologischen Forschung sind folgende Linien als Expressionssysteme von besonderem Interesse: beispielsweise die Chinese Hamster Ovar (CHO)-Zelllinien, Baby Hamster Kidney (BHK)-Zelllinien, Affennieren-Zelllinien vom Vero-Typ in der Impfstoffproduktion und Maus-Myelomzellen (NSO-GS) als Genexpressionssysteme für rekombinante Proteine.
Pflanzen

Als eine Alternative zu den etablierten Produktionssystemen werden zunehmend genetisch veränderte Pflanzen, sogenannte Pharmapflanzen, genutzt. So werden beispielsweise Wasserlinsen wie Lemna minor oder das Moos Physcomitrella patens zur Produktion von Biopharmazeutika eingesetzt.[1][2] Diese Pflanzen lassen sich, ebenso wie Pflanzenzellkulturen, in geschlossenen Systemen kultivieren (Photobioreaktoren, z. B. Moosbioreaktor) und ermöglichen somit Herstellbedingungen nach GMP-Richtlinien.[3] Im Optimalfall ist eine direkte Aufreinigung des Proteins aus dem Kulturmedium möglich, was den Downstream-Prozess erleichtert und die Produktionskosten senkt.[4]
Zellbänke
Die nachhaltige Qualität eines produzierten Wirkstoffs hängt entscheidend von dem eingesetzten Produzenten ab. Die Pflege und Aufrechterhaltung einer Produzentenlinie mit hoher Qualität für die chargenweise Produktion über einen längeren Zeitraum ist für den Pharmazeutischen Unternehmer von hohem Interesse, da das zugelassene Produkt nur in der von der Zulassungsbehörde genehmigten Zelllinie hergestellt werden darf. Die Validierung von Zellbänken und Säugerzelllinien muss deshalb durchgeführt werden, um die Zuverlässigkeit eines Produktionsprozesses zu dokumentieren und eine hohe Produktqualität zu reproduzieren. Die genetisch konstruierte Zelllinie zur Produktion wird aus diesem Grunde als sogenannter Master-Seed kultiviert, um einen Grundstock zur Aliquotierung für Arbeitszelllinien (Working-Seeds) mit mehreren hundert Ampullen zu ermöglichen, die in flüssigem Stickstoff gelagert und bei Bedarf entnommen werden. Ein Verlust des angezeigten Saatgutsystems oder der Verbrauch des auf Vorrat gehaltenen Master-Seed kann nur durch erneut validierte und genehmigte Zellbanken ersetzt werden.
Nach dem Gentechnikgesetz (GenTG) werden über den Wirt oder Produzenten Angaben zu der eindeutigen taxonomischen Charakterisierung sowie Angaben zu der gentechnischen Veränderung verlangt. Weitere vorgeschriebene Angaben sind, ob natürlicherweise Plasmide oder endogene Viren vorkommen, und ob mit toxischen, mutagenen, karzinogenen oder allergenen Wirkungen des Wirtes zu rechnen ist. Zum Schutze des Menschen und der Umwelt verlangt das GenTG ferner, dass anzugeben ist, welches Risiko für Tiere oder Pflanzen bei nicht beabsichtigter Freisetzung besteht. Im Rahmen des Betriebs- und Produktionsablauf muss beschrieben werden, wie der Wirtsorganismus möglicherweise übertragen werden kann, wie hoch die Mindestinfektionsdosis bei bekanntem Applikationsweg ist, welche Notfalltherapeutika oder Impfstoffe bevorratet sein müssen, und wie Dekontaminationen oder Desinfektionen durchzuführen sind.
Nach Entnahme und Anzucht zu einer Arbeitskultur auf festen Agar (Mikroorganismen) oder in flüssiger Kultur (Mikroorganismen und Säugerzellen) erfolgt sukzessives Scaling Up vom Schüttelkolben über den Laborfermenter zum industriellen Bioreaktor. Scaling Up erfolgt nach Erfahrungswerten in dekadischen Schritten, beispielsweise von einem Inokulum mit 30 ml Volumen über 300-ml-Erlenmeyerkolben und 3- bzw. 30-l-Laborfermenter zu 300-l-Industriefermentern.
Vektorsysteme
Die Schaffung eines gentechnisch veränderten Organismus bedeutet die Einführung einer zusätzlichen, meist artfremden DNA in das Wirtsgenom. Dieser technische Vorgang wird als Klonierungsstrategie bezeichnet, bei dem durch Insertion meist eine komplementäre DNA (cDNA) in Expressionsvektoren integriert wird. Diese cDNA ist eine exakte Kopie der mRNA, die nicht mehr die informationslosen Intronbereiche enthält. Die aneinandergesetzten Expressionssequenzen können für die kontrollierte Biosynthese in den Wirt überführt und klar von dem Ursprungsgen unterschieden werden.
Bei der Beschreibung des zur Klonierung verwendeten Vektors sind für die Zulassungsbehörde Angaben zu machen, welche die Herkunft des oder der für die Replikation verantwortlichen Kontrollelemente (Replikons), betreffen, die Promotor oder Enhancer als expressionsregulierende Informationseinheiten beschreiben, und die über die Herkunft der Gene für Selektionszwecke Auskunft geben. Weitere wichtige Informationen sind Daten zur Stabilität des Expressionsvektor in den Wirtszellen sowie die Einschätzung des Infektions- und Tumorpotentials (Bsp. Proonkogene).
Neben der Frage der Transformation und des Einbringen des Vektors ist die Charakterisierung der rekombinanten DNA in der Wirtszelle von Interesse. Diese Prüfungen sind nicht nur für Saatgutzellen, sondern auch für Produktionszellen nach einem oder mehreren Fermentationsschritten zu prüfen. Mit Hilfe von Restriktionsenzymen, Southern-Blot-Analysetechniken und PCR muss bestimmt werden, ob Status und Stabilität des Expressionskonstrukt korrekt ist. Von Interesse ist die extrachromosomale Lage der rekombinanten DNA bei Prokaryoten, Ort und Art der Integration in das Wirtsgenom bei Eukaryoten, die Kopienzahl in der Zelle und die genetische wie mögliche phänotypische Expression nach Zellteilungen. Die Bedeutung der genetischen Stabilitätsuntersuchungen liegt in dem erhöhten Informationsgehalt zur Kopienzahl im Verhältnis zur Produktivität der Kultur, Hinweise auf Deletionen und Insertionen des Expressionsvektors, und sie erlauben Aussagen zur Proteinidentität.
Produktion und Bioprozesstechnik
Die Produktion rekombinanter Proteine erfolgt durch Fermentation im Bioreaktor, die für die Kultivierung optimale Bedingungen für Wachstum und Wirkstoffbildung bieten. Zu unterscheiden ist zwischen der diskontinuierlichen, sogenannter batch-wise Produktion, und der kontinuierlichen Produktion, wie oben bereits erklärt. Im Rahmen der Wirkstoffproduktion muss der gesamte Prozess durch Dokumentation der Produktionsparameter wie beispielsweise Temperatur, pH-Wert, Sauerstoff- und Kohlendioxid-Sättigung, Prozessdauer und eingesetzte Hilfsstoffe beschrieben werden. Idealerweise sollte nur mit einer Zelllinie im Produktionsbereich gearbeitet werden, um Fremd- oder Kreuzkontaminationen zu vermeiden. Zusätzliche In-Prozess-Kontrollen müssen die tatsächliche Qualität belegen. Häufiges Problem ist eine mögliche Fremdkontamination von außen oder die Aktivierung von Retroviren, die mit der Produktionslinie eingebracht werden.
Je nach Anforderungen des zu kultivierenden Organismus sind verschiedene Bioreaktorsysteme zu wählen. Prokaryoten mit einer stabilen Zellwand können in Bioreaktoren mit Rührwerken kultiviert werden, da sie wenig empfindlich gegenüber den entstehenden Scherbewegungen sind. Eukaryotische Zellen besitzen keine Zellwand und sind sehr empfindlich gegenüber physikalischen Einwirkungen, weshalb zu ihrer Kultivierung häufig Airlift-Bioreaktoren genommen werden, um Zellschäden durch rotierende Flügel zu vermeiden. Bei Airlift-Bioreaktoren wird bodenständig das Luft/CO2-Gemisch eingeblasen, das durch eingesetzte Prallbleche zu einer Konvektion des Flüssigmediums führt.
Ein dritter Bioreaktortyp, welcher häufig zu finden ist, ist der sogenannte Membranbioreaktor oder auch Hohlfaserreaktor genannt. Technisch handelt es sich um die Kombination einer Ultrafiltrationseinheit und eines Bioreaktors. Durch die semipermeable Membran der Hohlfasern, die häufig aus Polysulfon oder mikroporösem Polypropylen bestehen, werden Zellen zurückgehalten bzw. vom durchfließenden Medium getrennt, so dass nur der Durchtritt meist niedermolekularer Produkte oder Metabolite möglich ist. Vorteil ist ferner, dass unerwünschte polymere Produkte wie Polysaccharide, Fremdproteine und Enzyme zurückgehalten werden und so die Produktaufarbeitung erleichtert wird. In der pharmazeutischen Industrie wird der Reaktortyp technisch zur Biosynthese des Blutgerinnungsfaktors VIII genutzt, welcher in BHK-Zellen (Baby Hamster Kidney) exprimiert wird. Dabei zeichnet sich die Produktion durch eine hohe Zelldichte im Perfusionsreaktor und durch entsprechend hohe Ausbeute aus.
Die qualitative Zusammensetzung des Nährmediums hängt von den Anforderungen des zu kultivierenden Organismus ab. Für tierische Zellen sind diese häufig wesentlich komplexer als für Mikroorganismen. Typische Medien für Säugerzellen sind beispielsweise zusammengesetzt aus Mineralsalzen, Antibiotika, Vitaminen und physiologischen Proteinen wie Wachstumsfaktoren, Insulin oder Transferrin. Häufig wird dem Medium fetales Kälberserum hinzugesetzt, dessen Einsatz wegen der möglichen Prionenkontamination nicht ohne Risiko ist. Neuere Entwicklungen werden in der Zukunft vermutlich einen Verzicht auf FKS erlauben, da ein gentechnisch hergestelltes Albumin oder auch das humane Plättenlysat Alternativen bieten.
Säugerzellen können nach ihrem Wachstumsverhalten in adhärierende und nicht-adhärierende Zelltypen unterschieden werden. Adhärierende Zellen wachsen nur auf festen Medien, sie bilden einen Zellmonolayer und stellen bei vicinalen Kontakt ihr Wachstum ein. Der überwiegende Teil der eingesetzten Produktionslinien zeigen adhärentes Verhalten, weshalb sie auf Glas-, Zirkon- oder Polystyrolkugeln angezüchtet werden können. Erfolgreiche Techniken nutzen bei der Kultivierung von Säugerzellen mit hoher Zelldichte Verfahren zur Immobilisierung. Ihr Vorteil ist, dass Zellen in offenporigen Mikroträgern und bei Einsatz im Wirbelschichtreaktor deutlich länger und effizienter kultiviert werden können und somit die Raum-Zeit-Ausbeute erhöht wird. Nach diesem Verfahren wird beispielsweise Follitropin hergestellt.
Neben der detaillierten Darstellung der Produktion im Bioreaktor sei der Vollständigkeit halber kurz auf die chemische Synthese kurzkettiger Peptide mit weniger als 70 Aminosäuren eingegangen, die im Routinebetrieb mit Hilfe von Syntheseautomaten gewonnen werden. Beispiele sind Oxytocin, Gonadoliberin und Desmopressin, aber auch die 2002 durch die FDA zugelassene Antisense-RNA Fomivirsen wird chemisch hergestellt.
Extraktion und Anreicherung
Die Gewinnung des gewünschten Endproduktes aus einem Kulturansatz wird in der Gesamtheit aller Arbeitsschritte als Downstream-Prozess bezeichnet. Zu diesen Arbeitsschritten wird in der pharmazeutischen Industrie die Gewinnung, Isolierung, Aufreinigung, Formulierung und Konfektionierung eines Fermentationsproduktes zum fertigen Endprodukt gezählt. Alle Aufarbeitungsschritte müssen auch hier validiert sein und müssen für die Zulassungsbehörden und zur eigenen Sicherheit des pharmazeutischen Unternehmers dokumentiert werden. Eine allgemein gültige Beschreibung des Downstream-Prozesses ist nicht möglich. da er sich nach den Anforderungen und physikalisch-chemischen Eigenschaften des jeweiligen Produktes richten muss.
Im Gegensatz zu niedermolekularen Stoffen und Metaboliten liegen gewünschte Proteine als sogenannte Single Cell-Proteine intrazellulär vor. Prokaryotische Produzenten wie E. coli sezernieren dieses nicht in das Medium, sondern akkumulieren das Protein im Zytosol, wo es als Inklusionskörper (inclusion body) nach Überschreiten des Löslichkeitsproduktes ausfällt oder aggregiert. Inklusionskörper zeigen Probleme hinsichtlich der Renaturierung des präzipitierten Proteins. Unter Einsatz verschiedener Renaturierungsreagienzen (Einsatz von Harnstoff, Guanidinhydrochlorid, EDTA, Dithiothreitol), werden Proteine wieder gelöst und erlangen im Idealfall ihre native Konformation wieder, die wichtig für die biologische oder pharmakologische Wirkung ist. Die nachträgliche in vitro Faltung der Proteinkonformation ist aber ein komplizierter meist empirischer Prozess, der stark von Faktoren wie Temperatur, Ionenstärke, pH, Eigenschaften des Renaturierungsmediums und auch der Viskosität abhängen.
Validierung des Herstellungsprozesses
Gültige Richtlinien, die von den wichtigsten Zulassungsbehörden der FDA und der europäischen EMEA regelmäßig über das Internet veröffentlicht werden, haben keinen gesetzlichen und nur empfehlenden Charakter. Ihre Erstellung beruht auf Ergebnissen aus der Zusammenarbeit zwischen den Zulassungsbehörden und den Pharmazeutischen Unternehmern. Aus diesem Grunde sind aber Abweichungen immer gesondert zu begründen. Zusammengefasst beschreiben die Empfehlungen (Guidelines, Notes of Guidance) Verfahrensabläufe zur Produktion und Prüfung von rekombinant hergestellten Produkten, die Dokumentation von Ergebnissen, aber auch das Verfassen von Zulassungsanträgen. Einige wesentliche Qualitätskriterien sollen kurz diskutiert werden:
Verunreinigungen durch Bakterien und Pilze
Eine Verunreinigung durch Bakterien oder Pilze im biotechnologischen Herstellungsprozess ist selten anzutreffen, da alle Ausgangsstoffe durch selektive Sterilitätstest ausreichend geprüft werden können. Typische Kontaminationen sind deshalb virale Kontaminationen oder das Einbringen von Mycoplasmen, die nicht durch gebräuchliche Sterilfiltration mit 0,22-µm-Filter zurückgehalten werden können. Um dieses Problem zu umgehen, werden vielfach 0,1-µm-Filter eingesetzt, die sicher Mycoplasmen entfernen können. Neben Mikroorganismen selbst sind mikrobielle Produkte wie Lipopolysaccharide als Pyrogene ein ernstes Problem. Bei unsachgemäßer Verdünnung oder Zubereitung von Nährlösungen besteht ein Kontaminationsrisiko. Durch Ultrafiltration oder spezielle Zeta-Filter können Pyrogene abgetrennt werden.
Virale Kontaminationen
Eine virale Verunreinigung ist im Herstellungsprozess und bei der Prüfung des Endproduktes schwerer nachzuweisen und zu beseitigen. Viren können nicht durch Standardsteriltests nachgewiesen werden und lassen sich nicht mit Sterilfiltern (0,1 µm) abtrennen. Häufig erfolgt eine Kontamination durch Retroviren aus der Produktionslinie selbst, wie beispielsweise HI-, Hepatitis B-, Epstein-Barr-, SV40- oder Cytomegalievirus, durch Einschleppen aus mangelhaft aufbereiteten tierischen Seren, die in Nährmedien eingesetzt werden, oder durch kontaminierte chromatographische Säulen im Downstream-Prozess. Der Nachweis viraler Infektionen erfolgt mit Hilfe der PCR-Technik oder mit Immuno-ELISA-Testverfahren, die zur Prüfung auf virale Infektion der Produktionslinien intensiv genutzt werden. Methoden zur Abtrennung von Viren sind vorwiegend physikalischer Natur, wie Ultrafiltration, Säulenchromatographie oder Nanofiltration. Die Anwendung von Hitze (z. B. Pasteurisierung) oder chemischen Stoffen kann zu einer biologischen Inaktivierung (Denaturierung) des therapeutischen Proteins führen. Daher können diese Verfahren nicht immer angewendet werden.
Fremdproteine
Bei jeder biotechnologischen Produktion sind durch den Produzenten unerwünschte Proteine zu finden, die durch verschiedene Methoden der Filtration oder Chromatographie abzutrennen sind. Wie am Beispiel des rekombinant gewonnenen Insulins, rekombinanten Erythropoietin oder Follitropin in der Vergangenheit gezeigt, ist bei Anwesenheit fremder Proteine mit einem hohen allergischen Potential für den Patienten zu rechnen, das von leichten Immunreaktionen bis zum anaphylaktischen Schock reichen kann. Unter Fremdproteine sind nicht nur chemisch unterschiedliche Proteine zu fassen, sondern auch durch den Produzenten falsch oder unvollständig biosynthetisierte, gewünschte therapeutische Proteine. Quelle möglicher Fremdproteine muss nicht unbedingt der Produzent sein, sondern auch Nährmedien oder Liganden aus dem Säulenmaterial sind denkbar. Nachweisverfahren zur qualitativen und quantitativen Bestimmung von Fremdproteinen und Qualitätssicherung sind die 2D-Gelelektrophorese, HPLC-MS und Immunassays.
Fremd-DNA
DNA im Endprodukt ist zum einen eine wirtsspezifische Verunreinigung oder ist als Marker-DNA zur Kontrolle des Downstream-Prozesses absichtlich hinzugegeben worden. Auf Grund einer möglichen onkogenen Wirkung muss DNA aus dem Endprodukt entfernt werden, und nach internationalen Richtlinien ist der maximale Gehalt auf 10 pg pro Dosis begrenzt. Fremd-DNA, aber auch Fremd-RNA, kann effektiv durch Nukleasen abgebaut werden. Ein Beispiel ist Benzonase, welche eine gentechnisch veränderte Endonuklease ist, die spezifisch Nukleinsäuren abbaut ohne rekombinante Proteine zu zerstören.
Chemische Verunreinigungen
Chemische Verunreinigungen sind meist niedermolekulare Stoffe wie Lipide, Vitamine, Antibiotika oder hochmolekulare Stoffe wie Polysaccharide, die durch den Produzenten oder durch das Nährmedium eingeführt wurden. Der Großteil stammt aber aus exogenen Quellen wie Nährmedien oder als Rückstände aus Lösungsmitteln (Bsp. Detergentien, Salze, proteolytische Inhibitoren), die bei der Reinigung und Pflege von Bioreaktoren und angeschlossenen technischen Anlagen zurückbleiben. Der Nachweis von Rückständen erfolgt durch HPLC-MS oder GC-MS.
Identität der aktiven Substanz
Rekombinant hergestellte therapeutische Proteine werden nach internationalen Standards der Zulassungsbehörden und des International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) geprüft. Die pharmakologisch aktive Substanz wird auf Identität, Reinheit und Gehalt untersucht, die Parameter wie beispielsweise relative Molare Masse, isoelektrischer Punkt, Ladung, Löslichkeit und Hydrophobizität umfassen. Im Rahmen dieses kurzen Beitrages und der Vielfalt der heute auf dem Markt befindlichen Proteine ist eine vollständige Auflistung wichtiger analytischer Größen nicht möglich, und es sei auf die im Internet veröffentlichten Vorschriften und Monographien verwiesen. Neben den physikalisch-chemischen Eigenschaften müssen therapeutische Proteine auf ihre korrekte Primärstruktur und Proteinfaltung mit Hilfe der NMR, Röntgenspektroskopie oder immunchemischer Methoden untersucht werden. Die Primärstruktur wird nach enzymatischer Spaltung in kurze Fragmente mit Hilfe der Gelelektrophorese oder HPLC charakterisiert. Von hohem Interesse ist die HPLC-MALDI-TOF Methode, welche eine Sequenzanalyse direkt aus dem intakten Protein erlaubt. Besondere Berücksichtigung finden chemische Veränderungen wie die N-terminale Methionylierung, Anwesenheit des N-Formylmethionin oder Signalsequenzen, die durch die bakterielle Proteinbiosynthese zu erklären sind. Ferner sind N- und C-terminale Modifizierungen des therapeutischen Proteins durch proteolytische Prozesse zu finden oder die Ausbildung von falschen oder zusätzlichen Disulfidbrücken (Bsp. Insulin) durch Oxidation.
Handelt es sich um glykosylierte therapeutische Proteine, so ist das Muster der Zuckerketten zu prüfen und gegebenenfalls mit der natürlichen humanen Form abzugleichen. Posttranslationale Prozesse, wie bereits oben beschrieben, führen zu signifikant anderen N- und O-Glykosylierungen aber auch zu möglichen Acetylierungen, Hydroxylierungen, Carboxylierungen, Deamidierungen und unerwünschten Oxidationen. Nachweis der korrekten posttranslationalen Modifizierung durch den Produzenten kann mit Hilfe der isoelektrischen Fokussierung, Kapillarelektrophorese und Massenspektrometrie geführt werden.
Gehalt und Wirksamkeit
Die Bestimmung des Gehaltes erfolgt mit Absolutmethoden, die sich auf die Aminosäurezahl oder Stickstoffmenge (Mikro-Kjeldahl-Bestimmung; Kjeldahlsche Stickstoffbestimmung) im Molekül bezieht. Die Proteinbestimmung nach Lowry oder Bradford werden genutzt, allerdings muss eine Validierung auf die Absolutmenge vorab durchgeführt werden. Das Europäische Arzneibuch beschreibt nur ein relativ kleines Spektrum an möglichen bioanalytischen Methoden, die zur Charakterisierung des Produktes genutzt werden. Häufig werden in den einzelnen Monographien weitere substanzspezifische Untersuchungen gefordert.
Die Prüfung auf Wirksamkeit muss für jede Charge durchgeführt werden und muss in nationalen oder internationalen Einheiten pro mL angegeben sein. Wenn dieses nicht möglich ist, so erfolgt die Angabe in biologischen Einheiten, die mit einem hinterlegten internationalen Standard kalibriert wurde. Es wird empfohlen, dass die biologische Wirkung mit physikochemischen Eigenschaften korreliert wird.
Proteinformulierung
Rekombinante therapeutische Proteine müssen wegen ihrer Instabilität bei oraler Gabe parenteral appliziert werden. Sie unterliegen der Monographie „Parenterale Zubereitungen“ und müssen frei von Schwebstoffen sein, sie dürfen keine Pyrogene enthalten und sollten als Injektionslösung hinsichtlich Gewebetonizität und pH-Wert physiologischen Bedingungen angepasst sein.
Biotechfirmen
So gut wie keines der traditionellen Pharmaunternehmen unternimmt heutzutage keine F&E-Aktivitäten in Sachen Biotechnologie.
„Reine“ Biotechfirmen
Amgen ist das weltweit größte unabhängige Biotechnologie-Unternehmen, das ausschließlich auf Biotechnologie setzt.[5] Weitere Unternehmen sind BiogenIdec, Celgene, Gilead, Genzyme und Vertex Pharmaceuticals.[6]
Pharma-/Biotech-Unternehmen
Mit Blick auf die F&E-Ausgaben der 400 forschungsstärksten Firmen in der EU bzw. der 1000 forschungsstärksten Firmen in Drittländern stehen Roche und Pfizer 2010 mit jeweils rund 7 Milliarden Euro auf den Plätzen 1 und 2. Danach folgen die Unternehmen US-Merck (Platz 5), Novartis (Platz 8) und Johnson & Johnson (Platz 10).[6]
Einzelnachweise
- J. R. Gasdaska, D. Spencer, L. Dickey: Advantages of Therapeutic Protein Production in the Aquatic Plant Lemna. In: BioProcessing Journal. März 2003, S. 49–56.
- A. Büttner-Mainik, J. Parsons, H. Jérome, A. Hartmann, S. Lamer, A. Schaaf, A. Schlosser, P. F. Zipfel, R. Reski, E. L. Decker: Production of biologically active recombinant human factor H in Physcomitrella. In: Plant Biotechnology Journal. 9, 2011, S. 373–383. doi:10.1111/j.1467-7652.2010.00552.x
- Eva L. Decker, Ralf Reski: Moss bioreactors producing improved biopharmaceuticals. In: Current Opinion in Biotechnology. 18, 2007, S. 393–398. doi:10.1016/j.copbio.2007.07.012.
- A. Baur, R. Reski, G. Gorr: Enhanced recovery of a secreted recombinant human growth factor using stabilizing additives and by co-expression of human serum albumin in the moss Physcomitrella patens. In: Plant Biotech. J. 3, 2005, S. 331–340. doi:10.1111/j.1467-7652.2005.00127.x
- Biotechnologie für intelligente Medikamente Über Amgen – Unternehmenswebsite, abgerufen am 7. April 2012.
- Pharma- und Biotech-Unternehmen sind weltweit Spitze bei F&E-Investitionen 2010 vfa-bio.de, abgerufen am 7. April 2012.
Literatur
- O. Kayser: Grundwissen Pharmazeutische Biotechnologie. Teubner, Wiesbaden 2002.
- O. Kayser, H. Warzecha: Pharmaceutical Biotechnology. Wiley-VCH, Weinheim 2012.
- T. Dingermann, T. Winckler, I. Zündorf, : Gentechnik Biotechnik. 3. Auflage, Wissenschaftliche Verlagsgesellschaft, Stuttgart 2019.
- I. Krämer, W. Jelkmann: Rekombinante Arzneimittel – medizinischer Fortschritt durch Biotechnologie. 2. Auflage. Springer-Verlag, Berlin/ Heidelberg 2011.