Transferrin
Transferrin (aus lateinisch ferrum ‚Eisen‘ und transferre ‚hinübertragen‘) ist ein Glykoprotein, das von der Leber hergestellt wird und welches in Wirbeltieren hauptsächlich für den Eisentransport verantwortlich ist. Es hat zwei Bindungsstellen für Fe3+-Ionen, bindet freies Eisen im Serum und transportiert es zu Zellen, wo es von Transferrinrezeptoren aufgenommen wird. Es gibt verschiedene Glykoformen des Transferrins, insbesondere: pentasialo-, tetrasialo-, trisialo- und desialo-Isoform (CDT). Transferrin wird hauptsächlich in der Leber produziert; geringe Mengen werden außerdem in den Hoden, im Gehirn, der Milz und den Nieren gebildet.[1]
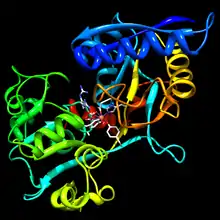
| Serotransferrin | ||
|---|---|---|
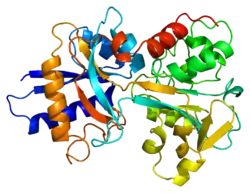 | ||
|
Vorhandene Strukturdaten: 1a8e, 1a8f, 1b3e, 1bp5, 1btj, 1d3k, 1d4n, 1dtg, 1fqe, 1fqf, 1jqf, 1n7w, 1n7x, 1n84, 1oqg, 1oqh, 1ryo, 1suv, 2hau, 2hav, 2o7u, 2o84 | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 679 AS; 75,2 kDa | |
| Sekundär- bis Quartärstruktur | Monomer; 3 Glycosyl- | |
| Isoformen | mehrere polymorphische Varianten | |
| Bezeichner | ||
| Gen-Namen | TF ; PRO1400 | |
| Externe IDs | ||
| Vorkommen | ||
| Homologie-Familie | Transferrin | |
| Übergeordnetes Taxon | Euteleostomi | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 7018 | 22041 |
| Ensembl | ENSG00000091513 | ENSMUSG00000032554 |
| UniProt | P02787 | Q921I1 |
| Refseq (mRNA) | NM_001063 | NM_133977 |
| Refseq (Protein) | NP_001054 | NP_598738 |
| Genlocus | Chr 3: 133.75 – 133.78 Mb | Chr 9: 103.2 – 103.23 Mb |
| PubMed-Suche | 7018 | 22041 |
Mit vier Prozent Anteil im Plasmaprotein ist Transferrin das vierthäufigste Protein im Blutplasma. Bei der Serumelektrophorese läuft Transferrin in der Fraktion der β-Globuline. Das in Transferrin gebundene Eisen beträgt ca. 0,1 % des gesamten Eisens im menschlichen Organismus. Bei voller Sättigung kann das Plasmatransferrin ca. 12 mg Eisen aufnehmen, eine vergleichsweise kleine Menge. Transferrin ist aber noch in ähnlicher Menge in der Lymphe und weiteren Körperflüssigkeiten vorhanden. Das Transferrin ist im Normalfall zu 30 Prozent mit Eisen besetzt. Bei Vergiftungen mit Eisen kann dieser Anteil auf 45 Prozent steigen und daher kann die Bindungskapazität des Transferrins schnell erschöpft werden, so dass freies Eisen im Plasma vorliegt, welches toxisch ist. Eine sehr seltene Stoffwechselkrankheit, die Hypotransferrinämie, hat als Ursache eine rezessive Mutation im für Transferrin codierenden Gen. Als Entdecker des Transferrins gelten Arthur L. Schade und Leona Caroline von der Overly Biochemical Research Foundation in New York City.[2][3] Sie veröffentlichten 1946 in Science einen Artikel über ihre Entdeckung.[4]
Funktion im Eisenstoffwechsel
Bisher sind zwei Transferrinrezeptoren bekannt: Transferrin-Rezeptor 1 (TfR1) wird in allen Zellen exprimiert, Transferrin-Rezeptor 2 (TfR2) hauptsächlich in der Leber. Bindet eisenbeladenes Transferrin an einen der Rezeptoren, wird der gesamte Komplex (Eisen, Transferrin, Rezeptor) über Rezeptor-vermittelte Endozytose aufgenommen und vesikulär zu den Endosomen transportiert. In den frühen Endosomen löst sich wegen des sauren Milieus das Fe3+ vom Transferrin.
Das Transferrin selbst (jetzt als Apotransferrin bezeichnet) bleibt an seinen Rezeptor gebunden. Der Rezeptor/Ligand-Komplex wird zur Plasmamembran transportiert (rezyklisiert) und im neutralen Milieu der extrazellulären Flüssigkeit dissoziiert Apotransferrin vom Rezeptor. Der Zyklus kann von neuem beginnen. Dies ist insofern eine Besonderheit, als normalerweise bei dieser Art der Endozytose meist entweder die Liganden oder sogar der Ligand/Rezeptor-Komplex durch Fusion des Vesikels mit Lysosomen abgebaut werden. Die Transferrinrezeptoren und das Transferrin erreichen über diesen Mechanismus sehr schnell wieder die Zelloberfläche. Fe3+ wird über ein Bindeprotein aus dem Endosom in das Zellplasma transportiert und dabei zu Fe2+ reduziert. In den Zellen wird Fe2+ dann von Ferritinen aufgenommen und zu Fe3+ oxidiert.
Eisen kommt z. B. in aktiven Zentren von Enzymen vor und ist wichtig für das Zellwachstum. Außerdem sind Eisenionen ein wichtiger Bestandteil des sauerstoffbindenden Hämoglobins. Eisenüberladung ist ebenso wie Eisenunterversorgung schädlich für den Organismus. Mutationen im TfR2 oder in der Regulation des TfR1 führen zum Krankheitsbild der Hämochromatose, einer gesundheitsschädlichen Eisenüberladung. Bei Eisenmangel kann es zu einer sogenannten Eisenmangelanämie kommen.
Interpretation des Transferrinspiegels
Die normale Eisen-Transferrinsättigung des Erwachsenen liegt bei etwa 25–30 %. Der Normwert des Transferrinspiegels (Transporteisen) beim Menschen beträgt 200–400 mg/dl. Eine Erhöhung des Transferrinspiegels wird bei Eisenmangel und in der Schwangerschaft beobachtet. Zu einer Verringerung des Transferrinspiegels kommt es bei chronischen Entzündungen, Tumorerkrankungen, Eisenüberladung (wie z. B. bei der primären (genetischen) oder sekundären Hämochromatose) oder einer Hämolyse. Bei regelmäßigem Alkoholmissbrauch steigt die disialo-Isoform, welche üblicherweise 1 % des Gesamttransferrins ausmacht, um das bis zu 10–15fache an.
Zur Detektion von Liquor, z. B. in Nasensekret bei einem Schädelbasisbruch kann β2-Transferrin bestimmt werden. Diese Isoform ist spezifisch für Liquor und nicht im Serum enthalten. β1-Transferrin ist dagegen sowohl in Liquor als auch in Serum enthalten.
Löslicher Transferrinrezeptor
Eine Erhöhung dieses Rezeptortyps (sTfR) im Serum korreliert sehr empfindlich bereits mit einem latenten Eisenmangel.
Evolution
Das menschliche Transferrin gehört zur Proteinfamilie der Transferrine, welche nicht nur beim Menschen vorkommen, sondern homologe Gene finden sich auch bei anderen Wirbeltieren und Wirbellosen.[5][6] Zur Proteinfamilie der Transferrine zählen auch die Lactoferrine der Säugetiere.[5][7]
Transferrine und das Eisen Fe+3 bindende Protein aus Haemophilus influenzae (hFBP) gehören einer gemeinsamen Protein-Superfamilie an. Die Eisen-bindenden Strukturen in Transferrinen und hFBP gingen jedoch aus Parallelentwicklungen hervor.[8]
Siehe auch
Einzelnachweise
- Bowman BH, Yang FM, Adrian GS: Transferrin: evolution and genetic regulation of expression. In: Adv. Genet.. 25, 1988, S. 1–38. PMID 3057819.
- Simon Welch: Transferrin: the iron carrier. CRC Press, Boca Raton 1992, ISBN 0-8493-6793-X.
- Jacobs EM, Verbeek AL, Kreeftenberg HG, et al.: Changing aspects of HFE-related hereditary haemochromatosis and endeavours to early diagnosis. In: Neth J Med. 65, Nr. 11, Dezember 2007, S. 419–24. PMID 18079564.
- Schade AL, Caroline L: An Iron-binding Component in Human Blood Plasma. In: Science. 104, Nr. 2702, Oktober 1946, S. 340–341. doi:10.1126/science.104.2702.340. PMID 17774530.
- Williams, John: The evolution of transferrin. Trends in Biochemical Sciences, Band 7, Nr. 11, 1982, S. 394–397.
- Ciuraszkiewicz, Justyna et al.: Reptilian transferrins: evolution of disulphide bridges and conservation of iron-binding center. Gene, Band 396, Nr. 1, 2007, S. 28–38, doi:10.1016/j.gene.2007.02.018
- Liang, Guo Ming, Xun Ping Jiang: Positive selection drives lactoferrin evolution in mammals. Genetica, Band 138, Nr. 7, 2010, S. 757–762.
- Bruns, Christopher M. et al.: Structure of Haemophilus influenzae Fe+3-binding protein reveals convergent evolution within a superfamily. Nature Structural & Molecular Biology, Band 4, Nr. 11, 1997, S. 919–924, doi:10.1038/nsb1197-919
Weblinks
- Eintrag zu Serum-Transferrin im Flexikon, einem Wiki der Firma DocCheck