Guanidinhydrochlorid
Guanidinhydrochlorid, genauer Guanidiniumchlorid, ist das Chlorid-Salz des Guanidinium-Kations.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
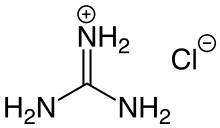 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Guanidinhydrochlorid | |||||||||||||||
| Andere Namen | ||||||||||||||||
| Summenformel | CH5N3·HCl | |||||||||||||||
| Kurzbeschreibung |
farb- und geruchsloser Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 95,53 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[3] | |||||||||||||||
| Dichte |
1,354 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Dampfdruck |
> 310 °C (Zersetzung)[3] | |||||||||||||||
| Löslichkeit |
gut in Wasser (2150 g·l−1 bei 20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Darstellung
Guanidinhydrochlorid wird bei der Umsetzung von Cyanamid mit Ammoniumchlorid in alkoholischer Lösung bei 100 °C gebildet.[6] Die Reaktionsgleichung ist wie folgt:
Verwendung
Es wird als chaotropes Renaturierungs- oder Denaturierungsmittel für Proteine in der Biochemie benutzt.[7][8] Weiterhin wird es als Zusatz für Flussmittel zum Löten eingesetzt.[9]
Einzelnachweise
- Eintrag zu GUANIDINE HCL in der CosIng-Datenbank der EU-Kommission, abgerufen am 20. November 2021.
- Datenblatt Guanidinhydrochlorid (PDF) bei Merck, abgerufen am 14. Dezember 2010.
- Eintrag zu Guanidiniumchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu Guanidinium chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Guanidinhydrochlorid (PDF) bei Carl Roth, abgerufen am 14. Dezember 2010.
- L. F. Fieser, M. Fieser, in: Lehrbuch der organischen Chemie, 3. Auflage, Verlag Chemie, 1957, Seite 267
- Werner A. Eckert, Jürgen Kartenbeck: Proteine: Standardmethoden der Molekular- und Zellbiologie : Präparation, Gelelektrophorese, Membrantransfer und Immundetektion. Springer, 1997, ISBN 978-3-540-61278-0, S. 32.
- David Nelson, Michael Cox, Albert L. Lehninger: Lehninger Biochemie. 3. Auflage, Springer, 2005, ISBN 978-3-540-41813-9, S. 200.
- Patent DE69420752T2: Lötflussmittel. Angemeldet am 27. Januar 1994, veröffentlicht am 18. Mai 2000, Anmelder: Cookson Group Plc, Erfinder: Dosten Baluch, Anthony Ellis Ingham.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. The authors of the article are listed here. Additional terms may apply for the media files, click on images to show image meta data.
