Magnetit
Magnetit, veraltet auch als Magneteisen, Magneteisenstein oder Eisenoxiduloxid sowie unter seiner chemischen Bezeichnung Eisen(II,III)-oxid bekannt, ist ein Mineral aus der Mineralklasse der „Oxide und Hydroxide“ und die stabilste Verbindung zwischen Eisen und Sauerstoff. Er kristallisiert im kubischen Kristallsystem mit der allgemeinen chemischen Zusammensetzung Fe3O4, die präziser als Fe2+(Fe3+)2O4[4] formuliert werden kann.
| Magnetit | |
|---|---|
 | |
| Allgemeines und Klassifikation | |
| Andere Namen |
|
| Chemische Formel | Fe3O4 genauer: Fe2+(Fe3+)2O4 |
| Mineralklasse (und ggf. Abteilung) |
Oxide und Hydroxide |
| System-Nr. nach Strunz und nach Dana |
4.BB.05 (8. Auflage: IV/B.02) 07.02.02.03 |
| Kristallographische Daten | |
| Kristallsystem | kubisch |
| Kristallklasse; Symbol | kubisch-hexakisoktaedrisch; 4/m 3 2/m |
| Raumgruppe | Fd3m (Nr. 227) |
| Gitterparameter | a = 8,3985(5) Å[1] |
| Formeleinheiten | Z = 8[1] |
| Häufige Kristallflächen | {111}, seltener {110} oder {100} |
| Zwillingsbildung | häufig nach dem Spinellgesetz: Durchkreuzungszwillinge nach (111) |
| Physikalische Eigenschaften | |
| Mohshärte | 5,5 bis 6,5[2] |
| Dichte (g/cm3) | gemessen: 5,175; berechnet: 5,20[2] |
| Spaltbarkeit | undeutlich nach (111)[3] |
| Bruch; Tenazität | muschelig, spröde |
| Farbe | schwarz |
| Strichfarbe | schwarz |
| Transparenz | undurchsichtig, an dünnen Kanten schwach transluzent |
| Glanz | schwacher Metallglanz |
| Magnetismus | ferrimagnetisch |
| Kristalloptik | |
| Brechungsindex | n = 2,42[2] |
| Doppelbrechung | keine, da optisch isotrop |
| Weitere Eigenschaften | |
| Chemisches Verhalten | säure- und basenstabil |
Magnetit entwickelt bei natürlicher Entstehung meist zentimetergroße, oktaederförmige Kristalle, aber auch körnige bis massige Aggregate von graubrauner bis schwarzer, metallisch glänzender Farbe. Aufgrund seines hohen Eisenanteils von bis zu 72,4 % und seines starken Magnetismus gehört Magnetit zu den wichtigsten Eisenerzen und Rohstoffen für die Elektroindustrie. Das Mineral kommt weltweit gesehen zwar eher selten vor, bildet aber bei lokaler Anhäufung große Erzlagerstätten.
Magnetit bildet mit Ulvöspinell (Fe2TiO4) eine Mischkristallreihe, deren Zwischenglieder als Titanomagnetit bezeichnet werden.[5]
Etymologie und Geschichte

Aus dem lateinischen Wortstamm magnet- (mit dem Nominativ magnes – Magnet) entstanden die Bezeichnungen Magnet (von mittelhochdeutsch magnete), als mittelalterlicher Mineralname Magneteisenstein (auch „magnetenstain“)[6] und der 1845 von Wilhelm Haidinger eingeführte Name Magnetit.
Bereits seit dem 11. Jahrhundert v. Chr. nutzten die Chinesen die magnetischen Eigenschaften des Minerals.
Ein Stein magnetis war Berichten des Theophrast zufolge den Griechen bekannt.[7] Bei dem römischen Schriftsteller Plinius dem Älteren lässt sich der Hinweis auf einen Stein namens magnes, der nach einem Hirten gleichen Namens bezeichnet sein soll, finden.[8] Dieser Hirte habe den Stein auf dem Berg Ida gefunden, als die Schuhnägel und die Spitze seines Stocks am Erdboden haften blieben. Plinius unterschied mehrere Arten des magnes, vor allem aber einen „männlichen“ und einen „weiblichen“, von denen jedoch nur der männliche die Kraft besaß, Eisen anzuziehen, und damit dem eigentlichen Magnetit entsprach. Bei „weiblichen“ magnes handelte es sich vermutlich um Manganerz, dem „männlichen“ im Aussehen ähnlich, oder auch um ein Mineral von weißer Farbe, das später als Magnesit MgCO3 bezeichnet wurde.
Wahrscheinlicher ist allerdings die Deutung, dass das Mineral nach Magnesia, einer Landschaft in Thessalien oder der Stadt Magnesia am Mäander, benannt wurde. Möglich ist auch die Benennung von Magnetit nach anderen griechischen bzw. kleinasiatischen Orten gleichen Namens, in denen schon vor über 2500 Jahren Eisenerzbrocken mit magnetischen Eigenschaften gefunden wurden.
Klassifikation
Die Mineral-Systematiken von Strunz und Dana ordnen den Magnetit aufgrund seines kristallchemischen Aufbaus in die Mineralklasse der Oxide und die Abteilung Stoffmengenverhältnis Metall : Sauerstoff = 3 : 4 ein. In der neuen Systematik der Minerale nach Strunz (9. Auflage) werden die Minerale dieser Abteilung zusätzlich nach der Größe der beteiligten Kationen sortiert, wobei das positiv geladene Eisenion zu den mittelgroßen Kationen zählt.
Die Systematik der Minerale nach Dana sortiert dagegen nach dem beteiligten Metallion (Fe) und der Kristallsymmetrie, sodass der Magnetit hier in der eisenhaltigen Untergruppe mit der gemeinsamen Punktgruppe 4/m 3 2/m innerhalb der Abteilung der „Mehrfachen Oxide mit der allgemeinen Formel (A+B2+)2X4, Spinellgruppe“ zu finden ist.
Kristallstruktur
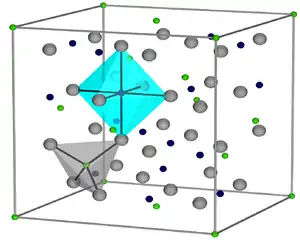 Elementarzelle von Magnetit | |
| Kristallsystem | kubisch |
| Raumgruppe | Fd3m (Nr. 227) |
| Gitterparameter (Elementarzelle) |
a = 8,3985(5) Å |
| Zahl (Z) der Formeleinheiten |
Z = 8 |

Kristallographisch gehört Magnetit zur Spinell-Gruppe und zeigt als natürlich gewachsener Kristall Oktaederflächen {111} und seltener Rhombendodekaederflächen {110}. Häufig kommt es zu Zwillingen nach dem Spinellgesetz (Durchkreuzungszwillinge nach (111)), jedoch nur selten bei eingewachsenen Kristallen.
Die Kristallstruktur von Magnetit (chemische Summenformel Fe3O4) kann nach der allgemeinen Formel für Spinelle AB2O4 als Fe3+[Fe3+Fe2+]O4 geschrieben werden. Die Bezeichnung inverse Spinell-Struktur für Magnetit trägt der Tatsache Rechnung, dass 1/3 der Eisenionen (Fe3+-Ionen) tetraedrisch und 2/3 der Eisenionen (Fe2+- und Fe3+-Ionen im Verhältnis 1:1) oktaedrisch vom Sauerstoff koordiniert sind, was gerade invers zum normalen Spinell ist. Die Symmetrie der Hochtemperaturphase (T > 120 K) von Magnetit wurde schon sehr früh im Jahre 1915 aufgeklärt[9], sie ist kubisch. Genauer gesagt handelt es sich um die Raumgruppe Fd3m (Raumgruppen-Nr. 227) bzw. O7h mit einem Gitterparameter a = 8,394 Å. Somit ergeben sich acht Formeleinheiten pro Elementarzelle mit insgesamt 56 Atomen.
Die Struktur der kubischen Hochtemperaturphase (T > 120 K) ist im Bild links schematisch dargestellt. Hier sind die kubisch dichteste Kugelpackung von Oxidionen (grau), die Oktaeder- (türkis) und Tetraederlücken (grau) dargestellt. Die Fe3+-Ionen in den Tetraederlücken sind grün und die Fe2+-/Fe3+-Ionen in den Oktaederlücken dunkelblau hervorgehoben. Das A-Untergitter, das von den tetraedrisch koordinierten Fe3+-Ionen aufgebaut wird bildet ein Diamantgitter, während das B-Untergitter der Fe2+- bzw. Fe3+-Ionen der oktaedrischen Sauerstoffumgebung ein Pyrochlorgitter bildet, das geometrisch frustriert ist. Geometrische Frustration bedeutet dabei, dass eine lokale Ordnung, die durch lokale Wechselwirkungen stabilisiert wird, sich nicht frei durch den Kristall fortsetzen kann. Diese besonderen geometrischen Eigenschaften ermöglichen eine große Anzahl unterschiedlicher Wechselwirkungen mit großer oder geringer Reichweite und sehr ähnlicher Energie, oft mit einem vielfach entarteten Grundzustand. Eine der Möglichkeiten die Entartung aufzuheben, ist eine langreichweitige Ladungs- oder Spinordnung, was zu extrem komplexen Kristallstrukturen führen kann, von denen bis heute nur wenige aufgeklärt sind.
Die genaue Raumgruppe der Tieftemperaturphase (T < 120 K) war bis ins Jahr 1982 nicht eindeutig bestimmt und wird sogar bis heute kontrovers diskutiert. Erst durch eine sorgfältig durchgeführte Neutronenbeugungsanalyse an synthetischen Einkristallen, die bei gleichzeitigem Anlegen von Druck entlang der [111]-Richtung und Kühlen im Magnetfeld gemessen wurden, konnte die kristalline Ordnung unterhalb von T = 120 K aufgeklärt werden. Es handelt sich um eine Verzerrung der monoklinen Raumgruppe Cc (Raumgruppen-Nr. 9) mit pseudo-orthorhombischer Symmetrie (Pmca (Nr. 57, Stellung 3); ac /√2 ⊗ ac /√ 2 ⊗ 2ac), wobei ac der Länge einer Achse der ungestörten kubischen Elementarzelle entspricht.
Eigenschaften
Magnetit ist von hoher Beständigkeit gegen Säuren und Laugen. Seine Mohshärte schwankt je nach Reinheit zwischen 5,5 und 6,5 und seine Dichte zwischen 5,1 und 5,2 g/cm³. Seine Strichfarbe ist schwarz.
Magnetismus
Magnetit ist eines der am stärksten (ferri)magnetischen Minerale. Beim Unterschreiten der Curie-Temperatur von 578 °C richtet sich die Magnetisierung größtenteils in Erdmagnetfeldrichtung aus, so dass eine remanente magnetische Polarisation in der Größenordnung von bis zu 500 nT resultiert. Magnetitkristalle können auf diese Art die Richtung des Erdmagnetfeldes zur Zeit ihrer Entstehung konservieren. Die Untersuchung der Magnetisierungsrichtung von Lavagestein (Basalt) führte Geologen zu der Ansicht, dass sich in ferner Vergangenheit tatsächlich die magnetische Polarität der Erde von Zeit zu Zeit umgekehrt haben müsse.

Die lange Zeit bekannten und verwendeten magnetischen Eigenschaften von Magnetit lassen sich sehr gut durch eine Betrachtung der lokalen Kristallstruktur erklären. Fe3O4 ist ein Ferrimagnet, archetypisch für die Ferrite der Spinelle. Die magnetische Ordnung in Magnetit kann man gut im Rahmen des Modells von zwei Untergittern nach Néel verstehen. In dem Modell wird angenommen, dass die Austauschwechselwirkung zwischen den oktaedrisch und tetraedrisch mit Sauerstoff koordinierten Eisenionenplätzen stark negativ, und die Austauschwechselwirkung zwischen den Ionen auf den gleichen Untergittern ebenfalls negativ ist, jedoch geringer im Betrag. Daraus folgt, dass die Ionen desselben Untergitters zueinander eine antiferromagnetische Spinstellung einnehmen würden, wenn dieser Neigung nicht durch eine stärkere Austauschwechselwirkung zwischen den Ionen der unterschiedlichen Untergitter entgegengewirkt würde. Die relative Stärke der Austauschwechselwirkung zwischen den Ionen unterschiedlicher Untergitter kommt durch die Unterschiede in den Distanzen zwischen den Ionen desselben Untergitters und Ionen unterschiedlicher Untergitter zustande. Diese Konstellation bevorzugt eine antiparallele Anordnung der magnetischen Momente der Untergitter, deren Untergitterionen zueinander eine parallele Spin-Anordnung aufweisen. In Magnetit koppeln die effektiven Momente der A-/B-Untergitter antiferromagnetisch über Superaustausch. Das Fe2+-Ion besitzt den Spin S=2 (4µB) und das Fe3+-Ion den Spin S = 5/2 (5µB), so dass sich bei der oben erklärten antiparallelen Anordnung der Fe3+-Ionen auf dem A-Untergitter bzw. der Fe2+/3+-Ionen auf dem B-Untergitter ein effektives Sättigungsmoment von (5-5+4)µB =4µB ergibt. Die Neel- bzw. Curie-Temperatur von Magnetit ist ungewöhnlich hoch und beträgt TN = 850 K.[10]
Verwey-Übergang
In der Leitfähigkeitskurve von Magnetit, in der die Leitfähigkeit über der Temperatur aufgetragen wird, ist das auffallendste Merkmal eine abrupte Änderung bei T=120K um zwei Größenordnungen. Magnetit wechselt dabei von einem schlechten Leiter in der Hochtemperaturphase (ca. 0,2 mΩm bei T > 120 K) zu einem Isolator in der Tieftemperaturphase (40 mΩm bei T < 120 K). Dieses Verhalten wurde 1939 von Evert Verwey systematisch untersucht und eine erste theoretische Erklärung für den Effekt veröffentlicht.[11] Ihm zu Ehren wird dieser Übergang und alle physikalisch ähnlichen Übergänge als Verwey-Übergänge bezeichnet. Erste Hinweise auf einen Phasenübergang in einem Temperaturbereich um 120 K lieferten frühe Wärmekapazitätsmessungen an synthetisch hergestellten Proben.[12] Der Phasenübergang ist als Isolator-Isolatorübergang zu charakterisieren.[13]
Modifikationen und Varietäten
Als Titanomagnetit (englisch auch Titaniferous Magnetite[14] werden die Mischkristalle der Reihe Magnetit (Fe3O4) und Ulvöspinell (Fe2TiO4) bezeichnet. Die Mischkristallformel wird allgemein mit Fe2+(Fe3+,Ti)2O4[15][14] (genauer auch mit xFe2TiO4·(1-x)Fe3O4[5]). Diese Mischreihe ist nur oberhalb von etwa 600 °C vollständig. Bei sinkender Temperaturen zerfallen die Mischkristalle und es bilden sich Entmischungslamellen von Ulvöspinell und Magnetit. Die am häufigsten auftretende Variante von Titanomagnetiten ist der sogenannte TM60 mit einem Ulvöspinellgehalt von rund 60 %.[5]
Titanomagnetit ist von großer Bedeutung bei der Erforschung des Paläomagnetismus, da diese bei der Abkühlung unterhalb der jeweiligen Curie-Temperatur ferrimagnetisch werden und sich dann im umgebenden Gestein dauerhaft (remanent) nach dem Erdmagnetfeld ausrichten. So ließ sich beispielsweise an den Basalten beiderseits des Juan-de-Fuca-Rückens nicht nur allgemein das zunehmende Alter des Gesteins in Abhängigkeit von dessen Entfernung des Rückens feststellen, sondern auch anhand des enthaltenen Titanomagnetits die mehrfach wechselnde Polung des Erdmagnetfeldes.[16]
Bildung und Fundorte
Natürliche Entstehung

Magnetit kann sowohl in Magmatiten wie auch in Metamorphiten und Sedimentiten gebildet werden.[17] So stellt er in mafischen Magmatiten wie Basalten oder Gabbros häufig einen wichtigen Nebenbestandteil, der oft früh auskristallisiert und deshalb oft gut definierte Kristalle bildet. In schnell erstarrten Gesteinen (Limburgiten) kann er aber auch Dendriten bilden. Daneben kann er akzessorisch in zahlreichen weiteren vulkanischen und plutonischen Gesteinen gefunden werden.
Bemerkenswert sind hauptsächlich aus Magmatit und Apatit bestehende Gesteine, die wichtige kommerzielle Lagerstätten darstellen (z. B. Kiruna in Nordschweden), und von denen angenommen wird, dass sie liquidmagmatischer Entstehung sind: Durch magmatische Differentiation ist dabei eine Teilschmelze entstanden, die oxidischen Charakters ist, d. h., praktisch keine Silikatbestandteile mehr enthält. In Kiruna bildete diese Teilschmelze einen Intrusionskörper; es sind aber auch Lavaströme aus solchem Gestein bekannt (etwa bei El Laco in Chile).[18]
Im Verbund mit vulkanischer Aktivität kann Magnetit auch durch Pneumatolyse gebildet werden, wenn eisenhaltige vulkanische Gase (die flüchtige Eisenverbindungen wie Eisen(III)-chlorid führen) etwa mit karbonatischen Nebengesteinen reagieren können. Auch durch diesen Mechanismus können Lagerstätten (Skarnerzlagerstätten) mit Magnetit gebildet werden.
In metamorphen Gesteinen ist Magnetit ein häufiges Mineral, welches aus zahlreichen eisenhaltigen Vorläufermineralen entstehen kann, insbesondere unter den Bedingungen der Kontaktmetamorphose. Ein Beispiel für Metamorphite mit häufig hohem Magnetitgehalt sind die aus Bauxiten entstandenen Schmirgelgesteine. Beispiele für regionalmetamorph gebildete Magnetitgesteine sind die quarzgebänderten Eisensteine (Itabirite),[19] die ebenfalls als Eisenlagerstätten von Bedeutung sind.
Auch durch hydrothermale Alterationsvorgänge kann Magnetit aus dem Eisenanteil verschiedener Vorläuferminerale entstehen. Ein bekanntes Beispiel ist der Magnetitgehalt in Serpentiniten, der oft so hoch ist, dass das Gestein erkennbar von einem Magneten angezogen wird.
Da Magnetit sehr verwitterungsbeständig ist, kann er akzessorisch in zahlreichen klastischen Sedimentgesteinen gefunden werden. Auch hier ist er manchmal bis zu kommerziell relevanten Konzentrationen angereichert (Magnetitsande). Sehr selten tritt er auch als primäre Mineralbildung in Sedimenten auf, so etwa in der Minette von Lothringen.
Je nach Bildungsbedingungen tritt Magnetit in Paragenese mit anderen Mineralen auf, so unter anderem mit Chromit, Ilmenit, Ulvöspinell, Rutil und Apatiten in Eruptivgesteinen; mit Pyrrhotin, Pyrit, Chalkopyrit, Pentlandit, Sphalerit, Hämatit in hydrothermalen oder metamorphen Gesteinen und mit Hämatit und Quarz in Sedimentgesteinen.[2]
Synthetische Herstellung
Für die Herstellung von Fe3O4 hat sich eine Methode, die von V.A.M. Brabers[20] erstmals zur Herstellung von einkristallinem Magnetit angewandt wurde, als die geeignetste herausgestellt. Dabei werden mit Hilfe des Zonenschmelzverfahrens in einem Spiegelofen Kristalle gezogen. Durch das Heizen eines Stabes aus α-Fe2O3 mit 99,9 % Reinheit im Spiegelofen, wird eine vertikale Schmelzzone zwischen Vorrat und Kristall erzielt, die allein durch die Oberflächenspannung gehalten wird, was eine Verunreinigung z. B. durch das Tiegelmaterial verhindert. Die so erhaltenen Kristalle, die zwischen 2 und 5 cm lang sind und einen Durchmesser von etwa 5 mm haben, werden im Anschluss an die Kristallisation im Spiegelofen 70 h bei 1130 °C in einer Atmosphäre aus CO2 und H2 getempert, um Gitterbaufehler auszuheilen und die richtige Stöchiometrie für Magnetit einzustellen. Die Orientierung der Kristalle längs der Stabachse entspricht grob der [100]-, [111]- und [110]-Richtung. Die Kristalle zeichnen sich durch ihre hervorragende Qualität, gemessen an dem Merkmal der Übergangstemperatur und der Schärfe des Übergangs wie er sich im Linienverlauf der Leitfähigkeitskurve (siehe Verwey-Übergang) ausdrückt, aus.



Vorkommen
Magnetit kommt in massiver oder gekörnter Form und daneben auch als Kristalle vor, welche oft oktaedrisch geformt sind, besitzen also je acht dreieckige Begrenzungsflächen. Er ist ein durchaus häufiges Mineral, das allerdings selten den Hauptbestandteil eines Gesteins stellt. Man findet Magnetit in zahlreichen magmatischen Gesteinen wie Basalt, Diabas und Gabbro, in metamorphen Gesteinen und durch Verwitterungsprozesse aufgrund seiner Härte weitgehend intakt verbracht als Magnetitsand in Flusssedimenten. Aus diesen wird er zum Teil noch heute von Hand ausgewaschen.
Magnetit kann in größeren Mengen an Sandstränden gefunden werden, wo er zu der typischen schwarzen Färbung des Sandes führt. Solche schwarzen Strände findet man z. B. in Kalifornien, an der Westküste von Neuseeland und an den Küsten von Fuerteventura und Island.
Weltweit konnte Magnetit bisher (Stand: 2010) an über 9600 Fundorten nachgewiesen werden. Sehr große Lagerstätten von Magnetit findet man in Kiruna (Schweden), in der Pilbara Region in (Westaustralien) und in der Adirondack Region des Staates New York (USA). Größere Vorkommen von Magnetit sind in Norwegen, Deutschland, Italien, der Schweiz, Südafrika, Indien, Mexiko und in Oregon, New Jersey, Pennsylvania, North Carolina, Virginia, New Mexico, Utah und Colorado in den USA gefunden worden.[21]
Auch in Gesteinsproben des Mittelatlantischen Rückens und des ostpazifischen Rückens konnte Magnetit nachgewiesen werden.[21]
Verwendung
Als Rohstoff

Magnetit ist mit 72 % Eisengehalt neben dem Hämatit (70 %) eines der wichtigsten Eisenerze.[22]
Magnetit dient als wichtiger Grundstoff zur Herstellung von Ferrofluid. Dabei werden im ersten Schritt Magnetit-Nanopartikel (Größenordnung ca. 10 nm) hergestellt, die dann in einer Trägerflüssigkeit kolloidal suspendiert werden. Um das Agglomerieren der Kristalle zu verhindern, werden den Nanopartikeln langkettige Tenside, wie z. B. Ölsäure zugefügt, die sich um die Magnetit-Partikel gruppieren und das erneute Sedimentieren verhindern. Die so erhaltene Flüssigkeit behält auf diese Art die Eigenschaft von Magnetit, auf Magnetfelder zu reagieren.
Als Baustoff
Magnetit wird in der Bauindustrie als natürlich gekörnter Zuschlag mit hoher Rohdichte (4,65 bis 4,80 kg/dm3) für Kalksandsteine und Schwerbeton und für bautechnischen Strahlenschutz verwendet.
Als Pigment
Aufgrund der hervorragenden magnetischen Eigenschaften wird Magnetit als Magnetpigment zur Daten-Speicherung eingesetzt und bis heute beim Bau von Kompassen verwendet. Feinteiliger synthetischer Magnetit wird unter der Bezeichnung Eisenoxidschwarz (Pigment Black 11)[23] (siehe auch Eisenoxidpigment) als Pigment, z. B. für Lacke eingesetzt.
In der Halbleiterelektronik
Aufgrund der von der Theorie vorhergesagten 100%igen Spinpolarisation[24] der Ladungsträger wird Magnetit auch als heißer Kandidat für Spinventile[25] in der Spinelektronik[26] gehandelt.
In Lebewesen
Verschiedene Tierarten sind zur Orientierung im Erdmagnetfeld auf Magnetit angewiesen. Hierzu gehören Bienen und Weichtiere (Mollusca). Besonders erwähnenswert sind Haustauben, die durch Einlagerung kleiner eindomäniger Magnetitkörner in den Schnabel die Feldstärke des Erdmagnetfeldes bestimmen und sich so orientieren können (siehe auch Magnetsinn).[27]
Die Raspelzunge der Käferschnecken ist teilweise mit Zähnen aus Magnetitkristallen besetzt. Die Tiere sind somit in der Lage Substrataufwuchs abzuweiden. Dadurch wirken sie abrasiv auf Gesteinsoberflächen ein.[28]
Einige Bakterien, sogenannte magnetotaktische Bakterien, wie z. B. Magnetobacterium bavaricum, Magnetospirillum gryphiswaldense oder Magnetospirillum magnetotacticum, bilden 40 bis 100 nm große Magnetit-Einkristalle im Inneren ihrer Zellen, die von einer Membran umgeben sind. Diese Partikel werden als Magnetosomen bezeichnet und sind in Form von linearen Ketten angeordnet. Die Ketten stellen gewissermaßen Kompassnadeln dar und erlauben den Bakterien geradliniges Schwimmen entlang der Erdmagnetfeldlinien.[29][30]
Auch die meisten Regionen des menschlichen Gehirns enthalten etwa fünf Millionen Magnetit-Kristalle pro Gramm und die Hirnhaut, genauer die äußere und innere Hirnhaut (Dura und Pia), enthält mehr als 100 Millionen Magnetit-Kristalle mit einer Größe von rund 50 nm.[31][32]
In der Krebstherapie
Magnetit kann, neben anderen Eisenoxid-, Kupfer- und Goldpartikeln,[33] dazu genutzt werden eine Krebsbehandlung zu unterstützen. Dazu werden Magnetitnanopartikel so modifiziert, dass sie in einer Suspension dispergiert im Körper bevorzugt von Tumorzellen aufgenommen werden. Dies führt zur Anreicherung der Teilchen in den betreffenden Bereichen. Durch ein äußeres Magnetfeld werden die Partikel anschließend zum Schwingen gebracht. Die resultierende Wärme erzeugt ein künstliches Fieber (sog. Hyperthermie), welches die betreffende Zelle empfänglicher gegenüber weiteren Behandlungsmethoden macht.[34]
Leben auf dem Mars?
Im Jahr 1996 veröffentlichten Wissenschaftler in der anerkannten Fachzeitschrift Science einen Artikel[35] über den möglichen Nachweis von Leben in Form von Bakterien auf dem Mars anhand eines Meteoriten (ALH 84001), der von dort stammt. Der Meteorit enthält kleine eindomänige Magnetitpartikel, wie sie typischerweise auch in magnetotaktischen Bakterien auf der Erde vorkommen. Die Debatte über die Interpretation der Messergebnisse hält allerdings bis heute an.
Esoterik
Die Eigenschaften, die dem Stein Magnetit zugeschrieben werden, beschrieb im 12. Jahrhundert Hildegard von Bingen. Nach der esoterischen Lehrmeinung sind sie: Aktivierung (geistig und körperlich), Erhöhung der Reaktionsfähigkeit sowie Anregung des Energieflusses und der Drüsentätigkeit. Magnetit ist demnach ein Stein, welcher in der Meditation insgesamt entstrahlt und eine besonders entspannende Aura bewirkt. Er soll z. B. gegen Hungergefühle, Körpergeruch und starkes Schwitzen, Verspannungen und Verkrampfungen helfen. Des Weiteren ist er angeblich entzündungshemmend, hilft bei Vergiftungen und Zellerneuerungen. Er bringt Harmonie, Wärme, löst Blockaden und macht glücklicher und unbeschwerter.
Siehe auch
Literatur
- Hans Berckhemer: Grundlagen der Geophysik. 2. Auflage. Institut für Meteorologie und Geophysik, Frankfurt am Main 2005, ISBN 3-534-13696-9.
- Martin Okrusch, Siegfried Matthes: Mineralogie. Eine Einführung in die spezielle Mineralogie, Petrologie und Lagerstättenkunde. 7., vollständig überarbeitete und aktualisierte Auflage. Springer, Berlin [u. a.] 2005, ISBN 3-540-23812-3, S. 83–84.
- Albert Radl: Der Magnetstein in der Antike. Quellen und Zusammenhänge. Franz Steiner Verlag, Wiesbaden, Stuttgart 1988, ISBN 3-515-05232-1.
Weblinks
- Mineralienatlas: Magnetit und Mineralienatlas: Mineralienportrait/Magnetit (Wiki)
- Magnetite. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 20. September 2019 (englisch).
- Magnetite search results. In: rruff.info. Database of Raman spectroscopy, X-ray diffraction and chemistry of minerals (RRUFF), abgerufen am 20. September 2019 (englisch).
- American-Mineralogist-Crystal-Structure-Database – Magnetite. In: rruff.geo.arizona.edu. Abgerufen am 20. September 2019 (englisch).
- Rätsel um Magnetsinn von Bakterien gelöst: Forscher entschlüsseln Entstehung der Magnetosomenketten. 21. November 2005, abgerufen am 20. September 2019.
Einzelnachweise
- Michael E. Fleet: The structure of magnetite: Symmetry of cubic spinels. In: Journal of Solid State Chemistry. Band 62, Nr. 1, 15. März 1986, S. 75–82, doi:10.1016/0022-4596(86)90218-5.
- Magnetite. In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America. 2001 (handbookofmineralogy.org [PDF; 147 kB; abgerufen am 20. September 2019]).
- Helmut Schröcke, Karl-Ludwig Weiner: Mineralogie. Ein Lehrbuch auf systematischer Grundlage. de Gruyter, Berlin; New York 1981, ISBN 3-11-006823-0, S. 363.
- Malcolm Back, William D. Birch, Michel Blondieau und andere: The New IMA List of Minerals – A Work in Progress – Updated: September 2019. (PDF 2672 kB) In: cnmnc.main.jp. IMA/CNMNC, Marco Pasero, September 2019, abgerufen am 20. September 2019 (englisch).
- Lexikon der Geowissenschaften – Titanomagnetit. In: wissenschaft-online.de. Spektrum.de, 4. Dezember 2014, abgerufen am 20. September 2019.
- vgl. etwa Jürgen Martin: Die ‚Ulmer Wundarznei‘. Einleitung – Text – Glossar zu einem Denkmal deutscher Fachprosa des 15. Jahrhunderts (= Würzburger medizinhistorische Forschungen. Band 52). Königshausen & Neumann, Würzburg 1991, ISBN 3-88479-801-4, S. 149 (zugleich Medizinische Dissertation Würzburg 1990).
- Theophrast von Eresos: Über die Steine.
- Gaius Plinius Secundus: Naturalis historia.
- W. H. Bragg, F. R. S. Cavendish: The Structure of the Spinel Group of Crystals. In: The philosophical magazine. Band 30, Nr. 176, 1915, ISSN 1478-6435, S. 305–315, doi:10.1080/14786440808635400.
- G. A. Samara, A. A. Giardini: Effect of Pressure on the Neel Temperature of Magnetite. In: The physical review. Band 186, Nr. 2, 1969, ISSN 0031-899X, S. 577–580, doi:10.1103/PhysRev.186.577 (documents.htracyhall.org [PDF; 2,1 MB; abgerufen am 20. September 2019]).
- E. J. W. Verwey: Electronic Conduction of Magnetite (Fe3O4) and its Transition Point at Low Temperatures. In: Nature. Band 144, August 1939, ISSN 0028-0836, S. 327–328, doi:10.1038/144327b0.
- Russell W. Millar: The heat capacities at low temperatures of „Ferrous Oxide“ magnetite and cuprous and cupric oxides. In: Journal of the American Chemical Society. Band 51, Nr. 1, 1929, ISSN 0002-7863, S. 215–224, doi:10.1021/ja01376a026.
- D. Schrupp, M. Sing, M. Tsunekawa, H. Fujiwara, S. Kasai, A. Sekiyama, S. Suga, T. Muro, V. A. M. Brabers, R. Claessen: High-energy photoemission on Fe3O4: Small polaron physics and the Verwey transition. In: epl, a letters journal exploring the frontiers of physics. Band 70, Nr. 6, 2005, ISSN 0302-072X, S. 789–795, doi:10.1209/epl/i2005-10045-y.
- Titaniferous Magnetite. In: mindat.org. Hudson Institute of Mineralogy, abgerufen am 20. September 2019 (englisch).
- Titanomagnetit. In: Mineralienatlas Lexikon. Stefan Schorn u. a., abgerufen am 26. November 2020.
- Victor Vacquier: Geomagnetism in Marine Geology. Elsevier Science Ltd, 1972, ISBN 978-0-444-41001-6, S. 40. In: Helmut Schröcke, Karl-Ludwig Weiner: Mineralogie. Ein Lehrbuch auf systematischer Grundlage. de Gruyter, Berlin; New York 1981, ISBN 3-11-006823-0, S. 363.
- Paul Ramdohr, Hugo Strunz: Klockmanns Lehrbuch der Mineralogie. 16. Auflage. Enke, Stuttgart 1978, ISBN 3-432-82986-8, S. 503–505.
- Walter Pohl: Mineralische und Energie-Rohstoffe. 5. Auflage. Schweizerbart, Stuttgart 2005, ISBN 3-510-65212-6, S. 12–13.
- Roland Vinx: Gesteinsbestimmung im Gelände. 3. Auflage. Spektrum, Heidelberg 2011, ISBN 978-3-8274-2748-9, S. 428–429.
- V. A. M. Brabers: The preparation of tetragonal single crystals in the MnxFe3-xO4 system. In: Journal of crystal growth. Band 8, Nr. 1, Januar 1971, ISSN 0022-0248, S. 26–28, doi:10.1016/0022-0248(71)90017-0.
- Fundortliste für Magnetit beim Mineralienatlas und bei Mindat, abgerufen am 26. November 2020.
- David Barthelmy: Mineral Species sorted by the element Fe (Iron). In: webmineral.com. Abgerufen am 20. September 2019 (englisch).
- Eintrag zu Eisenoxid-Pigmente. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. Juni 2014.
- Akira Yanase, Kiiti Siratori: Band Structure in the High Temperature Phase of Fe3O4. In: Journal of the Physical Society of Japan. Band 53, Nr. 1, 1984, ISSN 0031-9015, S. 312–317, doi:10.1143/JPSJ.53.312.
- W. Eerenstein, T. T. M. Palstra, S. S. Saxena, T. Hibma: Spin-Polarized Transport across Sharp Antiferromagnetic Boundaries. In: Physical review letters (PRL). Band 88, Nr. 24, 2002, ISSN 0031-9007, doi:10.1103/PhysRevLett.88.247204.
- A. M. Haghiri-Gosnet, T. Arnal, R. Soulimane, M. Koubaa, J. P. Renard: Spintronics, perspectives for the half-metallic oxides. In: Physica status solidi. A: Applications and materials science. Band 201, Nr. 7, 2004, ISSN 0031-8965, S. 1392–1397, doi:10.1002/pssa.200304403.
- Michael Winklhofer: Vom magnetischen Bakterium zur Brieftaube. In: Physik Unserer Zeit. Band 35, Nr. 3, 2004, ISSN 0031-9252, S. 120–127, doi:10.1002/piuz.200401039 (Vom magnetischen Bakterium zur Brieftaube (Memento vom 31. Dezember 2017 im Internet Archive) [PDF; 633 kB; abgerufen am 20. September 2019]).
- Michaela Falkenroth, Miklos Kázmér, Silja Adolphs, Mirjam Cahnbley, Hassan Bagci, Gösta Hoffmann: Biological Indicators Reveal Small-Scale Sea-Level Variability During MIS 5e (Sur, Sultanate of Oman). In: Open Quaternary. Band 6, Nr. 1, 2020, S. 1–20, doi:10.5334/oq.72 (pdfs.semanticscholar.org [abgerufen am 26. November 2020]).
- Marianne Hanzlik: Elektronenmikroskopische und magnetomineralogische Untersuchungen an magnetotaktischen Bakterien des Chiemsees und an bakteriellem Magnetit eisenreduzierender Bakterien. Herbert Utz Verlag, München 1999, ISBN 978-3-89675-632-9 (eingeschränkte Vorschau in der Google-Buchsuche – Dissertation. Ludwig-Maximilians-Universität).
- André Scheffel, Manuela Gruska, Damien Faivre, Alexandros Linaroudis, Jürgen M. Plitzko, Dirk Schüler: An acidic protein aligns magnetosomes along a filamentous structure in magnetotactic bacteria. In: Nature. Band 440, 2005, S. 110–114, doi:10.1038/nature04382.
- Joseph L. Kirschvink, Barbara J. Woodford: Superparamagnetism in the human brain. In: Thirteenth Annual Meeting of the Bioelectromagnetics Society. Band 80, 1991.
- Joseph L. Kirschvink, Atsuko Kobayashi-Kirschvink, Barbara J. Woodford: Magnetite biomineralization in the human brain. In: Proc. Natl. Acad. Sci. USA. Band 89, Nr. 16, 1992, S. 7683–7687, doi:10.1073/pnas.89.16.7683 (authors.library.caltech.edu [PDF; 1,7 MB; abgerufen am 20. September 2019]).
- Eva Richter-Kuhlmann: Hoffnungsvolle Einsatzgebiete der Nanomedizin. In: aerzteblatt.de. Ärzteblatt online, 2008, abgerufen am 26. Januar 2022.
- Andreas Jordan, Burghard Thiesen: Thermotherapie mit magnetischen Nanopartikeln (Nano-Krebs-Therapie). In: Konrad-Adenauer-Stiftung (Hrsg.): Innovationen in Medizin und Gesundheitswesen. Herder, Freiburg 2011, ISBN 978-3-451-30383-8, S. 308–325 (kas.de [PDF; 151 kB; abgerufen am 26. Januar 2022] kompletter Buchinhalt online verfügbar auf kas.de).
- David S. McKay, Everet K. Gibson Jr., Kathi L. Thomas-Keprta, Hojatolla Vali, Christopher S. Romanek, Simon J. Clemett, Xavier D. F. Chillier, Claude R. Maechling, Richar N. Zare: Search for past life on Mars. Possible relic biogenic activity in martian meteorite ALH 84001. In: Science. Band 273, 1996, ISSN 0036-8075, S. 924–930, doi:10.1126/science.273.5277.924 (websites.pmc.ucsc.edu [PDF; 2,9 MB; abgerufen am 20. September 2019]).