Lecithine
Lecithine (oder Lezithine; von griechisch λέκιθος lekithos, deutsch ‚Eidotter‘) ist ein in der Chemie synonym verwendeter Name für eine Gruppe chemischer Verbindungen, die sogenannten Phosphatidylcholine (PC). Dabei handelt es sich um Phospholipide, die Ester aus Fettsäuren, Glycerin, Phosphorsäure und Cholin darstellen. In der praktischen Verwendung im Bereich der Lebensmittel und der Pharmazie versteht man unter Lecithin hingegen technisch gewonnene Produkte, die neben Phosphatidylcholinen als Hauptbestandteilen auch andere Phospholipide und Begleitstoffe enthalten.

Phosphatidylcholine sind Bestandteile der Zellmembran tierischer und pflanzlicher Lebewesen. In den Membranen der meisten Bakterien kommen sie hingegen nicht vor.[1] Sie sind Begleitstoffe in Fetten und Ölen und besonders reich in Eidotter und Zellen pflanzlicher Samen vorhanden.
Lecithine erlauben das Emulgieren (Vermischen) von Fetten und Wasser und sind somit wichtige natürliche Emulgatoren für Lebens- und Futtermittel. In der EU sind sie als Lebensmittelzusatzstoff (E 322) für Lebensmittel (auch für „Bio-Produkte“) zugelassen mit Höchstmengenbeschränkung ausschließlich bei Säuglingsnahrung. Auf Zutatenlisten werden sie als Lecithin, Sojalecithin, Rapslecithin oder E 322 aufgeführt. In der Medizin und in der Kosmetik werden sie auch als Wirkstoff, in der Ernährung zu diätetischen Zwecken und zur Nahrungsergänzung genutzt.
Technisch gewonnene Lecithin-Produkte, wie Extrakte aus Sojabohnen, Raps oder Eiern, enthalten in Abhängigkeit von ihren Quellen neben Lecithinen ferner andere Phospholipide sowie Sphingomyeline und Glycolipide. Auch diese Stoffgruppen haben ähnliche physikalische Eigenschaften und sind Emulgatoren. Der Anteil der polaren Lipide (unlöslich in Aceton) muss entsprechend einer EU-Richtlinie in Lecithin-Produkten mindestens 60 % betragen.
Entdeckung und Erforschung
1811 berichtete der französische Apotheker Louis-Nicolas Vauquelin erstmals von fetthaltigen Präparaten aus Hirnmasse, die organisch gebundenen Phosphor enthielten und die bereits 1719 von dem deutschen Chemiker Johann Thomas Hensing gefunden wurden.
Der Franzose Nicolas-Theodore Gobley isolierte 1846/1847 aus dem Eigelb eine klebrige, orangefarbene Substanz, in der Ölsäure, Margarinsäure, Glycerinphosphorsäure sowie eine stickstoffhaltige organische Base vorhanden waren. Vergleichbare Stoffe fand er 1847–1858 in Hirnmasse, Karpfeneiern, Blut, Galle und anderen Organen. 1850 gab er seiner Entdeckung den Namen Lecithin nach dem griechischen Wort lekithos ‚Eigelb‘.
Der Deutsche Felix Hoppe-Seyler, Begründer der Biochemie und Molekularbiologie, fand 1867 organisch gebundenen Phosphor in Pflanzensamen. 1899 isolierten die deutschen Chemiker Ernst Schulze und Ernst Steiger aus Pflanzensamen Phospholipide, die sie ebenfalls als Lecithin bezeichneten. Nach ihren Erkenntnissen hatten die Sojabohnen und Lupinen mit 1,5–2,5 % den höchsten Lecithin-Gehalt der von ihnen untersuchten Pflanzensamen.
Die Forscher Diakonow und Adolph Strecker (1822–1871) isolierten Lecithin, z. B. aus Eigelb, in größerer Reinheit und erkannten, dass der stickstoffhaltige Anteil des Lecithins Cholin war.
Johannes Ludwig Wilhelm Thudichum (1829–1901), der Begründer der Gehirnchemie, fand eine analoge Verbindung und nannte sie Kephalin nach dem griechischen Wort kephalos ‚Kopf‘ und konnte das Sphingomyelin separieren.
Von Anfang 1900 bis in die späten 1930er-Jahre sind keine wesentlichen Fortschritte im Wissen um die Phospholipide zu erkennen. Ernst Klenk (1896–1971) und Sakat fanden 1939 im Sojalecithin Inosit und Inositphosphorsäure. 1944 extrahierte der amerikanische Chemiker Jon Pangborn aus dem Lipid des Rinderherzmuskels Cardiolipin und 1958 beschrieben Carter und seine Mitarbeiter die komplexen Phytoglykolipide, die nur in pflanzlichen Phospholipidmischungen vorkommen.
Als 1925 die Hansamühle Hamburg, heute ADM Ölmühle Hamburg AG, das Bollmannsche Extraktionsverfahren einführte, konnte aus rohem Pflanzenöl wirtschaftlich Lecithin isoliert werden. Die industrielle Produktion begann. Hauptquelle für Lecithin wurde das Öl der Sojabohnen. Lecithin aus Eidotter hat in speziellen Anwendungen, z. B. in der Pharmazie und Kosmetik, weiterhin eine Bedeutung.
Einer der ersten Anwendungsforscher für Lecithin war um 1925 Bruno Rewald, der als einer der ersten Lecithin-Technologen das Lecithin als Emulgator und Dispersionsmittel empfahl.
Hamburg wurde der Ausgangspunkt und das Zentrum für die industrielle Sojabohnen- und Lecithin-Verarbeitung. Der Amerikaner Josef Eichberg war der erste, der 1930 den Wert der Lecithine für die USA erkannte und dort das ‚Hamburger Lecithin‘ der Hansamühle vermarktete. Ab 1935 wurde Lecithin – in guter Qualität – auch in Amerika hergestellt. Es waren die Firmen Pillsbury und Central Soya (beide USA), die sich dieser vielseitigen Substanz annahmen.
Ab 1948 verschrieb sich Lucas Meyer, Hamburg, der Anwendungstechnik und dem Verkauf von Lecithinen. Mit Rüdiger Ziegelitz und Volkmar Wywiol, die ab 1953 die Vermarktung und Weiterentwicklung des Lecithins vorantrieben, gelang der weltweite Durchbruch für Lecithin als Hilfs- und Wirkstoff. Die Anwendungsvielfalt der Lecithine in den Bereichen Lebensmittel, Futter und Technik wurde von ihnen auf eine breite Basis gestellt.
In der diätetischen Anwendung leistete der Arzt Buer Pionierarbeit und brachte 1935 mit dem Produkt ‚Buer-Lecithin‘ eines der ersten Lecithinpräparate auf den Markt. H. Eickermann, A. Nattermann & Cie. (heute Konzern Sanofi-Aventis-Gruppe), konzentrierte sich auf die Wirksubstanz Phosphatidylcholin und entwickelte eine Reihe bedeutender pharmazeutische Präparate, die noch heute angeboten werden.
Herbert Rebmann entwickelte aus dem Eigelb Phospholipid-Spezialitäten als hochwertige Pharma-Emulgatoren für Fettnährstofflösungen.
Die Forschung und Anwendungstechnik ist längst noch nicht abgeschlossen. Derzeit sind beispielsweise Lecithine aus Meeresalgen, die Verwendung von Liposomen in der Nahrungsmittelindustrie und Phospholipide in der Aquakultur im Fokus der Wissenschaft.
Vorkommen und Verfügbarkeit

Vorkommen
Polare Lipide, besonders Phospholipide, sind wichtige Strukturbestandteile von biologischen Membranen und kommen in allen Lebewesen (Menschen, Tieren, Pflanzen und Algen) und in vielen Mikroorganismen vor. In der Leber und im Gehirn, in Lunge und Herz sowie im Muskelgewebe finden sich die höchsten Lecithin-Konzentrationen. Auch in manchen Körperflüssigkeiten sind Phospholipide – vor allem im Blutplasma der Wirbeltiere – vorhanden.[2] Phosphatidylcholin wird – wie auch Phosphatidylethanolamin – im Kennedy-Stoffwechselweg erzeugt.[3]
Verfügbarkeit
Derzeit werden pro Jahr etwa 180.000 t Lecithin vorwiegend aus den Sojabohnen (2 % Lecithin-Gehalt), die in den USA, in Brasilien und Argentinien geerntet werden, hergestellt. Andere Soja-Produzenten, wie China, Indien, Paraguay oder Kanada, haben für die weltweite Lecithin-Gewinnung derzeit wenig Bedeutung. Der Anbau von Soja in Europa ist marginal. Mehr als 70 % der weltweiten Soja-Ernte stammt aus gentechnisch veränderten Soja-Pflanzen (Stand 2011).[4] Neben Soja zählen, wenn auch in geringerem Umfang, Raps und Sonnenblumen als Rohstoffquellen. Eigelb, mit seinem hohen Anteil an Lecithin (ca. 10 %), kann den Markt wegen der beschränkten Verfügbarkeit kaum versorgen. Die relativ niedrigen Mengen gehen vor allem in die Pharmazie, Medizin und Kosmetik.
Wirkung von Lecithin im Körper
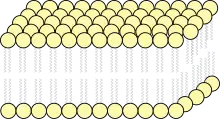
Den Lecithinen werden neben ihren strukturbildenden Eigenschaften zahlreiche funktionelle Aufgaben zugeschrieben. Sie sind sowohl am anabolen Lipidstoffwechsel (Synthese und Verteilung von Lipiden) als auch am katabolen Fettstoffwechsel (Abbau und Umbau von Lipiden) aktiv beteiligt.
- Die Zellmembran fast aller Zellen besteht aus einer Lipid-Doppelschicht. Lecithin ist essentiell für die Bildung der Biomembranen und Teilen der Zellorganellen. Insbesondere die Mitochondrien sind hinsichtlich ihrer Syntheseleistung mit den in der Molekularstruktur assoziierten Glykoproteinen auf Bestandteile des Lecithins angewiesen.
- Da Fette nicht wasserlöslich sind, sind zur Fettverdauung verschiedene körpereigene Schritte notwendig, um die mit der Zerlegung von Fetttröpfchen (Micellen) beginnende Verdauung durchführen zu können.
- Der Export von Fettsäuren aus der Leber ist insbesondere bei den landwirtschaftlichen Nutztieren wichtig.
Hühner nehmen mit der Nahrung vor allem Stärke auf, aus der in der Leber Fette für die Eibildung synthetisiert werden müssen; Lecithin ist hier notwendig, um die gebildeten Fette aus der Leber zu exportieren (Very Low Density Lipoproteins, VLDL), sonst besteht die Gefahr, dass das Tier an einer Fettleber erkrankt. Bei Kühen besteht diese Gefahr auch teilweise, allerdings ist dies hier Folge eines anderen Vorganges: Kurz nach der Geburt des Kalbes beginnt die sehr energieaufwendige Milchbildung. Hierzu werden Körperfettreserven mobilisiert, die zunächst in die Leber transportiert werden und von hier wiederum als VLDL in das Blut. Soweit die Versorgung der Kuh mit Aminosäuren zu diesem Zeitpunkt nicht adäquat ist (insbesondere: Lysin und Methionin), kann es ebenfalls zu einer Fetteinlagerung in der Leber kommen, was letztlich wohl zu einer Leistungsdepression führen kann. Die Forschung auf diesem Gebiet dauert noch an.
Chemische Struktur und Eigenschaften
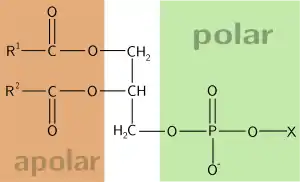
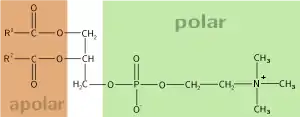
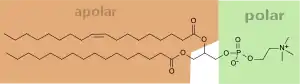
und der ungesättigten Ölsäure
(POPC = Palmityloleylphosphatidylcholin)
Lecithine (Phosphatidylcholine) sind eine weit verbreitete Verbindungsgruppe, die zu der übergeordneten Gruppe der Phosphoglyceride zählt. Phosphoglyceride sind Verbindungen, die mit Glycerin und zwei Fettsäuren einen Dicarbonsäureester bilden. Dieser Teil der Phosphoglyceride entspricht dem Aufbau von gewöhnlichen Fetten. Die dritte OH-Gruppe des Glycerins bildet jedoch mit einem Phosphat-Ion einen Phosphorsäurediester; einerseits mit Glycerin und andererseits mit einer weiteren, nicht näher definierten funktionellen Gruppe X. Die Gruppe X ist im Fall der Lecithine Cholin. Cholin ist eine quartäre Ammoniumverbindung, trägt also eine positive Ladung und ist ein Kation. Die Phosphat-Gruppe liegt über einen breiten pH-Bereich als Anion vor, trägt also eine negative Ladung. Somit kann man Lecithine als Zwitterionen bzw. Innere Salze auffassen. Lecithine haben keinen charakteristischen Schmelzpunkt, da die Verbindungen unterschiedliche Fettsäurezusammensetzung haben. Ungesättigte Fettsäuren wie Ölsäure oder Linolensäure sind bei Lecithinen recht häufig vertreten.
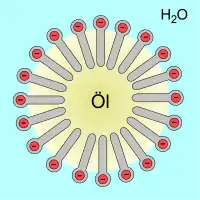
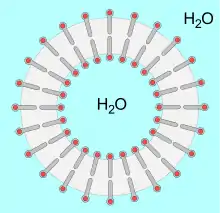
Der Aufbau dieser Verbindungen führt zu der Eigenschaft, als Tensid zu wirken: Ein Teil des Moleküls hat eine polare (hydrophile), ein anderer Teil eine apolare (hydrophobe) Eigenschaft. Sie sind somit amphiphil, können die Grenzflächenspannung zwischen unterschiedlichsten Substanzen (Phasen) herabsetzen und wirken als Emulgatoren oder Dispergiermittel. Sie erlauben daher das Mischen von eigentlich nicht mischbaren Flüssigkeiten wie Öl und Wasser und das Suspendieren von Partikeln in einer wässrigen Phase.
Analog können Lecithine Liposomen bilden, die als Modellvorstellung für die Entwicklung von Zellen dienen und in der Medizin als Transporthilfe von Wirkstoffen helfen können. Lecithine sind auch in der Lage, lamellare flüssigkristalline Phasen zu bilden, was von besonderem Interesse für die kosmetische Anwendung ist.
Andere Phospholipide
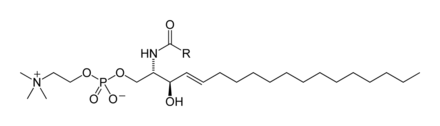
Lecithine, die aus natürlichen Quellen gewonnen werden, enthalten neben Lecithinen weitere Phosphoglyceride wie Phosphatidylethanolamin mit Ethanolamin, Phosphatidylserin mit Serin und Phosphatidylinositol mit Inosit als polare Gruppe X. Dazu liegen auch Sphingomyeline und Glycolipide vor, wobei letztere keine Phospholipide sind. Auch diese Verbindungsgruppen zeigen ähnliche physikalische Eigenschaften und wirken als Tenside. Natürliche Quellen für Lecithine sind z. B. Eier und Sojabohnen. Die Tabelle zeigt die ungefähre Zusammensetzung von Hühnerei- und Soja-Lecithin.
| Name | polare funktionelle Gruppe | Ei-Lecithin | Soja-Lecithin |
|---|---|---|---|
| Phosphatidylcholin | Cholin | 73 | 30 |
| Phosphatidylethanolamin | Ethanolamin | 15 | 22 |
| Phosphatidylserin | Serin 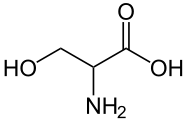 | – | 3–4 |
| Phosphatidylinositol | Inosit 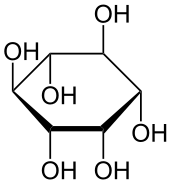 | 1 | 18 |
| Sphingocholine | Cholin | 2–3 | - |
| Glycolipide | Monosaccharide Oligosaccharide | – | 13 |
Physikalische Eigenschaften
Lecithine sind hygroskopisch. An der Luft bilden sie klebrige, wachsartige Massen. Bei längerer Erwärmung über 70 °C verfärben sich Lecithine dunkelbraun bis schwarz. Grundsätzlich sind Lecithine, die verwandten Phospholipide und deren modifizierten Abkömmlinge löslich in Fetten und Ölen und dispergierbar in Wasser. In organischen Lösemitteln wie Chloroform oder Hexan sind Lecithine gut löslich. In Aceton sind sie hingegen unlöslich. Die Löslichkeit in Ethanol ist abhängig von der Kettenlänge und dem Sättigungsgrad der Fettsäuren. Bei niedrigem Sättigungsgrad geht die Ethanollöslichkeit des Phosphatidylcholins zurück. Phosphatidylethanolamin und Phosphatidylinosit sind in Ethanol wenig bis unlöslich.
Lecithine sollten dicht verschlossen, vor Licht geschützt und nicht über 15 °C gelagert werden. Da es zu Oxidation mit molekularem Sauerstoff neigt (Autooxidation), können zur Stabilisierung Antioxidantien zugegeben werden.
Tabellarische Übersicht
| Name(n) | Summenformel | Acylreste |
|---|---|---|
| 1,2-Diacyl-sn-glycero-3-phosphocholin, (3-sn-Phosphatidyl)cholin, Lecithine | - | - |
| Eilecithin[6] (Phospholipide aus Eigelb) | - | - |
| Sojabohnenlecithin[7] (Phospholipide aus Sojabohnen) | - | - |
| 1,2-Didecanoyl-sn-glycero-3-phosphocholin,[8] Dicaprylphosphatidylcholin, DCPC | C28H56NO8P | Caprinsäure (10:0) |
| 1,2-Dilauroyl-sn-glycero-3-phosphocholin,[9] Dilauroylphosphatidylcholin, DLPC | C32H64NO8P | Laurinsäure (12:0) |
| 1,2-Ditetradecanoyl-sn-glycero-3-phosphocholin,[10] Dimyristoylphosphatidylcholin, DMPC, Colfosceriltetradecanoat (INN) | C36H72NO8P | Myristinsäure (14:0) |
| 1,2-Dipalmitoyl-sn-glycero-3-phosphocholin,[11] Dipalmitylphosphatidylcholin, DPPC, Colfoscerilpalmitat (INN) | C40H80NO8P | Palmitinsäure (16:0) |
| 1,2-Distearoyl-sn-glycero-3-phosphocholin, Distearylphosphatidylcholin, DSPC, Colfoscerilstearat (INN) | C44H88NO8P | Stearinsäure (18:0) |
| 1,2-Dioleoyl-sn-glycero-3-phosphocholin,[12] Dioleoylphosphatidylcholin, DOPC, Colfosceriloleat (INN) | C44H84NO8P | Ölsäure (18:1) |
| 1,2-Dilinoleoyl-sn-glycero-3-phosphocholin,[13] Dilinoleoylphosphatidylcholin, DLOPC | C44H80NO8P | Linolsäure (18:2) |
| 1,2-Diicosanoyl-sn-glycero-3-phosphocholin[14], Diarachidoylphosphatidylcholin, Colfoscerilicosanoat (INN) | C48H96NO8P | Arachinsäure (20:0) |
| 1,2-Dierucoyl-sn-glycero-3-phosphocholin,[15] Dierucoylphosphatidylcholin, DEPC, Colfoscerilerucat (INN) | C52H100NO8P | Erucasäure (22:1) |
| 1,2-Docosahexanoyl-sn-glycero-3-phosphocholin[16] | C52H80NO8P | Docosahexaensäure (DHA) (22:6) |
| 1-Palmitoyl-2-oleoyl-sn-glycero-3-phosphocholin[17] | C42H82NO8P | Palmitinsäure (16:0), Ölsäure (18:1) |
| 1-Palmitoyl-2-linoleoyl-sn-glycero-3-phosphocholin[18] | C42H80NO8P | Palmitinsäure (16:0), Linolsäure (18:2) |
| 1-Myristoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin[19] | C44H76NO8P | Myristinsäure (14:0), DHA (22:6) |
| 1-Palmitoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin[20] | C46H80NO8P | Palmitinsäure (16:0), DHA (22:6) |
| 1-Stearoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin[21] | C48H84NO8P | Stearinsäure (18:0), DHA (22:6) |
Gewinnung von Soja-Lecithin
Rohstoff: Sojabohne

Die Sojabohnen der Haupterzeugerländer stehen als nachwachsender Rohstoff ausreichend zur Verfügung (Ernte 2005: 214 Mio. t). Ausgereifte und sorgfältig gelagerte Bohnen sind für gute Lecithin-Qualitäten von großer Bedeutung. Die Bohnen müssen zunächst gereinigt, gebrochen und zu Plättchen gewalzt werden.
Rohstoff: Rohes Sojaöl
Die Plättchen (2–5 mm) werden in einer Extraktionsanlage im Gegenstrom mit Hexan extrahiert. Das dabei entstehende Gemisch (Miscella) wird destilliert und eingedampft und schließlich im Vakuum durch direktes Zuführen von Dampf vom Lösemittel befreit.
Das dabei entstandene Rohöl ist das Ausgangsprodukt für das Sojalecithin. Durch Dämpfung der Ölsaaten vor der Extraktion kann der Lecithingehalt des Rohöles um 50–100 % erhöht werden. Dabei sinkt dann der Anteil nicht hydratisierbarer Phospholipide im entschleimten Öl.
Ergebnis: Lecithin

Das Rohöl, das als Begleitstoff etwa 2 % Lecithin enthält, wird in einem Quellbehälter auf 70–90 °C erwärmt und mit 1–4 % Wasser intensiv vermischt. Dabei quillt das Lecithin auf, fällt als gallertartige Masse aus und wird mit hochtourigen Spezial-Separatoren vom Rohöl abgetrennt. Diesem Lecithin-Nass-Schlamm – mit etwa 12 % Öl, 33 % Phospholipiden und 55 % Wasser – wird in einem Dünnschichtverdampfer das Wasser entzogen. Es entsteht ein Rohlecithin, das 60–70 % polare Lipide und 27–37 % Sojaöl enthält. Der Wasseranteil beträgt jetzt nur noch 0,5–1,5 %.
Die Hauptbestandteile der durch die Entschleimung gewonnenen Rohlecithine sind: Phospholipide (auch als Phosphatide bezeichnet), Triglyceride, Glykolipide und Kohlenhydrate. Nebenbestandteile: Sterine, freie Fettsäuren, Farbstoffe und eine Reihe anderer Verbindungen.
Neben der Entschleimung durch das Quellverfahren mit Wasser gibt es die Entschleimung mit Säuren (Super Degumming) und ein Entschleimungsprozess mit dem Enzym Phospholipase A2. Hierbei werden besonders auch die sonst nicht oder nur schwer erfassbaren sogenannten nicht hydratisierbaren Phospholipide gefällt.
Reinlecithin – Fraktionen – Modifikationen
Für viele Anwendungen kann Lecithin in seiner ursprünglichen Form genutzt werden. Vielfach ist es aber sinnvoll, natives (ursprüngliches) Lecithin zu entölen, zu fraktionieren oder zu modifizieren, um für besondere Anwendungen spezifische Lecithine zu erhalten:
- Die Entölung dient zur Herstellung pulverförmiger oder granulierter „Reinlecithine“, indem das Öl und die freien Fettsäuren aus dem nativen Lecithin entfernt werden. Sie sind geschmacksneutral, gut dosierbar, besitzen eine hohe Phospholipidkonzentration und haben verbesserte O/W-Emulgiereigenschaften.
- Fraktionierung bedeutet die Auftrennung des Lecithinkomplexes in eine alkohollösliche und eine alkoholunlösliche Komponente. Aus der alkohollöslichen Fraktion kann durch ein chromatografisches Verfahren eine weitere Aufteilung in zwei Fraktionen mit spezifischen Eigenschaften erfolgen.
- Die Modifizierung beruht auf der Abtrennung eines Fettsäuremoleküls aus dem Phospholipidmolekül. Dies geschieht mit Hilfe der Phospholipase A2. Man nennt den Vorgang enzymatische Hydrolyse. Das dadurch entstandene „Lysolecithin“ ist besonders hydrophil, wodurch die O/W-Emulgiereigenschaften verstärkt werden und die Calciumionenverträglichkeit erhöht wird.
- Die Acetylierung, eine andere Form der Modifizierung, verändert das Phosphatidylethanolamin, indem an die Aminogruppe ein Essigsäuremolekül angelagert wird. Dadurch wird das entstandene Lysolecithin besonders hydrophil.
- Eine weitere Möglichkeit zur Verbesserung der Emulgieraktivität der Lecithine ist die Hydroxylierung der im Phospholipidmolekül gebundenen ein- und mehrfach ungesättigten Fettsäuren. Diese erfolgt durch die Umsetzung mit Wasserstoffperoxid.
Eigenschaften
Rohe vegetabilische Lecithine sind braune bis gelbliche Substanzen von plastischer und flüssiger Konsistenz. Die Farbe ist abhängig von der Herkunft der Saat, den Ernte- und Lagerbedingungen sowie den Verarbeitungsverfahren und -anlagen. Die Konsistenz wird durch den Ölgehalt, durch die Menge an freien Fettsäuren und den Feuchtigkeitsanteil bestimmt. Entölte Lecithine sind pulvrig bzw. granuliert. Gut gereinigte (raffinierte) Lecithine haben einen charakteristischen (bohnigen) bis neutralen Geruch und Geschmack. Grundsätzlich sind Lecithine, deren modifizierte Abkömmlinge und die fraktionierten Phospholipide löslich in Ölen und Fetten.
Anwendungen von Lecithin
Der Einsatz von Lecithin in der Nahrungs- und Futtermittelproduktion, in der Pharmazie und Medizin sowie in kosmetischen Erzeugnissen und im Nonfood-Bereich ist vielfältig. Nachstehend sind einige Verwendungsmöglichkeiten dargestellt.
Lebensmittel
 Brot und Backwaren
Brot und Backwaren Margarine
Margarine Schokolade und Schokoladenüberzug
Schokolade und Schokoladenüberzug Instantgetränk
Instantgetränk
Die größte Menge von industriell erzeugtem Lecithin, vorwiegend aus Sojabohnen, geht in die Lebensmittelwirtschaft. Zunächst war Pflanzen-Lecithin ein Ersatz für Ei-Lecithin. Längst gilt es aber als gleichwertig, teilweise sogar als überlegen. Einen festen Platz hat es als Emulgator und Dispersionsmittel, sowohl für hydrophile Stoffe in öligen und hydrophobe in wässrigen Medien als auch als Stabilisator von Grenzflächen in gasförmig/wässrigen und gasförmig/festen Nahrungsmittelsystemen. Sojalecithin aus gentechnisch veränderten Pflanzen ist in der Regel nicht nachweisbar, da es aufgrund des Herstellungsprozesses keine DNA aus der Pflanze mehr enthält. Lecithin aus gentechnisch veränderten Pflanzen ist kennzeichnungspflichtig.[22]
- Lecithin in Brot- und Backwaren: Lecithine sind vor allem wichtige Hilfsstoffe bei Backprozessen. Sie erleichtern das Aufschlagen fetthaltiger Teige und ermöglichen die Verwendung kleberarmer Teige. Die höhere Volumensausbeute, feinere Porung und knusprigere Kruste, die erzielt werden können, kommt besonders der Brötchenherstellung zugute. Die Fähigkeit des Lecithins, das Altbackenwerden von Brot- und Backwaren zu verzögern, ist besonders bedeutsam. Dem Teig wird 0,1–0,3 % reines Lecithin zugesetzt[23]. Kommerzielles Lecithinpulver besteht aus 50–95 % Mehl, diese Verdünnung erleichtert die Dosierung kleiner Mengen.
- Lecithin bei der Herstellung von Margarine: Anfangs hatte Margarine gegenüber der Butter den Nachteil des Spritzens beim Ausbraten sowie das feste Anhaften des Milchcaseins, das unter Geruchsbelästigung verbrannte. Um das zu verhindern, wurde zunächst Lecithin aus Eigelb als Emulgator eingesetzt. Die Probleme ließen sich aber erst mit geschmacksneutralem Sojalecithin wirtschaftlich lösen. Neue Verfahrenstechniken und Rezepturen sorgten für eine wesentliche Qualitätssteigerung, die aber zur Abkehr vom nativen Sojalecithin hin zu speziellen Lecithinfraktionen führten. Damit konnte dann auch eine bessere Oxidationsbeständigkeit und Stabilisierung erzielt werden. Eine gute Antispritzwirkung bei Halbfettmargarine (40 % Fett und 60 % Wasser) lässt sich mit Lecithin-Zusatz allein nicht erreichen. Dies gelingt nur in Verbindung mit grenzflächenaktiven Substanzen, wie Sojaproteinkonzentraten.
- Lecithin in Schokolade: Wie fast überall hat auch hier Lecithin eine Doppelfunktion: eine Qualitätssteigerung der Schokolade und eine Reihe von Vorteilen bei der Herstellung. Um in der Schokoladenherstellung die richtige Konsistenz zu erzielen und das typische Aroma zu erreichen, muss die Masse mehrere Stunden in der Conche gerührt werden. Durch den Einsatz von Lecithin wird dabei die Viskosität herabgesetzt, die Bearbeitungszeit verkürzt und Kakaobutter eingespart. Aber auch die Eigenschaften werden günstig beeinflusst. Die Schokolade wird widerstandsfähiger gegenüber erhöhten Temperaturen, die Haltbarkeit verlängert, der Glanz der Oberfläche erhöht und ein vorzeitiges Vergrauen vermindert. Die Industrie verwendet fast ausschließlich Sojalecithine, aber auch Lecithine aus Raps- und Sonnenblumensaaten werden eingesetzt. Synthetische Lecithine und Lecithin-Kombinationen können sich bei der Produktion als vorteilhaft erweisen. Das Gleiche gilt beim Einsatz von Lecithinfraktionen, die eine bessere Verflüssigung der Schokolade beim Conchieren zulassen als native Lecithine.
- Lecithin in Instant-Lebensmitteln: Pflanzenlecithine haben sich bei der Instantisierung von Kakao- und Kaffeepulver bewährt. Aber besonders effektiv lassen sie sich bei Voll- und Magermilchpulver einsetzen. Darüber hinaus dienen sie als Dispergiermittel in Sojaproteinerzeugnissen, Kartoffelstärke und Trockensuppen.
- Lecithin in Speiseeis: Industriell hergestelltem Speiseeis werden häufig Hilfsstoffe wie Bindemittel, Emulgatoren, Stabilisatoren, pflanzliche Fette sowie Aroma- und Farbstoffe zugesetzt. Als natürlicher Emulgator wird oft das in Eigelb vorkommende Lecitin eingesetzt. Mit seiner Hilfe wird eine feinste Verteilung der Fetttröpfchen im Wasser erreicht, ein Aufrahmen, also die Trennung des Fetts vom Wasser, verhindert. Vor allem tiefgekühlte Desserts wie Eiscreme oder Sorbets enthalten besonders viel Emulgatoren.[24]
- In Kaugummi wird Lecithin zu 0,3 % eingesetzt.[25]
Medizin
Lecithin ist beim Menschen in der Dickdarmschleimhaut vorhanden und schützt diese vor Nahrungsbestandteilen und Darmbakterien. Bei Colitis-Ulcerosa-Patienten kommt Lecithin dort in geringerer Menge als bei Gesunden vor. Es wird angenommen, dass eine externe Zufuhr von Lecithin diesem Mangel an Ort und Stelle entgegenwirken könne.[26][27] Da Magensäure Lecithin zu spalten vermag, sind magensaftresistente Formulierungen (z. B. magensaftresistenter Überzug, Mikroverkapselung) erforderlich, um einem Abbau entgegen zu wirken. Eine klinische Studie mit einem solchen Präparat wurde in der Phase 3 abgebrochen, nachdem sich im Vergleich zu Placebo keine Wirksamkeit abzeichnete.[28]
Futtermittel

- Kälber und Rinder: In Futtermitteln für Rinder hat Lecithin vornehmlich eine technologische Bedeutung. Lecithin verhindert z. B. bei der Herstellung mehlförmiger Kraftfuttermischungen die Staubbildung. Gleichzeitig sinkt die Gefahr von Staubexplosionen bei der Produktion. Es verzögert durch seine Emulgierfähigkeit das Aufrahmen des Fettes und die Sedimentation unlöslicher Bestandteile in der Tränke. Bei den Jungtieren allerdings stehen die physiologischen Aspekte eher im Vordergrund. So werden bei Kälbermilchaustauschern, bei denen die Kuhmilch durch Magermilch ersetzt und mit milchfremden Fetten und Proteinen angereichert werden, sehr gute – der Kuhmilch mindestens vergleichbare – Fütterungsergebnisse erzielt.

- Schweine: Bei künstlicher Sauenmilch, die häufig bei der Ferkelaufzucht notwendig wird, hat der Einsatz von Lecithin etwa die gleiche Bedeutung wie bei Kälbermilchaustauschern. Die Zugabe von Lecithin im Mastfutter bewirkt eine wesentlich bessere Fettverwertung, so dass sich die Mastzeit in der Regel verringern lässt.
- Hühner: Ein schnelleres Wachstum und eine vermehrte Vitamin-A-Speicherung in der Leber ließen sich bei Küken, wenn diese mit dem Futter Lecithin aufnahmen, nachweisen. Das Fettlebersyndrom, das seit 1956 in Deutschland beschrieben wird, wird durch die Zugabe von Lecithin – mit seinem hohen Anteil an Cholin und Inosit – im Legehennen-Futter günstig beeinflusst. Die Psoriasis trat ebenfalls nicht mehr auf. Ebenso kann die Legeleistung und das Ei-Gewicht von Hybriden erhöht werden.
- Aquakultur: In der Zucht von Forellen und Salmoniden führt die Unverdaulichkeit von Fetten zu Problemen und zu einer erhöhten Todesrate. Auch Seetier-Öle bewirkten Leber- und Nierenschäden und Depigmentierungen, so dass Forellen lange Zeit fettfrei gefüttert wurden. Lecithine sowie Geflügelfett allerdings haben einen günstigen Einfluss auf die Gesundheit und das Wachstum der Fische. Die Linol- und Linolensäure und das Cholin des Lecithins fördern das Wachstum und erhöhen die Futterverwertung. Nieren- und Darmblutungen sowie das Fettlebersyndrom lassen sich vermeiden. Die Verwendung von Lecithin in der Aquakultur gewinnt zunehmend an Bedeutung, wie etwa bei der Zucht von Krusten- und Schalentieren und Meeresfrüchten.
- Pelztiere: Zuerst vermutete man nur, dass die Verfütterung von Lecithin, z. B. bei Kaninchen und Nerzen, sinnvoll sein könnte, um Lebererkrankungen vorzubeugen – besonders während der Trächtigkeit. Spätere Fütterungsversuche bewiesen es. Das Wachstum ist zügiger, die Pelze der Jungnerze werden größer und von besserer Qualität. Die Fettleber ist bei Nerzen weit verbreitet. Das liegt einerseits an einer meist einseitigen Ernährung, aber auch an fehlenden Substanzen wie sie im Lecithin vorhanden sind und sich beim Leberstoffwechsel bewährt haben.
Non-Food-Bereich
Heute werden in den unterschiedlichsten Industrien aus wirtschaftlichen Überlegungen statt reinem Öl wässrige Emulsionen aus Ölen, Fetten und Wachsen eingesetzt. Dabei spielt das Lecithin als Emulgator und Wirkstoff eine herausragende Rolle. Etwa 20 % des verwendeten Lecithins geht in die technische Industrie.
Wichtige Anwendungsbereiche sind die Bauindustrie, die Behandlung von Bauholz, der Einsatz bei Chemiefasern, Bekleidungs- und Handschuhleder, Lederpflegemittel, beim Schmälzen von Wolle, Färben oder Bedrucken von Geweben und im Kohletransport durch Rohrleitungen sowie in Farben und Lacken.
Lecithin in der Kosmetik:
Phospholipide sind rückfettend. So verhindern sie bei normaler und besonders bei trockener Haut das Austrocknen nach dem Waschen. Diese Eigenschaft wird auch in Haarwaschmitteln genutzt. Sie regulieren den pH-Wert der Haut und unterstützen den natürlichen Schutzmantel gegen aggressive Umwelteinflüsse. Ihr hoher Gehalt an Linol- und Linolensäure wirkt bei Hautkrankheiten positiv. Relativ jung ist die Anwendung der Phospholipide zur Herstellung kugelförmiger Vesikel, den Liposomen. Die Kugeln sind durch Lipiddoppelmembranen aus Phospholipiden begrenzt. In ihrem Innern enthalten sie eine wässrige Phase, in der spezielle Wirkstoffe gelöst sind, die auf diese Weise leichter in die Haut eingeschleust werden können. In Kosmetikartikeln wird es in der Liste der Inhaltsstoffe als LECITHIN (INCI)[29] aufgeführt.
Phospholipide in Pflanzenschutzmitteln:
Pflanzenschutzmittel enthalten neben den Wirkstoffen Lösungsmittel und Emulgatoren und eventuell noch andere Hilfsstoffe. Ist Lecithin der Emulgator, reduziert er den bioziden Wirkstoffanteil bei gleichzeitiger Erhöhung der Wirksamkeit des verbleibenden Wirkstoffgehaltes. Die wässrige Emulsion bleibt beständig und ermöglicht eine bessere Verteilung der Wirkstoffe.
Als physisch wirksames Insektizid wird Lecithin auch zur Bekämpfung von Larven und Puppen von Stechmücken eingesetzt. Lecithin bildet einen besonders dünnen Film auf der Wasseroberfläche, wodurch das Anheften der aquatischen Entwicklungsstadien der Stechmücken mit ihren Atemorganen verhindert wird. Diese sterben aufgrund von Sauerstoffmangel ab, ohne dass dadurch andere Organismen geschädigt werden.[30]
Literatur
- Hermann Pardun: Pflanzenlecithine. Gewinnung, Eigenschaften, Verarbeitung und Anwendung pflanzlicher Phosphatidpräparate. Ziolkowsky, Augsburg 1988, ISBN 3-87846-128-3.
- Werner Schäfer, Volkmar Wywiol: Lecithin – Der unvergleichliche Wirkstoff. Strohte, Frankfurt 1986, ISBN 3-87795-031-0.
- Rüdiger Ziegelitz: Lecithine – Eigenschaften und Anwendungen. Lucas Meyer, Hamburg 1989.
- Jean Pütz, Christine Niklas: Schminken, Masken, schönes Haar – Die sanfte Kosmetik. vgs Verlagsges., Köln 1987, ISBN 3-8025-6151-1.
- D. D. Lasic: Liposomes. From Physics to Applications. Elsevier, Amsterdam 1993, ISBN 0-444-89548-5.
- Dietrich Arndt, Iduna Fichtner: Liposomen, Darstellung – Eigenschaften – Anwendung. Akademie-Verlag, Berlin 1986, ISBN 3-05-500148-6.
- Rüdiger Ziegelitz, Lutz Popper: Lecithin – bewährte Funktionalität (PDF; 743 kB). In: bmi aktuell. Hrsg. v. Backmittelinstitut. Bonn 2005,1 (Mai). (pdf).
- Tamas Balla: Phosphoinositides. Tiny lipids with giant impact on cell regulation. In: Physiological reviews. Band 93, Nr. 3, 2013, S. 1019–1137 (englisch).
Weblinks
- Lecithin/Sojalecithin, auf phytodoc.de
Einzelnachweise
- Suzanne Jackowski, John E. Cronan, jr., Charles O. Rock: Lipid metabolism in procaryotes. In: Dennis E. Vance, J. Vance (Hrsg.): Biochemistry of Lipids, Lipoproteins and Membranes. Elsevier, 1991, ISBN 0-444-89321-0, S. 80–81.
- H. U. Melchert, N. Limsathayourat, H. Mihajlović, J. Eichberg, W. Thefeld, H. Rottka: Fatty acid patterns in triglycerides, diglycerides, free fatty acids, cholesteryl esters and phosphatidylcholine in serum from vegetarians and non-vegetarians. Atherosclerosis. Mai 1987, 65 (1–2): S. 159–166, PMID 3606730
- F. Gibellini, T. K. Smith: The Kennedy pathway–De novo synthesis of phosphatidylethanolamine and phosphatidylcholine. In: IUBMB life. Band 62, Nummer 6, Juni 2010, S. 414–428, doi:10.1002/iub.337. PMID 20503434.
- transgen.de: Futter für Europas Nutztiere: Kaum Alternativen zum Import von (gentechnisch veränderten) Sojabohnen. (Memento vom 4. Juni 2012 im Internet Archive) 23. Februar 2012.
- Fachlexikon ABC Chemie. Bd. 2. 3. Auflage. Harri Deutsch, Frankfurt 1987, S. 855, ISBN 3-87144-899-0.
- Externe Identifikatoren von bzw. Datenbank-Links zu Eilecithin: CAS-Nummer: 93685-90-6, EG-Nummer: 297-639-2, ECHA-InfoCard: 100.088.721, DrugBank: DB14233, Wikidata: Q72470630.
- Externe Identifikatoren von bzw. Datenbank-Links zu Sojabohnenlecithin: CAS-Nummer: 8030-76-0, EG-Nummer: 310-129-7, ECHA-InfoCard: 100.100.049, DrugBank: DB14161, Wikidata: Q57657253.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Didecanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 3436-44-0, PubChem: 16219892, ChemSpider: 17347207, Wikidata: Q27147690.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Dilauroyl-sn-glycero-3-phosphocholin: CAS-Nummer: 18194-25-7, EG-Nummer: 242-086-4, ECHA-InfoCard: 100.038.246, PubChem: 512874, ChemSpider: 447460, Wikidata: Q27133754.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Ditetradecanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 18194-24-6, EG-Nummer: 242-085-9, ECHA-InfoCard: 100.038.245, PubChem: 5459377, ChemSpider: 4573168, Wikidata: Q27120592.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Dipalmitoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 63-89-8, EG-Nummer: 200-567-6, ECHA-InfoCard: 100.000.516, PubChem: 452110, ChemSpider: 398235, DrugBank: DB09114, Wikidata: Q5144764.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Dioleoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 4235-95-4, EG-Nummer: 224-193-8, ECHA-InfoCard: 100.021.995, PubChem: 10350317, ChemSpider: 8525772, Wikidata: Q27144815.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Dilinoleoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 998-06-1, EG-Nummer: 213-647-0, ECHA-InfoCard: 100.012.406, PubChem: 5288075, ChemSpider: 4450312, DrugBank: DB04372, Wikidata: Q27459459.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Diicosanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 61596-53-0, PubChem: 22880141, ChemSpider: 18879817, Wikidata: Q27279878.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Dierucoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 51779-95-4, PubChem: 24779126, ChemSpider: 24767239, Wikidata: Q27253299.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1,2-Docosahexanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 99296-81-8, PubChem: 24779134, ChemSpider: 24767409, Wikidata: Q27289797.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1-Palmitoyl-2-oleoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 26853-31-6, EG-Nummer: 248-056-7, ECHA-InfoCard: 100.043.673, PubChem: 5497103, ChemSpider: 4593686, Wikidata: Q10860475.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1-Palmitoyl-2-linoleoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 17708-90-6, Wikidata: Q107413593.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1-Myristoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 1191904-88-7, PubChem: 52923675, ChemSpider: 24767383, Wikidata: Q27160539.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1-Palmitoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 99265-04-0, PubChem: 24779131, ChemSpider: 24767386, Wikidata: Q27158963.
- Externe Identifikatoren von bzw. Datenbank-Links zu 1-Stearoyl-2-docosahexanoyl-sn-glycero-3-phosphocholin: CAS-Nummer: 99264-99-0, PubChem: 52923691, ChemSpider: 24767388, Wikidata: Q27275608.
- transgen.de: Lecithin - Gentechnik (Memento vom 27. Februar 2015 im Internet Archive) 27. Februar 2015.
- J. Schormüller: Lexikon der Lebensmittelchemie. 2013, ISBN 978-3-642-65779-5, S. 488.
- dradio.de: Bedenkliche Lebensmittelzusätze: Emulgatoren stören die Darmflora. 27. Februar 2015.
- Richard W. Hartel, Joachim H. von Elbe, Randy Hofberger: Confectionery Science and Technology. Springer, 2017, ISBN 978-3-319-61740-4, S. 398.
- W. Stremmel, H. Vural, O. Evliyaoglu, R. Weiskirchen: Delayed Release Phosphatidylcholine is Effective for Treatment of Ulcerative Colitis: A Meta-Analysis. In: Digestive Diseases. 2021, doi:10.1159/000514355.
- R. Weisshof, K. El Jurdi, N. Zmeter, D. T. Rubin: Emerging Therapies for Inflammatory Bowel Disease. In: Advances in Therapy. Band 35, 2018, S. 1746–1762, doi:10.1007/s12325-018-0795-9.
- Leben mit einer CED > Komplementäre Methoden >Lecithin, www.dccv.de, 13. Oktober 2016.
- Eintrag zu LECITHIN in der CosIng-Datenbank der EU-Kommission, abgerufen am 23. Oktober 2021.
- D. S. Kettle: Medical and Veterinary Entomology – Second Edition, (1995), Cab International