Docosahexaensäure
Docosahexaensäure (die Abkürzung DHA steht für englisch Docosahexaenoic acid) ist eine mehrfach ungesättigte Fettsäure. Sie gehört der Klasse der Omega-3-Fettsäuren an.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
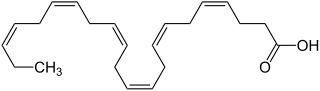 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Docosahexaensäure | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C22H32O2 | |||||||||||||||||||||
| Kurzbeschreibung |
hellgelbe Flüssigkeit[3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 328,49 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
0,95 g·cm−3[3] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen

Docosahexaensäure wird von phototrophen und heterotrophen, marinen Mikroalgen produziert. In hohen Konzentrationen kommt es in den Arten Ulkenia, Pavlova und in der heterotrophen Art Schizochytrium vor. Sie bilden die Basis für die Bereitstellung von DHA in der marinen Nahrungskette. Am häufigsten werden deshalb fettreiche Seefische wie Lachs (Salmo salar) oder Atlantischer Hering (Clupea harengus) als Nahrungsquelle für Eicosapentaensäure (EPA = Eicosapentaenoic acid) und DHA genannt. Über Fisch und vor allem auch Fischmehl, Fischöl und Tran gelangt es zuletzt in die menschliche Nahrung.
Der Mensch synthetisiert DHA aus α-Linolensäure (ALA), welche daher als essentiell eingestuft ist. Studien zeigen, dass etwa 5–10 % der aufgenommenen α-Linolensäure in EPA und 2–5 % in DHA umgewandelt werden. Andere Studien sprechen von Umwandlungsraten in EPA und DHA geringer als 5 %. Eine Studie kommt zu dem Schluss, dass die Umwandlungsrate ALA zu DHA bei Säuglingen gleich 1 %, bei Erwachsenen unter 1 % liegt.[4][5][6] Eine Steigerung des DHA-Spiegels im Blut durch Supplementierung von zusätzlicher ALA, EPA oder anderer Vorstufen ist laut International Society for the Study of Fatty Acids and Lipids (ISSFAL) nicht möglich.[4] Barcel-Coblijn & Murphy kommen zu dem Schluss, dass der Körper ausreichend DHA bilden kann, wenn genug α-Linolensäure (>1200 mg) pro Tag aufgenommen wird.[7] Eine Übersichtsarbeit von 2016, welche die Umwandlungsraten von ALA in DHA untersuchte, kommt zu dem Schluss, dass ALA ein ungeeigneter Ersatz für DHA ist.[8]
Sie kommt jedoch auch in wenigen Pflanzenarten in geringer Menge vor.[9]
Eigenschaften
Docosahexaensäure ist eine farblose ölige Flüssigkeit. Die sechs Doppelbindungen liegen in der cis-Form vor. Sie ist eine sogenannte Polyensäure und eine Isolensäure weil die Doppelbindungen durch eine Methylengruppe getrennt sind. Sie besitzt einen sehr tiefen Schmelzpunkt von −44 °C.
Analytik
Zur zuverlässigen qualitativen und quantitativen Bestimmung der Docosahexaensäure eignet sich nach angemessener Probenvorbereitung die Kopplung der Gaschromatographie, vorzüglich unter Einsatz von Kapillartrennsäulen, mit der Massenspektrometrie.[10][11][12] Durch den Einsatz der Massenspektrometrie lassen sich auch spezielle Fragen zur natürlichen oder synthetischen Herkunft der Docosahexaensäure beantworten.[13]
Biologische Funktion
Docosahexaensäure hat wichtige Stoffwechselfunktionen inne. Als Fettsäurekomponente von Phospholipiden ist sie integraler Bestandteil von Membranen, vor allem der Nervenzellen. So findet sich Docosahexaensäure insbesondere im Gehirn und in der Netzhaut angereichert: Bis zu 97 Prozent der Omega-3-Fettsäuren des Gehirns und bis zu 93 Prozent der Omega-3-Fettsäuren in der Netzhaut bestehen aus DHA. Im Gegensatz zu EPA kann DHA Blutdruck und Herzfrequenz senken.[14] DHA ist Ausgangsstoff der Biosynthese von Docosatrienen, Resolvinen und Neuroprotectinen (sogenannte Docosanoide).
Ihre Biosynthese im tierischen Organismus erfolgt ausgehend von der essentiellen Omega-3-Fettsäure α-Linolensäure über die für den Stoffwechsel ebenfalls bedeutsame EPA. Alter, Krankheiten und Stress genauso wie eine übermäßige Aufnahme an Omega-6-Fettsäuren (Maiskeimöl, Sonnenblumenöl etc.) beeinträchtigen zusätzlich noch die Umwandlung in Docosahexaensäure, z. B. wenn man den Fisch in Sonnenblumenöl anbrät. Die Aufnahmemenge hängt daher auch von der Zubereitung ab.[15] Der regelmäßige Genuss zum Beispiel fetter Seefische, die also am besten gedünstet, gebacken oder in Omega-6-Fettsäuren-armen Fetten gebraten werden, verbessert die Versorgung mit diesen Omega-3-Fettsäuren.
Zu den Geweben im menschlichen Körper, die Docosahexaensäure synthetisieren, gehören die Milchdrüsen (Brüste). DHA ist in Muttermilch enthalten, nicht jedoch in Kuhmilch, was eine Eigenheit der Spezies Mensch sein mag: Der Säugling erhält durch die Muttermilch so zusätzliche Docosahexaensäure zum Aufbau des relativ großen Menschengehirns im Gegensatz zu der Menge, die die Leber des Kleinkinds selbst synthetisieren kann.
Neuere Untersuchungen aus Italien konnten zeigen, dass die Spermaqualität mit dem Gehalt an Docosahexaensäure einher zu gehen scheint.[16] Die Ermittlung des Gehalts an Docosahexaensäure könnte daher die Aussagen eines Spermiogramms sinnvoll ergänzen.
Nahrungsergänzung
Seitens der Deutschen Gesellschaft für Ernährung gibt es keine allgemeine Zufuhrempfehlung für DHA/EPA (Ausnahme: Schwangere sollten 250 mg DHA pro Tag zuführen).[17]
DHA wird seit einigen Jahren in Form von Kapseln sowie mit Docosahexaensäure angereicherten Lebensmitteln angeboten. Zur Herstellung der Docosahexaensäure gibt es zwei derzeit industriell genutzte Möglichkeiten: die Aufarbeitung von Fischölen aus Fischabfällen fetter Seefische und die biotechnologische Gewinnung durch Züchtung Docosahexaensäure bildender Mikroalgen (Schizochytrium und Ulkenia[18]). Fische können diese Fettsäure selbst herstellen. Die aufgenommenen kurzkettigen Omega-3-Fettsäuren werden von Desaturasen und Elongasen zu Docosahexaensäure metabolisiert. Neben der eigenen Kapazität der Fischzellen, die Fettsäuren selbst zu synthetisieren, akkumulieren sie darüber hinaus Docosahexaensäure durch die Aufnahme von docosahexaensäure-haltigen Mikroalgen und Plankton.
Eine von der EU eingesetzte Expertenkommission rät Schwangeren zu einer Zufuhr von mindestens 200 mg DHA pro Tag,[19] was sich vor allem auf die Entwicklung der Augen- und Gehirnfunktionen des Ungeborenen positiv auswirken soll.[20] Auch zu einer ausreichenden Versorgung mit DHA vor allem in den ersten zwei Lebensjahren wird geraten. Mittlerweile setzen auch einige Hersteller von Säuglingsnahrung ihren Produkten Fischöl zu,[21] um den Bedarf von Säuglingen an Omega-3-Fettsäuren zu decken, welche in Muttermilch natürlicherweise vorhanden sind.
Das Bundesinstitut für Risikobewertung nennt als mögliche negative Auswirkungen bei einer Supplementierung mit DHA und EPA: Erhöhung des LDL-Cholesterins, Beeinträchtigung der Immunabwehr bei älteren Menschen, mögliche Erhöhung der kardiovaskulären Mortalität bei entsprechender Vorerkrankung, mögliche erhöhte Blutungsneigung und offene Fragen bei der Kinderernährung in Bezug auf Blutdruck und BMI.[22]
Einzelnachweise
- John W. Blunt, Murray H. G. Munro: Dictionary of Marine Natural Products. Chapman & Hall, 2008, ISBN 978-0-8493-8216-1, S. 701 f.
- H. M. Rauen: Biochemisches Taschenbuch. Springer, 1956, ISBN 978-3-642-53241-2 (Reprint), S. 232.
- Datenblatt cis-4,7,10,13,16,19-Docosahexaenoic acid, ≥98% bei Sigma-Aldrich, abgerufen am 19. Dezember 2019 (PDF).
- J. T. Brenna, N. Salem, A. J. Sinclair, S. C. Cunnane: alpha-Linolenic acid supplementation and conversion to n-3 long-chain polyunsaturated fatty acids in humans. In: Prostaglandins, leukotrienes, and essential fatty acids. Band 80, Nummer 2–3, 2009, S. 85–91, ISSN 0952-3278, doi:10.1016/j.plefa.2009.01.004, PMID 19269799.
- Breanne M. Anderson, David W. L. Ma: Are all n-3 polyunsaturated fatty acids created equal? In: Lipids in Health and Disease. 8, 2009, S. 33, doi:10.1186/1476-511X-8-33.
- J. T. Brenna: Efficiency of conversion of alpha-linolenic acid to long chain n-3 fatty acids in man. In: Current opinion in clinical nutrition and metabolic care. Band 5, Nummer 2, 2002, S. 127–132, ISSN 1363-1950, PMID 11844977.
- Gwendolyn Barcel-Coblijn, Eric J. Murphy: Alpha-linolenic acid and its conversion to longer chain n–3 fatty acids: Benefits for human health and a role in maintaining tissue n–3 fatty acid levels. In: Progress in Lipid Research. 48, 2009, S. 355–374, doi:10.1016/j.plipres.2009.07.002.
- E. J. Baker, E. A. Miles, G. C. Burdge, P. Yaqoob, P. C. Calder: Metabolism and functional effects of plant-derived omega-3 fatty acids in humans. In: Progress in lipid research. Band 64, 2016, S. 30–56, doi:10.1016/j.plipres.2016.07.002, PMID 27496755 (Review).
- 4,7,10,13,16,19-Docosahexaenoic acid bei PlantFA Database, abgerufen am 30. Oktober 2017.
- T. Yi, S. M. Li, J. Y. Fan et al.: Comparative analysis of EPA and DHA in fish oil nutritional capsules by GC-MS. In: Lipids Health Dis. 13, 2014, 190, PMID 25496531.
- J. Wang, D. Wang, H. Zhang et al.: Analysis of docosahexenoic acid in human blood using heterocyclic derivatization-gas chromatography-triple quadrupole mass spectrometry. In: Se Pu. 31(8), 2013, 734–8, PMID 24369605, (chinesisch).
- Y. Schober, H. G. Wahl, H. Renz, W. A. Nockher: Determination of red blood cell fatty acid profiles: Rapid and high-confident analysis by chemical ionization-gas chromatography-tandem mass spectrometry. In: J. Chromatogr. B Analyt. Technol. Biomed Life Sci. 1040, 2017, 1–7, PMID 27880928.
- R. J. S. Lacombe, V. Giuliano, S. M. Colombo et al.: Compound-specific isotope analysis resolves the dietary origin of docosahexaenoic acid in the mouse brain. In: J. Lipid Res. 58(10), 2017, 2071–2081, PMID 28694298.
- T. A. Mori, D. Q. Bao, V. Burke, I. B. Puddey, L. J. Beilin: Docosahexaenoic acid but not eicosapentaenoic acid lowers ambulatory blood pressure and heart rate in humans. In: Hypertension. 34(2), 1999, S. 253–60, PMID 10454450.
- Michael Lukas: Meuterei bei Käpt’n Iglo. Meldung bei DocCheck.com vom 13. Januar 2010.
- C. Zerbinati, L. Caponecchia, R. Rago et al.: Fatty acids profiling reveals potential candidate markers of semen quality. In: Andrology. 4(6), 2016, 1094–1101, PMID 27673576.
- Fett, essenzielle Fettsäuren. Abgerufen am 22. Februar 2021.
- Algenöl: Neuartiges Öl aus marinen Mikroalgen. Abgerufen am 12. September 2017.
- Pahrmiweb.com: New EU Recommendation Suggests Pregnant Women Need Higher Levels of Omega-3. Perinatal Lipid Nutrition group (PeriLip) (Memento des Originals vom 15. Dezember 2014 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis. auf pharmiweb.com, 29. August 2007.
- W. C. Heird: The role of polyunsaturated fatty acids in term and preterm infants and breastfeeding mothers. In: Pediatr. Clin. North Am. 48(1), 2001, S. 173–188, PMID 11236724.
- HiPP BIO Combiotik® Anfangsmilch Inhaltsangaben (PDF) Website Hersteller Hipp. Abgerufen am 26. November 2014.
- BfR: Für die Anreicherung von Lebensmitteln mit Omega-3-Fettsäuren empfiehlt das BfR die Festsetzung von Höchstmengen Stellungnahme Nr. 030/2009 des BfR vom 26. Mai 2009. (PDF) Abgerufen am 18. Februar 2021.
Literatur
- A. Hahn, A. Ströhle: ω-3-Fettsäuren: Prävention degenerativer Erkrankungen. In: Chemie in unserer Zeit. Band 38, Nr. 5, 2004, S. 310–318, doi:10.1002/ciuz.200400292.
- J. R. Marszalek, H. F. Lodish: Docosahexaenoic Acid, Fatty Acid-Interacting Proteins, and Neuronal Function: Breastmilk and Fish Are Good for You. In: Annual Review of Cell and Developmental Biology. Band 21, 2005, S. 633–657, doi:10.1146/annurev.cellbio.21.122303.120624, PMID 16212510.
Weblinks
- Philipp Kressirer: Nahrungszufuhr von omega-3 Fettsäuren bei Schwangeren. Klinikum der Universität München, Pressemitteilung vom 24. August 2007 beim Informationsdienst Wissenschaft (idw-online.de), abgerufen am 24. August 2015.