Phytosterine
Phytosterine, auch Phytosterole, sind eine Gruppe von in Pflanzen vorkommenden chemischen Verbindungen aus der Klasse der Sterine. Zusammen mit den Mycosterinen der Pilze unterscheiden sie sich von den tierischen Zoosterinen durch C1- oder C2-Substituenten an C-24 und in manchen Fällen durch eine Doppelbindung an C-22. Die hydrierten Formen (5α-Hydrierung) der jeweiligen Phytosterine werden als Phytostanole bezeichnet. Die Phytosterine kommen in den Pflanzen frei, in Ester- oder in Glycosid-Form sowie im unverseifbaren Anteil von pflanzlichen Fetten und Ölen vor. Die häufigsten pflanzlichen Sterine sind Stigmasterin, β-Sitosterin, Campesterin[1] und Brassicasterin.[2] Phytosterine fungieren als strukturelle Komponente in der Zellmembran von Pflanzen, analog dem Cholesterin in der Zellmembran von Tieren, das selbst jedoch kein Phytosterin ist, da es nicht in Pflanzen vorkommt. Das Vorliegen von Cholesterin kann daher auch zum Nachweis der Verfälschung von Pflanzenfetten mit tierischen Fetten eingesetzt werden.[3]
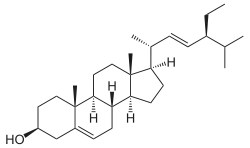
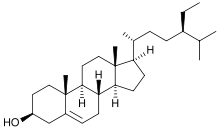
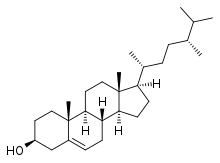
Im Europäischen Arzneibuch hingegen wird unter "Phytosterol" ein nach Gehalt (mind. 70 % β-Sitosterol) und Herkunft (nur Hypoxis-, Pinus- und Picea-Pflanzengattungen) definierter Stoff monographiert.
Analytik
Die zuverlässige qualitative und quantitative Bestimmung von Phytosterinen gelingt nach adäquater Probenvorbereitung z. B. aus dem unverseifbaren Anteil von Fetten und Ölen durch die Kopplung chromatographischer Verfahren mit der Massenspektrometrie[4][5]
Vorkommen
Phytosterine kommen hauptsächlich in fettreichen Pflanzenteilen vor. Besonders reich sind sie in Sonnenblumensamen, Weizenkeimen, Sesam und Sojabohnen sowie Kürbiskernen enthalten. Durch Verarbeitung, z. B. Raffinieren von Ölen, verlieren diese einen hohen Teil ihres Gehalts. Wertvoll sind daher besonders die unbehandelten nativen Öle, Fette und Samen.
Phytosterine werden kommerziell aus Sojabohnen bzw. aus Nadelhölzern als Nebenprodukt der Papierherstellung (Finnland) gewonnen. Eine besonders ergiebige Quelle für Phytosterine sind die unverseifbaren Bestandteile von Pflanzenfetten und -ölen sowie die bei der Raffination von Pflanzenfetten/-ölen anfallenden Nebenprodukte.[6]
β-Sitosterin ist mit ca. 65 % das in der normalen Nahrung am häufigsten vertretene Phytosterin. Weitere Sterine sind Stigmasterin und Campesterin, Ein wichtiger Vertreter der Phytostanole ist das Stigmastanol.
Resorption und Metabolismus
Bei normaler, westeuropäischer Ernährung werden täglich 160–360 mg an Phytosterinen aufgenommen. Vegetarier kommen auf ungefähr die doppelte Menge. Dies spiegelt sich auch in der höheren Sitosterin-Konzentration im Serum von Vegetariern wider.[7] 5–10 % der verzehrten Menge werden resorbiert (im Darm aufgenommen), der Rest mit dem Stuhlgang ausgeschieden. Der resorbierte Anteil wird über die Galle ausgeschieden.
Die Phytosterin-Konzentrationen im Serum liegen entsprechend weit unter jenen des Cholesterins und schwanken bei normaler Ernährungsweise zwischen 0,3 und 1,7 mg/dl.
| Modifikation des Grundgerüsts | Modifikation der Seitenkette | Resorption |
|---|---|---|
| Sterole | Cholesterin | > 40 % |
| Campesterin | 9,6 % | |
| Stigmasterin | 4,8 % | |
| Sitosterin | 4,2 % | |
| Stanole | Campestanol | 12,5 % |
| Stigmastanol | ||
| Sitostanol | 0–3 % |
Phytosterine als Wirkstoffe
Phytosterine werden therapeutisch zur Cholesterinsenkung und zur symptomatischen Behandlung der benignen Prostatahyperplasie eingesetzt. Auch zur Behandlung von Hautreizungen und Juckreiz finden sie Verwendung.
Wirkungsmechanismus
Als Wirkungsmechanismus wird eine kompetitive Hemmung der Cholesterinaufnahme im Darm angenommen, d. h. durch die Anwesenheit von Phytosterinen wird die Aufnahme von Cholesterin reduziert. Da Cholesterin jedoch nahrungsunabhängig vom Körper zu ca. 90 % selbst produziert wird, tritt infolge der Phytosterinaufnahme eine vermehrte endogene (körpereigene) Synthese ein. Dennoch kommt es insgesamt zu einer leichten Senkung des Gesamt- und des LDL-Cholesterins (Teilkompensation).
Neben der verminderten Resorption scheinen noch andere Mechanismen – eine beschleunigte Ausscheidung der resorbierten Sterine und andere – eine Rolle zu spielen. Phytosterine senken Gesamt- und LDL-Cholesterin unabhängig davon, ob das Individuum normale oder erhöhte Blutfettwerte aufweist. Phytosterine bewirken denselben Effekt bei Männern und Frauen und wirken altersunabhängig.
Triglyceride und HDL-Cholesterin bleiben unverändert. Soweit geprüft, bleiben alle klinischen Parameter außer Serumcholesterin (GPT, GOT, Hämoglobin, Glucose, Serumproteine, Serumbilirubin) unbeeinträchtigt.[9]
Phytosterine besitzen aufgrund ihrer starken Ähnlichkeit zum Cholesterin selbst atherogenes (Arteriosklerose auslösendes) Potential. Ab welcher Konzentration dieses atherogene Potential zu Tragen kommt, ist derzeit umstritten.[10][11][12]
Zufuhr
Als wirksame Mindestmenge gilt die Aufnahme von 2 g pro Tag. Diese Menge kann durch den Konsum von 100 ml Joghurtdrink (mit 1,6 g Phytosterinen angereichert) bzw. 20–30 g Streichfett/Margarine mit Phytosterinzusatz (normalerweise ca. 10 %) zusätzlich zu den mit einer normalen Mischkost aufgenommenen 0,2–0,4 g pro Tag erreicht werden.
Unerwünschte Wirkungen, Wechselwirkungen, Toxizität
In praktisch allen Studien wurde außer der Senkung des Gesamtcholesterins und des LDL-Cholesterins kein Einfluss auf andere Stoffwechselparameter festgestellt. Phytosterine zeigen eine additive Wirkung mit Statinen und anderen Cholesterinsenkern in Bezug auf die Senkung der Blutfette. Erfahrungsgemäß kann durch eine Verdopplung der Statindosis eine zusätzliche LDL-Cholesterin-Senkung um 6–8 % erzielt werden. Durch eine Kombinationstherapie (Statin + z. B. phytosterinangereicherter Joghurt) kann der LDL-Cholesterin-Spiegel um 10 % gesenkt werden.
Bislang gibt es keine Studie, die eine gesundheitsschädigende Wirkung von mit Phytosterinen angereicherten Lebensmitteln wie zum Beispiel Becel bei Personen ohne Phytosterinämie eindeutig belegt. Laut neuesten Erkenntnissen können pflanzliche Sterine jedoch auch negative Effekte auf die Gefäßgesundheit haben und daher nicht die herzschützende Wirkung haben, mit der sie beworben werden.[13] Eine wichtige Rolle spielen dabei genetische Polymorphismen, die einen Einfluss auf die Phytosterin-Resorption haben. Ihre Trägerschaft ist einerseits mit erhöhten Phytosterinspiegeln im Blut und gleichzeitig mit einem gesteigerten Herz-Kreislauf-Risiko verbunden.[14]
Um potenzielle Hypovitaminosen (A und E) zu vermeiden, sollten Kinder unter 5 Jahren, Schwangere und Stillende keine mit Phytosterinen angereicherten Produkte konsumieren.
Einfluss auf andere fettlösliche Nährstoffe
Es gibt Hinweise darauf, dass Phytosterine die Aufnahme von fettlöslichen Vitaminen beeinträchtigen. So wurden verminderte Carotin-, Vitamin-E- (α-Tocopherol) und Lycopenspiegel festgestellt.
Die Aufnahme von Vitamin D wird nicht beeinträchtigt.
Phytosterinprodukte
Die größte Bedeutung haben im Markt die Functional-Food-Produkte (Margarine, Milch, Joghurtprodukte). Einzelne Nahrungsergänzungsmittel sind im Markt. Arzneimittel sind in Deutschland (derzeit) nicht verfügbar. Im Bereich der benignen Prostatahyperplasie sind vornehmlich Arzneimittel und einzelne Nahrungsergänzungsmittel im Handel.
Die cholesterinsenkende Wirkung pflanzlicher Sterine wurde erstmals 1951 beschrieben und in der Folge durch zahlreiche klinische Studien bestätigt. Demnach lässt sich durch die Zufuhr von 1–4 g Phytosterinen pro Tag eine dosisabhängige LDL-Cholesterin-Reduktion um 5–15 % der Ausgangswerte erreichen. Am Markt werden mittlerweile mit Phytosterinen angereicherte Lebensmittel (Joghurtdrink, Margarine) angeboten.
Mehrere randomisierte, placebokontrollierte Studien belegen die Verbesserung des Lipidprofils nach dem 6-wöchigen Konsum eines mit Phytosterinen (1,6 g pro Portion) angereicherten Joghurtdrinks. Innerhalb von 3 Wochen sank das LDL-Cholesterin in der Phytosterin-Gruppe gegenüber Placebo um bis zu 12,2 %, innerhalb von 6 Wochen um bis zu 10,6 %. HDL-Cholesterin und Triglyzeride zeigten keine signifikanten Veränderungen.
20 g Streichfett mit 2–3 g Sterinen können den Cholesterinspiegel um durchschnittlich 6–10 % senken.
Der Nachweis der Wirksamkeit auf relevante klinische Endpunkte (wie die Verminderung der Mortalität, von Herzinfarkten und Schlaganfällen) fehlt.
Die Präparate im Bereich der benignen Prostatahyperplasie enthalten deutlich geringere Tagesdosen von um die 100 mg. Sie werden beim Thema β-Sitosterin besprochen.
Phytosterinämie
Ist eine sehr seltene, rezessiv vererbte Störung der Phytosterinaufnahme.[15] Bei Vorliegen einer Phytosterinämie werden deutlich mehr Sterine resorbiert (50–60 % der Nahrungssterine). Betroffene sollten die Zufuhr von Phytosterinen so weit wie möglich einschränken.
Kritikpunkte
Stichwortartige Zusammenfassung der Kritikpunkte und Bedenken der EFSA (European Food Safety Authority):
- Die maximale Menge an Sterinen soll 3 g pro Tag nicht überschreiten.
- Mögliche Gefahr einer Karotinunterversorgung
- Besondere Gefährdung
- Menschen mit Phytosterinämie
- Patienten unter cholesterinsenkender Medikation
- stillende Mütter
- Schwangerschaft
- mögliches Risiko durch Dauereinnahme oder kumulierte Einnahme in verschiedenen Nahrungsmitteln
- Effekt auf die Aufnahme von fettlöslichen Vitaminen und Karotinoiden
- die genaue Zusammensetzung und Stabilität des Phytosteringemisches
- die mögliche Einnahme durch Personen, die keinen zu hohen Cholesterinspiegel aufweisen
- die Schwierigkeiten einer adäquaten Kennzeichnung
Weitere Anwendungen
Derivate von Phytosterolen (P.-Ethoxylate und -Polyoxyethylene) werden in Kosmetika als Emulgatoren verwendet.[16][17]
Literatur
- Opinion of the Scientific Panel on Dietetic Products, Nutrition and Allergies on a request from the Commission related to a Novel Food Application from Forbes Medi-Tech for approval on plant sterol-containing milk-based beverages. In: The EFSA Journal. 15, Parma 2003, S. 1–12. (Request No. EFSA-Q-2003-075)
- B. Watzl, G. Rechkemmer: Phytosterine. Charakteristik, Vorkommen Aufnahme, Stoffwechsel, Wirkung. (Memento vom 14. März 2012 im Internet Archive) (PDF; 40 kB). In: Ernährungs-Umschau. (48), 2001, S. 161–164.
- I. Kiefer, Ch. Haberzettl, Ch. Panuschka, A. Rieder: Phytosterine und ihre Bedeutung in der Prävention. In: Journal für Kardiologie. Gablitz, Jg. 9. Nr. 3, 2002, S. 96–101. (PDF; 968 kB)
- E. Mutschler: Arzneimittelwirkungen. Lehrbuch der Pharmakologie und Toxikologie. 5. Auflage. Wissenschaftliche Verlagsbuchhandlung, Stuttgart 1986, ISBN 3-8047-0839-0.
- Alice H. Lichtenstein u. a.: Stanol/Sterol-Containing Foods and Blood Cholesterol Levels. In: Circulation. Philadelphia 2001, S. 1177–1179. (Abstract)
- M. Law: Plant sterol and stanol margarines and health. In: British Medical Journal. (BMJ). London 320.2000, S. 861–864. PMID 10731187.
- J. H. O'Keefe Jr, L. Cordain, W. H. Harris, R. M. Moe, R. Vogel: Optimal low-density lipoprotein is 50 to 70 mg/dl: lower is better and physiologically normal. In: Journal of the American College of Cardiology. New York 43.2006, S. 2142–2146. PMID 15172426.
- Manoj D. Patel, Paul D. Thompson: Phytosterols and vascular disease. In: Atherosclerosis. Amsterdam 186.2006, S. 12–19, doi:10.1016/j.atherosclerosis.2005.10.026.
- L. Van Horn, M. McCoin, P. M. Kris-Etherton, F. Burke, J. A. Carson, C. M. Champagne, W. Karmally, G. Sikand: The evidence for dietary prevention and treatment of cardiovascular disease. In: Journal of the American Dietetic Association. Chicago 108.2008, S. 287–331. PMID 18237578.
- N. Plana, C. Nicolle, R. Ferre, J. Camps, R. Cos, J. Villoria, L. Masana: Plant sterol-enriched fermented milk enhances the attainment of LDL-cholesterol goal in hypercholesterolemic subjects. In: European Journal of Clinical Nutrition. Basingstoke 47.2008, S. 32–39. PMID 18193377.
- B. Hansel, C. Nicolle, F. Lalanne, F. Tondu, T. Lassel, Y. Donazzolo, J.Ferrières, M. Krempf, J. L. Schlienger, B. Verges, M. J. Chapman, E. Bruckert: Effect of low-fat, fermented milk enriched with plant sterols on serum lipid profile and oxidative stress in moderate hypercholesterolemia. In: The American journal of clinical nutrition. Bethesda 86.2007, S. 790–796. PMID 17823447.
- O. Weingärtner u. a.: Controversial role of plant sterol esters in the management of hypercholesterolaemia. In: European Heart Journal. Oxford 30.2009, S. 404–409. PMID 19158117.
- O. Weingärtner, M. Böhm, U. Laufs: Pflanzliche Sterole als Nahrungsmitteladditiva zur Prävention kardiovaskulärer Erkrankungen. In: Dtsch. Med. Wochenschr. 133, 22, Mai 2008, S. 1201–1204. doi:10.1055/s-2008-1077238 PMID 18491276
Einzelnachweise
- Eintrag zu Phytosterole. In: Römpp Online. Georg Thieme Verlag, abgerufen am 10. Dezember 2014.
- C. L. Flakelar, P. D. Prenzler, D. J. Luckett, J. A. Howitt, G. Doran: A rapid method for the simultaneous quantification of the major tocopherols, carotenoids, free and esterified sterols in canola (Brassica napus) oil using normal phase liquid chromatography. In: Food Chem. 214, 1. Jan 2017, S. 147–155. PMID 27507459
- B. Xu, P. Li, F. Ma, X. Wang, B. Matthäus, R. Chen, Q. Yang, W. Zhang, Q. Zhang: Detection of virgin coconut oil adulteration with animal fats using quantitative cholesterol by GC × GC-TOF/MS analysis. In: Food Chem. 178, 1. Jul 2015, S. 128–135. PMID 25704693
- D. Kim, J. B. Park, W. K. Choi, S. J. Lee, I. Lim, S. K. Bae: Simultaneous determination of β-sitosterol, campesterol, and stigmasterol in rat plasma by using LC-APCI-MS/MS: Application in a pharmacokinetic study of a titrated extract of the unsaponifiable fraction of Zea mays L. In: J Sep Sci. 2. Sep 2016. PMID 27591043.
- C. L. Flakelar, P. D. Prenzler, D. J. Luckett, J. A. Howitt, G. Doran: A rapid method for the simultaneous quantification of the major tocopherols, carotenoids, free and esterified sterols in canola (Brassica napus) oil using normal phase liquid chromatography. In: Food Chem. 214, 1. Jan 2017, S. 147–155. PMID 27507459
- Patent DE10038457B4: Verfahren zur Gewinnung von Sterinen und Tocopherolen. Angemeldet am 7. August 2000, veröffentlicht am 25. September 2008, Anmelder: Cognis IP Management GmbH, Erfinder: Wolfgang Albiez et al.
- Sabine Junglas: Der Einfluss vegetarischer Ernährung auf die unverseifbaren Lipidkomponenten des Humanserums. Dissertation. TU Berlin, 1988, DNB 890684782.
- B. Watzl, G. Rechkemmer: Phytosterine. Charakteristik, Vorkommen Aufnahme, Stoffwechsel, Wirkung. (Memento vom 14. März 2012 im Internet Archive) (PDF; 40 kB). In: Ernährungs-Umschau. 48, 2001, S. 161–164.
- W. Ling, P. J. Jones: Dietary Phytosterols, A Review of Metabolism, Benefits and Side Effects. In: Life Sciences. 57 (3), 1995, S. 195–206 (PMID 7596226).
- O. Weingärtner u. a.: Controversial role of plant sterol esters in the management of hypercholesterolaemia. In: Eur Heart J. 30, 2009, S. 404–409. PMID 19158117.
- O. Weingärtner u. a.: The Relationships of Markers of Cholesterol Homeostasis with Carotid Intima-Media Thickness. In: PLoS ONE. 5(10), S. e13467. doi:10.1371/journal.pone.0013467
- O. Weingärtner u. a.: Differential Effects on Inhibition of Cholesterol Absorption by Plant Stanol and Plant Sterol Esters in ApoE -/- Mice. In: Cardiovasc Res. 2011. doi:10.1093/cvr/cvr020
- Schädigen Pflanzen-Sterine das Herz? In: aerztezeitung.de. 6. Juni 2008, abgerufen am 30. April 2015.
- D. Teubser u. a.: Genetic regulation of serum phytosterol levels and risk of coronary artery disease. In: Circ Cardiovasc Genet. 3(4), Aug 2010, S. 331–339. PMID 20529992.
- B. O. Ajagbe, R. A. Othman, S. B. Myrie: Plant Sterols, Stanols, and Sitosterolemia. In: J AOAC Int. 98(3), Mai-Jun 2015, S. 716–723. PMID 25941971.
- Moghis U. Ahmad: Lipids in Nanotechnology. Elsevier, 2015, ISBN 978-0-12-804345-5, S. 36.
- Krister Holmberg: Novel Surfactants. CRC Press, 2003, ISBN 0-203-91173-3, S. 231.