Helicobacter pylori
Helicobacter pylori ist ein gramnegatives, mikroaerophiles Stäbchenbakterium, das den menschlichen Magen besiedeln kann. Der spiralig gekrümmte Keim bewegt sich mittels seiner lophotrich angeordneten Geißeln fort.[1] Der Organismus ist vollständig DNA-sequenziert.
| Helicobacter pylori | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
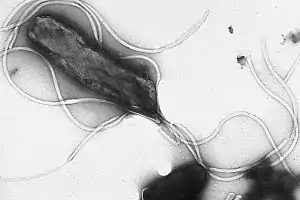
Helicobacter pylori | ||||||||||||
| Systematik | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
| Helicobacter pylori | ||||||||||||
| (Marshall et al. 1985) Goodwin et al. 1989 |
Geschichte
Vor der Entdeckung des Helicobacter pylori als Ursache von Geschwüren im Magen und Zwölffingerdarm (gastroduodenale Ulkuskrankheit) wurden „Übersäuerung des Magens“ sowie psychische Faktoren als Grund für die Krankheiten angenommen. Sie wurden mit Medikamenten behandelt, die Magensäure neutralisieren (Antazida) oder ihre Produktion blockieren (Magensäureblocker). Man nahm an, das saure Magenmilieu schließe eine Magenflora aus (vgl. hierzu die Voruntersuchungen und Erkenntnisse von Georg Ernst Konjetzny), obwohl bereits im Jahr 1905 von Walter Krienitz Bakterien im Magen beobachtet worden waren.[2]
Barry Marshall und John Robin Warren aus Perth, Western Australia, entdeckten 1983 H. pylori, was aber von der medizinischen Forschung lange Zeit nicht ernstgenommen wurde. Erst 1989 kam es zum Durchbruch und das Bakterium wurde weltweit als Ursache des Ulcus anerkannt. Im Dezember 2005 wurden Warren und Marshall für ihre Arbeiten über H. pylori je zur Hälfte mit dem Nobelpreis für Physiologie oder Medizin ausgezeichnet.
Ursprünglich wurde der Keim „Campylobacter pyloridis“ genannt (nach dem Pylorus). Später wurde er in „Campylobacter pylori“ umbenannt. Dieser Name passt besser zu den Namen anderer pathogener Keime im Magen-Darm-Trakt. 1989 erhielt er wegen seiner spiralig gekrümmten Form (Helix = Spirale) endgültig seinen heutigen Namen.
Weitere Helicobacter-Arten wurden seitdem auch in den Mägen anderer Säugetiere und von Vögeln entdeckt.
Häufigkeit und Verbreitung
Mit einer Prävalenz von weltweit ca. 50 % ist die Helicobacter-pylori-Infektion eine der häufigsten chronischen bakteriellen Infektionen. Hierbei ist die Infektionsrate in Entwicklungsländern sehr viel höher als in den Industrienationen. In Deutschland sind insgesamt etwa 33 Millionen Menschen mit H. pylori infiziert, von denen ungefähr 10 bis 20 % ein peptisches Geschwür entwickeln.
Es wurde zeitweise behauptet, dass das Vorkommen des Bakteriums im Zusammenhang mit dem sozioökonomischen Status stehe. Jedoch haben Arbeiten aus der Schweiz und Deutschland diese Ansicht nicht stützen können. So sind etwa sieben Prozent der Jugendlichen in der Schweiz und Deutschland von H. pylori befallen, unabhängig vom Status. Nach bisherigen Untersuchungen sind etwa 50 Prozent der älteren Erwachsenen mit dem Bakterium kontaminiert, jedoch nicht jeder entwickelt eine gastroduodenale Ulkuskrankheit.
Eine Studie an 2.219 Kindern in Leipzig ergab die Feststellung, dass bei H. pylori-infizierten Vorschülern etwa 2/3 der Eltern infiziert waren – doppelt so hoch, wie es statistisch zu erwarten war. Etwa 40 % der Kinder gaben Bauchschmerzen an. Die infizierten Kinder waren im Durchschnitt 1,4 cm kleiner und 1,3 kg leichter als die nicht infizierten Kinder.[3]
Für das weltweit verbreitete Bakterium konnten insgesamt 370 Stämme nachgewiesen werden, die in Details ihrer DNA-Sequenzen sehr große Unterschiede aufweisen. Bei einem Vergleich des Bakteriengenoms wurde festgestellt, dass es bevorzugt innerhalb von Familien weitergegeben wird. Das führt dazu, dass Bakterienstämme in unterschiedlichen geographischen Bevölkerungsgruppen genetisch unterscheidbar sind. Durch Vergleiche des Bakterienerbguts ist es Epidemiologen und Ethnologen möglich, die Ausbreitung der Bakterien und somit indirekt Wanderbewegungen der Menschheit seit mindestens 60.000 Jahren nachzuverfolgen.[4]
Erkrankung
Infektionen mit H. pylori werden für eine Reihe von Magenerkrankungen verantwortlich gemacht, die mit einer verstärkten Sekretion von Magensäure einhergehen. Darunter fallen beispielsweise die Typ-B-Gastritis, etwa 75 Prozent der Magengeschwüre und ca. 90–95 % Zwölffingerdarmgeschwüre. Die Untersuchung auf eine Infektion mit H. pylori ist daher heute ein wesentlicher Bestandteil der Diagnostik von Magenerkrankungen. Eine chronische Infektion mit H. pylori ist ein Risikofaktor für die Entstehung des Magenkarzinoms und des MALT-Lymphoms. Aus diesem Grund hat die WHO H. pylori 1994 in die Gruppe I der definierten Karzinogene eingeordnet. Darüber hinaus wurde H. pylori mit vielen anderen Erkrankungen in Zusammenhang gebracht, z. B. idiopathische chronische Urticaria, chronische Immunthrombozytopenie, ätiologisch unerklärliche Eisenmangelanämie, Morbus Parkinson.
Kolonisation
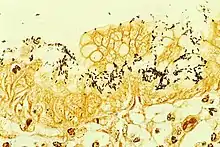
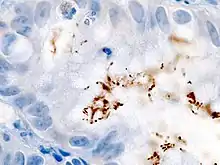
Der Übertragungsweg von H. pylori ist bis heute ungeklärt. Es scheint sich auf fäkal-oralem Weg zu verbreiten, also Ausscheidung des Bakteriums über den Stuhl und Wiederaufnahme durch Wasser oder verschmutzte Nahrung. Epidemiologische Daten weisen außerdem auf die Möglichkeit eines oral-oralen oder gastro-oralen (Kontakt mit durch H. pylori infiziertem Magenschleim bei Erbrechen) Übertragungsmechanismus hin. Der Magen gilt nach derzeitigem Kenntnisstand als das Hauptreservoir für die Keime, was die letzteren Auffassungen stärkt.
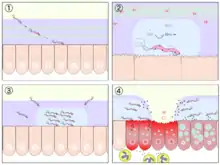
Ferner wird auch eine mögliche Übertragung durch Schmeißfliegen diskutiert. Die Besiedlung mit H. pylori erfolgt ausgehend vom Antrum cardiacum der Speiseröhre aboral in Richtung Mageneingang (Kardia) und Magenpförtner (Antrum pyloricum). Hierbei bewegt sich der Keim durch Geißelschlag fort. Spezialisierte Haftstrukturen ermöglichen ihm die besonders feste Anbindung an die Epithelzellen der Magenschleimhaut, die die Voraussetzung für das entzündliche Geschehen darstellt.
Im Magen schützt sich der säureempfindliche H. pylori vor der Zerstörung durch Magensäure
- durch Einnistung in und unter der Magenschleimhautbarriere (Schleim, der die Magenschleimhaut vor Selbstverdauung schützt) und
- durch die Spaltung von Harnstoff in Ammoniak und Kohlendioxid, wobei Ammoniak den pH-Wert in der unmittelbaren Umgebung des Keims anhebt (neutrales Mikromilieu, „Ammoniakmantel“). Diese Reaktion wird durch das von H. pylori produzierte Enzym Urease katalysiert, welches auch dem diagnostischen Nachweis dient (Helicobacter-Urease-Test).
Pathomechanismus
Die durch die Urease-Reaktion gebildete Ammoniakmenge ist normalerweise gering und bei intakter Magenschleimbarriere nicht toxisch. Vielmehr werden folgende schädigende Vorgänge beschrieben.
- H. pylori sezerniert eine Reihe von schleimhautschädigenden und die körpereigene Immunabwehr paralysierenden Enzymen. Die Entzündung führt zu einer vermehrten Gastrin- und infolgedessen zu einer vermehrten Magensäureproduktion. Dennoch verlaufen viele Typ-B-Gastritiden symptomlos. Nicht selten lässt erst eine zusätzliche Schwächung der Magenschleimhautbarriere (beispielsweise durch Alkoholkonsum, Nikotin, Arzneimittel, Stress usw.), die den Keim vorübergehend zu einer vermehrten Ammoniakbildung veranlasst, um sich selbst zu schützen (Ammoniaksprung)[5], ein Geschwür entstehen, meist im Bereich des Pylorus oder im Zwölffingerdarm.
- H.-pylori-Stämme vom Typ I weisen zusätzliche Pathogenitätsfaktoren auf und sind stark krankheitserregend in Bezug auf die gastroduodenale Ulkuskrankheit und auch Krebs. So ist ein grundlegender Auslöser die Exprimierung des entzündungsfördenden sogenannten vakuolisierenden Zytotoxins (VacA Genprodukt). Wie Cesare Montecucco zwischen 1993 und 2000 nachwies, bewirkt es die Bildung von kleinen Zellsafträumen (Vakuolen) in den Epithelzellen, die sich bis zum Zerplatzen mit Säure füllen und damit das Gewebe zerstören.
- Einen weiteren Mechanismus fanden Forscher des Institut Pasteur in Paris. Demzufolge injiziert das Bakterium über einen nadelartigen Fortsatz ein Peptidoglycan ins Innere der Magenepithelzelle. Dort dockt dieses an einen Rezeptor an und setzt eine Reaktionskette in Gang, die letztlich zur Entzündung der Magenschleimhaut führt.[6] Der Mechanismus ist genetisch codiert, der entsprechende Abschnitt auf dem Bakterienchromosom wird als „Zytotoxin-assoziierte-Gene-Pathogenitätsinsel“ (engl. cytotoxin-associated genes (cag)[7] pathogenicity island) bezeichnet.
Infektionen mit H.-pylori-Stämmen vom Typ II, denen die cag-Pathogenitätsinsel und die VacA-Sezernierung fehlen, gehen im Vergleich zu Infektionen mit Stämmen vom Typ I sehr viel seltener mit der gastroduodenalen Ulkuskrankheit einher. - Forscher des Deutschen Zentrums für Infektionsforschung entdeckten im Jahr 2016[8][9], welche Rezeptoren an der Bindung zwischen Bakterium H. pylori und Wirtszelle beteiligt sind. Dabei konnten sie Rezeptoren auf der Oberfläche der Epithelzellen identifizieren, die sogenannten CEACAMs (karzinoembryonale Antigen-Zelladhäsionsmoleküle, engl.: carcinoembryonic antigen-related cell adhesion molecule).[7] Auf bakterieller Seite vermittelt das Protein HopQ (die engl. Abkürzung Hop steht für 'H. pylori outer membrane protein'[7]) die Bindung, wirkt also als Adhäsin. CEACAMs kommen nicht im gesunden Magengewebe, sondern vor allem bei einer durch eine Infektion mit Helicobacter pylori hervorgerufenen Magenschleimhautentzündung vor. Das Molekülpaar CEACAM-HopQ ist nicht nur für die Bindung der Bakterien an ihre Wirtszellen wichtig, sondern auch für die pathogene Wirkung der Bakterien. Krankheitsauslöser ist das bakterielle Protein CagA.[7]
Diagnostik

Der direkte Nachweis des H. pylori geschieht durch Probeentnahmen (Biopsien) aus dem unteren Magendrittel und Mikroskopie. Auch kann aus den Proben mittels des Helicobacter-Urease-Test auf das Vorhandensein der Urease geschlossen werden und damit indirekt auf das Vorhandensein des Bakteriums.
Durch einen Atemtest kann der Keim ebenfalls mit hoher Wahrscheinlichkeit nachgewiesen werden. Dazu schluckt der Patient 13C- oder 14C-isotopenmarkierten Harnstoff in Form einer Lösung zusammen mit etwas Saft (Verlängerung der Kontaktzeit zwischen Urease und Substrat durch verzögerte Magenentleerung) oder in Form einer Kapsel mit etwas Wasser. Bei einer bestehenden Infektion wird der Harnstoff durch die von H. pylori produzierte Urease gespalten und das dabei entstehende 13C- oder 14C-markierte Kohlendioxid in der Ausatemluft nachgewiesen. Der Nachweis erfolgt bei 13C massenspektroskopisch im Labor oder mittels Infrarotspektroskopie in der Arztpraxis,[10] bei 14C mittels geeigneter Strahlungsdetektoren.
Diagnostisch existieren ferner der H.-pylori-Antigen-Test im Stuhl und der Antikörpernachweis im Serum (ELISA, Western-Blot). Stuhlantigen-Tests eignen sich gut bei Kindern und Erwachsenen und stellen eine kosteneffiziente Methode zur Helicobacter-pylori-Diagnostik dar.[11][12]
Therapie (Eradikation)
Bis zur Entdeckung der Helicobacter-pylori-Infektion als Ursache der Magenschleimhautentzündung und der gastroduodenalen Ulkuskrankheit bestand deren Therapie in der Verabreichung von Antazida oder Magensäureblockern (Protonenpumpenhemmer). Heute wird zunächst auf eine Infektion mit H. pylori untersucht. (Bei endoskopisch nachgewiesenem Zwölffingerdarmgeschwür ist zur Indikation einer antibiotischen Eradikation ein eindeutig positiver Urease-Schnelltest ausreichend[13]). Im Falle einer Infektion ist eine Eradikationstherapie zur Elimination des Bakteriums wirksam.
Gemäß den Maastricht-Leitlinien der European Helicobacter pylori Study Group (EHPSG)[14] ist die Eradikation von H. pylori indiziert bei:
- symptomatischer Helicobacter-pylori-Gastritis
- atrophischer Helicobacter-pylori-Gastritis, Riesenfaltengastritis
- gastroduodenaler Ulkuskrankheit mit Helicobacter-pylori-Nachweis
- positiver Familienanamnese eines Magenkarzinoms
- nach Magenteilresektion
- malignem MALT-Lymphom (Maltom)
- nach Resektion eines Magenfrühkarzinoms
- vor Dauertherapie mit NSAR (Ulkusprophylaxe)
Die Eradikationstherapie von H. pylori besteht aus der Kombination eines Protonenpumpenhemmers (Omeprazol, Pantoprazol, Lansoprazol, Esomeprazol oder Rabeprazol[15]) mit mindestens zwei Antibiotika, da antibiotische Monotherapien keinen ausreichenden Erfolg zeigen.
Es bestehen verschiedene Therapieschemata. Je nach Resistenzlage kommt ein Protonenpumpenhemmer in Kombination mit Amoxicillin, Metronidazol und Clarithromycin (PAMC), oder ein Protonenpumpenhemmer mit Bismutcitratkalium, Metronidazol und Tetracyclin (PBMT) zur Anwendung[16] (Kombinierte Vierfachtherapie oder Bismuthaltige Vierfachtherapie[17]). In Bereichen mit niedriger Resistenz gegen Clarithromycin kann eine Dreifachtherapie verwendet werden, bestehend aus einem Protonenpumpenhemmer, Clarithromycin und entweder Amoxicillin oder Metronidazol[16] („französische“ oder „italienische“ Standard-Triple-Therapie[17]). Reservetherapien sind PBMT oder eine Kombination von einem Protonenpumpenhemmer mit Levofloxacin und Amoxicillin[16] (Fluorchinololon-Triple-Therapie, alternativ zu Levofloxacin ist auch Moxifloxacin möglich[17]). Rifabutin-enthaltende Therapien sollten nur für Patienten verwendet werden, die auf drei verschiedene andere Therapien nicht angesprochen haben.[16]
Die Eradikation scheitert oft daran, dass eine Reinfektion über die orale Plaque stattfindet. Bereits 1999 hatten Riggio et al. nachgewiesen, dass H. pylori in der subgingivalen Plaque von 38 Prozent der untersuchten Parodontitis-Patienten vorhanden war. Zari et al. zeigen den Vorteil einer Kombination von Parodontitis-Therapie zur Reduzierung der Keime in der Mundhöhle und medikamentöser Triple-Therapie.
Als Ursachen für einen Misserfolg kommen des Weiteren neben mangelnder Compliance auch eine Antibiotika-Resistenz in Betracht. Vor einem erneuten Therapieversuch sollte der Erreger daher kultiviert und eine Resistenzbestimmung durchgeführt werden.
Mit dem 13C- oder 14C-Harnstoff-Atemtest (siehe Diagnostik) kann etwa vier bis sechs Wochen nach Therapieende der Eradikationserfolg nachgewiesen werden. Die Reinfektionsrate ist gering und liegt bei etwa 1 % pro Jahr.
Prophylaxe – Ausblick
2005 trafen sich am Max-Planck-Institut für Infektionsbiologie in Berlin Helicobacter-Experten aus Nordamerika, China und Europa, um über die Entwicklung und den Einsatz eines Impfstoffs zu diskutieren. Nach Thomas F. Meyer, Direktor des Instituts, wird „die Gefährlichkeit von H. pylori immer noch generell unterschätzt. Mehr als die Hälfte aller Menschen ist damit infiziert und man muss davon ausgehen, dass etwa zehn Prozent der Weltbevölkerung einmal im Leben an einem Magengeschwür erkranken.“ Ein Teil davon leidet danach an einem Magenkarzinom, das weltweit jährlich etwa 750.000 Opfer fordert. Es ist zehn- bis zwanzigfach häufiger als der seltene Speiseröhrenkrebs. Um den Zusammenhang dieser Krebsform, des Sodbrennens und des Verschwindens des Magenkeims H. pylori geht es vor einer Entscheidung über die Impfstrategie.
Die Berliner Forscher warnen vor verfrühter Hoffnung auf die Möglichkeit zur Impfung. Ein zuverlässiger Impfstoff stand auch 2011 noch nicht zur Verfügung.[18] Eines der Probleme bei der Entwicklung eines Impfstoffs ist darin begründet, dass alle mit Helicobacter Infizierten eine Antikörperantwort gegen das Bakterium zeigen, auch wenn die Infektion oft symptomlos verläuft. Die Reaktion des Körpers ist offensichtlich nicht ausreichend, um den Keim zu eliminieren. Ein Mechanismus ist, dass Helicobacter das Enzym γ-Glutamyltransferase (GGT) produziert, das die T-Zellen blockiert. Strukturelemente des Enzyms werden als Epitop für die Induktion von Antikörpern erforscht, die dann das Enzym gezielt lahmlegen können.[19]
Erste Erfolge bei der Impfstoffentwicklung wurden 2013 aus China berichtet. Hier wurde ein Impfstoff gegen Helicobacter pylori entwickelt, der eine gute lokale und humorale Immunität bewirkt.[20]
Genomforschung
Bereits im Jahr 1997 wurde die erste komplette Genomsequenz eines Vertreters der Art H. pylori publiziert. 1999 wurde eine zweite Sequenz veröffentlicht, womit sich erstmals die Möglichkeit ergab, die Genomsequenzen von zwei Isolaten derselben Bakterienart zu vergleichen. Dabei zeigte sich, dass sich die beiden Isolate in etwa 10 % der Gene unterschieden.[21][22]
Literatur
Fachliteratur
- M. Kist, E. Glocker, S. Suerbaum: Pathogenese, Diagnostik und Therapie der Helicobacter-pylori-Infektion. In: Bundesgesundheitsblatt, Berlin 48.2005,6 (Juni), S. 669–678. ISSN 0007-5914
- B. J. Marshall: Unidentified curved bacillus on gastric epithelium in active chronic gastritis. In: The Lancet, London 1983,1(Nr. 8336), 1273–1275. PMID 6134060 ISSN 0140-6736
- B. J. Marshall, J. R. Warren: Unidentified curved bacilli in the stomach patients with gastritis and peptic ulceration. In: Lancet. London 1984,1 (Nr. 8390), 1311–1315. PMID 6145023 ISSN 0140-6736
- Helicobacter pylori in peptic ulcer disease. in: Consensus Development Conference Statement. National Institutes of Health (NIH). Bethesda 12.1994,1 (Jan. 7–9), 1–23.
- Helicobacter pylori and peptic ulcer. Centers for Disease Control and Prevention, Atlanta . (Cited 2004 Dec 21, online).
- M. J. Blaser: An Endangered Species in the Stomach. In: Scientific American. New York 292.2005, 2, 38–45. PMID 15715390 ISSN 0036-8733
- R. P. H. Logan, M. M. Walker: Clinical review. ABC of the upper gastrointestinal tract. Epidemiology and diagnosis of Helicobacter pylori infection. In: British Medical Association (BMJ). London 323.2001, 920–922. PMID 11668141 ISSN 0959-8138
- S. Tsuji, N. Kawai u. a.: Review article: inflammation-related promotion of gastrointestinal carcinogenesis – a perigenetic pathway. Review. in: Alimentary Pharmacology and Therapeutics. Oxford 2003,18(Suppl 1), 82–89. PMID 12925144 ISSN 0269-2813
- J. Viala, C. Chaput, I. G. Boneca, A. Cardona, S. E. Girardin, A. P. Moran, R. Athman, S. Mémet, M. R. Huerre, A. J. Coyle, P. S. DiStefano, P. J. Sansonetti, A. Labigne, J. Bertin, D. J. Philpott, R. L. Ferrero: Nod1 responds to peptidoglycan delivered by the Helicobacter pylori cag pathogenicity island. In: Nature Immunology. Band 5, Nummer 11, November 2004, ISSN 1529-2908, S. 1166–1174, doi:10.1038/ni1131, PMID 15489856.
- M. P. Riggio u. a.: Identification by PCR of Helicobacter pylori in subgingival plaque of adult periodontitis patients. In: The journal of medical microbiology (J Med Microbiol). Reading 1999, 48, 317–322. ISSN 0022-2615
- S. Zari u. a.: Periodontal Therapy Improves Gastric Helicobacter pylori Eradication. In: Journal of Dental Research. Thousand Oaks Ca 2009, 88, 946–950. ISSN 0022-0345
- A. Kandulski, M. Selgrad, P. Malfertheiner: Helicobacter pylori infection – a clinical overview. In: Dig Liver Dis. 40.2008.8 (Aug), 619–626. PMID 18396114, doi:10.1016/j.dld.2008.02.026
- Marianne Abele-Horn: Antimikrobielle Therapie. Entscheidungshilfen zur Behandlung und Prophylaxe von Infektionskrankheiten. Unter Mitarbeit von Werner Heinz, Hartwig Klinker, Johann Schurz und August Stich, 2., überarbeitete und erweiterte Auflage. Peter Wiehl, Marburg 2009, ISBN 978-3-927219-14-4, S. 202–204.
Leitlinien
- S3-Leitlinie Helicobacter pylori und gastroduodenale Ulkuskrankheit der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten (DGVS). In: AWMF online (Stand 2008); auch in: Zeitschrift für Gastroenterologie. Band 47, 2009, S. 68–102.
Populärwissenschaftlich
- Harro Albrecht: Einspruch vor der Hinrichtung − Ein Bakterium gilt als Auslöser von Magenkrebs. Einige Experten halten es jedoch für nützlich. In: Die Zeit. Nr. 38, Hamburg 2001.
- Hans Schuh: Das Brennen im Bauch. In: Die Zeit. 19. September 2005.
Weblinks
- Helicobacter pylori – Informationen des Robert Koch-Instituts
- „Bakterium liefert Hinweise auf Völkerwanderung“ – science.orf.at
- European Helicobacter pylori Study Group (englisch)
- Magenbakterium schützt vor Asthma
- Text zu Walter Krienitz
Einzelnachweise
- J. Stein, M. Kist: Helicobacter heilmannii (früher: Gastrospirillium hominis) und andere Helicobacterspezies. In: Infektiologie des Gastrointestinaltraktes 2006, S. 185–187.
- W. Krienitz: Ueber das Auftreten von Spirochäten verschiedener Form im Mageninhalt bei Carcinoma ventriculi. In: Dtsch. Med. Wochenschr. Band 32, 1906, S. 872.
- Tilo Richter: Untersuchungen zur Epidemiologie und Klinik der Helicobacter-pylori-Infektion von Leipziger Einschülern und Familienangehörigen (eine populationsbezogene Studie). Dissertation. Medizinische Fakultät der Universität Leipzig, Leipzig 2002.
- Magenbakterium. Menschen tragen seit 60.000 Jahren blinden Passagier im Bauch. In: Der Spiegel. Hamburg 8. Februar 2007.
- S. E. Miederer u. a.: Digestive diseases and sciences. New York 1996, S. 41 und 944.
- Jérôme Viala u. a., in: Nature Immunology 5.2004, 11(Nov.), 1166–1174. ISSN 1529-2908
- Lea Charlotte Holsten: Charakterisierung neuer Adhäsinrezeptoren von Helicobacter pylori und deren Rolle bei der Translokation des Cytotoxins CagA. (PDF) Ludwig-Maximilians-Universität München, 7. Juli 2015, S. V-VI (Abkürzungsverzeichnis), abgerufen am 19. Oktober 2016 (Dissertation am Max von Pettenkofer-Institut für Hygiene und Medizinische Mikrobiologie).
- Verena Königer, Lea Holsten, Ute Harrison, Benjamin Busch, Eva Loell, Qing Zhao, Daniel A. Bonsor, Alexandra Roth, Arnaud Kengmo-Tchoupa, Stella I. Smith, Susanna Mueller, Eric J. Sundberg, Wolfgang Zimmermann, Wolfgang Fischer, Christof R. Hauck, Rainer Haas: Helicobacter pylori exploits human CEACAMs via HopQ for adherence and translocation of CagA. In: Nature Microbiology 2, Artikel-Nummer: 16188. 17. Oktober 2016, abgerufen am 19. Oktober 2016.
- Anahita Javaheri, Tobias Kruse, Kristof Moonens, Raquel Mejías-Luque, Ayla Debraekeleer, Carmen I. Asche, Nicole Tegtmeyer, Behnam Kalali, Nina C. Bach, Stephan A. Sieber, Darryl J. Hill, Verena Königer, Christof R. Hauck, Roman Moskalenko, Rainer Haas, Dirk H. Busch, Esther Klaile, Hortense Slevogt, Alexej Schmidt, Steffen Backert, Han Remaut, Bernhard B. Singer, Markus Gerhard: Helicobacter pylori adhesin HopQ engages in a virulence-enhancing interaction with human CEACAMs. In: Nature Microbiology 2, Artikel-Nummer: 16189. 17. Oktober 2016, abgerufen am 19. Oktober 2016.
- J. Keller et al.: Klinisch relevante Atemtests. In: Z Gastroenterol. Band 42, 2005, S. 1071–1090. DOI10.1055/s-2005-858479
- J. P. Gisbert, J. M. Pajares: Stool antigen tests for the diagnosis of Helicobacter pylori infection. A systemic review. In: Helicobacter. 2004; 9, 347–368.
- Stuhlantigen-Tests zur H.-pylori-Diagnostik? In: Deutsches Ärzteblatt. 102, Ausgabe 39 vom 30. September 2005, Seite A-2649 / B-2239 / C-2115
- Marianne Abele-Horn (2009), S. 202.
- European Helicobacter pylori Study Group (EHPSG)
- Marianne Abele-Horn (2009), S. 203.
- C. A. Fallone, N. Chiba, S. V. van Zanten, L. Fischbach, J. P. Gisbert, R. H. Hunt, N. L. Jones, C. Render, G. I. Leontiadis, P. Moayyedi, J. K. Marshall: The Toronto Consensus for the Treatment of Helicobacter pylori Infection in Adults. In: Gastroenterology. Band 151, Nummer 1, Juli 2016, S. 51–69.e14, doi:10.1053/j.gastro.2016.04.006, PMID 27102658.
- Leitlinie Helicobacter pylori und gastroduodenale Ulkuskrankheit der Deutsche Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten e.V. (DGVS). In: AWMF online (Stand 5. Februar 2016)
- Impfstoff gegen Bakterium Helicobacter pylori
- Magenkrebs – Impfen gegen Helicobacter pylori, Pharmazeutische Zeitung Online, 10/2010
- F. .. Hongying, W. .. Xianbo, Y. .. Fang, B. .. Yang, L. .. Beiguo: Oral immunization with recombinant Lactobacillus acidophilus expressing the adhesin hp0410 of Helicobacter pylori induces mucosal and systemic immune responses. In: Clinical and Vaccine Immunology., S. , doi:10.1128/CVI.00434-13.
- J.-F. Tomb u. a.: The complete genome sequence of the gastric pathogen Helicobacter pylori. in: Nature. London 388.1997, 539–547. ISSN 0028-0836
- R.A. Alm u. a., in: Genomic-sequence comparison of two unrelated isolates of the human gastric pathogen Helicobacter pylori. in: Nature. London 397.1999, 176–180. ISSN 0028-0836