Butyllithium
Unter Butyllithium versteht man in der Regel n-Butyllithium (n-BuLi), eine metallorganische Verbindung des Elements Lithium (Organolithium-Verbindung). Daneben gibt es noch die isomeren Formen sec-Butyllithium und tert-Butyllithium. Butyllithium dient als Reagenz bei der Herstellung eines naturähnlichen Kautschuks (cis 1,4 Anteil) aus Isopren. Für diesen Einsatzzweck wurden bereits 1985 etwa 600 Tonnen Butyllithium benötigt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemeines | |||||||||||||||||||
| Name | Butyllithium | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C4H9Li | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit, kommerziell erhältliches n-Butyllithium ist oft gelblich[1][2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 64,05 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Schmelzpunkt |
−34 °C (Hexamer)[3] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Die Synthese erfolgt analog zur Herstellung von Grignard-Verbindungen durch Reaktion von 1-Chlorbutan[6] mit elementarem Lithium in Diethylether:
Eigenschaften
Physikalische Eigenschaften
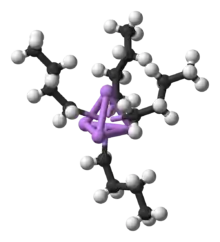
n-Butyllithium ist eine sehr starke Base. Die Basizität der isomeren Butyllithiumverbindungen nimmt in der Reihe n-Butyllithium < sec-Butyllithium < tert-Butyllithium zu. Durch die große Elektronegativitätsdifferenz zwischen Kohlenstoff (2,55) und Lithium (0,98) ist die Bindung zwischen C und Li stark polarisiert. Aufgrund der Reaktionen von n-BuLi könnte man davon ausgehen, dass sich n-BuLi aus dem Butylanion und dem Lithiumkation zusammensetzt, also eine Ionenbindung besitzt. Diese Annahme ist jedoch falsch, denn n-BuLi ist nicht ionisch. Als Feststoff und sogar als Lösung existiert n-BuLi, wie die meisten Organolithiumverbindungen, als Molekülgruppen mit kovalenten Bindungen zwischen Lithium und Kohlenstoff. Für den Reinstoff wurde massenspektrometrisch eine Hexamerstruktur nachgewiesen.[7] In unpolaren Lösungsmitteln wie Cyclohexan ist n-BuLi hexamerisch, in Ether ist es tetramerisch angeordnet.
Chemische Eigenschaften
Reines n-Butyllithium ist eine pyrophore farblose Flüssigkeit, entzündet sich also in Gegenwart von Sauerstoff selbst. Es ist daher im Handel als (meist leicht gelbe) Lösung erhältlich, die zudem unter Inertgas aufbewahrt werden muss,[2] wobei Konzentrationen von 1,6 bis 11 mol/l in n-Hexan üblich sind.
Als Lösungsmittel verwendete Ether wie THF oder Diethylether sind als Lagerlösungsmittel für n-BuLi ungeeignet, da sie langsam zersetzt würden. Die Halbwertszeit von n-BuLi in THF bei 0 °C mit Deaggregierungsadditiv TMEDA (Tetramethylethylendiamin) beträgt nur 38 Minuten.[8] n-Butyllithium reagiert zudem exotherm mit Kohlendioxid und Sauerstoff, sowie mit Wasser.[9] Die Hydrolysewärme beträgt −240 kJ·mol−1[10] Die thermische Zersetzung von n-Butyllithium führt zum Lithiumhydrid und 1-Buten.[9]
Reaktionen
Lithium-Halogen-Austausch: Das Halogen in einer Verbindung kann gegen Lithium ausgetauscht werden. Dieses ergibt Reagenzien mit nukleophilen Kohlenstoffzentren, welche für die Herstellung von zahlreichen Verbindungen verwendet werden können. Den Austausch nimmt man in der Regel in Ether bei −78 °C vor (Ar steht für einen aromatischen Rest):
Als starke Base (die konjugierte Säure ist Butan!) kann n-BuLi Amine und C-H-acide Verbindungen deprotonieren:
n-BuLi kann für die Herstellung von bestimmten Aldehyden und Ketonen aus disubstituierten Amiden verwendet werden:
Beim Erhitzen von n-BuLi findet eine β-Eliminierung statt. Hierdurch entstehen primär Buten und Lithiumhydrid. Butyllithium reagiert wiederum mit entstandenen Buten, wobei über Butadien auch polymere Produkte entstehen können. Der Zerfall verläuft nach einem Zeitgesetz erster Ordnung. Die Halbwertszeiten betragen bei 130 °C 315 min, bei 140 °C 115,5 min und bei 150 °C 49,5 min.[11]
Lagert man n-BuLi oder t-BuLi längere Zeit als etherische Lösung, z. B. in Tetrahydrofuran, so findet ein Zerfall des Lösungsmittels statt:[12]
Verwendung
n-BuLi hat in der modernen synthetischen organischen Chemie große Bedeutung als sehr starke Base bzw. als Lithiierungsreagenz erlangt. So wird z. B. die häufig verwendete Base Lithiumdiisopropylamid (LDA) in der Regel in situ durch Deprotonieren von Diisopropylamin mit n-BuLi in THF hergestellt.
Gehaltsbestimmung
Da Butyllithium nur begrenzt stabil ist und auch empfindlich gegen Wasser und Sauerstoff ist, muss der Gehalt einer Lösung vor dem Einsatz bestimmt werden. Zur Gehaltsbestimmung wird ein Aliquot der Lösung mit Wasser versetzt und gegen eine verdünnte Lösung Salzsäure titriert. Dabei wird der Gesamtbasen-Gehalt bestimmt. Um jedoch Lithiumhydrid, Lithiumhydroxyd und Alkoholate von der Gesamtbase abziehen zu können wird ein Aliquot der Lösung in THF mit einem großen Überschuss an Benzylchlorid umgesetzt. Dabei reagiert Benzylchlorid in einer Wurtz-Fittig-Reaktion zum 1,2-Diphenylethan und es entsteht Lithiumchlorid. Nach Hydrolyse wird die Restbase ebenfalls gegen eine Salzsäure titriert. Die Differenz beider Werte liefert jetzt den Anteil an Butyllithium.[13]
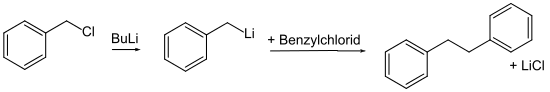
Sicherheitshinweise
Wie bereits erwähnt, ist reines n-BuLi äußerst pyrophor. Aber auch die Lösungen, insbesondere wenn sie höher konzentriert sind, können sich spontan entzünden. Sie reagieren zudem heftig mit Wasser zu Lithiumhydroxid und Butan. Durch längeres Stehen kann sich daher in den Lösungen ein Niederschlag bilden, der durch Eindringen von Feuchtigkeit entsteht. Es kann sich aber auch um Lithiumhydrid handeln, da n-BuLi sehr langsam in Buten und Lithiumhydrid zerfällt.
Literatur
- Autorenkollektiv: Organikum. 21. Auflage. Wiley-VCH, Weinheim 2001, ISBN 3-527-29985-8.
- Christoph Elschenbroich: Organometallchemie. 5. Auflage. Teubner, Wiesbaden 2005, ISBN 3-519-53501-7.
Einzelnachweise
- Eintrag zu Butyllithium in der GESTIS-Stoffdatenbank des IFA, abgerufen am 31. Oktober 2021. (JavaScript erforderlich)
- Ullmann’s Encyclopedia of Industrial Chemistry. 6. Auflage. 2002.
- T. Kottke, D. Stalke: Strukturen der klassischen Synthesereagentien (nBuLi)6 und (tBuLi)4 sowie vom metastabilen (tBuLi·Et2O)2. In: Angew. Chem. 105, 1993, S. 619–621, doi:10.1002/ange.19931050433.
- Eintrag zu Butyllithium. In: Römpp Online. Georg Thieme Verlag, abgerufen am 5. Mai 2014.
- Teile der Gefahrstoffkennzeichnung beziehen sich auf die Gefahren, die durch das Lösungsmittel verursacht werden.
- K. Ziegler, H. Colonius: Untersuchungen über alkali-organische Verbindungen. V. Eine bequeme Synthese einfacher Lithiumalkyle. In: Justus Liebigs Ann. Chem. 479, 1930, S. 135–149, doi:10.1002/jlac.19304790111.
- D. Plavsic, D. Srzic, L. Klasinc: Mass spectrometric investigations of alkyllithium compounds in the gas phase. In: J. Phys. Chem. 90, 1986, S. 2075–2080, doi:10.1021/j100401a020.
- P. Stanetty, H. Koller, M. Mihovilovic: Directed ortho lithiation of phenylcarbamic acid 1,1-dimethylethyl ester (N-BOC-aniline). Revision and improvements. In: J. Org. Chem. 57, 1992, S. 6833–6837, doi:10.1021/jo00051a030.
- T. L. Rathman, J. A. Schwindeman: Preparation, Properties, and Safe Handling of Commercial Organolithiums: Alkyllithiums, Lithium sec-Organoamides, and Lithium Alkoxides. In: Org. Process Res. Dev. 18, 2014, S. 1192–1210, doi:10.1021/op500161b.
- P. A. Fowell, C. T. Mortimer: Heats of Formation and Bond Energies. Part V. n-Butyllithium. In: J. Chem. Soc. 1961, S. 3793–3796, doi:10.1039/JR9610003793.
- R. A. Finnegan, H. W. Kutta: Organometallic Chemistry. X1I. The Thermal Decomposition of n-Butyllithium, a Kinetic Study. In: J. Org. Chem. 30, 1965, S. 4138–4144, doi:10.1021/jo01023a038.
- J. Clayden, S. A. Yasin: Pathways for decomposition of THF by organolithiums: the role of HMPA. In: New J. Chem. 26, 2002, S. 191–192, doi:10.1039/b109604d.
- Chemetall, Hausmitteilung Sparte Lithium 1995, 1-8.




