Wurtz-Fittig-Synthese
Bei der Wurtz-Fittig-Synthese handelt es sich um eine Namensreaktion in der Organischen Chemie. Sie stellt eine von Rudolph Fittig (1835–1910) erweiterte Form der Wurtzschen Synthese dar und dient der Synthese von alkylierten Aromaten.[1][2] Da jedoch die Ausbeuten bedingt durch Nebenreaktionen meist gering sind, besitzt die Wurtz-Fittig-Reaktion keine besondere synthetische Bedeutung.
Übersichtsreaktion
Bei der Reaktion wird ein Halogenalkan und ein Halogenaromat mit einem Alkalimetall in einem inerten Lösungsmittel zu einem alkylierten Aromaten umgesetzt.[1][2]
Mechanismus
Die Reaktion weist starke Analogien zur Wurtzschen Synthese auf. Anstatt Chlorid oder Bromid können auch andere Halogenide gebunden sein.

In einem ersten Schritt wird das im Vergleich zum Arylhalogenid reaktivere Alkylhalogenid vom Natrium zum Carbanion reduziert. Dieses kann in einer nucleophilen Substitutionsreaktion mit dem Arylhalogenid zum entsprechenden alkylierten Aromaten reagieren.[3]
Nebenreaktionen
Triebkraft des Prozesses ist die Bildung des aus der Lösung ausfallenden Natriumhalogenids, da dieses eine hohe Gitterenthalpie aufweist. Die Nebenreaktionen sind vielfältig und senken die Ausbeuten beträchtlich. Folgende Reaktionen sind zum Beispiel möglich:
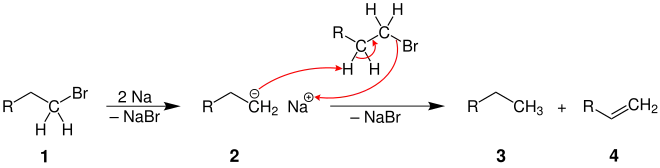
- Voraussetzung dafür ist das Vorhandensein von β-Wasserstoff in der Alkylkette des Halogenalkans 1. Das Carbanion 2 hat eine ausgeprägt starke Basizität und nimmt ein Proton eines weiteren Alkylhalogenids auf. So entstehen Alkane 3 und Alkene 4.

- Kopplung des Carbanions 1 mit einem weiteren Halogenalkan 2. Dabei entstehen weitere Alkane 3.

- Reaktion des Natriums mit dem Arylhalogenid 1. Das entstandene Carbanion 2 reagiert mit einem weiteren Halogenaromaten. Hier minimieren Biphenyle 3 die Ausbeute der Wurtz-Fittig-Synthese. Diese Nebenreaktion findet jedoch meistens nicht statt, da die Kupplung von Halogenaromaten untereinander aufgrund ihrer geringeren Reaktivität im Allgemeinen nicht gelingt.[4]
Einzelnachweise
- Bernhard Tollens, Rudolph Fittig: Ueber die Synthese der Kohlenwasserstoffe der Benzolreihe (p 303). In: Annalen der Chemie und Pharmacie. Band 131, Nr. 3, 1864, S. 303–323, doi:10.1002/jlac.18641310307.
- Rudolph Fittig, Joseph König: Ueber das Aethyl- und Diäthylbenzol (p ). In: Annalen der Chemie und Pharmacie. Band 144, Nr. 3, 1867, S. 277–294, doi:10.1002/jlac.18671440308.
- László Kürti, Barbara Czakó: Strategic Applications of Named Reactions in Organic Synthesis. Elsevier Science & Technology Books, 2005, ISBN 0-12-369483-3, S. 498.
- T. Laue, A. Plagens: Namens- und Schlagwortreaktionen der Organischen Chemie. Teubner Verlag, 2006, ISBN 3-8351-0091-2, S. 360.