Zimtsäure
Zimtsäure (trans-3-Phenylacrylsäure, FEMA 2288[1]) ist ein weißer Feststoff mit charakteristischem Geruch. Zimtsäure kommt in manchen Pflanzen natürlich vor und ist ungiftig. Neben Zimtaldehyd und Eugenol ist sie ein wichtiger Bestandteil des Zimtes. Zimtsäure gehört zu den Aromaten und ist eine ungesättigte Carbonsäure mit einer trans-substituierten Kohlenstoff-Kohlenstoff-Doppelbindung in der Seitenkette. Die isomere cis-Zimtsäure (Allozimtsäure)[6] hat nur eine geringe Bedeutung. Die Angaben in diesem Artikel beziehen sich nur auf die trans-Zimtsäure.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
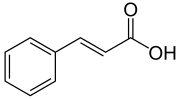 | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Zimtsäure | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C9H8O2 | ||||||||||||||||||
| Kurzbeschreibung |
weiße Kristalle mit charakteristischem Geruch[3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 148,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,25 g·cm−3[3] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
Zersetzung (Decarboxylierung zu Styrol)[3] | ||||||||||||||||||
| pKS-Wert |
4,44[4] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Darstellung
Zimtsäure kann aus Benzaldehyd hergestellt werden, beispielsweise über die Aldoladdition mit Malonsäure[7] (Doebner-Variante).
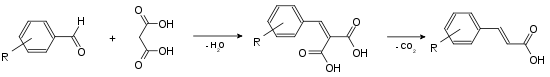
Ein speziell für die Zimtsäure entwickelter Reaktionsweg ist die Perkin-Reaktion:
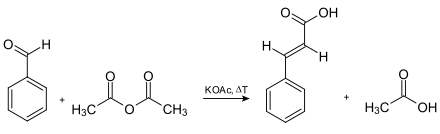
Ein anderer Syntheseweg verläuft über eine Aldolkondensation von Benzaldehyd und Acetaldehyd.
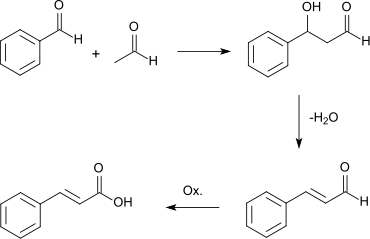
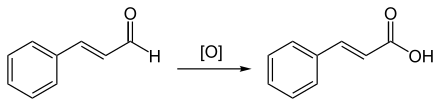
Zimtsäure entsteht auch durch die schon an der Luft stattfindende Oxidation von Zimtaldehyd.
Eigenschaften
Physikalische Eigenschaften
Zimtsäure kristallisiert im monoklinen Kristallsystem in der Raumgruppe P21/n (Raumgruppen-Nr. 14, Stellung 2) und den Gitterparametern a = 779 pm, b = 1807 pm, c = 567 pm und β = 97°. In der Elementarzelle befinden sich vier Formeleinheiten.[8] Es sind mit der β- und γ–Modifikation zwei weitere metastabile Formen bekannt.[9][10] Die Kristallstruktur dieser β-Modifikation ist isomorph zu 4-Chlorzimtsäure.[11]
Chemische Eigenschaften
Bei einer Destillation bei 146 °C und ca. 4 hPa findet eine Zersetzung durch Decarboxylierung zu Styrol statt.[3]
Biosynthese
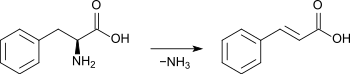
Zimtsäure entsteht aus der Aminosäure L-Phenylalanin im Zuge einer Desaminierung durch die Phenylalanin-Ammoniak-Lyase (EC 4.3.1.24), die in einer analogen Reaktion auch die Aminosäure L-Tyrosin zur para-Cumarsäure (4-Hydroxyzimtsäure) desaminiert. Sie ist ein Zwischenprodukt der Biosynthese von Chalkonen (und damit Vorstufe der Flavonoidbiosynthese) und Stilbenen.
Verwendung und Reaktivität
Zimtsäure kann zur Darstellung von Phenylacetylen verwendet werden. Einige ihrer Ester sind als Riechstoffe in Anwendung. Bei der UV-Bestrahlung von trans-Zimtsäure erfolgt eine Isomerisierung unter Bildung von cis-Zimtsäure (Allozimtsäure):[12]

Photochemisch dimerisiert Zimtsäure unter Bildung eines Cyclobutanrings. In Abhängigkeit von der Kristallform entstehen hierbei zwei verschiedene Isomere. Aus dem α–Polymorph entsteht die α–Truxillsäure. Das β–Polymorph bildet die β–Truxinsäure. Das γ–Polymorph kann photochemisch nicht dimerisiert werden.[13][14][15]
Derivate
Am Phenylring durch eine Hydroxygruppe substituierte Derivate gehören zur Gruppe der Phenolsäuren. Die Sinapinsäure (3,5-Dimethoxy-4-hydroxy-zimtsäure) und auch α-Cyano-4-hydroxy-zimtsäure (HCCA) kommen als organische Matrix bei der MALDI-MS (Matrix assisted laser desorption ionization mass spectrometry) zum Einsatz. Dazu gehören zum Beispiel auch die Ferulasäure und die Kaffeesäure.
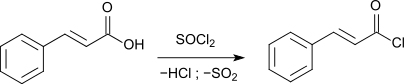
Durch die Reaktion mit Thionylchlorid (SOCl2) wird Zimtsäure in das reaktionsfreudige Zimtsäurechlorid umgewandelt.
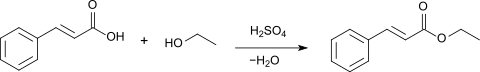
Durch Veresterung mit Ethanol in Gegenwart von Schwefelsäure[16] oder Salzsäure[17] als Katalysator kann der Aromastoff Zimtsäureethylester gewonnen werden.
Toxikologie
Für Ratten liegt der orale LD50 bei 2,5 g/kg und der dermale LD50 bei 5 g/kg. Zimtsäure führt auf Hasenhaut zu Irritationen. Eine 4%ige Lösung in Vaseline führt bei Menschen zu keiner Hautreaktion.[18]
Weblinks
Siehe auch
Einzelnachweise
- Eintrag zu FEMA 2288 in der Datenbank der Flavor and Extract Manufacturers Association of the United States.
- Eintrag zu CINNAMIC ACID in der CosIng-Datenbank der EU-Kommission, abgerufen am 25. Februar 2020.
- Eintrag zu Zimtsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 6. August 2013. (JavaScript erforderlich)
- CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- Eintrag zu Zimtsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 17. Juli 2014..
- Externe Identifikatoren von bzw. Datenbank-Links zu cis-Zimtsäure: CAS-Nummer: 102-94-3, EG-Nummer: 827-073-9, ECHA-InfoCard: 100.262.470, PubChem: 5372954, ChemSpider: 10286933, Wikidata: Q4062664.
- R. Brückner: Reaktionsmechanismen: Organische Reaktionen, Stereochemie, Moderne Synthesemethoden. 3. Auflage. Spektrum, 2004, ISBN 3-8274-1579-9, S. 569–570.
- J. Ladell, T. R. R. McDonald, G. M. J. Schmidt: The crystal structure of α-trans-cinnamic acid, in: Acta Cryst., 1956, 9, S. 195 (doi:10.1107/S0365110X56000474).
- J. H. Urbanus, S. Jiang: Polymorphism of trans-cinnamic acid, MSc graduation assignment (Volltext (PDF; 153 kB)).
- G. M. J. Schmidt: 385. Topochemistry. Part III. The crystal chemistry of some trans-cinnamic acids, in: J. Chem. Soc., 1964, S. 2014–2021 (doi:10.1039/JR9640002014).
- I. Abdelmoty, V. Buchholz, L. Di, C. Guo, K. Kowitz, V. Enkelmann, G. Wegner, B. M. Foxman: Polymorphism of Cinnamic and α-Truxillic Acids: New Additions to an Old Story, in: Crystal Growth & Design, 2005, 5 (6), S. 2210–2217 (doi:10.1021/cg050160s).
- Siegfried Hauptmann: Organische Chemie, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1985, ISBN 3-342-00280-8, S. 407.
- D. Wöhrle, M.W. Tausch, W.-D. Stohrer: Photochemie: Konzepte, Methoden, Experimente, Wiley-VCH Verlag, Weinheim 1998, ISBN 3-527-29545-3, S. 96.
- M. D. Cohen: Photochemie organischer Festkörper, in: Angew. Chem., 1975, 87, S. 439–447 (doi:10.1002/ange.19750871204).
- V. Ramamurthy, K. Venkatesan: Photochemical reactions of organic crystals, in: Chem. Rev., 1987, 87, S. 433–481 (doi:10.1021/cr00078a009).
- C. S. Marvel, W. B. King: Ethyl Cinnamate In: Organic Syntheses. 9, 1929, S. 38, doi:10.15227/orgsyn.009.0038; Coll. Vol. 1, 1941, S. 252 (PDF).
- E. Fischer, A. Speier: Darstellung der Ester, in: Berichte der deutschen chemischen Gesellschaft, 1895, 28, S. 3252–3258 (Digitalisat auf Gallica).
- Wiley-VCH, Wiley-VCH: Ullmann's Encyclopedia of Industrial Chemistry, 2005, Kapitel: Cinnamic Acid
