Desaminierung
Als Desaminierung oder Deaminierung bezeichnet man die chemische Abspaltung einer Aminogruppe als Ammonium-Ion oder Ammoniak. Desaminierungen finden sowohl in der Biochemie als auch in chemisch-technischen Prozessen statt.[1] Man unterscheidet oxidative, hydrolytische und eliminierende Desaminierung.
Die Desaminierung ist der erste Schritt des biochemischen Abbaus von Aminosäuren. Bei Säugetieren läuft dieser Prozess hauptsächlich in der Leber ab. Das gebildete Ammoniumion wird anschließend zu Harnstoff umgesetzt, um die zelltoxische Wirkung der konjugierten Base Ammoniak zu verhindern.
Oxidative (dehydrierende) Desaminierung
Im ersten Schritt der oxidativen Desaminierung wird die Aminogruppe der Aminosäure L-Glutamat 1 durch Abspaltung von Wasserstoff zur Imino-Gruppe oxidiert, wobei der Wasserstoff auf NAD+ oder NADP+ übertragen wird. Hierauf folgt die hydrolytische Abspaltung der Amino-Gruppe als Ammoniumion und die Bildung einer α-Ketosäure, des α-Ketoglutarats 2:
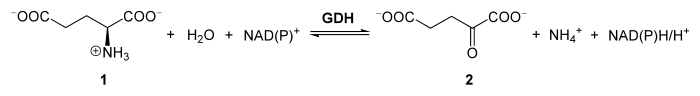
Auch FMN und FAD katalysieren Redoxreaktionen, unter anderem oxidative Desaminierungen. Sie sind im Gegensatz zum löslichen NAD+ oder NADP+ als prosthethische Gruppe an ihr Enzym gebunden und müssen auch dort wieder regeneriert werden.
Hydrolytische Desaminierung
Hierbei wird Ammoniak (NH3) aus der Säureamid-Gruppe einer Aminosäure hydrolytisch abgespalten. Die Amid-Gruppe wird durch Wassereinlagerung abgespalten und durch eine OH-Gruppe ersetzt. Dementsprechend entstehen aus Säureamiden Carbonsäuren (COOH-Gruppe).
Weitere Verwertung des freigesetzten Ammoniaks
Das bei der Desaminierung von Aminosäuren frei gewordene Ammoniak stellt ein Zellgift dar und muss dementsprechend gebunden oder ausgeschieden werden. Er kann einerseits an alpha-Ketosäuren gebunden werden, die damit zu Aminosäuren werden oder er wird über den Urin ausgeschieden. Letzteres erfolgt im menschlichen Körper hauptsächlich durch die Synthese von Harnstoff im Harnstoffzyklus, der in der Leber abläuft. Anschließend wird der Harnstoff an das Blut abgegeben und über die Niere im Urin ausgeschieden. Weiterhin verfügt die Niere über einen Mechanismus, der zur direkten Ausscheidung von Ammoniak über den Urin führt. Der gleichzeitige Transport von Ammoniak (NH3) und Protonen (H+) in den Nierentubuli führt dazu, dass sich diese zu einem Ammonium-Ion (NH4+) verbinden. Ammonium kann die Membran der Nierenzellen nicht mehr durchqueren und wird mit dem Urin ausgeschieden. (Dieser dient jedoch primär der Regelung des Säure-Base-Haushaltes, denn so werden Protonen aus dem Körper entfernt, was bei der Kompensation von Azidosen wichtig ist.)
Siehe auch
Literatur
- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6 Auflage. Spektrum Akademischer Verlag, Heidelberg 2007, ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage. John Wiley & Sons, New York 2004, ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell. 5. Auflage. Taylor & Francis 2007, ISBN 978-0-8153-4106-2.
Einzelnachweise
- Brockhaus ABC Chemie. VEB F. A. Brockhaus Verlag Leipzig 1965, S. 276.