Pharmakodynamik
Die Pharmakodynamik ist die Lehre über die Wirkung von Arzneistoffen im Organismus und ein Teilgebiet der Pharmakologie. Sie behandelt verschiedene Aspekte wie das Wirkprofil, die Dosis-Wirkungsbeziehung, den Wirkmechanismus sowie Wechselwirkungen eines Arzneistoffes mit anderen Molekülen.
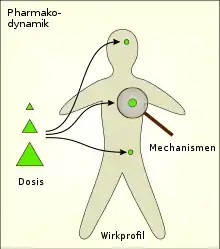
Während die Pharmakodynamik die Wirkung auf den Körper beschreibt, behandelt die Pharmakokinetik die Verteilung und Verstoffwechselung im Körper.[1]
Wirkprofil
Das Wirkprofil wird bestimmt durch die Art und den Ort der Wirkung eines Arzneimittels (Welche Effekte treten auf? Welche Organe/Strukturen oder biologische Funktionen werden beeinflusst?).
Die meisten Wirkstoffe wirken spezifisch. Ihre Wirkung ist weitgehend von der molekularen Struktur abhängig, d. h. an bestimmte chemische, funktionelle Strukturen gebunden. Daher können analoge Verbindungen aufgrund ihrer teilweise ähnlichen Struktur ähnliche Wirkungen haben. Wirkstoffe wirken meistens in niedrigen Dosen bzw. Konzentrationen und an einem genau definierbaren Angriffsort. Das Vorhandensein mehrerer Wirkungen bei einem Wirkstoff wird als Pleiotropie bezeichnet. Wenige Wirkstoffe wirken unspezifisch. Trotz unterschiedlicher chemischer Strukturen haben sie ähnliche Wirkungen. Sie sind eher in hohen Dosen bzw. Konzentrationen wirksam. Im Zuge eines Wirkstoffdesigns werden die Eigenschaften eines Wirkstoffs gezielt angepasst.
Dosis-Wirkungs-Beziehung
Vor dem Hintergrund der Wirksamkeit und Sicherheit eines Arzneimittels ist die Dosis-Wirkungs-Beziehung von zentraler Bedeutung (Welche Dosen sind wirkungslos? Ab welchen Dosen treten Effekte auf? Wie stark sind die Effekte in Abhängigkeit von der Dosis? Welche Dosen sind toxisch?).
So verursacht beispielsweise eine doppelte Dosis nicht zwingend einen doppelt so großen Effekt. Man spricht dann von einer nicht-linearen Dosis-Wirkungs-Beziehung.
Manche Arzneimittel haben eine geringe therapeutische Breite. Das bedeutet, dass die effektive Dosis nahe der toxischen Dosis liegt. Die Effekte solcher Arzneimittel müssen somit sorgfältig überwacht werden. Die Sinnhaftigkeit solcher Verordnungen muss generell kritisch hinterfragt werden.
Wirkmechanismus
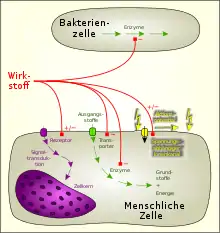
Der Wirkmechanismus erklärt das Zustandekommen der Wirkung auf biochemischer bzw. biophysikalischer Ebene. Besonders aufschlussreich für das Verständnis des Wirkmechanismus ist die Struktur-Wirkungs-Beziehung. Neben der chemischen Formel kann auch die räumliche Anordnung der Atome im Molekül den Wirkmechanismus ausmachen. Man kennt Substanzen, die in Abhängigkeit von ihrer isomeren Form unterschiedlich wirksam sind.
Fast alle Arzneimittelwirkungen beruhen auf einigen wenigen Wirkmechanismen, die sich wie folgt einteilen lassen:
- Wechselwirkung mit Rezeptoren (Stimulation, Blockade)
- Beeinflussung der Enzymaktivität (Aktivierung, Hemmung)
- Beeinflussung spannungsabhängiger Ionenkanäle (Öffnung, Blockade)
- Beeinflussung von Transportsystemen
- Hemmung von Biosynthesen in Mikroorganismen
Wechselwirkung mit Rezeptoren
Rezeptoren sind Zellstrukturen, die durch die Bindung mit einem Liganden (z. B. ein Neurotransmitter) gemäß dem Schlüssel-Schloss-Prinzip eine Signaltransduktion auslösen, welche wiederum einen bestimmten Effekt hervorruft. Man unterscheidet intrazelluläre (also im Cytoplasma oder Zellkern lokalisierte) und membranständige Rezeptoren. Durch die Reizung oder Blockade eines solchen Rezeptors mit einer dem natürlichen Liganden ähnlichen Substanz bzw. Struktur kann ein Effekt erzeugt oder unterdrückt werden.
Beispiele: Blockade von Adrenozeptoren durch Sympatholytika (Alphablocker, Betablocker), Stimulation von Adrenozeptoren durch Sympathomimetika, Blockade von Histamin-Rezeptoren durch Antihistaminika Wirkstoffe können durch ihre Wirkung am Rezeptor als Agonist, Partieller Agonist, Antagonist eingeteilt werden. Bei mehreren Liganden gibt es aufgrund von Wechselwirkungen oftmals Änderungen im Ausmaß einer Wirkung, z. B. in Form einer Synergie, einer Loewe-Additivität, einer Bliss independence oder eines Antagonismus.[2]
Beeinflussung der Enzymaktivität
Ein ebenfalls häufig anzutreffender Wirkmechanismus ist die Aktivierung oder Hemmung einer Enzymaktivität. Enzyme sind neben der Katalyse zahlreicher biochemischer Reaktionen im Organismus auch für die Regulation verantwortlich, z. B. Proteinkinasen.
Beispiele: Erniedrigung der Konzentration von Angiotensin II durch ACE-Hemmer (mit dem Ziel der Gefäßerweiterung und damit diuretischen Auswirkung); Hemmung der bakteriellen Gyrase durch Gyrase-Hemmer wie die Fluorchinolone (Antibiose).
Beeinflussung spannungsabhängiger Ionenkanäle
Ionenkanäle ermöglichen den Transport von Ionen wie z. B. Natrium, Kalium, Calcium und Chlorid durch die Zellmembranen. Sie können durch verschiedene Mechanismen aktiviert werden. Neben der Rezeptoreninteraktion (siehe oben: Wechselwirkung mit Rezeptoren) ist die Beeinflussung mittels einer Veränderung des Membranpotentials möglich.
Beispiele: Verringerung der intrazellulären Calciumkonzentrationen durch Blockieren der Resorptionscarrier oder -kanäle durch Calciumkanalblocker (Senkung der Herzlast durch verminderten Sauerstoffbedarf und geringeren Blutdruck); Erniedrigung der Natriumionenkonzentration in Axonen durch Lokalanästhetika (Störung der Reizweiterleitung bzw. Ausfall davon abhängiger Schmerzempfindungen, siehe dazu Lokalanästhetikum#Wirkungsmechanismus).
Beeinflussung von Transportsystemen
Arzneistoffe können ihre Wirkung auch durch Beeinflussung von Ionenpumpen oder Carrier-Systemen entfalten.
Beispiel: Hemmung der Protonen-Kalium-Pumpe durch Protonenpumpenhemmer (Unterdrückung der Salzsäureproduktion im Magen)
Hemmung von Biosynthesen in Mikroorganismen
Eine Vielzahl von antiinfektiven Therapien beruht auf der Störung von Biosynthesen der Erreger.
Beispiele: Hemmung der bakteriellen Zellwandsynthese durch β-Lactam-Antibiotika, Störung der bakteriellen Folsäure-Synthese durch Sulfonamide, Hemmung der bakteriellen Proteinsynthese durch Makrolide, Hemmung der mykotischen Ergosterolsynthese durch Azol-Antimykotika
Literatur
- E. Mutschler, G. Geisslinger, H.K. Kroemer, P. Ruth, M. Schäfer-Korting: Mutschler – Arzneimittelwirkungen, Lehrbuch der Pharmakologie und Toxikologie; Basiswissen Pharmakologie / Toxikologie. Mit einführenden Kapiteln in die Anatomie, Physiologie und Pathophysiologie, WVG Stuttgart 2005, ISBN 3-8047-2251-2.
- Philipp F. W. Vogt: Lehrbuch der Pharmakodynamik, Gießen 1821 (Erstes Einzelwerk über Pharmakodynamik).
Einzelnachweise
- Aktories, Klaus; Förstermann, Ulrich; Hofmann, Franz; Starke, Klaus (Hrsg.): Allgemeine und spezielle Pharmakologie und Toxikologie. (Begründet von W. Forth, D.Hentschler und W. Rummel). 10. Auflage. Urban & Fischer, München/Jena 2009, ISBN 978-3-437-42522-6, S. 2, 5, 7f.
- P. J. Yeh, M. J. Hegreness, A. P. Aiden, R. Kishony: Drug interactions and the evolution of antibiotic resistance. In: Nat Rev Microbiol. (2009), Band 7, Nr. 6, S. 460–466. doi:10.1038/nrmicro2133. PMID 19444248; PMC 2855488 (freier Volltext).