Cortison
Cortison (von lateinisch cortex ‚Rinde‘, Schreibweise auch Kortison) ist ein Steroidhormon, das um 1935 in der Nebennierenrinde des Menschen gefunden wurde und auch synthetisch hergestellt werden kann. Cortison ist die durch Oxidation inaktivierte Form des Glucocorticoids Cortisol, das im Kohlenhydrathaushalt, dem Fettstoffwechsel und dem Proteinumsatz Bedeutung besitzt. Zu Therapiezwecken wurde der Essigsäureester Cortisonacetat eingesetzt.[2] Umgangssprachlich werden Glucocorticoide,[4] Medikamente mit Cortisolwirkung – vor allem Prednisolon und Dexamethason – häufig als „Cortison“ bezeichnet. Wenn von den Nebenwirkungen von Cortison die Rede ist, geht es um die Nebenwirkungen der Glucocorticoide.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
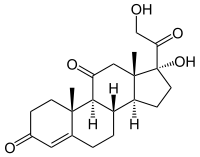 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Cortison | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
H02AB10 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
Zersetzung ab 240 °C[2] | |||||||||||||||||||||
| Löslichkeit |
sehr schwer in Wasser (Cortison, 280 mg·l−1 bei 25 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Entdeckungsgeschichte
1929/30 wurde entdeckt, dass Tiere, denen man die Nebenniere entfernt hatte, am Leben blieben, wenn ihnen Extrakte aus der Nebennierenrinde verabreicht werden.[5] Cortison wurde in den Jahren 1935–1940 von verschiedenen Arbeitsgruppen aus tierischen Nebennierenrinden isoliert und unterschiedlich bezeichnet: als „compound F“ von Oskar Wintersteiner, als „Substanz Fa“ durch Tadeus Reichstein und als „compound E“ von der Arbeitsgruppe um Edward Calvin Kendall. Die hydrierte Form Cortisol oder Hydrocortison wurde 1937/38 von Reichstein hergestellt. Später stellte sich heraus, dass Cortison ein Oxidationsprodukt des eigentlichen Hormons Cortisol ist. Die Partialsynthese von Cortison aus Desoxycholsäure gelang zuerst während des Zweiten Weltkriegs Lewis Hastings Sarett bei Merck.[6] Der Mediziner Philip Hench injizierte im Jahr 1948 erstmals einer Patientin mit schwerem Rheuma Cortison, die daraufhin schmerzfrei war.[5] Zwei Jahre später erhielten Kendall, Reichstein und Hench gemeinsam „für ihre Entdeckungen bei den Hormonen der Nebennierenrinde, ihrer Struktur und ihrer biologischen Wirkungen“ den Nobelpreis für Medizin. Im Jahr 1951 fand Robert Woodward erstmals einen Weg für die Totalsynthese von Cortison.
Physiologische Wirkung
Cortison selbst besitzt keinerlei Wirkung auf den Organismus, da es weder an den Glucocorticoid-Rezeptor noch an den Mineralocorticoid-Rezeptor bindet. Deshalb ist eine topische Anwendung, zum Beispiel auf der Haut, nicht sinnvoll. In der Lokaltherapie kommen statt Cortison Corticosteroide zum Einsatz, die nicht metabolisiert werden müssen, um biologisch aktiv zu sein.[7] Bei peroraler oder intravenöser Aufnahme wird Cortison durch das Enzym 11β-Hydroxysteroid-Dehydrogenase 1 in der Leber zu Cortisol umgewandelt, das die eigentliche Wirkung zeigt (siehe Cortisolwirkung).[8]
Therapeutische Anwendung
Zu Therapiezwecken ist der synthetisch hergestellte Resorptionsester Cortisonacetat geeignet, da er nach oraler Verabreichung schnell resorbiert wird. Nach der Hydrolyse zu Cortison wird in der Leber das biologisch aktive Cortisol gebildet.
Einsatzgebiet
Cortisonacetat ist für die systemische Aufnahme in Form von Tabletten vorgesehen. Der Wirkstoff kann verwendet werden, um einen Mangel an körpereigenem Cortisol, wie er bei der primären Nebennierenrindeninsuffizienz auftritt, auszugleichen (Substitutionstherapie).[9] Heute werden für solche Therapiezwecke allerdings andere Glucocorticoide eingesetzt, zum Beispiel Hydrocortison (Cortisol) und Prednisolon.[9]
Pharmakologische Eigenschaften
Cortisonacetat verfügt über glucocorticoide und mineralocorticoide Eigenschaften. Letztere sind ausgeprägter als bei anderen (neueren) synthetischen Steroiden. Die Bioverfügbarkeit von Cortisol aus Cortisonacetat entspricht etwa 80 % einer vergleichbaren, oral verabreichten Cortisol-Dosis.[10] Die Wirkungsdauer beträgt etwa acht bis zwölf Stunden, womit Cortison(acetat) ein kurzwirksames Glucocorticoid ist. Die Halbwertszeit im Blutplasma liegt bei etwa einer Stunde.[8]
Nebenwirkungen
Bei Substitutionstherapie mit physiologisch angepassten Dosen – wie nach Indikation vorgesehen – sind keine Nebenwirkungen zu erwarten.[11]
Nach Überdosierung über einen längeren Zeitraum können sich Symptome eines Cushing-Syndroms einstellen, die sich in Muskelschwäche oder Muskelschwund (Cortisonmyopathie), Osteoporose, aseptischen Knochennekrosen (Kopf des Oberarm- und Oberschenkelknochens), Dehnungsstreifen (Striae rubrae), verzögerter Wundheilung, Steroidakne, punktförmigen Hautblutungen (Petechien), Blutergüssen, Steigerung des Augeninnendrucks (Glaukom), Linsentrübung (Grauer Star), Hemmung der Magenschleimproduktion, in seltenen Fällen lang anhaltendem Schluckauf, erhöhtem Blutzuckerspiegel, Zuckerkrankheit (Diabetes mellitus), Wassereinlagerung im Gewebe, Vollmondgesicht, vermehrter Kaliumausscheidung, Wachstumsstörungen bei Kindern, Störungen der Sexualhormonsekretion (Ausbleiben der Menstruationsblutung, abnormem Haarwuchs, Impotenz), „Stiernacken“, Blutbildveränderungen (Leukozytose, Lymphopenie, Eosinopenie, Polyglobulie), Erhöhung des Infektrisikos und Immunschwäche äußern.
Kurzfristige, hochdosierte systemische Anwendung:
Bei kurzfristiger, hochdosierter systemischer Anwendung können vor allem neuropsychiatrische Symptome auftreten, wie Konvulsionen, Schwindel, Kopfschmerzen, Schlaflosigkeit, Euphorie, Depressionen und Psychosen. Darüber hinaus kann diese Anwendung zur Manifestation einer latenten Epilepsie führen.
Handelspräparate
Nach Herstellerangaben wurde im Jahre 2008 das letzte auf dem deutschen Markt verfügbare Fertigpräparat, Cortison CIBA, wegen Qualitätsproblemen des Zulieferers vom Markt genommen.[12]
Literatur
- Lea Haller: Cortison. Geschichte eines Hormons, 1900–1955.[13] Chronos, Zürich 2012. ISBN 978-3-0340-1115-0.
- Hanns Kaiser, Norbert Klinkenberg: Cortison. Die Geschichte eines Medikaments. Wissenschaftliche Buchgesellschaft, Darmstadt 1988, ISBN 978-3-534-80037-7.
Weblinks
- Cortison, die Wunderdroge gegen Rheuma. kraniopharyngeom.de
- Warum muß Cortison ausgeschlichen werden? rheuma-online.de – Einführung zu Cortison allgemein und Cortison in der Rheuma-Therapie
Einzelnachweise
- Eintrag zu Cortisone in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM), abgerufen am 14. Juli 2021.
- A. W Frahm, H. H. J. Hager, F. v. Bruchhausen, M. Albinus, H. Hager: Hagers Handbuch der pharmazeutischen Praxis. Folgeband 4: Stoffe A–K. Birkhäuser, 1999, ISBN 978-3-540-52688-9, S. 1099.
- Datenblatt Cortisone, ≥ 98 % bei Sigma-Aldrich, abgerufen am 14. September 2011 (PDF).
- Gemeint sind künstliche Glucocorticoide.
- Peter Dilg: Cortison. In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 275.
- Arthur A. Patchett: Lewis Hastings Sarett 1917–1999. (PDF; 156 kB) In: Biographical Memoirs, Vol. 81, 2002, The National Academy Press, Washington DC.
- Florian Horn: Biochemie des Menschen: Das Lehrbuch für das Medizinstudium, 3. Auflage, Thieme-Verlag 2005; S. 371. ISBN 3-13-130883-4.
- Eintrag zu Cortison bei Vetpharm, abgerufen am 23. Juni 2012.
- K. Hardtke et al. (Hrsg.): Kommentar zum Europäischen Arzneibuch Ph. Eur. 4.0, Cortisonacetat. Loseblattsammlung, 18. Lieferung 2004, Wissenschaftliche Verlagsgesellschaft Stuttgart
- V. J. Heazelwood, J. P. Galligan, G. R. Cannell, F. Bochner, R. H. Mortimer: Plasma cortisol delivery from oral cortisol and cortisone acetate: relative bioavailability. In: Br. J. Clin. Pharmacol, 17(1), 1984, S. 55–59; PMC 1463287 (freier Volltext).
- Fachinformation zu Cortison Ciba®
- Wichtige Information! In: Glandula, Novartis Pharma GmbH, Heft 01/08, S. 23, glandula-online.de (PDF; 2,4 MB)
- Rezensionen bei Perlentaucher.