Aluminiumorthophosphat
Aluminiumorthophosphat, auch kurz Aluminiumphosphat genannt, ist ein rhombische Kristalle bildendes Aluminiumsalz. In dieser Verbindung liegt Aluminium als dreifach positiv geladenes Kation (Al3+) vor, das mit dem Phosphat-Anion (PO43−) in elektrostatischer Wechselwirkung steht.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
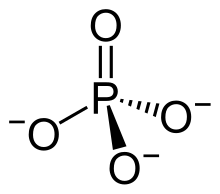 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Aluminiumorthophosphat | |||||||||||||||||||||
| Andere Namen |
Berlinit | |||||||||||||||||||||
| Summenformel | AlPO4 | |||||||||||||||||||||
| Kurzbeschreibung |
weißer, geruchloser Feststoff[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
A02AB03 | |||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 121,95 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
2,57 g·cm−3 [1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
nahezu unlöslich in Wasser[2] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||||||||
| ΔHf0 |
−1733,8 kJ/mol[3] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen
In der Natur kommt Aluminiumorthophosphat in der wasserfreien Form als farbloses bis hellrosafarbenes Mineral Berlinit und in der wasserhaltigen Form als Variscit vor.
Synthese

Das Orthophosphat lässt sich aus Natriumphosphat und einer Aluminiumsalzlösung gewinnen, z. B.:
Verwendung
Aluminiumorthophosphat wird als Flussmittel bei der Herstellung von Gläsern, Keramiken und Glasuren verwendet. Im Gemisch mit Calciumsulfat und Natriumsilikaten ist es unter dem Begriff Zement bekannt.
Gele, die Aluminiumorthophosphat enthalten, finden in der Medizin Anwendung als Antazidum.
Außerdem wird es als Adjuvans in manchen Impfstoffen eingesetzt, beispielsweise im Pneumokokkenimpfstoff Synflorix[4] bzw. Prevenar 13[5] oder als Kombination bei AS04 in Hepatitis B- und HPV-Impfstoffen.[6][7] Es liegt in einer chemisch amorphen Form vor, bei der manche OH-Gruppen mit Phosphatgruppen ersetzt sind.[8] Dies führt zu einer großen Oberfläche und Absorptionskapazität. Der isoelektrische Punkt des kommerziell erhältlichen Adjuvans' liegt im Bereich von 4,5 bis 5,5.
Handelsnamen
Aluminiumphosphat ist in Deutschland unter dem Namen Phosphalugel im Handel erhältlich.
Einzelnachweise
- Datenblatt Aluminiumorthophosphat bei AlfaAesar, abgerufen am 7. Januar 2010 (PDF) (JavaScript erforderlich).
- Eintrag zu Aluminiumphosphat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. Januar 2013. (JavaScript erforderlich)
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- Synflorix. In: Europäische Arzneimittel-Agentur. 17. September 2018, abgerufen am 4. Februar 2020 (englisch).
- Prevenar 13. In: Europäische Arzneimittel-Agentur. 26. März 2020, abgerufen am 20. April 2020 (englisch).
- H. Ronneberger: Adjuvantien bei Humanimpfstoffen. In: H. Schöffl et al. (Hrsg.): Forschung ohne Tierversuche 1996. Springer, Wien 1997, S. 218–223, doi:10.1007/978-3-7091-6833-2_28.
- Ralf Wagner und Eberhard Hildt: Zusammensetzung und Wirkmechanismen von Adjuvanzien in zugelassenen viralen Impfstoffen. In: Bundesgesundheitsblatt. Band 62, Nr. 4, 1. April 2019, ISSN 1437-1588, S. 462–471, doi:10.1007/s00103-019-02921-1.
- Nathalie Garçon und Martin Friede: Evolution of Adjuvants Across the Centuries. In: Stanley A. Plotkin et al. (Hrsg.): Plotkin's Vaccines. 7. Auflage. Elsevier, 2017, ISBN 978-0-323-35761-6, S. 64, doi:10.1016/B978-0-323-35761-6.00006-7 (elsevier.com).