Isophoron
Isophoron ist eine chemische Verbindung aus der Gruppe der cyclischen Enone und ein Derivat von 2-Cyclohexen-1-on.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
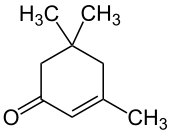 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Isophoron | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C9H14O | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 138,21 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,92 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
schlecht in Wasser (14,5 g·l−1 bei 20 °C)[1] | |||||||||||||||
| Brechungsindex | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK | ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Vorkommen
Natürlich kommt Isophoron in Großfrüchtigen Moosbeeren[7] Safran[8] Papaya, Kohlrabi, Grapefruit, Parmesan, Weißwein, Schwarztee, Haselnuss, Ume, Sternfrucht, Mango, Backpflaumen, Reis, Buchweizen, Okra, Hafer und Süßgras vor.[2]
 Moosbeeren
Moosbeeren Kohlrabi
Kohlrabi_-_whole_with_kernels.jpg.webp) Haselnuss
Haselnuss Parmesan
Parmesan
Geschichte
Isophoron wurde als Lösemittel auf der Basis von Aceton, einem Nebenprodukt, welches in großen Mengen bei der Phenolsynthese entsteht, entwickelt. Die erste Produktion wurde von der Hibernia AG 1962 in deren Stickstoffwerk in Herne aufgenommen. 1967 wurde die Fertigung in das Werk I der Hibernia, dem heutigen Evonik-Werk Herne verlagert.[9] Der Isophoron-Verkauf sicherte den Standort in Herne.[10] 1979 übernahm die Hüls AG die inzwischen zur Veba gehörende Werkgruppe Herne und damit auch die Produktion von Isophoron und Isophoronderivaten. Ab 1992 wurden Isophoronderivate auch im Evonik-Standort in Mobile, Alabama produziert.
Gewinnung
Isophoron kann durch eine Aldolreaktion von drei Molekülen Aceton hergestellt werden.[11]
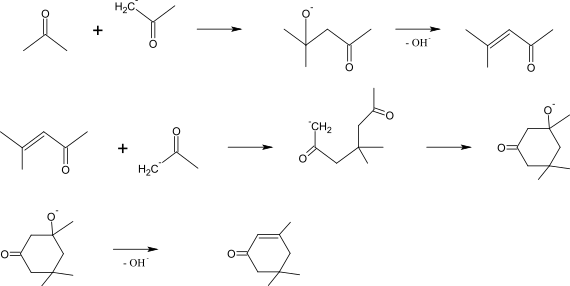
2003 betrug die jährliche Produktionskapazität für Isophoron 50000 t/a.[3]
Eigenschaften
Isophoron ist eine farblose bis gelbliche Flüssigkeit mit charakteristischem Geruch (nach Campher). Sie ist mit aromatischen und aliphatischen Kohlenwasserstoffen, Aldehyden, Ketonen, Alkoholen, Estern und Ethern mischbar. Der Flammpunkt liegt bei 95 °C, die Zündtemperatur bei 470 °C.[3]
Es existieren zwei Konstitutionsisomere, die oft unter dem Namen Isophoron zusammengefasst werden, nämlich das hier beschriebene α-Isophoron und das β-Isophoron. Ersteres trägt die C=C-Doppelbindung zwischen C-Atom 2 und 3, ist also ein α,β-ungesättigtes Carbonyl; letzteres trägt die Doppelbindung zwischen C-Atom 3 und 4. Meistens ist im α-Isophoron 1–3 % des β-Isomers als Verunreinigung enthalten.
Verwendung
Isophoron wird als Lösungsmittel in der Lack-, Farben- und Klebstoffindustrie benutzt.
In der Synthese wird es hauptsächlich als Zwischenprodukt zur Herstellung von Isophorondiamin,[3] Isophorondiisocyanat,[3] 3,3,5-Trimethylcyclohexanol,[2][3] 3,5-Dimethylphenol[2][3] oder 2,3,5-Trimethylphenol[3] verwendet.
Isophoron ist Bestandteil von farbigen Indikatoren mit positiver Solvatochromie (L.S.G. Brooker und Ralf E. Lemke) und der negativ solvatochromen Anionen mit positiver Thermochromie (Ralf E. Lemke).
Weiterhin kann Isophoron zu 3,3,5-Trimethylcyclohexanon oder 3,3,5-Trimethylcyclohexanol hydriert werden, welches zur Trimethyladipinsäure oxidiert werden kann.[3]
Risikobewertung
Isophoron wurde 2012 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Isophoron waren die Besorgnisse bezüglich der Einstufung als CMR-Substanz, Exposition von Arbeitnehmern, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung. Die Neubewertung fand ab 2013 statt und wurde von Frankreich durchgeführt.[12]
Einzelnachweise
- Eintrag zu 3,5,5-Trimethylcyclohex-2-enon in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- George A. Burdock: Fenaroli’s Handbook of Flavor Ingredients. CRC Press, 2004, ISBN 1-4200-3787-0, S. 950 (eingeschränkte Vorschau in der Google-Buchsuche).
- M. Bohnet, C. J. Brinker, B. Cornils, T. J. Evans, H. Greim, L.L. Hegedus, J. Heitbaum, W.A. Herrmann, W. Keim, A. Kleemann, G. Kreysa, T. Laird, J. Löliger, R. O. McClellan, J.L. McGuire, J.W. Mitchell, A. Mitsutani, T. Onoda, L. Plass, G. Stephanopoulos, D. Werner, P. Woditsch, N. Yoda: Ullmanns Encyclopedia of industrial chemistry. 6. Auflage. Band 18: Information Storage to Ketones. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim 2003, ISBN 3-527-30385-5, S. 745 f.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Physical Constants of Organic Compounds, S. 3-312.
- Eintrag zu 3,5,5-trimethylcyclohex-2-enone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 78-59-1 bzw. Isophoron), abgerufen am 2. November 2015.
- Chronic Toxicity Summary (Memento vom 22. September 2006 im Internet Archive) (PDF; 36 kB),
- ISOPHORONE (engl., PDF) In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 14. September 2021.
- Wolfgang Hasenpusch: Isophoron – Produkt einer Verlegenheit. In: clb. Band 63, Nr. 7, August 2012, S. 288–293 ( [PDF]).
- Isophoron. Damit der Lack nicht ab ist. Beitrag bei Evonik Industries, abgerufen am 28. Oktober 2015.
- U.S. Patent 5849957.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): 3,5,5-trimethylcyclohex-2-enone, abgerufen am 26. März 2019.

