Pyrethroide
Pyrethroide sind synthetische Insektizide, die an die Hauptwirkstoffe des natürlichen Insektizids Pyrethrum angelehnt sind. Eine Definition allein anhand der chemischen Struktur ist nicht möglich. Die Struktur eines Pyrethroids sollte von einem der natürlichen Pyrethrine hergeleitet werden können und seine biologischen Eigenschaften im Wesentlichen mit denen der bekannten Pyrethroide übereinstimmen.[1] Typisch für Pyrethroide sind ihre rasche Wirksamkeit („knock down“) auch bei niedriger Dosierung, die geringe Giftigkeit für Warmblüter, Lipophilie und ein niedriger Dampfdruck. Pyrethroide sind billiger und in größeren Mengen herstellbar als Pyrethrum, meist sind sie besser wirksam. Einige Pyrethroide sind photostabil und damit relativ langlebig.
Geschichte
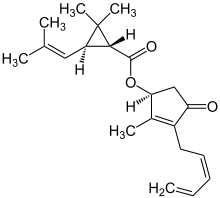
Die wirksamen Bestandteile des Pyrethrums wurden um 1924 durch Leopold Ružička und Hermann Staudinger ermittelt. Sie klärten die Struktur der wirksamen Pyrethrine weitgehend auf und stellten die ersten synthetischen Derivate her.[1] Die kommerziell hergestellten Pyrethroide können je nach Entwicklungszeit vier unterschiedlichen Generationen zugeordnet werden.
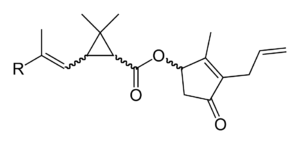
Zur ersten Generation gehört nur das 1949 erstmals synthetisierte und 1954 von der japanischen Firma Sumitomo Chemical auf den Markt gebrachte Allethrin I, dessen Struktur dem Pyrethrin I noch sehr ähnlich ist. Unter Lichteinwirkung zersetzt es sich sehr schnell, die Synthese ist aufwändig. Allethrin I ist gegen die meisten Insekten weniger wirksam als natürliche Pyrethrine.[2] Eine zweite Generation von Pyrethroiden kam zwischen 1965 und 1973 mit Tetramethrin, Resmethrin, Bioresmethrin, Bioallethrin und Phenothrin auf den Markt. Einige Wirkstoffe dieser zweiten Generation waren 20-fach (Resmethrin) oder 50-fach (Bioresmethrin) stärker wirksam als Pyrethrum. Fenvalerat und Permethrin sind Wirkstoffe der dritten Pyrethroid-Generation. Sie waren aufgrund ihrer verbesserten Photostabilität als erste Pyrethroid-Wirkstoffe in der Landwirtschaft einsetzbar.
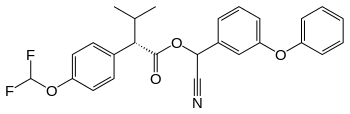
Alle später auf den Markt gekommenen Wirkstoffe zählen zur vierten Generation, die beispielsweise Bifenthrin, Cypermethrin, Cyfluthrin, Deltamethrin, Flucythrinat und Prallethrin umfasst.[3] Der wirtschaftliche Durchbruch der Pyrethroide kam mit der Einführung photostabiler Verbindungen für die Landwirtschaft. Auf dem Weltmarkt wurden 1976 Pyrethroide im Endverkaufswert von 10 Millionen US-$ abgesetzt, bereits 1983 waren es 630 Millionen US-$. Dieser kommerzielle Erfolg beruhte fast ausschließlich auf Fenvalerat, Deltamethrin, Cypermethrin und Permethrin.[4] Die Zahl der bisher im Labormaßstab synthetisierten Pyrethroide wird auf rund 1000 geschätzt.[5]
Einen wesentlichen Anteil an der Entwicklung hatte Michael Elliott vom britischen Rothamsted Research, dessen Gruppe in den 1960er Jahren Bioresmethrin und Resmethrin und später in den 1970er Jahren Deltamethrin, Cypermethrin und Permethrin entwickelte.
Chemische Strukturen
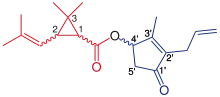
Die natürlich vorkommenden Pyrethrine und die Mehrzahl der Pyrethroide sind Ester aus einer Säurekomponente und einem Alkoholrest. Die Moleküle besitzen meist ein oder mehrere Chiralitätszentren, die dadurch unterscheidbaren Enantiomere oder Diastereomere sind fast immer verschieden wirksam. Allethrin ist beispielsweise der Ester des racemischen Alkohols Allethrolon mit racemischer cis/trans-Chrysanthemumsäure. Zur Herstellung des weit stärker wirksamen Bioallethrin wird bei identischer Struktur ausschließlich (1R)-trans-Chrysanthemumsäure verwendet. Ähnliches gilt für (S)-Bioallethrin, das zudem nur aus dem (S)-Enantiomer des Allethrolon besteht.[1]
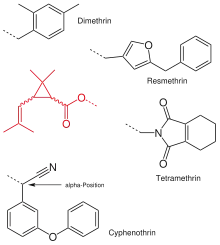
Bei der Suche nach neuen Wirkstoffen wurde zunächst der Chrysanthemumsäurerest beibehalten und die Alkoholkomponente variiert. Sie wurde beispielsweise durch einen 3,4-Dimethylbenzylrest (Dimethrin), Furyl- (Resmethrin) oder Phthalimidderivate (Tetramethrin) ersetzt. Anfang der 1970er Jahre wurde der Alkoholrest durch eine 3-Phenoxybenzylgruppe ersetzt, bei der durch Hinzufügen einer Cyanogruppe an der α-Position die Wirksamkeit deutlich gesteigert werden kann (Cyphenothrin u. a.).
Durch Einfügen einer Dichlor-, Dibrom- oder Difluorvinylgruppe in den Chrysanthemumsäurerest konnten photostabile Pyrethroide wie Permethrin, Deltamethrin und Cypermethrin hergestellt werden. Auch der Ersatz der Chrysanthemumsäure durch Derivate der Phenylessigsäure führte wie bei Fenvalerat zu photostabilen Produkten.[1]
Physikalisch-Chemische Eigenschaften
Die Pyrethroide sind stark lipophil, ihr logarithmierter Oktanol-Wasser-Verteilungskoeffizient liegt im Bereich von 4,2 (Tetramethrin) bis 8,6 (Flumethrin). Die Wasserlöslichkeit ist mit 5 mg/l (Tetramethrin) bis 0,0003 mg/l (Flumethrin) gering bis sehr gering.[6]
Wirkungsweise
Wie Pyrethrum sind Pyrethroide Kontaktgifte, die die spannungsabhängigen Natriumkanäle in den Nervenmembranen irreversibel blockieren, so dass sie vom offenen Zustand aus nicht wieder geschlossen werden können. Sie wirken in der Regel sehr schnell gegen fast alle Insekten. Die Wirkung tritt bei den weniger lipophilen Pyrethroiden rascher ein als bei den stark lipophilen. Pyrethroide sind nicht nützlingsschonend. Sie wirken jedoch auch vergrämend, wodurch beispielsweise ihre hohe Giftigkeit für Bienen im Freiland nicht zum Tragen kommt. Sie sind zudem sehr giftig für Fische, Amphibien und Reptilien.[7]
Durch die Blockierung der Natriumkanäle kommt es zu einer spastischen Lähmung (Paralyse) der Insekten und einem schnellen immobilisierenden Effekt, der noch vor dem Tod eintritt und als „knockdown“ bezeichnet wird.
Resistenzen
Resistenzen gegen Pyrethroide gehen hauptsächlich auf die vermehrte Produktion von abbauenden Enzymen wie Esterasen und „mischfunktionellen“ Oxidasen zurück. Bei einer hohen Aktivität dieser Enzyme werden auch einige andere Insektizide wie DDT, Phosphorsäureester und Carbamate schneller abgebaut, man spricht hier von Kreuzresistenz. Synergisten wie das häufig verwendete Piperonylbutoxid stören den enzymatischen Abbau von Pyrethroiden. Damit verbessern sie deren Wirksamkeit und erschweren die Resistenzbildung. Bei der Entwicklung neuer Wirkstoffe wird versucht, die enzymatische Abbaubarkeit durch Anpassen der Molekülstruktur zu verringern. Einige Insektizide aus anderen Wirkstoff-Familien werden durch Esterasen und Oxidasen erst in ihre „aktive“ Form überführt. Sie zeigen somit eine „negative Kreuzresistenz“, wirken also auf pyrethroid-resistente Insektenstämme stärker als auf nicht-resistente.
Eine Resistenz gegen Pyrethroide kann auch erworben werden, wenn das Protein am Natriumkanal der Nervenzelle verändert wird. Es sind mehrere durch Mutationen ausgelöste Veränderungen der α-Untereinheit des Kanalproteins (VGSC-Protein) bekannt, die einzeln oder gemeinsam auftreten und zu einer Insensitivität gegenüber dem Pyrethroid führen. Da die Hemmung des Natriumkanals eine schnelle Immobilisierung der Insekten durch eine spastische Lähmung auslöst, was als „knockdown“ bezeichnet wird, nennen sich die Resistenzen „knockdown resistance“ (abgekürzt kdr). Während einzelne Mutationen die Empfindlichkeit gegen alle Pyrethroide um den Faktor 20 bis 50 senken, können andere auch als „super-kdr“ bezeichnete Mutationen die Toleranz für bestimmte Typ I-Pyrethroide um das 500-fache erhöhen. Diese Mutationen verstärken andererseits die Empfindlichkeit gegen zwei andere Klassen von Insektiziden, die N-Alkylamide und die Dihydropyrazole.[2] Die häufigste Form der Resistenz ist aber inzwischen eine Kombination dreier Punktmutationen (M815I, T917I, L920F), die zunehmend häufiger zu finden sind. So wurden diese Mutationen 2010–2012 bei Kopfläusen zu 33–100 % in Kalifornien, Florida und Texas, zu 97 % in Kanada und zu 98,7 % in Paris gefunden.[8]
Verwendung
Medizin
Pyrethroide sind als insektizide Wirkstoffe in Präparaten gegen Läuse enthalten. In Deutschland sind Allethrin und Permethrin Wirkstoffe zugelassener Präparate gegen Kopf-, Filz- und Kleiderläuse sowie gegen Krätzemilben (Krätze).[9] Seit 2004 ist dort zur Behandlung der Krätze auch eine permethrinhaltige Salbe zugelassen.[10] Bei einer Studie in Wales fand man bei Kopfläusen bei 82 % der Fälle Resistenz oder verminderte Wirksamkeit von Pyrethroiden. Eine israelische Studie berichtet ebenfalls von verbreiteter Pyrethroid-Resistenz bei Kopfläusen. Nach Angaben des Robert Koch-Instituts sind diese Ergebnisse nicht direkt auf Deutschland übertragbar, wo bislang nur vereinzelt resistente Läuse aufgetreten sind.[11]
Vektorbekämpfung
Einige Staaten schreiben vor, das Innere ankommender Flugzeuge mit Insektiziden zu behandeln, damit keine Krankheitsvektoren eingeschleppt werden. Dazu versprüht man Pyrethroide mit Kurzzeitwirkung (Pyrethrine, d-Phenothrin, Resmethrin, Bioresmethrin) in der Kabinenluft, Substanzen mit Langzeitwirkung (Permethrin) werden zur Behandlung von Oberflächen eingesetzt.[12][13]
Bei der Bekämpfung der malariaübertragenden Anopheles-Mücken spielen Pyrethroide heute eine wichtige Rolle. Sie können allerdings nicht auf dieselbe Weise wie DDT zum Besprühen der Wände (englisch Indoor Residual Spraying) verwendet werden. Ihre starke Repellent-Wirkung verhindert, dass sich die Mücken auf den Wänden absetzen. Falls sich dennoch Mücken setzen, werden sie durch die „knock down“-Wirkung betäubt, fallen auf den Boden und erholen sich nach einiger Zeit oft wieder.[4] Langlebige Pyrethroide werden allerdings zum Imprägnieren von Moskitonetzen verwendet, was von der WHO seit 1992 zur Malariabekämpfung empfohlen wird.[14]
Tiermedizin
In der Tiermedizin werden Pyrethroide eingesetzt, um Ektoparasiten bei Haustieren abzuwehren oder zu behandeln. Hierzu gehören unter anderem Kopf- und Weidestechfliegen, Bremsen, Flöhe und Tierläuse, Lausfliegen, Zecken, diverse Milben, Haar- und Federlinge. In Deutschland sind dafür zurzeit Cyfluthrin, Cypermethrin, Deltamethrin, Flumethrin und Permethrin Wirkstoffe zugelassener Arzneimittel, in der Vergangenheit waren es auch Fenvalerat und Flucythrinat. Für lebensmittelliefernde Tiere sind in der EU nach Anhang 1 der Verordnung (EWG) Nr. 2377/90 über Höchstmengen für Tierarzneimittelrückstände in Nahrungsmitteln Cypermethrin, Cyhalothrin, Cyfluthrin, Deltamethrin, Flumethrin, Fenvalerat und Permethrin zugelassen.
Cypermethrin und Deltamethrin haben eine besonders langanhaltende Wirkung und werden daher vorbeugend als Wirkstoffe in insektenabwehrenden Ohrmarken oder Halsbändern eingesetzt. Gegen die Varroamilbe bei Honigbienen werden teilweise mit Fluvalinat oder Flumethrin getränkte Streifen in die Stöcke eingehängt. In der Fischzucht kann gegen Lachs- und Fischläuse Cypermethrin verwendet werden.[7]
Bei Katzen gibt es Anwendungsbeschränkungen für Pyrethroide, da sie diese schlechter abbauen können als viele andere Tierarten. Katzen sind daher besonders anfällig für Pyrethroid-Vergiftungen, die bei ihnen üblicherweise tödlich verlaufen.[15]
Pflanzenschutz
Ein Hauptanwendungsgebiet für Pyrethroide ist der Einsatz gegen Schmetterlingsraupen im Baumwolle-Anbau. Pyrethroide werden weiterhin gegen eine Vielzahl von Schadinsekten angewendet; Ausnahmen sind die sich gut schützenden Woll- und Schildläuse sowie die kaum empfindlichen pflanzenpathogenen Milbenarten.[4]
In Deutschland ist die Gesamtmenge der als Pflanzenschutzmittel verwendeten Pyrethroide gering. Im Jahre 2001 waren dort mit 52 Tonnen nur etwa 0,8 % der im Pflanzenschutz eingesetzten Insektizide Pyrethroide.[16] Wegen ihrer hohen Wirksamkeit werden nur Aufwandmengen von 10 bis 200 g Wirkstoff pro Hektar benötigt, was deutlich weniger ist als bei den meisten anderen Insektiziden.[5]
Für ein relativ breites Einsatzspektrum, insbesondere im Getreide- und Rapsanbau, sind in Deutschland und Österreich alpha- und zeta-Cypermethrin, Esfenvalerat, Deltamethrin und lambda-Cyhalothrin zugelassen. Die Verwendung von Cypermethrin ist in Österreich und der Schweiz erlaubt. In der Schweiz sind neben alpha- und zeta-Cypermethrin und Deltamethrin auch Bifenthrin und Cypermethrin high-cis zulässige Pflanzenschutzmittelwirkstoffe.[17] Die Einsatzbereiche können unterschiedlich sein: Cyfluthrin ist in Deutschland gegen den Apfelwickler zugelassen, in der Schweiz gegen Vorratsschädlinge und in Österreich für eine Vielzahl landwirtschaftlicher Anwendungsfälle. Tefluthrin und beta-Cyfluthrin sind Bestandteile in Deutschland und Österreich zugelassener Saatgutbehandlungsmittel.[18][19]
Schädlingsbekämpfung und Haushalte
Im Jahr 2000 wurden in Deutschland von den Mitgliedsfirmen des Industrieverbands Agrar, die etwa 70 % des Marktes abdecken, 2,7 t Pyrethroide für den „häuslichen Gebrauch“ verkauft. Dazu kommen jährlich etwa 2,6 t Permethrin, die für die Ausrüstung von Wollteppichen gegen Motten- und Käferfraß verwendet werden.[5]
Pyrethroide, die in Haushalten eingesetzt worden sind, sind sehr langlebig und stellen eine anhaltende Kontamination dar. So wird Permethrin binnen 112 Tagen erst um 10 % abgebaut, für Cypermethrin konnten ähnliche Verläufe beobachtet werden.[20]
Toxikologie
Über das Verdauungssystem werden Pyrethroide nur teilweise resorbiert, über die Haut ist ihre Aufnahme sehr gering und geschieht daher überwiegend über die Atmung.[21] Resorbierte Pyrethroide werden im Körper größtenteils innerhalb weniger Stunden oder Tage durch Esterasen und Monooxygenasen abgebaut.[22] Eine Anreicherung im Fettgewebe ist möglich, dort beträgt die Halbwertszeit für den Abbau bis zu 30 Tage.[23]
Die akute Toxizität von Pyrethroiden bei Warmblütern ist im Vergleich zu Insektiziden aus den Gruppen der Organophosphate und Chlororganischen Verbindungen gering. Die LD50 bei der Ratte liegt für Pyrethroide zwischen 100 und 5000 mg/kg Körpergewicht.[23] Akute Vergiftungen beim Menschen treten selten auf. Nach oraler Aufnahme kommt es innerhalb von 10 bis 60 Minuten zu Übelkeit, Erbrechen oder Durchfall. Falls eine nennenswerte Menge resorbiert wurde, leidet der Patient einige Tage lang an Bewusstseinsstörungen und Krämpfen. Bleibende Nervenschäden nach einer akuten Vergiftung sind möglich.[24] Ein direkter Hautkontakt mit den Reinstoffen oder stark damit kontaminierten Oberflächen kann innerhalb weniger Minuten bis einiger Stunden zu lokalen Parästhesien führen. Die sensiblen Nervenenden in der Haut werden dabei gereizt, es kommt zu einem Kribbeln, Brennen oder Jucken, das etwa einen Tag anhält. Auf Hautkontakt mit Pyrethroiden reagieren Kinder wegen ihrer empfindlicheren Haut im Allgemeinen stärker.[22]
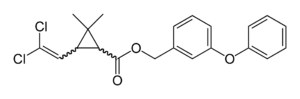
Typ I-Pyrethroide (ohne alpha-cyano-Gruppe) und Typ II-Pyrethroide (mit alpha-cyano-Gruppe) unterscheiden sich hinsichtlich ihrer akuten Wirkungen. Typ I führt im Tierversuch zum „T-Syndrom“, so benannt nach dem auftretenden Tremor. Beim „T-Syndrom“ werden auch Ataxie, erhöhte Erregbarkeit und Reiz-Überempfindlichkeit beobachtet.
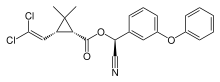
Pyrethroide vom Typ II bewirken ein „CS-Syndrom“, das nach den charakteristischen Symptomen Choreo-Athetose (unwillkürliche langsame Bewegungen) und Speichelfluss benannt ist. Daneben treten hier auch ein grobschlägiger Tremor und klonische Krämpfe auf.
Im Tierversuch zeigten Pyrethroide keine embryotoxische oder teratogene Wirkung. Die US-Umweltbehörde EPA hat Permethrin bei oraler Aufnahme als wahrscheinlich krebserregend eingestuft. Dies geschah aufgrund reproduzierbarer Studien mit Mäusen, die nach Fütterung mit Permethrin Lungen- und Leber-Tumore entwickelten.[25]
Verschiedene Pyrethroide wirken als endokrine Disruptoren, insbesondere auf Androgen-Rezeptoren. Bei Kaninchen wurde festgestellt, dass Cypermethrin an den Testosteron-Rezeptor bindet und so die männliche Sexualentwicklung und das Immunsystem schädigt. Permethrin kann ebenfalls an den Testosteron-Rezeptor binden, in hohen Konzentrationen kann es hingegen wie Östrogen wirken. Fenvalerat hemmt bei Mäusen die Funktion von Schilddrüsenhormonen.[5]
Umweltverhalten
Über die Nahrungskette reichern sich Pyrethroide nicht an. Rückstände in Lebensmitteln sind eine Folge direkter Kontamination.[23]
Nachweis
Da Pyrethroide für aquatische Organismen zu den toxischsten Insektiziden gehören, ist für Oberflächengewässer eine analytische Nachweismethode notwendig, welche sehr empfindlich ist, d. h. bis in den Bereich von Pikogramm pro Liter reicht.[26][27]
Weitere Nachweiswege basieren etwa auf der Bestimmung der Konzentrationen von Metaboliten im Urin oder Hausstaubproben.[28]
Weblinks
- Pyrethroide in der Umwelt – Infoblatt des Ökotoxzentrums
Einzelnachweise
- J. H. Davies: The pyrethroids: an historical introduction. In: J. P. Leahey (Hrsg.): The Pyrethroid Insecticides. Taylor & Francis, London/ Philadelphia 1985, ISBN 0-85066-283-4.
- Bhupinder P. S. Khambay: Pyrethroid Insecticides. (PDF; 144 kB) Pesticide Outlook – April 2002, S. 49–54.
- George W. Ware, David M. Whitacre: An Introduction to Insecticides. Auszug aus: The Pesticide Book, 6. Auflage, 2004 (abgerufen am 22. September 2007).
- J. J. Hervé: Agricultural, public health and animal health usage. in J. P. Leahey (Hrsg.): The Pyrethroid Insecticides. Taylor & Francis, London/ Philadelphia 1985, ISBN 0-85066-283-4.
- Susanne Smolka, Patricia Cameron: Gefahren durch hormonell wirksame Pestizide und Biozide (Memento vom 9. November 2012 im Internet Archive) (PDF; 1,1 MB). WWF Deutschland (Hrsg.), Frankfurt am Main, Stand Mai 2002.
- Klaus Naumann: Synthetic Pyrethroid Insecticides: Structures and Properties. Springer-Verlag, Berlin, 1990, ISBN 0-387-51313-2.
- Eintrag zu Permethrin bei Vetpharm, abgerufen am 5. August 2012.
- Olivier Chosidow, Bruno Giraudeau: Topical Ivermectin – A Step toward Making Head Lice Dead Lice? In: New England Journal of Medicine. 2012, Band 367, Ausgabe 18 vom 1. November 2012, S. 1750–1752, doi:10.1056/NEJMe1211124.
- Richter, Müller-Stöver, Walter, Mehlhorn, Häussinger: Kopfläuse – Umgang mit einer wieder auflebenden Parasitose. In: Deutsches Ärzteblatt. 102, 9. September 2005, S. A-2395.
- Haustein, Paasch: Krätze weiterhin verbreitet: Endemien in Pflegeheimen erfordern konsequente Synchronbehandlung. In: Deutsches Ärzteblatt. 102, 10. Januar 2005, S. A-45.
- aerzteblatt-studieren.de: Walisische Kopfläuse proben den Widerstand – Häufige Pyrethorid-Resistenzen. (Memento vom 4. September 2007 im Internet Archive) 16. Juni 2006.
- BfR: Neues Verfahren zur Flugzeugdesinfektion schont Passagiere und Besatzung (PDF; 40 kB).
- Christian Felten: Luftqualität in der Kabine (unter besonderer Berücksichtigung von Pyrethroiden), 15. Mai 2003. (Memento vom 3. Dezember 2008 im Internet Archive)
- Christian Simon: DDT – Kulturgeschichte einer chemischen Verbindung. Christoph Merian Verlag, Basel 1999, ISBN 3-85616-114-7.
- Arzneimittelkommission: Anwendungsbeschränkungen für Pyrethroide bei Katzen. (Nicht mehr online verfügbar.) ABDA, archiviert vom Original am 23. Januar 2007; abgerufen am 13. November 2012.
- Stellungnahme der Kommission „Human-Biomonitoring“ des Umweltbundesamtes: Innere Belastung der Allgemeinbevölkerung in Deutschland mit Pyrethroiden und Referenzwerte für Pyrethroid-Metabolite im Urin. In: Bundesgesundheitsblatt. 48 (2005), S. 101187–101193.
- Bundesamt für Landwirtschaft (Schweiz): Pflanzenschutzmittelverzeichnis.
- BVL (Deutschland): Verzeichnis zugelassener Pflanzenschutzmittel.
- Pflanzenschutzmittel-Register. Abgerufen am 28. Juni 2019.
- Lia Emi Nakagawa, Cristiane Mazarin do Nascimento, Alan Roberto Costa, Ricardo Polatto, Solange Papini: Persistence of indoor permethrin and estimation of dermal and non-dietary exposure. In: Journal of Exposure Science & Environmental Epidemiology. März 2019, doi:10.1038/s41370-019-0132-7.
- Kinderärztliches Portal Allum.
- Franz-Xaver Reichl (Hrsg.): Taschenatlas der Toxikologie. Georg Thieme Verlag, Stuttgart 1997, ISBN 3-13-108971-7.
- Forth, Henschler, Rummel, Förstermann, Starke: Allgemeine und spezielle Pharmakologie und Toxikologie. 8. Auflage. Urban & Fischer, München 2001, ISBN 3-437-42520-X.
- H Müller-Mohnssen: Chronic sequelae and irreversible injuries following acute pyrethroid intoxication, Toxicology Letters, Band 107, Ausgabe 1–3, 30. Juni 1999, S. 161–176 doi:10.1016/S0378-4274(99)00043-0.
- EPA (2009): Permethrin Facts., United States Environmental Protection Agency, Washington DC 2009, abgerufen am 30. Juni 2017 (PDF; englisch).
- Christoph Moschet, Etiënne L. M. Vermeirssen, Remo Seiz, Hildegard Pfefferli, Juliane Hollender: Picogram per liter detections of pyrethroids and organophosphates in surface waters using passive sampling. In: Water Research. Band 66, Dezember 2014, S. 411–422, doi:10.1016/j.watres.2014.08.032.
- Andrea Rösch, Birgit Beck, Juliane Hollender, Christian Stamm, Heinz Singer: Geringe Konzentrationen mit grosser Wirkung – Nachweis von Pyrethroid- und Organophosphatinsektiziden in Schweizer Bächen im pg·l−-Bereich. In: Aqua & Gas. Band 11, 2019, S. 54–66 (PDF).
- Edith Berger-Preiß, Susanne Gerling, G. Leng, et al: Pyrethrum and pyrethroid metabolites (after liquid phase extraction) in urine [Biomonitoring Methods, 2013]. In: The MAK-Collection for Occupational Health and Safety. Pt.4: Biomonitoring methods. Vol.13. 2013, ISBN 978-3-527-60041-0, S. 215–248, doi:10.1002/3527600418.bi800334e0013b (fraunhofer.de).