Cyphenothrin
Cyphenothrin ist ein Insektizid aus der Gruppe der Pyrethroide. Es wurde Ende der 1980er-Jahre von der Firma Sumitomo unter dem Handelsnamen Gokilaht in den Handel gebracht.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
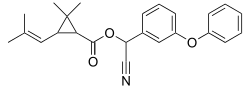 | |||||||||||||||||||
| Strukturformel ohne Stereochemie | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cyphenothrin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C24H25NO3 | ||||||||||||||||||
| Kurzbeschreibung |
gelblich-bräunliches wachsartiges Öl oder gelber, wachsartiger Feststoff[1][2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 375,47 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig/fest | ||||||||||||||||||
| Dichte |
1,08 g·cm−3[3] | ||||||||||||||||||
| Schmelzpunkt |
25 °C[3] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck |
1,2·10−4 Pa (20 °C)[3] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Die Darstellung von Cyphenothrin erfolgt über eine mehrstufige Reaktion. Phenol wird mit m-Bromtoluol zur Reaktion gebracht. Das entstehende m-Phenoxytoluol wird dann mit Brom oder N-Bromsuccinimid und anschließend mit Urotropin umgesetzt. Das Produkt reagiert mit Salzsäure zu m-Phenoxybenzaldehyd und danach mit Natriumcyanid, Kaliumcyanid oder Blausäure zum m-Phenoxycyanobenzylalkohol (PCBA). Dies kann dann mit Chrysanthemumsäure zum Cyphenothrin umgesetzt werden.[6][7]
Eigenschaften
Cyphenothrin ist ein gelber bis gelbbrauner Stoff mit öliger bis wachsartiger Konsistenz. Es ist geruchlos und nahezu unlöslich in Wasser. Das Insektizid ist nicht persistent im Boden mit einer Halbwertszeit von zwölf Tagen. Das Molekül enthält drei Stereozentren, was bedeutet, dass es acht verschiedene Stereoisomere gibt. Die Isomere haben eine unterschiedliche insektizide Aktivität. Im technischen Produkt wird ein Stereoisomerengemisch eingesetzt.[3]
Wirkungsweise
Wie die meisten Pyrethroide ist Cyphenothrin ein Kontaktgift, welches über die Körperoberfläche aufgenommen und im gesamten Körper verteilt wird. Es zählt zu den Nervengiften, dessen Wirkung auf der Öffnung der Natriumkanäle beruht. Dadurch strömen Na+-Ionen ungehindert in die Nervenzelle, wodurch es zu unkontrollierten Nervenimpulsen kommt. Dies führt zunächst zu Erregungszuständen mit Krämpfen, dann zu Koordinationsstörungen und schließlich zu einer Lähmung. Das Insekt ist wenige Minuten nach dem Kontakt mit Cyphenothrin bewegungsunfähig (Knock-down-Effekt).[8] Der Tod tritt erst nach einiger Zeit ein.
Einsatzgebiete
Cyphenothrin baut sich bei Licht schnell ab. Dadurch hat es in der Landwirtschaft keine Bedeutung. Jedoch wird es vor allem im häuslichen Bereich zur Schädlingsbekämpfung verwendet. So wird es zum Beispiel erfolgreich gegen den Befall durch die Deutsche Schabe angewandt.[9] Darüber hinaus wird Cyphenothrin bei Haushunden gegen Zecken und Flöhe verwendet[10][11], allerdings sind diese Präparate in Deutschland nicht zugelassen.
Handelsnamen
- Pflanzenschutz
- Gokilaht-S 5% EC
- Detmol-cap
- Aco.mix C 10 MC
- Tiermedizin
Einzelnachweise
- WHO: d,d,trans-CYPHENOTHRIN. (PDF) Abgerufen am 11. März 2019 (englisch).
- Eintrag zu Cyphenothrin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 16. April 2018.
- Eintrag zu Cyphenothrin in der Pesticide Properties DataBase (PPDB) der University of Hertfordshire, abgerufen am 11. März 2019.
- Für diesen Stoff liegt noch keine harmonisierte Einstufung vor. Wiedergegeben ist eine von einer Selbsteinstufung durch Inverkehrbringer abgeleitete Kennzeichnung von α-cyano-3-phenoxybenzyl 2,2-dimethyl-3-(2-methylprop-1-enyl)cyclopropanecarboxylate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 16. April 2018.
- Datenblatt Cyphenothrin PESTANAL, analytical standard bei Sigma-Aldrich, abgerufen am 27. April 2018 (PDF).
- Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 944 (eingeschränkte Vorschau in der Google-Buchsuche).
- Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 938 (eingeschränkte Vorschau in der Google-Buchsuche).
- Terence Roberts, D. H. Hutson: Metabolic pathways of agrochemicals. Royal Society of Chemistry, Cambridge 2007, ISBN 978-1-84755-137-5.
- Rina Tilak, V. K. Agrawal, J. Dutta: Field performance of cyphenothrin: an integrated insecticide strategy against German cockroaches (Dictyoptera: Blatellidae). In: Journal of Vector Borne Diseases. Band 42, Nr. 2, Juni 2005, S. 68–73, PMID 16161703.
- Katharine M. Case, Natalia M. Vega, Ramesh C. Gupta, Michelle A. Lasher, Terry D. Canerdy: Safety Evaluation of Parastar® Plus in Dogs and Assessment of Transferable Residue of Fipronil and Cyphenothrin from Dogs to Humans. In: Frontiers in Veterinary Science. Band 3, 2016, doi:10.3389/fvets.2016.00089.
- O. M. Germant, N. I. Shashina: [EFFECT OF PYRETHROIDS ON TAIGA TICKS (IXODES PERSULCATUS IXODIDAE)]. In: Meditsinskaia Parazitologiia I Parazitarnye Bolezni. Nr. 1, Januar 2016, S. 60–62, PMID 27029149.

