Tefluthrin
Tefluthrin ist ein Gemisch von zwei enantiomeren chemischen Verbindungen aus der Gruppe der Pyrethroide.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
-rel-Tefluthrine_Formulae_V.1.svg.png.webp) | |||||||||||||||||||
| 1:1-Gemisch (Racemat) der (1R,3R)-Form (oben) und der (1S,3S)-Form (unten) | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tefluthrin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C17H14ClF7O2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 418,73 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,48 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
156 °C bei 1 mmHg[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
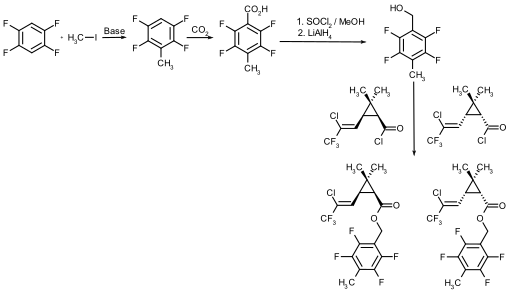
Die Synthese von Tefluthrin geht von zwei Vorstufen aus, die in zwei Synthesezweigen erhalten werden. Die Synthese der ersten Vorstufe erfolgt vom 1,2,4,5-Tetrafluorbenzol aus, welches über eine zweifache Metallierung mittels Butyllithium im ersten Schritt mit Methyliodid zum 1,2,4,5-Tetrafluortoluol und zweiten Schritt mit Kohlendioxid zur 4-Methyl-2,3,5,6-tetrafluorbenzoesäure umgesetzt wird.[6] Die Carbonsäure wird mit Thionylchlorid und Methanol intermediär über das Säurechlorid in den Methylester überführt, der dann mittels Lithiumaluminiumhydrid zum Vorstufe 1-Hydroxymethyl-4-methyl-2,3,5,6-tetrafluorbenzol reduziert wird.[6] Die zweite Vorstufe wird in einer mehrstufigen Synthese ausgehend vom 3,3-Dimethyl-4-pentensäureethylester erhalten.[7] Hier erfolgt zunächst durch die Umsetzung mit 1,1,1-Trichlor-2,2,2-trifluorethan in Gegenwart von Kupfer(I)-chlorid eine C-Kettenverlängerung und Einführung der Halogenfunktionen.[7] Bei der Umsetzung des resultierenden 4,6,6-Trichlor-7,7,7-trifluor-3,3-dimethylheptansäureethylesters mit Natriumethanolat wird durch Dehydrohalogenierungsreaktionen der Cyclopropanring und die Doppelbindung gebildet.[7] Der 3-[2-Chlor-3,3,3-trifluorpropenyl]-2,2-dimethylcyclopropancarbonsäureethylester fällt als racemisches cis-/trans-Gemisch an, woraus das interessierende trans-Isomer [Racemat, also 1:1-Gemisch aus (1S,3S)- und (1R,3R)-Form] mittels Destillation gewonnen wird.[7] Der Ester wird dann mit Natronlauge verseift und mit Thionylchlorid zur Säurechloridvorstufe umgesetzt.[7] Beide Vorstufen ergeben abschließend in einer Veresterungsreaktion die Zielverbindung ebenfalls als 1:1-Enantiomerengemisch aus (1S,3S)- und (1R,3R)-Form.[2][8]
Eigenschaften
Tefluthrin ist ein farbloser Feststoff, der praktisch unlöslich in Wasser ist. Das technische Produkt ist ein Racemat des (Z)-(1R, 3R)- und des (Z)-(1S, 3S)-Enantiomers. Es ist stabil unter neutralen Bedingungen.[1][9]
Verwendung
Tefluthrin wird als Insektizid gegen Bodenschädlinge (z. B. bei Zuckerrüben und Mais) verwendet.[1][9] Es wurde zuerst 1986 in Belgien zugelassen[10] und beeinflusst die Nervensignalübertragung der Natriumkanäle.[11] Im Gegensatz zu anderen Pyrethroiden wirkt Tefluthrin auch über den Boden.[9]
Regulierung
EU
Die derzeit gültige Zulassung läuft zum 31. Dezember 2021 aus. Auf nationaler Ebene ist Tefluthrin in 19 EU-Staaten zugelassen. Die Erlaubte Tagesdosis und die Akute Referenzdosis betragen 0,005 und die Annehmbare Anwenderexposition 0,0015 Milligramm pro Kilogramm Körpergewicht und Tag.[12]
Die EU-Kommission entschied im Dezember 2008 nach der Rücknahme eines Zulassungsantrags, Tefluthrin nicht in die Liste der Wirkstoffe in Anhang I der Richtlinie 91/414/EWG aufzunehmen. Der Wirkstoff wurde schließlich mit Wirkung zum 1. Januar 2012 für Anwendungen als Insektizid zugelassen.[13]
In Deutschland ist Force 20 CS von Syngenta das derzeit einzige zugelassene Pflanzenschutzmittel mit dem Wirkstoff Tefluthrin.[14] Das BVL verlängerte die seit 6. Dezember 2000 gültige Zulassung mit Stand 20. Februar 2014 bis 31. Juli 2014.[15] Force 20 CS ist ein Beizmittel für Zucker- und Futterrüben gegen den Moosknopfkäfer.[16] Das BVL hatte in der Vergangenheit außerdem dem Pflanzenschutzmittel Force 1,5 G zur Anwendung bei Mais gegen den Westlichen Maiswurzelbohrer Ausnahmegenehmigungen erteilt, die letzte lief am 28. Juli 2012 aus.[17][18]
In Österreich und der Schweiz sind Pflanzenschutzmittel (z. B. Force 20 CS) mit diesem Wirkstoff zur Saatgutbeizung bei Zucker- und Futterrüben zugelassen.[12]
Einzelnachweise
- EFSA: Conclusion on the peer review of the pesticide risk assessment of the active substance tefluthrin, 2010. doi:10.2903/j.efsa.2010.1709
- Eintrag zu Tefluthrin in der Hazardous Substances Data Bank, abgerufen am 14. August 2012 (online auf PubChem).
- Eintrag zu tefluthrin (ISO); 2,3,5,6-tetrafluoro-4-methylbenzyl (1RS,3RS)-3-[(Z)-2-chloro-3,3,3-trifluoroprop-1-enyl]-2,2-dimethylcyclopropanecarboxylate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 30. Dezember 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eintrag zu Tefluthrin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 30. Dezember 2019. (JavaScript erforderlich)
- Datenblatt Tefluthrin bei Sigma-Aldrich, abgerufen am 30. Dezember 2019 (PDF).
- Patent US4370346 Imperial ChemicalIndustries 1981.
- Patent US4332815 FMC Corporation 1980.
- Thomas A. Unger: PESTICIDE SYNTHESIS HDBK. William Andrew, 1996, ISBN 0-8155-1853-6, S. 959 (eingeschränkte Vorschau in der Google-Buchsuche).
- M. Bahadir, H. Parlar, Michael Spiteller: Springer Umweltlexikon. Gabler Wissenschaftsverlage, 2000, ISBN 3-540-63561-0, S. 1151 (eingeschränkte Vorschau in der Google-Buchsuche).
- UK Poison Information Documents (UKPID) für Tefluthrin, abgerufen am 9. Dezember 2014.
- Terry R. Roberts, David H. Hutson, Philip W. Lee, Peter H. Nicholls: Metabolic Pathways of Agrochemicals: Part 2: Insecticides and Fungicides. Royal Society of Chemistry, 1999, ISBN 0-85404-499-X, S. 714 (eingeschränkte Vorschau in der Google-Buchsuche).
- Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Tefluthrin in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 13. März 2016.
- Durchführungsverordnung (EU) Nr. 800/2011 der Kommission vom 9. August 2011 zur Genehmigung des Wirkstoffs Tefluthrin... (PDF)
- BVL: Verzeichnis zugelassener Pflanzenschutzmittel. Abgerufen am 25. Februar 2014.
- BVL: Verlängerungen von Zulassungen (letzte Änderung: 20. Februar 2014). Abgerufen am 25. Februar 2014.
- proplanta: Pflanzenschutzmittel: Force 20 CS (024006-00). Abgerufen am 25. Februar 2014.
- BVL - Presse- und Hintergrundinformationen - BVL genehmigt Pflanzenschutzmittel zur Bekämpfung des Maiswurzelbohrers. Abgerufen am 21. Oktober 2019.
- BVL: Zulassungen für Notfallsituationen (Memento vom 16. September 2014 im Internet Archive). Abgerufen am 21. Oktober 2019.

