Mangan(II)-chlorid
Mangan(II)-chlorid ist ein schwach rosarotes Pulver. Die Verbindung besteht aus Mangan und Chlor und liegt gewöhnlich als Tetrahydrat oder auch in wasserfreier Form vor.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
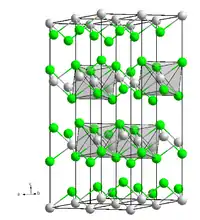 | |||||||||||||||||||
| _ Mn2+ _ Cl− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Mangan(II)-chlorid | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Verhältnisformel |
| ||||||||||||||||||
| Kurzbeschreibung |
weiß bis helllila (wasserfrei) oder blassrosafarbener (Tetrahydrat), geruchloser Feststoff[2] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | |||||||||||||||||||
| Aggregatzustand |
fest[2] | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
1190 °C[2] | ||||||||||||||||||
| Löslichkeit |
in Wasser:* 723 g·l−1 (wasserfrei, 20 °C)[2]* 1200 g·l−1 (Dihydrat, 20 °C)[2]* 1980 g·l−1 (Tetrahydrat, 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
0,5 mg·m−3[2] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Gewinnung und Darstellung
Mangan(II)-chlorid-Tetrahydrat lässt sich durch Reaktion von Mangan, Mangan(II)-carbonat oder Mangandioxid mit konzentrierter Salzsäure herstellen:
Beim Erhitzen im trockenen Chlorwasserstoffstrom kann aus dem Tetrahydrat das wasserfreie MnCl2 erhalten werden.
Eigenschaften
_chloride_tetrahydrate.jpg.webp)
Mangan(II)-chlorid bildet blassrosarote, hygroskopische Kristalle. Es ist sehr gut löslich in Wasser und Ethanol. In Lösung ist die Farbe auf das Hexaaquamangan(II)-Kation, [Mn(H2O)6]2+, zurückzuführen. Das Tetrahydrat liegt in Form eines oktaedrischen Komplexes vor, in dem die beiden Chlorid-Liganden cis-ständig sind. Mit einem Überschuss an Chloridionen bilden sich die komplexen Anionen MnCl42− (Tetrachloromanganat(II), tetraedrisch) bzw. MnCl64− (Hexachloromanganat(II), oktaedrisch).
Verwendung
Mangan(II)-chlorid wird zur Herstellung von Manganbraun Mn(O)OH und als Ausgangsstoff zur Synthese Mangan-haltiger Katalysatoren verwendet.
Einzelnachweise
- Eintrag zu MANGANESE CHLORIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. September 2021.
- Eintrag zu Mangan(II)-chlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)



