Imidacloprid
Imidacloprid ist ein systemisches Insektizid aus der Gruppe der Neonicotinoide. Die Substanz wurde 1985 in den Labors der Bayer AG erstmals synthetisiert. Bayer stellt Imidacloprid seit Anfang der 1990er-Jahre im industriellen Maßstab her, es wird in etwa 120 Ländern der Erde eingesetzt. Einige Experten nehmen an, dass Imidacloprid derzeit das weltweit meistverwendete Insektizid ist.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
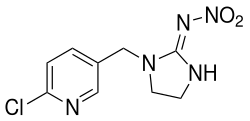 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Imidacloprid | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C9H10ClN5O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farbloses oder beiges Pulver mit schwachem Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 255,66 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
1,54 g·cm−3 [2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Gewinnung und Darstellung
Imidacloprid kann in einer vierstufigen Synthese hergestellt werden. Ausgehend vom 6-Chlorpyridin-3-carbaldehyd wird im ersten Schritt mit Ethylendiamin das entsprechende Azomethin erhalten, welches anschließend mit Natriumborhydrid reduziert wird. Der Ringschluss zur Imidazolidinsubstruktur erfolgt mit Bromcyan. Im letzten Schritt führt eine Nitrierung mit Salpetersäure zur Zielverbindung.[6]
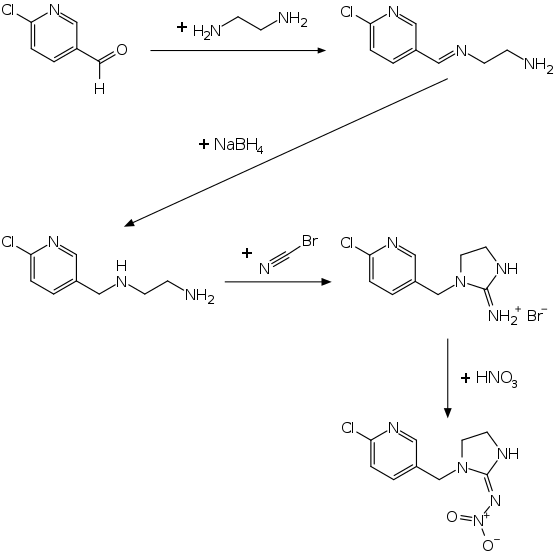
Es sind auch alternative Synthesevarianten wie zum Beispiel durch Reaktion von Ethylendiamin mit Bromcyan und Salpetersäure zu 2-Nitroimin-imidazolidin und dessen Reaktion mit 2-Chlor-5-chlormethylpyridin bekannt.[6]
Eigenschaften
Wie andere Nitroguanidine auch, sind für das Imidacloprid zwei Tautomere bekannt. Kristallstrukturanalysen zeigen, dass Imidacloprid, wie die meisten Nitroguanidine, in der Struktur 2 vorliegt.[7]

Imidacloprid kann in zwei polymorphen Kristallformen auftreten, die sich hinsichtlich des Schmelzpunktes unterscheiden.[8][9] Die Form I schmilzt bei 145,2 °C, die Form II bei 137,7 °C.[8] Beide Formen bilden ein monoklines Kristallgitter, wobei Form I in der Raumgruppe P21/n und Form II in der Raumgruppe P21/c vorliegt. Aus den kristallographischen Untersuchungen leiten sich mit 1,5125 g·cm−3 für Form I und 1,524 g·cm−3 für Form II leicht unterschiedliche Dichten ab.[8] Über Löslichkeitsmessungen bei verschiedenen Temperaturen konnte ein thermodynamischer Umwandlungspunkt zwischen beiden Formen von 53,8 °C ermittelt werden. Die beiden Formen stehen enantiotrop zueinander.[8]
Wirtschaft
Der jährliche Absatz in Deutschland liegt im Bereich von 25–100 t, über 1000 t werden exportiert. Der erzielte Umsatz liegt bei etwa 500–600 Millionen Euro, damit ist Imidacloprid das erfolgreichste Produkt von Bayer CropScience. Handelsnamen für das Insektizid sind Admire, Confidor (in Europa), Connect, Evidence, Gaucho (Beize), Leverage, Muralla, Provado und Trimax.
Wirkungsweise
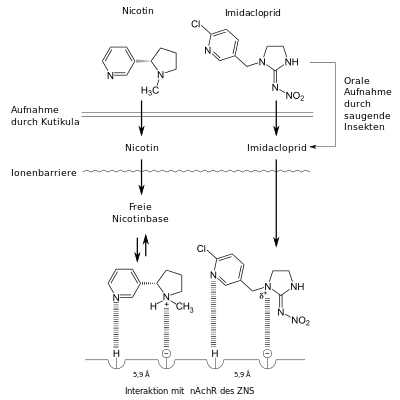
Imidacloprid ist ein systemisches Insektizid, das als Kontakt- wie auch Fraßgift wirken kann. Es wird gut über die Wurzeln aufgenommen und in die Blätter transportiert, die dann vor beißenden und saugenden Insekten geschützt sind. Wird es direkt auf die Blätter ausgebracht, verteilt es sich zwischen Blattober- und Blattunterseite und wird auch zu neugebildeten Blättern hin weitertransportiert. Da Imidacloprid in der Pflanze nur langsam abgebaut wird, hält seine Wirkung längere Zeit an.
Beim Insekt wirkt Imidacloprid wie Acetylcholin am nikotinischen Acetylcholinrezeptor der Nervenzellen, es wird aber nicht durch das Enzym Acetylcholinesterase abgebaut. Durch den ausgelösten Dauerreiz wird die chemische Signalübertragung gestört.
Verwendung
Pflanzenschutz
Imidaclopridhaltige Präparate sind in verschiedenen Formen erhältlich. Sie können beispielsweise als Suspension, wasserlösliches Konzentrat, Granulat, Stäbchen (für Topfpflanzen), Schlämmpulver (zur Saatgutbehandlung) oder Spray in den Handel kommen. Imidacloprid ist häufig der einzige Wirkstoff, es waren in der Vergangenheit auch Kombinationspräparate mit dem Pyrethroid Tefluthrin, dem Carbamat Methiocarb, anderen insektiziden Wirkstoffen und mit Nährstoffen im Handel.
Imidacloprid wird bzw. wurde zur Saatgutbeizung bei Zucker- und Futterrüben, Getreide, Kartoffeln, Mais, Zwiebeln und dem Ölkürbis eingesetzt. Hier wirkt es beispielsweise gegen Pflanzenläuse, Drahtwürmer, Kartoffelkäfer sowie die Frit-, Zwiebel- und Rübenfliege.
In Haus- u. Kleingärten wird Imidacloprid gegen Pflanzenläuse (einschließlich der Weißen Fliege) und Thripse eingesetzt.
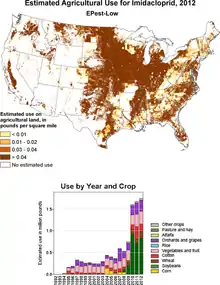
2012 wurden in den USA etwa 750 t Imidacloprid verwendet, davon knapp die Hälfte im Sojaanbau.
Tiermedizin
Imidacloprid kann seit 1996 gegen Tierläuse und Flöhe bei Hunden und Katzen verwendet werden. Handelsnamen sind Advantage, Clearspot (verkehrsfähig bis 23. Januar 2017) und Midaspot. Zudem ist es in Kombinationspräparaten mit Permethrin (Advantix und Ataxxa), mit Moxidectin (Advocate und Prinovox) und mit Flumethrin (Seresto) enthalten.
Biozidprodukte
Gemäß Richtlinie 98/8/EG[10] vom 16. Februar 1998 sollten nur noch solche Biozidprodukte zugelassen sein, deren Wirkstoffe in die Anhänge I, IA und IB besagter Richtlinie (für die jeweils definierte Produktart) aufgenommen wurden. Weiterhin zugelassen blieb dabei gemäß Übergangsregelung (Art. 16 Abs. 1 der Richtlinie 98/8/EG) aber auch das Inverkehrbringen von Biozidprodukten mit sogen. „alten Wirkstoffen“, also solchen, die zwar nicht in den Anhängen der Richtlinie 98/8/EG aufgeführt sind, aber mit Stichdatum 14. Mai 2000 bereits im Verkehr waren.
Gemäß Verordnung (EG) 1896/2000 vom 7. September 2000[11] mussten Hersteller, die die Aufnahme eines „alten Wirkstoffs“ in die Anhänge I, IA und IB beantragen wollten, den betreffenden Wirkstoff bis zum 28. März 2002 zur Notifizierung für die entsprechende Produktart gemeldet haben. Diese Frist wurde mit Verordnung (EG) 1687/2002 vom 25. September 2002[12] bis zum 31. Januar 2003 verlängert. Die „notifizierten Wirkstoffe“ durften folgend bis zum definitiven Entscheid über Aufnahme oder Nichtaufnahme in Anhang I, IA und IB EU-Richtlinie 98/8/EG weiterhin in Verkehr bleiben.
Der Wirkstoff Imidacloprid wurde folgend für die Produktart 18 (Insektizide) in die Liste der notifizierten Wirkstoffe aufgenommen.[13]
Mit der Verordnung (EG) 1451/2007 vom 4. Dezember 2007[14] über die zweite Phase des Zehn-Jahres-Arbeitsprogramms über das Inverkehrbringen von Biozid-Produkten wurde der Wirkstoff Imidacloprid in die abschließende Liste (Anhang II) der im Rahmen des Prüfprogramm zu untersuchenden Wirkstoffe aufgenommen.
Mit Erlass der Richtlinie 2011/69/EU vom 1. Juli 2011[15] liegt ein Entscheid vor, den Wirkstoff Imidacloprid ab 1. Juli 2013 in die entsprechende Liste (Anhang I der Richtlinie 98/8/EG) für die Produktart 18 (Insektizide) aufzunehmen. Die Abgabe von Biozidprodukten, die den Wirkstoff Imidacloprid enthalten, war in der EU (die Schweiz hat diese Bestimmung übernommen) für die Produktart 18 (Insektizide) weiterhin erlaubt.
Toxizität und Ökotoxizität
Säugetiere
Die akute Toxizität von Imidacloprid ist für Säugetiere gering, an männlichen Ratten wurde als LD50 424 mg/kg Körpergewicht ermittelt. Bei dreimonatigen Fütterungstests betrug die NOEC (no observed effect concentration) bei Rattenmännchen 150, bei Rattenweibchen 600 und bei Hunden 200 mg/kg Futter. Imidacloprid hat keine Reizwirkung auf Haut oder Augen. Die Substanz hat vermutlich eine schwach teratogene und mutagene Wirkung. Sie gilt als nicht krebserregend. Über den Magen-Darm-Trakt wird Imidacloprid schnell in den Körper aufgenommen. Innerhalb von 48 Stunden wird es im Körper zu ca. 80 % abgebaut und zu ca. 20 % unverändert ausgeschieden.
Konzentrationen über 1 µM Imidacloprid lösten bei Gehirnzellen neugeborener Ratten Nervenreize aus. Möglicherweise hat Imidacloprid ähnlich wie Nikotin Auswirkungen auf die Entwicklung des Nervensystems bei Menschen und Tieren.[16] Die Wirkung des Imidacloprid-Abbauprodukts Desnitro-Imidacloprid auf den nikotinischen Acetylcholinrezeptor von Nervenzellen ist ähnlich stark wie die Wirkung von Nikotin und damit deutlich stärker als die von Imidacloprid.[17]
Fische
Für Wasserlebewesen ist Imidacloprid mäßig giftig, die letale Konzentration im 96-Stunden-Test liegt für die Regenbogenforelle bei 211 mg/L. Beim Dauertest mit Regenbogenforellen über 21 Tage war unterhalb einer Konzentration von 28,5 mg/L kein Effekt mehr zu beobachten.
Eine Exposition mit Imidacloprid von Zebrabärbling und Medaka führte zu Fehlbildungen, Läsionen und einem reduzierten Wachstum.[18][19]
Wirbellose
Wasserflöhe (Daphnia magna) sind empfindlicher, nach 48 Stunden führten 85 mg/L dazu, dass die Hälfte der Daphnien ihre Ruderbewegungen einstellte. Über 21 Tage hinweg traten erst bei Konzentrationen unterhalb 1,8 mg/L keinerlei Wirkungen bei Daphnien mehr auf. Für Gewässerinsekten hingegen ist Imidacloprid hochtoxisch. So liegen die akut toxischen Konzentrationen für z. B. Stein- und Eintagsfliegenlarven im Bereich von wenigen µg/L.[20]
Vögel
Imidacloprid ist giftig für Vögel, die letale Dosis für Kanarienvögel und Tauben liegt im Bereich von 25–50 mg/kg Körpergewicht. Wenn Vögel gebeiztes Saatgut von den Feldern aufpicken, besteht für sie die Gefahr akuter Vergiftungen.
Nach einer Anwendung von Imidacloprid bei Straßenbäumen im kalifornischen Modesto starb eine größere Anzahl von Goldzeisigen. Sie hatten belastete Baumsamen gefressen. Die Imidacloprid-Konzentration beim Inhalt von Kropf und Magen lag im Mittel bei 4,8 mg/kg, das Lebergewebe enthielt 3,9 mg/kg.[21]
In den Niederlanden zeigte die Konzentration von Imidacloprid in Oberflächengewässern einen statistischen Zusammenhang mit dem Rückgang mehrerer insektenfressender Vogelarten seit Mitte der 1990er Jahre. Bezüglich eines möglichen Kausalzusammenhangs spekulieren die Autoren, dass der Einsatz von Imidacloprid die Nahrungsgrundlage dieser Vogelarten dezimiert habe.[22]
Bienen
Eine 2011 publizierte Meta-Analyse von 14 Studien bezüglich der Wirkung von Imidacloprid auf Honigbienen unter Labor- und semi-Feldbedingungen ergab, dass die unter Feldbedingungen erwartbaren Dosierungen keine letalen Effekte haben würden, jedoch die Leistung der Bienen um sechs bis zwanzig Prozent verringern würden.[23][24]
Eine Systematische Übersichtsarbeit aus dem Jahr 2012 stellte fest, dass viele Laborstudien letale und subletale Effekte von Neonicotinoiden auf das Futterbeschaffungs-, Lern- und Erinnerungsvermögen gezeigt hätten, in Studien unter realistischen Feldbedingungen mit entsprechend niedrigeren Dosen hingegen keine Auswirkungen nachgewiesen worden seien.[25]
Eine ebenfalls 2012 veröffentlichte Übersichtsarbeit konnte die Hypothese eines Völkerkollaps durch Neonicotinoidrückstände in Pollen und Nektar auf Basis der Bradford-Hill-Kriterien vorläufig nicht stützen, da erhebliche Wissenslücken bestünden.[26]
Laut einer 2014 veröffentlichten Übersichtsarbeit kann aufgrund von Wissenslücken bisher nicht auf einen alleinigen Kausalzusammenhang zwischen der Nutzung von Neonicotinoiden und Bienensterben geschlossen werden. Das Bienensterben sei bereits vor der breiten Verwendung von Neonicotinoiden aufgetreten und es liege eine schwache geografische Korrelation zwischen Neonicotinoidnutzung und Bienensterben vor.[27]
Eine ebenfalls 2014 erschienene Übersichtsarbeit zu Neonicotinoiden verglich eine Reihe jüngerer Laborstudien mit Feldstudien. Während Laborstudien subletale Effekte gefunden hätten, seien diese Effekte in Feldstudien nicht nachgewiesen worden. Die Autoren kommen zu dem Schluss, dass die Laborstudien die Konzentration, die Fütterungsdauer und die Futterwahl der Bienen überschätzt haben.[28]
Eine im August 2015 veröffentlichte systematische Übersichtsarbeit (Lundin et al., 2015) untersuchte die Forschungsmethoden und -lücken zu Neonicotinoiden und Bienen anhand von 216 bis Juni 2015 veröffentlichten Einzelstudien. Die Autoren kamen zu dem Schluss, dass trotz zahlreicher Forschungsaktivitäten noch erhebliche Wissenslücken bestehen. Die meisten Studien beschäftigten sich mit Europa und Nordamerika sowie einigen wenigen Nutzpflanzen (Mais, Raps, Sonnenblume) und Spezies (hauptsächlich Apis mellifera), obwohl die Zusammenhänge in anderen Regionen, Nutzpflanzen und Spezies möglicherweise anders geartet seien. Hinzu komme trotz vieler Laborstudien ein Mangel an Feldstudien, und bei Feldstudien habe man vor allem die Exposition der Bienen hinsichtlich Neonicotinoiden untersucht, Erkenntnisse zu den Auswirkungen dieser Exposition seien jedoch unzureichend vorhanden. Des Weiteren konzentrierte sich die Forschung bisher auf individuelle Bienen, wenngleich die Effekte auf Bienenkolonien anders ausfallen können. Wenngleich es Hinweise auf Interaktionen zwischen unterschiedlichen Insektizidklassen sowie synergistische Insektizid-Pathogen-/Parasiteninteraktionen gebe, seien letztere unter realistischen Feldbedingungen möglicherweise überschätzt worden. Auch müsse die Forschung noch aufklären, wie relevant Neonicotinoide im Vergleich zu anderen möglichen Ursachen von Bienensterben sind.[29]
Umweltverhalten
Der Wirkstoff wird in der Umwelt nur langsam abgebaut. Die Abbaugeschwindigkeit ist von der Intensität des Bodenlebens abhängig. Bei einer Untersuchung war auf bewachsenem Boden innerhalb von 48 Tagen die Hälfte des ausgebrachten Imidacloprids zersetzt, auf unbewachsenem Boden war dieser Zustand erst nach 190 Tagen erreicht. Als Metabolit wird 6-Chlornicotinsäure gebildet.[2]
Regulierung
EU
In der EU und 25 Mitgliedsstaaten war die Anwendung von Imidacloprid zugelassen, aber aufgrund von Risiken für Honigbienen ab dem 1. Dezember 2013 für zunächst zwei Jahre für mehrere wichtige Verwendungen, wie der Saatgutbeizung von Mais und Raps, stark eingeschränkt (siehe Neonicotinoide#EU-Beschränkungen ab 2013). Die meisten Zulassungen imidaclopridhaltiger Beizmittel gab es für Zuckerrübe, Mais, Kartoffel, Raps und Getreide, neben einer Reihe weiterer Pflanzenarten.[30] Ein am 28. Februar 2018 veröffentlichtes Gutachten der EFSA bestätigte abschließend die Risiken für Wild- und Honigbienen bei Freilandanwendungen. Dieses Gutachten sollte als Grundlage für weitere Zulassungsentscheidungen bzw. -einschränkungen dienen.[31][32]
Daraufhin beschloss am 27. April 2018 die EU-Kommission in einer Abstimmung ein Verbot für Freilandkulturen.[33] Mit dem Erlass der Durchführungsverordnung (EU) Nr. 783/2018[34] vom 29. Mai 2018 wurde die Verwendung von mit Imidacloprid behandeltem Saatgut in Freilandkulturen in der EU verboten. Im August 2018 wurde die Zulassung für die Verwendung im Freiland zum 18. September 2018 widerrufen. Pflanzenschutzmittel mit diesem Wirkstoff dürfen nur noch in dauerhaft errichteten Gewächshäusern und zur Behandlung von Saatgut, das zur Ausbringung im Gewächshaus bestimmt ist, angewendet werden. Behandeltes Saatgut, welches für die Aussaat im Freiland vorgesehen ist, durfte bis zum 18. Dezember 2018 ausgesät werden.[35] Danach wurden von einigen EU-Mitgliedstaaten Notfallzulassungen für den Zuckerrübenanbau erteilt.[36][37] In Deutschland und der Schweiz wurden Alternativen zugelassen.[38][39] In der Europäischen Union wurde die Zulassung von Imidacloprid zum 1. Dezember 2020 aufgehoben.[40] In Bezug auf das Verbot klagte Bayer vor dem Europäischen Gerichtshof, welcher das Verbot jedoch im Mai 2021 bestätigte.[41]
Die Erlaubte Tagesdosis (ADI) beträgt 0,06, die Akute Referenzdosis (ARfd) 0,08 und die Annehmbare Anwenderexposition 0,08 Milligramm pro Kilogramm Körpergewicht und Tag.[40] Die Europäische Behörde für Lebensmittelsicherheit schlug wegen möglicher Auswirkungen auf das sich entwickelnde Nervensystem im Dezember 2013 vor, die Akute Referenzdosis und die Annehmbare Anwenderexposition von 0,08 auf 0,06 mg/kg Körpergewicht zu senken. Die Erlaubte Tagesdosis wurde als angemessen erachtet, um Schutz im Hinblick auf mögliche entwicklungsneurotoxische Auswirkungen zu gewährleisten.[42]
Schweiz
In der Schweiz wurde die Bewilligung für Imidacloprid in Pflanzenschutzmitteln beendet. Die Ausverkaufsfrist läuft noch bis am 31. Dezember 2021, die Aufbrauchsfrist endet am 1. Juni 2022.[40] Als Alternativen werden derzeit (2021) Movento SC und Gazelle SG verwendet.[43]
Literatur
- Caroline Cox: Insecticide Factsheet Imidacloprid. Journal of Pesticide Reform, Frühjahr 2001, Bd. 21, Nr. 1.
Weblinks
- EXTOXNET: Pesticide Information Profile Imidacloprid (englisch)
- Eintrag zu Imidacloprid bei Vetpharm
Einzelnachweise
- Eintrag zu Imidacloprid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 25. Januar 2022. (JavaScript erforderlich)
- EXTOXNET: Pesticide Information Profile Imidacloprid.
- Eintrag zu Imidacloprid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. Juni 2021.
- Eintrag zu imidacloprid (ISO); 1-(6-chloropyridin-3-ylmethyl)-N-nitroimidazolidin-2-ylidenamine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 11. Dezember 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Datenblatt Imidacloprid bei Sigma-Aldrich, abgerufen am 13. Mai 2017 (PDF).
- Thomas A. Unger: Pesticide synthesis handbook. 1996, ISBN 978-0-8155-1401-5, S. 448 (eingeschränkte Vorschau in der Google-Buchsuche).
- Roberto Fusetto, Jonathan M. White, Craig A. Hutton, Richard A. J. O'Hair: Structure of olefin–imidacloprid and gas-phase fragmentation chemistry of its protonated form. In: Organic and Biomolecular Chemistry. Band 14, Nr. 5, 27. Januar 2016, ISSN 1477-0539, S. 1715–1726, doi:10.1039/C5OB02371H.
- Jing Zhao; Mingliang Wang; Baoli Dong; Qi Feng; Chunxiang Xu: Monitoring the Polymorphic Transformation of Imidacloprid Using in Situ FBRM and PVM in Org. Process Res. Dev. 17 (2013) 375–381, doi:10.1021/op300320a.
- Patent US9212162B1: Process for the preparation of polymorphs of imidacloprid. Angemeldet am 24. Juni 2014, veröffentlicht am 15. Dezember 2015, Anmelder: Rotam Agrochem Int Co Ltd, Erfinder: James Timothy Bristow, Yifan Wu.
- EU: Richtlinie 98/8/EG vom 16. Februar 1998 über das Inverkehrbringen von Biozid-Produkten (PDF) Amtsblatt der Europäischen Gemeinschaften L 123/1 vom 24. April 1998
- EU: Verordnung (EG) 1896/2000 vom 7. September 2000 über die erste Phase des Programms gemäß Artikel 16 Abs. 2 der Richtlinie 98/8/EG über Biozid-Produkte (PDF) Amtsblatt der Europäischen Gemeinschaften L 228/6 vom 8. September 2000
- EU: Verordnung (EG) 1687/2002 vom 25. September 2002 über eine zusätzliche Frist für die Notifizierung bestimmter Wirkstoffe (PDF) Amtsblatt der Europäischen Gemeinschaften L 258/15 vom 26. September 2002
- EU: Verordnung (EG) 2032/2003 vom 4. November 2003 über die zweite Phase des Zehn-Jahres-Arbeitsprogramms über das Inverkehrbringen von Biozid-Produkten (PDF) Amtsblatt der Europäischen Gemeinschaften L 307/1 vom 24. November 2003
- EU: Verordnung (EG) 1451/2007 über die zweite Phase des Zehn-Jahres-Arbeitsprogramms über das Inverkehrbringen von Biozid-Produkten (PDF) Amtsblatt der Europäischen Gemeinschaften L 325/3 vom 11. Dezember 2007
- EU: Richtlinie 2011/69/EU vom 1. Juli 2011 zur Änderung der Richtlinie 98/8/EG zwecks Aufnahme von Imidacloprid in Anhang I (PDF) Amtsblatt der Europäischen Gemeinschaften L 243/16 vom 1. Juli 2011
- Junko Kimura-Kuroda, Yukari Komuta, Yoichiro Kuroda, Masaharu Hayashi, Hitoshi Kawano: Nicotine-Like Effects of the Neonicotinoid Insecticides Acetamiprid and Imidacloprid on Cerebellar Neurons from Neonatal Rats. In: PLoS ONE. Band 7, Nr. 2, 2012, doi:10.1371/journal.pone.0032432.
- Dominik Loser, Karin Grillberger, Maria G. Hinojosa, Jonathan Blum, Yves Haufe, Timm Danker, Ylva Johansson, Clemens Möller, Annette Nicke, Susanne H. Bennekou, Iain Gardner, Caroline Bauch, Paul Walker, Anna Forsby, Gerhard F. Ecker, Udo Kraushaar, Marcel Leist: Acute effects of the imidacloprid metabolite desnitro-imidacloprid on human nACh receptors relevant for neuronal signaling. In: Archives of Toxicology. Band 95, 10. Oktober 2021, S. 3695–3716, doi:10.1007/s00204-021-03168-z.
- Stephanie Schnydrig: Nervengifte schädigen Wasserorganismen anders als erwartet. In: eawag.ch. 13. Juni 2019, abgerufen am 17. Juli 2019.
- Caroline Vignet, Tiziana Cappello, Qiuguo Fu, Kévin Lajoie, Giuseppe De Marco, Christelle Clérandeau, Hélène Mottaz, Maria Maisano, Juliane Hollender, Kristin Schirmer, Jérôme Cachot: Imidacloprid induces adverse effects on fish early life stages that are more severe in Japanese medaka (Oryzias latipes) than in zebrafish (Danio rerio). In: Chemosphere. 225, 2019, S. 470, doi:10.1016/j.chemosphere.2019.03.002.
- Francisco Sánchez-Bayo, Koichi Goka, Daisuke Hayasaka: Contamination of the Aquatic Environment with Neonicotinoids and its Implication for Ecosystems. In: Frontiers in Environmental Science. Band 4, 2016, ISSN 2296-665X, doi:10.3389/fenvs.2016.00071.
- Krysta H. Rogers, Stella McMillin, Katie J. Olstad, Robert H. Poppenga: Imidacloprid poisoning of songbirds following a drench application of trees in a residential neighborhood in California, USA. In: Environmental Toxicology and Chemistry. 2019, doi:10.1002/etc.4473.
- Caspar A. Hallmann, Ruud P. B. Foppen, Chris A. M. van Turnhout, Hans de Kroon, Eelke Jongejans: Declines in insectivorous birds are associated with high neonicotinoid concentrations. In: Nature. 9. Juli 2014, doi:10.1038/nature13531.
- James E. Cresswell: A meta-analysis of experiments testing the effects of a neonicotinoid insecticide (imidacloprid) on honey bees. In: Ecotoxicology. Band 20, Nr. 1, 2011, S. 149–157, doi:10.1007/s10646-010-0566-0.
- Abschlussbericht Beizung und Bienenschäden. Ministerium für Ernährung und Ländlichen Raum Baden-Württemberg, 17. Dezember 2008.
- T. Blacquière, G. Smagghe, CA. van Gestel, V. Mommaerts: Neonicotinoids in bees: a review on concentrations, side-effects and risk assessment. In: Ecotoxicology. Band 21, Nr. 4, 2012, S. 973–992, doi:10.1007/s10646-012-0863-x.
- James E Cresswell, Nicolas Desneux, Dennis van Engelsdorp: Dietary traces of neonicotinoid pesticides as a cause of population declines in honey bees: an evaluation by Hill’s epidemiological criteria. In: Pest Management Science. Band 68, Nr. 6, 2012, S. 819–827, doi:10.1002/ps.3290.
- H. Charles J. Godfray, Tjeerd Blacquière, Linda M. Field, Rosemary S. Hails, Gillian Petrokofsky, Simon G. Potts, Nigel E. Raine, Adam J. Vanbergen, Angela R. McLean: A restatement of the natural science evidence base concerning neonicotinoid insecticides and insect pollinators. In: Proceedings of the Royal Society B. Band 281, Nr. 1786, 2014, S. 20140558, doi:10.1098/rspb.2014.0558.
- Norman L Carreck, Francis L W Ratnieks: The dose makes the poison: have “field realistic” rates of exposure of bees to neonicotinoid insecticides been overestimated in laboratory studies? In: Journal of Apicultural Research. Band 53, Nr. 5, 2014, S. 607–614, doi:10.3896/IBRA.1.53.5.08.
- Ola Lundin, Maj Rundlöf, Henrik G. Smith, Ingemar Fries, Riccardo Bommarco: Neonicotinoid Insecticides and Their Impacts on Bees: A Systematic Review of Research Approaches and Identification of Knowledge Gaps. In: PLOS One. 27. August 2015, S. 1–20, doi:10.1371/journal.pone.0136928.
- EFSA: Conclusion on the peer review of the pesticide risk assessment for bees for the active substance imidacloprid. In: EFSA Journal. Band 11, Nr. 1, 2013, S. 3068, doi:10.2903/j.efsa.2013.3068.
- Evaluation of the data on clothianidin, imidacloprid and thiamethoxam for the updated risk assessment to bees for seed treatments and granules in the EU. European Food Safety Authority, abgerufen am 19. März 2018 (englisch).
- EFSA: Q&A: Schlussfolgerungen zu Neonicotinoiden 2018, 28. Februar 2018.
- Kampf gegen das Bienensterben: EU verbietet Neonikotinoide auf Äckern (Memento vom 24. Juli 2018 im Internet Archive) br.de, 27. April 2018.
- EU: Verordnung (EU) 2018/783 der Kommission vom 29. Mai 2018 zur Änderung der Durchführungsverordnung (EU) Nr. 540/2011 hinsichtlich der Bedingungen für die Genehmigung des Wirkstoffs Imidacloprid
- Bundesamt für Verbraucherschutz und Lebensmittelsicherheit: BVL – Fachmeldungen – Widerruf der Zulassung von Pflanzenschutzmitteln mit den neonikotinoiden Wirkstoffen Clothianidin, Imidacloprid und Thiamethoxam zum 18. September 2018, abgerufen am 8. Dezember 2018.
- Pestizide: EFSA überprüft Notfallanwendung von Neonicotinoiden. Europäische Behörde für Lebensmittelsicherheit, 8. Dezember 2020, abgerufen am 28. Februar 2021.
- Frankreich setzt Notfallzulassung für Imidacloprid und Thiamethoxam in Kraft. In: topagrar.com. 16. Februar 2021, abgerufen am 28. Februar 2021.
- Erläuterung zur Notfallzulassung des Pflanzenschutzmittels Carnadine. Bundesamt für Verbraucherschutz und Lebensmittelsicherheit, 29. März 2019, abgerufen am 28. Februar 2021.
- Madlaina Peter: 2020 – die Rübe am Scheideweg? UFA-Revue, 23. Februar 2021, abgerufen am 28. Februar 2021.
- Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Imidacloprid in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 25. März 2021.
- Bienensterben: Europäischer Gerichtshof bestätigt Verbot von Bayer-Insektiziden. In: zeit.de. 6. Mai 2021, abgerufen am 6. Oktober 2021.
- EFSA: EFSA bewertet möglichen Zusammenhang zwischen zwei Neonikotinoiden und Entwicklungsneurotoxizität, Pressemitteilung vom 17. Dezember 2013.
- Stefan Häne: EU-Behörde hält «Bienen-Killer» für alternativlos. Der Bund, 18. November 2021 (abgerufen am 19. November d. J. über www.msn.com)

