Carnitin
Carnitin ist eine chemische Verbindung, die in zwei isomeren Formen vorkommt. Eine davon, L-Carnitin (INN: Levocarnitin), wird in Lebewesen aus den Aminosäuren Lysin und Methionin hergestellt und spielt eine essentielle Rolle im Energiestoffwechsel beim Transport von Fettsäuren zwischen Cytosol und den Zellorganellen wie den Mitochondrien.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
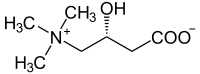 | ||||||||||||||||
| Strukturformel des L-Isomers von Carnitin | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Carnitin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H15NO3 | |||||||||||||||
| Kurzbeschreibung |
farbloses, kristallines Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code |
A16AA01 | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 161,20 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Schmelzpunkt |
190–195 °C (Zersetzung)[1] | |||||||||||||||
| Löslichkeit |
sehr gut löslich in Wasser: 100 g·l−1 (20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Stereoisomerie
Carnitin ist chiral, da es ein Stereozentrum enthält. Es gibt somit zwei Enantiomere, die (R)-Form [(–)-L-Carnitin] und die (S)-Form [(+)-D-Carnitin]. Dem D-Carnitin kommt praktisch keinerlei Bedeutung zu; wenn Carnitin ohne Deskriptor erwähnt wird, ist immer L-Carnitin gemeint.
| Isomere von Carnitin | ||
| Name | L-Carnitin | D-Carnitin |
| Andere Namen | (R)-Carnitin (–)-Carnitin |
(S)-Carnitin (+)-Carnitin |
| Strukturformel | -Carnitine_Structural_Formula_V1.svg.png.webp) |
-Carnitine_Structural_Formula_V1.svg.png.webp) |
| CAS-Nummer | 541-15-1 | 541-14-0 |
| 406-76-8 (DL) | ||
| EG-Nummer | 208-768-0 | 625-884-0 |
| 206-976-6 (DL) | ||
| ECHA-Infocard | 100.007.972 | 100.154.337 |
| 100.006.343 (DL) | ||
| PubChem | 10917 | 2724480 |
| 288 (DL) | ||
| DrugBank | DB00583 | – |
| – (DL) | ||
| Wikidata | Q20735709 | Q27108687 |
| Q243309 (DL) | ||
Eigenschaften
L-Carnitin reagiert im Stoffwechsel mit Fettsäuren, wodurch aktivierte Fettsäuren entstehen. Carnitin übt diese Funktion im Wechselspiel mit Coenzym A aus. Fettsäuren können nur gebunden an L-Carnitin durch die Mitochondrienmembranen transportiert werden.[3] Über das Carnitin-Acyltransferase-System werden Fettsäuren der β-Oxidation zugeführt.
Im Darm wird aus Carnitin durch die Darmflora zuerst Trimethylamin und in Folge Trimethylaminoxid gebildet.[4] Der menschliche Körper kann L-Carnitin aus den Aminosäuren Methionin und Lysin selbst bilden, nimmt es jedoch hauptsächlich über Fleisch auf.
Vorkommen
L-Carnitin befindet sich in großen Mengen in rotem Fleisch, insbesondere in Schaf- und Lammfleisch. Geflügelfleisch dagegen ist carnitinärmer, während vegetarische Lebensmittel wenig oder gar kein L-Carnitin enthalten. Bei einer gemischten Kost werden täglich zwischen 100 und 300 mg L-Carnitin durch die Nahrung aufgenommen, im Gegensatz zu Ovo-Lakto-Vegetariern, die nur 15–25 % dieser Menge aufnehmen, während der Anteil bei veganer Kost um die 3–10 % liegt.[5][6] Der restliche Bedarf wird durch die endogene Synthese gedeckt, wenn die essentiellen Kofaktoren Vitamin C, Vitamin B6, Niacin und Eisen in ausreichender Menge zur Verfügung stehen.[6] Die Bioverfügbarkeit von L-Carnitin aus der Nahrung beträgt 54 bis 87 %.[7] Die Resorption hängt stark vom Carnitingehalt der Nahrung, aber auch von deren Zusammensetzung ab.[7]
Der Gesamtbestand an L-Carnitin im Körper beträgt etwa 20–25 g, wobei der Anteil in Geweben mit hohem Fettsäuremetabolismus besonders hoch ist. In Herz- und Skelettmuskulatur sind 98 % der Reserven von Carnitin gespeichert.[6] Über die Nieren werden täglich etwa 20 mg in den Urin ausgeschieden. Der Normalwert des L-Carnitins im Plasma liegt zwischen 40 und 60 µmol/l,[8] wovon etwa 70–85 % als freies Carnitin verfügbar sind. Der Rest liegt mit einer Fettsäure verestert als Acylcarnitin vor.
Da L-Carnitin wasserlöslich ist, wird es bei einer Hämodialyse mit aus dem Blut der Nierenpatienten entfernt.[9] Dies hat die Folge, dass Dialysepatienten sehr niedrige L-Carnitin-Blutwerte haben. Patienten mit fortgeschrittener Niereninsuffizienz nehmen häufig L-Carnitin, entweder oral oder intravenös, um diese Verluste wieder auszugleichen.
Synthese
L-Carnitin kann über verschiedene Wege im industriellen Maßstab gewonnen werden.[10] Beispielsweise über einen die körpereigene Biosynthese imitierenden biotechnologischen Prozess: In großen Fermentationsbehältern wird dabei die Vorstufe von L-Carnitin (γ-Butyrobetain) mit Hilfe von gramnegativen Bakterien (Rhizobien) in L-Carnitin umgesetzt.
Verwendung
Patienten mit einer systemischen primären Carnitindefizienz (SPCD) erhalten Carnitin als Nahrungsergänzungsmittel.[11] Weiterhin wird Carnitin als Fatburner verwendet.
Carnitin als „Fettverbrenner“
Die zusätzliche Einnahme von Carnitin wird in Studien kontrovers diskutiert. Wissenschaftler des Institutes für Lebensmittelwissenschaft und Ökotrophologie der Uni Hannover stellten 1994 zusammenfassend fest, „dass L-Carnitin keine eigenständige Eigenschaft als ‚Fatburner‘ und ‚Schlankheitsmittel‘ zukommt.“[12] Der carnitinabhängige Fettsäuretransport erfolge bereits bei physiologischen Carnitinkonzentrationen mit Maximalgeschwindigkeit. Eine Umsatzsteigerung durch zusätzliche Carnitingaben sei daher auszuschließen. Aus Humanstudien geht hervor, dass Carnitinsupplemente zwar zu einem Anstieg der Carnitinwerte im Blut führen, eine entsprechende intrazelluläre Erhöhung lässt sich allerdings nicht belegen.[13] Die Verbraucherzentrale Nordrhein-Westfalen äußert sich über Carnitin als Nahrungsergänzungsmittel und angeblichen Fatburner wie folgt:
„Die Behauptung, dass der Körper zur Herstellung von 1 g Carnitin 34 g Muskel abbauen müsse, ist schlicht falsch, er nutzt dafür Eiweißbausteine aus der Nahrung. Eine zusätzliche Carnitin-Aufnahme in Tablettenform kann weder den Carnitingehalt in den Muskelzellen noch die Geschwindigkeit der Fettverbrennung steigern. Sie hat auch keinen Einfluss auf den Fettanteil des Körpers während einer Diät. (…) Überflüssiges Carnitin wird mit dem Urin ausgeschieden. Es ist jedoch nicht auszuschließen, dass bei einer dauerhaften hohen Zufuhr die körpereigene Carnitinbildung eingestellt wird. (…) Carnitin ist als Schlankheitsmittel genauso unwirksam wie als Leistungssteigerer, Herzstärkungs-, Potenzsteigerungs- und Antikrebsmittel.[14]“
Im Jahr 2016 wurde in einer Metaanalyse eine begrenzte Wirksamkeit festgestellt.[15]
Carnitin im Sport
Insbesondere Ausdauersportler nehmen L-Carnitin häufig als Nahrungsergänzungsmittel zu sich, da einige Studien suggerieren, dass durch die Einnahme von L-Carnitin Leistungssteigerungen erzielt werden könnten. Diese Leistungssteigerung bezieht sich auf die Regeneration nach großer sportlicher Anstrengung. Carnitin wird im Sport als einer der am stärksten wirkenden Fatburner gehandelt.
Carnitin bei Krebs
In einer randomisierten Doppelblind-Studie der Universität Greifswald konnte 2012 gezeigt werden, dass die tägliche Einnahme von 4 g L-Carnitin bei fortgeschrittenem Bauchspeicheldrüsenkrebs die gefährliche Gewichtsabnahme (Kachexie) aufhalten konnte.[16] Während sich das Gewicht in der Kontrollgruppe um durchschnittlich 1,4 % verringerte, nahm das Gewicht in der Carnitin-Gruppe um 3,4 % signifikant zu. Auch die mediane Überlebenszeit verlängerte sich von 399 auf 519 Tage und die Aufenthaltszeit im Krankenhaus verringerte sich von 41 auf 36 Tage (nicht signifikant). Carnitin wird zur Minderung des Muskelabbaus bei Krebs untersucht.[17]
Carnitin als Haarwuchsmittel
L-Carnitin wird als Nahrungsergänzungsmittel und in Shampoos als Mittel gegen Haarausfall vermarktet. Außer einer kleinen Studie aus dem Jahr 2007[18] (19 männliche, 32 weibliche Probanden, Alter 21–60 Jahre) mit topisch appliziertem Carnitintartrat gibt es dafür keine wissenschaftliche Grundlage. Die Autoren schrieben den Effekt einer Minderung der Bildung von haarwuchshemmenden Faktoren zu.[19]
L-Carnitingehalte in Lebensmitteln
L-Carnitingehalte in Lebensmitteln in mg pro 100 g Lebensmittel[5]
| Lebensmittel | L-Carnitin mg/100 g | Lebensmittel | L-Carnitin mg/100 g | Lebensmittel | L-Carnitin mg/100 g | Lebensmittel | L-Carnitin mg/100 g |
|---|---|---|---|---|---|---|---|
| Fleischextrakt | 36-86 | Kalb | 69,7–105 | Pilze | 1,3–15 | Muttermilchersatz | 1–4,3 |
| Reh, Hirsch, Elch, Rentier | 35–193 | Wildschwein | 18–46 | Geflügel | 4,3–13,3 | Speiseöl, Butter, Margarine | 0–1,1 |
| Schaf, Ziege | 16,7–190 | Fleischprodukte | 1,2–38,6 | Meerestiere | 1,7–13,2 | Cerealien (Brot, Nudeln, Reis) | 0,33–0,75 |
| Pferd, Känguru | 117–166 | Kaninchen | 10,2–24,4 | Käse | 0,6–12,7 | Nüsse | 0,02–0,67 |
| Rind | 45–143 | Hausschwein | 14,4–24 | Milch, Molkereiprodukte | 2,1–9,7 | Gemüse | 0,05–0,53 |
| Hase | 44,1–120 | Wildvögel | 3–21,1 | Brühen | 1,1–6,1 | Obst | 0,01–0,35 |
Geschichte
Karnitin wurde erstmals im Jahr 1905 von Wladimir Gulewitsch und dessen Mitarbeiter Robert Krimberg isoliert.[20][21] Sie präparierten darüber hinaus ein Platinsalz von Karnitin und bestimmten die Summenformel; die korrekte Strukturformel fand Krimberg im Jahr darauf.[22] Karnitin soll auch etwa zur selben Zeit von Friedrich Kutscher in Marburg gefunden worden sein,[23] der es Novain nannte. Seine Strukturformel war falsch und Krimberg bewies bald darauf, dass beide identisch sind. Im Jahr 1952 wurde es von Gottfried Fraenkel mit dem von ihnen isolierten Insekten-Wachstumsfaktor Vitamin identifiziert. Dies führte unmittelbar zur Entdeckung von dessen Rolle im Fettstoffwechsel und in den Mitochondrien.[24]
Literatur
- Heinz Löster: Carnitine and Cardiovascular Diseases. Ponte Press, Bochum 2003, ISBN 3-920328-45-0.
- Heinz Löster: Carnitin und seine Bedeutung bei kardiovaskulären Erkrankungen. Ponte Press, Bochum 2007, ISBN 978-3-920328-50-8.
Weblinks
- Wissenschaftliche Studie zu Carnitin und Fettstoffwechsel (PDF; 98 kB)
- Wissenschaftliche Studie zur Wirkung von L-Carnitin bei der Regeneration nach dem Sport
- Hanne Seline Marie Gustavsen: Bestimmung des L-Carnitingehaltes in rohen und zubereiteten pflanzlichen und tierischen Lebensmitteln. (PDF; 1,72 MB) Doktorarbeit
Einzelnachweise
- Datenblatt Carnitin (PDF) bei Merck, abgerufen am 19. Januar 2011.
- Datenblatt L-Carnitine inner salt bei Sigma-Aldrich, abgerufen am 3. November 2016 (PDF).
- Heinz Löster: Biochemical fundamentals of the effects of Carnitine. In: Carnitine and Cardiovascular Diseases. Ponte Press, Bochum 2003, ISBN 3-920328-45-0, S. 3–48.
- Robert A Koeth, Zeneng Wang, Bruce S Levison, Jennifer A Buffa, Elin Org, Brendan T Sheehy, Earl B Britt, Xiaoming Fu, Yuping Wu, Lin Li, Jonathan D Smith, Joseph A DiDonato, Jun Chen, Hongzhe Li, Gary D Wu, James D Lewis, Manya Warrier, J Mark Brown, Ronald M Krauss, W H Wilson Tang, Frederic D Bushman, Aldons J Lusis, Stanley L Hazen: Intestinal microbiota metabolism of l-carnitine, a nutrient in red meat, promotes atherosclerosis. In: Nature Medicine. 19, 2013, S. 576, doi:10.1038/nm.3145.
- Hanne Seline Marie Gustavsen: Bestimmung des L-Carnitingehaltes in rohen und zubereiteten pflanzlichen und tierischen Lebensmitteln. (PDF; 1,8 MB) Doktorarbeit am Physiologischen Institut der Tierärztlichen Hochschule Hannover, 2000.
- Axel G. Feller, Daniel Rudman: Role of carnitine in human nutrition. In: The Journal of nutrition. Volume 118, Issue 5, S. 541–547, Januar 1988 PMID 3284979. jn.nutrition.org (PDF; 1,6 MB)
- C. J. Rebouche, C. A. Chenard: Metabolic fate of dietary carnitine in human adults: identification and quantification of urinary and fecal metabolites. In: The Journal of nutrition. Volume 121, Issue 4, S. 539–546, April 1991 PMID 2007906. jn.nutrition.org (PDF; 1,3 MB)
- C. J. Rebouche: Carnitine function and requirements during the life cycle. In: FASEB journal: official publication of the Federation of American Societies for Experimental Biology. Band 6, Nummer 15, Dezember 1992, S. 3379–3386, PMID 1464372.
- G. Guarnieri: Carnitine in maintenance hemodialysis patients. In: Journal of renal nutrition: the official journal of the Council on Renal Nutrition of the National Kidney Foundation. Band 25, Nummer 2, März 2015, S. 169–175, doi:10.1053/j.jrn.2014.10.025, PMID 25600394.
- Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dieter Reichert: Pharmaceutical Substances. 4. Auflage. 2 Bände. Thieme, Stuttgart 2000, ISBN 3-13-558404-6 (online mit halbjährlichen Ergänzungen und Aktualisierungen)
- Pilar L Magoulas, Ayman W El-Hattab: Systemic primary carnitine deficiency: an overview of clinical manifestations, diagnosis, and management. In: Orphanet Journal of Rare Diseases. 7, 2012, S. 68, doi:10.1186/1750-1172-7-68.
- Alexander Ströhle, Maike Wolters, Andreas Hahn: Nährstoffsupplemente und Functional Food zur Gewichtsreduktion – Wunsch und Wirklichkeit. In: Ernährung & Medizin. 19, 2004, S. 121–128.
- M. D. Vukovich, D. L. Costill, W. J. Fink: Carnitine supplementation: effect on muscle carnitine and glycogen content during exercise. In: Med Sci Sports Exerc. 26, 1994, S. 1122–1129.
- ABC der Schlankmacher. Verbraucherzentrale NRW, Düsseldorf 2004, ISBN 3-933705-91-6.
- M. Pooyandjoo, M. Nouhi, S. Shab-Bidar, K. Djafarian, A. Olyaeemanesh: The effect of (L-)carnitine on weight loss in adults: a systematic review and meta-analysis of randomized controlled trials. In: Obesity reviews: an official journal of the International Association for the Study of Obesity. Band 17, Nummer 10, Oktober 2016, S. 970–976, doi:10.1111/obr.12436, PMID 27335245.
- M. Kraft u. a.: L-Carnitine-supplementation in advanced pancreatic cancer (CARPAN)--a randomized multicentre trial In: Nutrition Journal. 2012. PMID 22824168
- R. Ringseis, J. Keller, K. Eder: Mechanisms underlying the anti-wasting effect of L-carnitine supplementation under pathologic conditions: evidence from experimental and clinical studies. In: European Journal of Nutrition. Band 52, Nummer 5, August 2013, S. 1421–1442, doi:10.1007/s00394-013-0511-0, PMID 23508457.
- K. Foitzik et al.: Indications that topical L-Carnitin-L-tartrate promotes human hair growth in vivo. J. Dermatol. Sci. 2007, 48(2), 141.
- K. Foitzik et al.: L-Carnitin-L-tartrate promotes human hair growth in vitro. Exp. Dermatol. 2007, 16, 936.
- Gulevich, Krimberg: Zur Kenntnis der Extractivstoffe der Muskeln. In: Z. f. Physiol. Chemie, Band 45, 1905, S. 326–328
- Anatoly Bezkorovainy: Carnosine, carnitine, and Vladimir Gulevich. In: J. Chem. Education, Band 51, 1974, S. 652–654.
- Bezkorovainy. In: J. Chem. Education, Band 51, 1974, S. 653, er zitiert dazu R. Krimberg. In: Z. f. Physiol. Chemie, Band 49, 1906, S. 89, Band 50, 1907, S. 361.
- F. Kutscher: Zur Kenntnis des Novains In: Z. Physiol. Chem., Band 49, 1905, S. 47–49, Digitalisat
- George Wolf: The Discovery of a Vitamin Role for Carnitine: the First 50 Years In: Journal of Nutrition, Band 136, 2006, S. 2131–2134, jn.nutrition.org