Campher
Campher bzw. lateinisch Camphora (fachsprachlich, standardsprachlich Kampfer) ist ein durch Wasserdampfdestillation aus dem Holz von Kampferbäumen gewonnener farbloser, in Wasser kaum löslicher Feststoff. Er ist ein bicyclisches Monoterpen-Keton und leitet sich formal vom Bornan ab. Es gibt zwei Enantiomere des Camphers: (+)-Campher [Synonym: (1R,4R)-Campher] und (−)-Campher [Synonym: (1S,4S)-Campher]. Die Struktur wurde von Julius Bredt aufgeklärt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
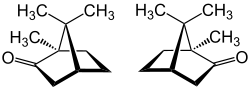 | ||||||||||||||||||||||
| (+)-Campher (links) und (–)-Campher (rechts) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Campher | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C10H16O | |||||||||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff mit aromatischem Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code |
C01EB02 | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 152,23 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||||||||
| Dichte |
1 g·cm−3 [(±)-Campher] [1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
209 °C [(±)-Campher][1] | |||||||||||||||||||||
| Löslichkeit |
löslich in Wasser (1,5 g·l−1 bei 20 °C)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Campher kommt in verschiedenen Gewächsen natürlich vor und wird industriell synthetisch hergestellt. Er ist arzneilich wirksam, in missbräuchlicher Dosierung psychoaktiv und toxisch. Er ist als Gefahrstoff geringerer Gefährlichkeit eingestuft und wird unter anderem als Bestandteil technischer und medizinischer Produkte eingesetzt.
Campher wird aus dem Holz, den Stümpfen, Zweigen und Blättern eines Kampferbaums destilliert. Bis ins 16. Jahrhundert nutzte man den Borneokampferbaum (Dryobalanops aromatica Gaertn., synonym Dryobalanops camphora[5][6]), ab dem 16. Jahrhundert vor allem den Kampferbaum (Cinnamomum camphora, synonym: Laurus camphora und Camphora lauri).[7] Seit der Spätantike (5. Jahrhundert) ist Kampfer (älter auch Campfer und lateinisch Camphora[8]) unter dem griechischen Namen kaphurá (καφουρά) bekannt, der auf Sanskrit karpura (‚weiß‘) bzw. Prakrit kappura zurückgeht. Der indische Name wiederum entstand durch Entlehnung aus einer austronesischen Sprache Sumatras. Mittelhochdeutsch und frühneuhochdeutsch[9] und bis ins 19. Jahrhundert[10] hieß Kampfer (ab etwa 1250 von altfranzösisch camphre[11]) bzw. das Harz vom Kampferbaum auch Gaffer, regional[12] auch Gauffer.
Vorkommen
Beide Enantiomere des Camphers [(+)-Campher bzw. (−)-Campher] sowie das Racemat (±)-Campher kommen in der Natur vor.[13] Campher findet sich hauptsächlich in den ätherischen Ölen von Lorbeergewächsen, Korbblütlern und Lippenblütlern. (+)-Campher kommt in der Rinde und im Harz des Kampferbaums (Cinnamomum camphora) vor, eines immergrünen Baums, der hauptsächlich in Asien wächst.[13]
Eigenschaften
Campher ist ein farbloses oder weißes, meist krümeliges und brockig zähes Pulver aus wachsweichen Kristallen. Aus Ethanol kristallisiert er rhomboedrisch. Beim Abschrecken geschmolzenen Camphers bilden sich kubische Kristalle. Campher hat einen charakteristischen, starken, wohlriechenden, aromatisch-holzigen, eukalyptusartigen Geruch. Der Geschmack ist scharf und bitter, auch leicht kühlend wie bei Menthol. Er schmilzt bei 179 °C[1] und siedet bei 209 °C.[1] In Wasser ist das Pulver kaum löslich (1,5 g pro Liter Wasser);[1] in Ethanol hingegen löst es sich gut. Außerdem ist es sehr leicht löslich in Petrolether, leicht löslich in Ether, Aceton, Chloroform und in fetten Ölen und sehr schwer löslich in Glycerin. Es bildet mit Ethanol farblose Lösungen, aus denen sich, wenn Wasser hinzugegeben wird, der Campher wieder abscheidet. Die Dichte beträgt 0,96 g/cm3. Campher ist leicht flüchtig und sublimiert schon bei Zimmertemperatur. Er verbrennt mit rußender Flamme. Beim Campher ist die molare Schmelzpunkterniedrigung auffällig groß, sie beträgt 39,7 K·(kg/mol). So verflüssigt sich Campher bereits, wenn er in Kontakt mit Menthol, Naphthol oder Chloralhydrat kommt. Der spezifische Drehwinkel beträgt +48°.
Bei der Reduktion von (+)-Campher [(1R,4R)-Campher] mit Natriumborhydrid oder Lithiumaluminiumhydrid entstehen zu 95 % Isoborneol [(1R,2R,4R)-Isoborneol] und zu 5 % dessen Stereoisomer Borneol [(1R,2S,4R)-Borneol]:[14]
-Camphor_Reduction_V.1.svg.png.webp)
Campher ist schwach wassergefährdend (WGK 1).
Sicherheitstechnische Kenngrößen
Campher bildet bei erhöhter Temperatur entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei 77 °C. Der Explosionsbereich liegt zwischen 0,6 Vol.‑% (38 g/m3) als untere Explosionsgrenze (UEG) und 4,5 Vol.‑% (280 g/m3) als obere Explosionsgrenze (OEG).[1] Die Zündtemperatur beträgt 460 °C.[1][15] Der Stoff fällt somit in die Temperaturklasse T1.
Wirkungen und Nebenwirkungen
Campher wirkt auf das zentrale Nervensystem und die Niere, in höheren Dosen auch (analeptisch) auf das Atemzentrum. Er ist durchblutungsfördernd und schleimlösend, kann aber auch zu Übelkeit, Angst, Atemnot und Aufgeregtheit führen. In Überdosis oral eingenommen, kommt es zu Verwirrtheits- und Dämmerzuständen, Depersonalisation, extremen Déjà-vu-Erlebnissen, Panik und akuten tiefgreifenden Störungen des Kurzzeitgedächtnisses bis hin zu Amnesie und epileptischen Anfällen. Die tödliche Dosis für einen Erwachsenen liegt bei 0,1 g/kg Körpermasse.[16] Der Metabolismus geht zunächst zum vom Campher abgeleiteten Alkohol 2-Borneol, welcher in der Leber weiter zum Glucuronid umgewandelt wird. Dieses wird schließlich über den Harn ausgeschieden.[17]
Verwendung
Chemische Produkte
Campher wird in Feuerwerkskörpern, teilweise in Sprenggelatine und in Mottenabwehrmitteln verwendet. Außerdem wird er für die Celluloidproduktion und als Weichmacher für Celluloseester verwendet.
Biologische und physikalische Anwendungen
In der Bienenpflege findet Campher als von der EU zugelassener Wirkstoff gegen Milbenbefall Anwendung. Er wird oftmals auch in entomologischen Sammlungen zur Desinfektion und zum Schutz vor Schädlingen genutzt. Auch in Sturmglasbarometern findet er Verwendung.
Wegen seiner hohen kryoskopischen Konstanten von 39,7 K·(kg/mol) wurde Campher früher zur Bestimmung der Molmasse nach Beckmann genutzt.
Medizin und Kosmetik

Campher ist in Kosmetik- und Medizinpräparaten enthalten, zum Beispiel in Produkten gegen Muskelzerrungen, Rheuma oder Neuralgien, Aftershaves wie Pitralon, in Mitteln gegen Erkältungen (beispielsweise enthält Wick VapoRub 5 % Campher)[18] und in der Zahnmedizin zur Desinfektion infizierter Wurzelkanäle. Früher wurde er auch als Analeptikum verwendet, heute seltener aufgrund der Wirkungen auf das Herz und den Kreislauf.
Gestreckt wurde Campher im Mittelalter durch Beimischung von „Firnis“.[19]
Genuss- und Rauschmittel, Lebensmittel
Seltene Fälle der Verwendung von Campher als Rauschmittel sind bekannt. Die Wirkungen beim Inhalieren von Campher zeigen sich in Lachanfällen trotz Schmerzen in den Atemwegen. Campher findet noch Verwendung in Schnupftabak aus England, wohingegen er in Deutschland laut Tabakverordnung zu den in Tabak verbotenen Stoffen zählt und nicht hinzugefügt werden darf. Historisch wurde er in China als geschmacks- und strukturverstärkender Zusatz in Speiseeis verwendet.[20] In der EU ist D(+)-Campher durch die Verordnung (EG) Nr. 1334/2008 (Aromenverordnung) mit der FL-Nummer 07.215 als Aromastoff für Lebensmittel zugelassen.[21]
Religiöse Praxis
Allein oder in Verbindung mit Baumharzen und/oder anderen Stoffen wird er als Räucherwerk beim Räuchern verwendet. Ferner werden im Islam die Verstorbenen während der letzten Waschung häufig mit Waschwasser gereinigt, dem zur Parfümierung Campher beigemischt ist.[22]
Pharmakologische Eigenschaften und Anwendungen
Campher wird in 2,5%iger Lösung bei hypotonen oder orthostatischen Dysregulationen zur peroralen bzw. oro-mukosalen Gabe (über die Mundschleimhaut) eingesetzt. Außerdem wird es äußerlich in Form 10%iger Salben angewendet, höhere Konzentrationen können zu schweren Vergiftungen führen. Die Salben wirken durchblutungsfördernd und werden bei chronischer Arthritis, Sehnenscheidenentzündung, traumatischer Schwellung, Myalgie, Bursitis, Zerrung, Verstauchung und entzündlichem Ödem eingesetzt. Konzentrationen von 0,1 % haben eine geringe lokalanästhetische und durch Reizung von Kälteempfindungen leitenden Nervenendigungen kühlende Wirkung. Campher wird schnell über die Haut resorbiert und gelangt über das Blutplasma vor allem in das Fettgewebe. Es passiert die Blut-Hirn-Schranke, die Blut-Milch-Schranke und die Plazentaschranke. Die Metabolisierung erfolgt zu Carbonsäuren und/oder Campheralkoholen, teilweise wird der Wirkstoff glukuronidiert. Die Ausscheidung erfolgt vor allem über die Niere, in geringer Menge auch über die Lunge, den Kot und die Milch.[16]
Campher ist das älteste Analeptikum und gehört zu den Parasympatholytika. Analeptika steigern in geeignetem Dosisbereich die Aktivität bestimmter Abschnitte des Zentralnervensystems. Campher entfaltet seine analeptische Wirkung durch das Blockieren von nikotinischen Cholin-Rezeptoren[23]. Die pharmakologische Anwendung von Campher wird heute als obsolet bezeichnet. Die früher übliche Anwendung von Campher zusammen mit Pentetrazol (Markenname Cardiazol) in der Cardiazolschocktherapie als Krampfbehandlung von Geisteskrankheiten erlebte einen Höhepunkt um 1938. Sie wurde vom Psychiater Ladislas J. Meduna entdeckt und propagiert.[24]
Gewinnung und Darstellung
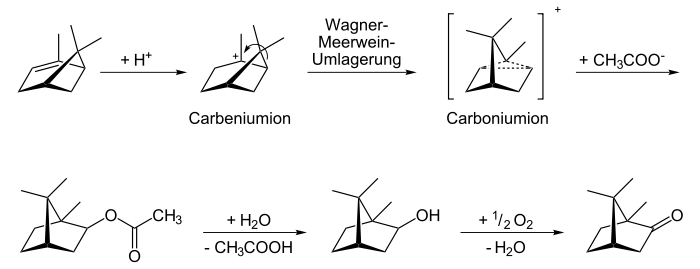
Campher kann synthetisch hergestellt, aber auch durch Wasserdampfdestillation und Kristallisation aus zerkleinerten Pflanzenteilen des Campherbaums gewonnen werden. Natürlicher Campher ist meistens rechtsdrehend [(+)-Campher, „Japancampher“]. In Matricariaarten findet sich aber auch linksdrehender (–)-Campher („Matricariacampher“).[3] Heutzutage wird Campher technisch ausgehend von α-Pinen synthetisiert. Über das intermediäre Carboniumion entsteht dabei hauptsächlich das thermodynamisch stabilere Isobornylacetat, welches in der Folge nach Hydrolyse des Esters zu (–)-Campher oxidiert wird.
Die Totalsynthese von Campher gelang Gustaf Komppa 1903 (Razemat) bzw. 1905.[25] Schon zuvor (1902) wurde bei Schering in Berlin unter Leitung von Ossian Aschan Campher in industrieller Synthese aus Terpentinölen (Pinenen) synthetisiert.
Biosynthese
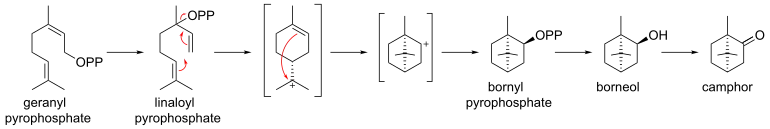
Aus Geranylpyrophosphat über Cyclisierung von Linalool-Pyrophosphat zu Bornyl-Pyrophosphat gefolgt von einer Hydrolyse zu Borneol und anschließender Oxidation entsteht Campher enzymatisch im Salbei (Salvia officinalis).[26]
Weblinks
- Eintrag zu Campher. In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD
Einzelnachweise
- Eintrag zu Campher in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 76-22-2 bzw. Kampfer), abgerufen am 2. November 2015.
- Eintrag zu Campher. In: Römpp Online. Georg Thieme Verlag, abgerufen am 12. Juni 2014.
- Datenblatt Campher bei Sigma-Aldrich, abgerufen am 8. Mai 2017 (PDF).
- Willem Hendrik de Vriese: De Kampferboom van Sumatra, Dryobalanops Camphora Colebr., volgens Dr. F. Junghuhn's Waarnemingen op de Plaats zelve, en door nadere Onderzoekingen toegelicht. Den Hoogleeraar C. G. C. Reinwardt, bij de Herinnering an zijn vijftigjarig Hoogleeraar-Ambt, op den 10den Junij 1851, Aangebden. Leiden 1851 (Online).
- Wouter S. van den Berg (Hrsg.): Eene Middelnederlandsche vertaling van het Antidotarium Nicolaï (Ms. 15624–15641, Kon. Bibl. te Brussel) met den latijnschen tekst der eerste gedrukte uitgave van het Antidotarium Nicolaï. Hrsg. von Sophie J. van den Berg, N. V. Boekhandel en Drukkerij E. J. Brill, Leiden 1917, S. 221 (Camphora).
- Otto Beßler: Die Identifikation mittelalterlicher Drogen und Arzneipflanzen. Stuttgart 1958 (= Veröffentlichungen der Internationalen Gesellschaft für Geschichte der Pharmazie. Neue Folge, Band 13), S. 47 f.
- Vgl. etwa Ute Obhof: Rezeptionszeugnisse des „Gart der Gesundheit“ von Johann Wonnecke in der Martinus-Bibliothek in Mainz – ein wegweisender Druck von Peter Schöffer. In: Medizinhistorische Mitteilungen. Zeitschrift für Wissenschaftsgeschichte und Fachprosaforschung. Band 36/37, 2017/2018, S. 25–38, hier: S. 31 (Camphora „campfer“).
- Frühneuhochdeutsches Wörterbuch: gaffer..
- Baierische Pharmacopoe (1823)
- Friedrich Kluge, Alfred Götze: Etymologisches Wörterbuch der deutschen Sprache. 20. Auflage. Hrsg. von Walther Mitzka. De Gruyter, Berlin / New York 1967; Neudruck („21. unveränderte Auflage“) ebenda 1975, ISBN 3-11-005709-3, S. 344 (dort erwähnt auch arabisch kāfūr, neugriechisch kafurá und englisch camphor).
- Jürgen Martin: Die ‚Ulmer Wundarznei‘. Einleitung – Text – Glossar zu einem Denkmal deutscher Fachprosa des 15. Jahrhunderts. Königshausen & Neumann, Würzburg 1991 (= Würzburger medizinhistorische Forschungen. Band 52), ISBN 3-88479-801-4 (zugleich Medizinische Dissertation Würzburg 1990), S. 130 und 141.
- The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals. 14. Auflage (Merck & Co., Inc.), Whitehouse Station, NJ, USA 2006, ISBN 978-0-911910-00-1, S. 279.
- Jonathan Clayden, Nick Greeves, Stuart Warren, Peter Wothers: Organic Chemistry. Oxford University Press, 2001, ISBN 978-0-19-850346-0, S. 862.
- E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen - Band 1: Brennbare Flüssigkeiten und Gase, Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003.
- Wolfgang Löscher et al.: Pharmakotherapie bei Haus und Nutztieren. 7. Aufl., Paul Parey, 2006, S. 503–504.
- Auterhoff-Knabe-Höltje: Lehrbuch der pharmazeutischen Chemie. Wissenschaftliche Verlagsgesellschaft Stuttgart 1999, ISBN 3-8047-1645-8.
- WICK VapoRub-Salbe, Zusammensetzung, abgerufen am 15. März 2015.
- Konrad Goehl: Beobachtungen und Ergänzungen zum ‘Circa instans’. In: Medizinhistorische Mitteilungen. Zeitschrift für Wissenschaftsgeschichte und Fachprosaforschung. Band 34, 2015 (2016), S. 69–77, hier: S. 70.
- A Sweet History of an Icy Treat, in: History Cooperative, 15. Dezember 2015.
- Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über Aromen und bestimmte Lebensmittelzutaten mit Aromaeigenschaften zur Verwendung in und auf Lebensmitteln sowie zur Änderung der Verordnung (EWG) Nr. 1601/91 des Rates, der Verordnungen (EG) Nr. 2232/96 und (EG) Nr. 110/2008 und der Richtlinie 2000/13/EG. Anhang I, Teil A, Tabelle 1. In: eur-lex.europa.eu. 16. Dezember 2008, abgerufen am 3. Januar 2021 (englisch).
- Anne-Sophie Fröhlich: Priesterliche Aufgaben im sunnitischen Islam. LIT Verlag, Berlin-Hamburg-Münster 1997, ISBN 3-8258-3045-4, S. 44.
- Use of borneol or camphor as an antagonist for nicotinic acetylcholine receptors. 11. Februar 2000 (google.com [abgerufen am 19. Oktober 2020]).
- Hans C. Bangen: Geschichte der medikamentösen Therapie der Schizophrenie. VWB, Berlin 1992, ISBN 3-927408-82-4, S. 51–55 Cardiazol-Krampf-Therapie
- Paul Walden, Geschichte der Organischen Chemie seit 1880, Springer, 1990, S. 557.
- Rodney Croteau, Frank Karp: Biosynthesis of monoterpenes: Hydrolysis of bornyl pyrophosphate, an essential step in camphor biosynthesis, and hydrolysis of geranyl pyrophosphate, the acyclic precursor of camphor, by enzymes from sage (Salvia officinalis). In: Archives of Biochemistry and Biophysics. 198, Nr. 2, 1979, S. 523–532. doi:10.1016/0003-9861(79)90527-7.





