Bernsteinsäureanhydrid
Bernsteinsäureanhydrid ist eine heterocyclische organische chemische Verbindung und das Säureanhydrid der Bernsteinsäure.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
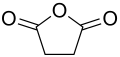 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bernsteinsäureanhydrid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C4H4O3 | |||||||||||||||
| Kurzbeschreibung |
farblose, stechend riechende Nadeln/Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 100,07 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
261 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−608,6 kJ/mol[4] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Bernsteinsäureanhydrid kann durch Reaktion von Bernsteinsäure und Essigsäureanhydrid, Acetylchlorid oder Phosphoroxychlorid gewonnen werden.[5] Auch bei Erhitzung von Bernsteinsäure über 200 °C bildet sich Bernsteinsäureanhydrid.[6] Die Verbindung kann auch durch die katalytische Hydrierung von Maleinsäureanhydrid erhalten werden.[7]
Eigenschaften
Physikalische Eigenschaften
Bernsteinsäureanhydrid ist ein weißer brennbarer Feststoff, der bei 119–120 °C schmilzt.[8] Bei Normaldruck siedet die Verbindung bei 261 °C.[9] Im Vakuum sublimiert die Verbindung.[6] Die Dampfdruckfunktion ergibt sich nach Antoine entsprechend log10(P) = A−(B/(T+C)) (P in bar, T in K) mit A = 3,65221, B = 1433,874 und C = −144,107 im Temperaturbereich von 365 K bis 534 K.[10] Die Löslichkeit in Wasser beträgt bei 20 °C 67 g·l−1 Dabei erfolgt eine langsame Hydrolyse. Die wässrige Lösung reagiert sauer.[1] In aromatischen Kohlenwasserstoffen sind die Löslichkeiten relativ gering. Sie betragen in Toluol 10 g·l−1, in Styrol 11 g·l−1, in Ethylbenzol 8 g·l−1 und in Cumol 5 g·l−1.[11] Die Bildungswärme des Feststoffes beträgt −608,6 kJ·mol−1.[12] Für die Verbrennungswärme wurde ein Wert von −1537,1 kJ·mol−1 bestimmt.[12]
 Dampfdruckfunktion von Bernsteinsäureanhydrid
Dampfdruckfunktion von Bernsteinsäureanhydrid
Chemische Eigenschaften
Bernsteinsäureanhydrid kann in Gegenwart von Natronlauge zur Bernsteinsäure hydrolysiert werden. In Dioxan/Wasser wurde bei 30 °C eine Reaktionswärme von −46,86 kJ·mol−1 bestimmt.[13] Die Umsetzung mit Alkoholen ergibt die entsprechenden Bernsteinsäurehalbester.[14] Die Verbindung kann als Reagenz für Friedel-Crafts-Acylierungen dienen. Die Umsetzung mit Benzol ergibt hier die γ–Oxocarbonsäure β–Benzoylpropionsäure.[15] Aus Grignard-Verbindungen und Bernsteinsäureanhydrid können ebenfalls einfach γ–Oxocarbonsäureester erhalten werden.[16] Die Umsetzung mit Ammoniak bei höheren Temperaturen ergibt das Succinimid.[17] Bei höheren Temperaturen ist der Stoff brennbar, aber er reagiert mit brandfördernden Stoffen sehr heftig. Die Schmelze bildet entzündbare Dampf-Luft-Gemische. Der Flammpunkt beträgt 157 °C.[1]
Verwendung
Bernsteinsäureanhydrid wird als Synthesechemikalie für andere chemische Verbindungen verwendet,[1] wie z. B. in den mehrstufigen Synthesen von 1-Tetralon, 1-Naphthol, Tetralin und Naphthalin[18] sowie von N-Chlor– und N-Bromsuccinimid.[17] Die industrielle Herstellung von Citraconsäureanhydrid (Methylmaleinsäureanhydrid) erfolgt durch Umsetzung von Bernsteinsäureanhydrid mit Formaldehyd.[7] Die Verbindung ist (formal) eine Ausgangsverbindung für Alkenylbernsteinsäureanhydride, das in der Papierindustrie als Leimungsmittel verwendet wird. Dessen Synthese erfolgt allerdings über Maleinsäureanhydrid und ein langkettiges Alken.
Gesundheitsgefahren
Die Folgen bei Berührung oder Einatmung des Bernsteinsäureanhydrid sind Reizungen der Haut und Atemwege, wobei die Schleimhäute sich entzünden können.[1] Die Verbindung wurde als Komponente im Hauptstrom einer filterlosen Zigarette nachgewiesen.[18]
Bernsteinsäureanhydrid wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Bernsteinsäureanhydrid waren die Besorgnisse bezüglich hoher (aggregierter) Tonnage und hohes Risikoverhältnis (Risk Characterisation Ratio, RCR) sowie der Gefahren ausgehend von einer möglichen Zuordnung zur Gruppe der CMR-Substanzen und der vermuteten Gefahren durch sensibilisierende Eigenschaften. Die Neubewertung fand ab 2013 statt und wurde von Österreich durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[19][20]
Literatur
- R. Kühn, V. Birett: Merkblätter gefährlicher Arbeitsstoffe. Ecomed, Landsberg, 1986, Erg. Lfg.
- Beilstein 17
Einzelnachweise
- Eintrag zu Bernsteinsäureanhydrid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 15. November 2019. (JavaScript erforderlich)
- Datenblatt Bernsteinsäureanhydrid (PDF) bei Merck, abgerufen am 27. April 2010.
- Eintrag zu Succinic anhydride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 15. November 2019. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-25.
- L. F. Fieser, E. L. Martin, R. L. Shriner, H. C. Struck: Succinic Anhydride In: Organic Syntheses. 12, 1932, S. 66, doi:10.15227/orgsyn.012.0066; Coll. Vol. 2, 1943, S. 560 (PDF).
- Arnold Willmes: Taschenbuch Chemische Substanzen: Elemente – Anorganika – Organika – Naturstoffe – Polymere. 3., vollst. überarb. und erw. Auflage. Frankfurt am Main 2007, ISBN 978-3-8171-1787-1.
- K. Lohbeck, H. Haferkorn, W. Fuhrmann, N. Fedtke: Maleic and Fumaric Acids. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim 2005. doi:10.1002/14356007.a16_053.
- A. Mclean, R. Adams: Succinic-α-d2,α'-d2, Acid and Its Derivatives. In: J. Am. Chem. Soc. 58, 1936, S. 804–810. doi:10.1021/ja01296a038.
- R. C. Weast, J. G. Grasselli, (Hrsg.): CRC Handbook of Data on Organic Compounds. 2. Auflage. CRC Press, Boca Raton, FL, 1989, S. 1.
- D. R. Stull: Vapor Pressure of Pure Substances Organic Compounds. In: Ind. Eng. Chem. 39, 1947, S. 517–540, doi:10.1021/ie50448a022.
- P. D. Bartlett, K. Nozaki: The Polymerization of Allyl Compounds. III. The Peroxide-induced Copolymerization of Allyl Acetate with Maleic Anhydride. In: J. Am. Chem. Soc. 68, 1946, S. 1495–1504, doi:10.1021/ja01212a033.
- Y. M. Yan, G. Pilcher: Enthalpies of combustion of succinic anhydride, glutaric anhydride, and glutarimide. In: J. Chem. Thermodyn. 22, 1990, S. 893–898, doi:10.1016/0021-9614(90)90177-R.
- J. B. Conn, G. B. Kistiakowsky, R. M. Roberts, E. A. Smith: Heats of organic reactions. XIII. Heats of hydrolysis of some acid anhydrides. In: J. Am. Chem. Soc. 64, 1942, S. 1747–1752, doi:10.1021/ja01260a001.
- J. Cason: β–Carbomethoxypropionyl Chloride In: Organic Syntheses. 25, 1945, S. 19, doi:10.15227/orgsyn.025.0019; Coll. Vol. 3, 1955, S. 169 (PDF).
- L. F. Somerville, C. F. H. Allen: β–Benzoylpropionic Acid In: Organic Syntheses. 13, 1933, S. 12, doi:10.15227/orgsyn.013.0012; Coll. Vol. 2, 1943, S. 81 (PDF).
- S. Hauptmann, J. Graefe, H. Remane: Lehrbuch der Organischen Chemie. Deutscher Verlag für Grundstoffindustrie, Leipzig 1980, S. 421.
- S. Hauptmann, J. Graefe, H. Remane: Lehrbuch der Organischen Chemie. Deutscher Verlag für Grundstoffindustrie, Leipzig 1980, S. 407.
- Römpp Chemie Lexikon. 9. Auflage. Georg Thieme Verlag, 1995.
- Europäische Chemikalienagentur (ECHA): Substance Evaluation Report und Conclusion Document.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Succinic anhydride, abgerufen am 26. März 2019.


