Nicotinamidadenindinukleotid
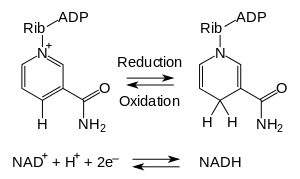
Nicotinamidadenindinukleotid (Nicotinamid-Adenin-Dinukleotid, abgekürzt NAD) ist ein Coenzym, das formal ein Hydridion überträgt (zwei Elektronen, kurz: 2 e-, und ein Proton, H+). Es ist an zahlreichen Redoxreaktionen des Stoffwechsels der Zelle beteiligt.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
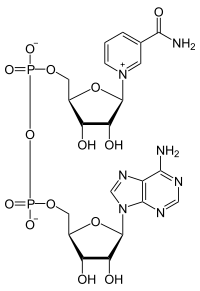 | ||||||||||||||||||||||
| NAD+ (oxidierte Form) | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Nicotinamidadenindinukleotid | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Kurzbeschreibung |
farbloses, hygroskopisches Pulver (oxidierte Form, inneres Salz)[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse |
| |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit |
wenig in Wasser (10 g·l−1)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Von der IUPAC/IUBMB werden die Abkürzungen NAD+ für die oxidierte Form, NADH+H+ für die reduzierte Form und NAD im Allgemeinen vorgeschlagen. Zuweilen findet sich noch NAD statt NAD+ und NADH2 statt NADH+H+.[2] Die Schreibweise von NADH2 ist falsch, da die Protonen an unterschiedlichen Stellen am Molekül binden.
Das Coenzym wurde 1906 von Arthur Harden und William Young entdeckt (Harden- und Young-Ester).[4] NAD+ war in der älteren Fachliteratur bis zu den frühen 1960er Jahren auch unter der Bezeichnung Diphosphopyridinnucleotid, abgekürzt DPN, oder unter den Namen Codehydrase I, Codehydrogenase I oder Coenzym I bekannt.[2]
Im Vergleich zum Nicotinamidadenindinukleotidphosphat (NADP+) und Nicotinsäureadenindinukleotidphosphat (NAADP), zwei sonst fast gleich gebauten Coenzymen, die beide am 2'C-Atom des Adenosins einen weiteren Phosphat-Rest besitzen, befindet sich dort beim NAD nur eine normale Hydroxygruppe.
Chemie
Redoxreaktion des NAD: NAD+ kann durch Aufnahme von zwei Elektronen (e−) und einem Proton (H+) zu NADH reduziert werden.
Biochemie
Funktion
Das Redoxpotential des Redox-Paares NAD+/NADH hängt entsprechend der Nernst-Gleichung vom Konzentrationsverhältnis NAD+/NADH ab. Ist dieses groß, so ist das Redoxpotential positiver (höheres Oxidationsvermögen); ist dieses klein, so ist es negativer (höheres Reduktionsvermögen). Da NAD+ im Organismus meist als Oxidationsmittel dient, ist das Verhältnis NAD+/NADH groß (≫1). Als Reduktionsmittel kommt dagegen vor allem NADPH zum Einsatz, welches ein entsprechend niedriges Verhältnis NADP+/NADPH (≪1) aufweist. Dass ein einzelnes Redox-Paar nicht gleichzeitig ein hohes Redoxpotential für biologische Oxidationen und ein niedriges Redoxpotential für biologische Reduktionen bereitstellen könnte, ist der Grund dafür, dass es zwei differenzierbare Redox-Cofaktoren gibt.
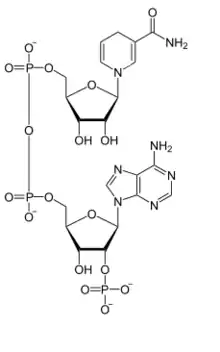
Die energiereiche reduzierte Form NADH dient im oxidativen Stoffwechsel als energielieferndes Coenzym der Atmungskette, wobei ATP generiert wird. Bei ihrer Oxidation gibt sie die zuvor im katabolen Glucose- und/oder Fettstoffwechsel aufgenommenen Elektronen wieder ab und überträgt sie so auf Sauerstoff. Dabei entstehen schließlich NAD+ und Wasserstoff.
NAD+ ist auch ein Coenzym von Dehydrogenasen, z. B. der Alkoholdehydrogenase (ADH), die Alkohol oxidieren.
Biosynthese
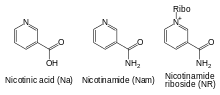
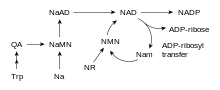
NAD+ wird im Körper sowohl aus Nicotinsäure (Niacin, Vitamin B3) und Nicotinamid als auch aus den Abbauprodukten der Aminosäure Tryptophan produziert.[5][6] Da beide Ausgangsstoffe essenziell sind, sind Mangelerscheinungen wie Pellagra möglich, aber wegen der zwei möglichen Stoffwechselwege in Europa eher selten.
Knotenpunkt beider Reaktionswege ist Nicotinat-D-ribonukleotid, das direkt aus Nicotinsäure mittels der Nicotinat-Phosphoribosyltransferase gebildet werden kann, oder das aus dem Tryptophan-Abbauprodukt Chinolinsäure mittels des Enzyms Chinolinat-Phosphoribosyltransferase entsteht. Letztere Reaktion findet hauptsächlich in der Leber statt.[7] An Nicotinat-D-ribonukleotid wird im nächsten Schritt Adenosinphosphat addiert. Diese Reaktion wird von der Nicotinamidnukleotid-Adenylyltransferase katalysiert, und es entsteht Deamido-NAD+. Dieses wird schließlich mittels der NAD-Synthase zu NAD+ aminiert.
Ein weiterer Syntheseweg beginnt mit Nicotinamid, das mit der Nicotinamid-Phosphoribosyltransferase zum Dinukleotid umgesetzt wird; dieses ist bereits ein Amid, so dass nur noch die Übertragung von Adenosinphosphat mit der o. g. Transferase notwendig ist, um NAD+ zu erhalten.
Die energiereiche reduzierte Form NADH entsteht im Katabolismus (bei der Glykolyse und im Citratzyklus).
Absorptionseigenschaften
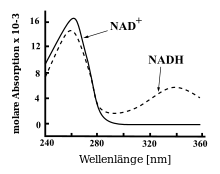
Das Nicotinamid-Adenin-Dinukleotid verfügt sowohl in seiner reduzierten (NADH) als auch in seiner oxidierten (NAD+) Form über einen identischen Adeninbereich (vgl. Strukturformel). Dieser absorbiert Licht bei einer Wellenlänge von 260 nm, dies erklärt das im Diagramm dargestellte, gemeinsame Absorptionsmaximum in dem Bereich 260 nm. Auffällig ist hier, dass bei gleicher Konzentration der Substanzen die Absorption des NAD+ in diesem Bereich höher ist als von NADH. Der Grund dafür ist, dass sich die Absorption des oxidierten, mesomeren Nicotinamidrings, der ebenfalls bei 260 nm absorbiert, mit der Absorption des Adenins überlagert und so für die erhöhte Absorption bei 260 nm sorgt. Wird der Nicotinamidring reduziert, so entsteht ein chinoides System, das Licht mit einer Wellenlänge von 340 nm absorbiert. Der molare Extinktionskoeffizient ԑ von NADH (sowie auch NADPH) bei 340 nm beträgt ԑ = 6300 l/(mol·cm).[8]
Dieser Unterschied zwischen NAD+ und NADH im UV-Spektrum ermöglicht es, die Konversion zwischen oxidierter und reduzierter Form des Coenzyms in einem Spektrophotometer zu beobachten. So kann photometrisch in einem Enzym-Assay die Oxidation von NADH oder die Reduktion von NAD+ beobachtet werden, wenn das eingesetzte Enzym NAD+ als Substrat verwendet. Die Menge des umgesetzten Substrats lässt sich durch die Änderung der Absorption bei 340 nm photometrisch verfolgen, die Konzentration kann dann mit Hilfe des Lambert-Beersches Gesetzes bestimmt werden. Da diese proportional zu der Menge des umgesetzten Cosubstrats ist, sind so indirekt quantitative Aussagen über die Menge an umgesetztem Substrat und hergestelltem Produkt möglich. Die direkte Verfolgung der Substrat- und Produktkonzentration ist dagegen oft schwieriger.
Weblinks
- reactome.org: Nicotinate metabolism
Einzelnachweise
- Eintrag zu NICOTINAMIDE ADENINE DINUCLEOTIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 28. Januar 2021.
- Eintrag zu Nicotinamid-Adenin-Dinucleotid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 9. Dezember 2014.
- Datenblatt NAD+, Free Acid - CAS 53-84-9 - Calbiochem (PDF) bei Merck, abgerufen am 21. Dezember 2019.
- A. Harden, W. J. Young: The alcoholic ferment of Yeast-juice. In: Proceedings of the Royal Society of London (Series B, Containing Papers of a Biological Character ed.), Band 78, Nr. 526, Oktober 1906, S. 369–375. (doi:10.1098/rspb.1906.0029).
- M. Nakamura, A. Bhatnagar, J. Sadoshima: Overview of pyridine nucleotides review series. In: Circulation research. Band 111, Nummer 5, August 2012, S. 604–610. (doi:10.1161/CIRCRESAHA.111.247924; PMID 22904040; PMC 3523884 (freier Volltext)).
- C. Cantó, J. Auwerx: NAD+ as a signaling molecule modulating metabolism. In: Cold Spring Harbor symposia on quantitative biology. Band 76, 2011, S. 291–298 (doi:10.1101/sqb.2012.76.010439; PMID 22345172; PMC 3616234 (freier Volltext)).
- Fukuwatari T, Morikawa Y, Hayakawa F, Sugimoto E, Shibata K: Influence of adenine-induced renal failure on tryptophan-niacin metabolism in rats. In: Bioscience, Biotechnology, and Biochemistry. 65, Nr. 10, Oktober 2001, S. 2154–2161. PMID 11758903.
- H. U. Bergmeyer: New values for the molar extinction coefficients of NADH and NADPH for the use in routine laboratories. In: Zeitschrift für klinische Chemie und klinische Biochemie. Band 13, Nr. 11. Walter de Gruyter, Berlin November 1975, S. 507–508, PMID 3038.