Autotrophie
Unter Autotrophie (wörtlich „Selbsternährung“, von altgriechisch αὐτός autos „selbst“ und τροφή trophe „Ernährung“) wird in der Biologie die Fähigkeit von Lebewesen verstanden, ihre Baustoffe (und organischen Reservestoffe) ausschließlich aus anorganischen Stoffen aufzubauen. Dieser Stoffaufbau erfordert Energie.

Als autotrophe Lebewesen sind vor allem Photosynthese betreibende Primärproduzenten (insbesondere Pflanzen) zu nennen. Bei ihnen dient Licht als Energiequelle (Photoautotrophie). Manche Organismen können aber auch chemische Stoffumsetzungen als Energiequelle nutzen (Chemoautotrophie).
Auf der Grundlage der Biomassenproduktion autotropher Lebewesen ist die Heterotrophie entstanden, eine Ernährungsform, bei der organische Verbindungen zur Bildung der Baustoffe verwendet werden. Tiere, Pilze und viele Bakterien und Archaeen leben heterotroph. Sie ernähren sich entweder als Konsumenten oder sind Destruenten.
Formen der Autotrophie
Der Begriff Autotrophie bezieht sich meistens auf die Kohlenstoffquelle eines Organismus. Organismen können aber auch in Bezug auf andere Baustoffe autotroph sein, zum Beispiel sind Stickstoff fixierende Bakterien hinsichtlich ihrer Stickstoffquelle autotroph.
Nach der Energiequelle unterscheidet man Photoautotrophie und Chemoautotrophie.
Photoautotrophie
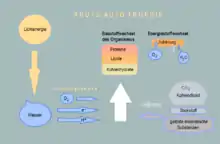
Photoautotrophie ist die Nutzung von Licht als Energiequelle bei Autotrophie. Lebewesen mit dieser Fähigkeit nennt man photoautotroph. Fast alle Pflanzen und Algen sowie einige Bakterien, wie z. B. Schwefelpurpurbakterien und Grüne Schwefelbakterien, wandeln mit Hilfe von Chlorophyll-haltigen Systemen Lichtenergie in chemische Energie (ATP) um (Phototrophie), die sie zum Aufbau von Bau- und Reservestoffen aus anorganischen Stoffen verwenden (siehe Photosynthese). Bei der oxigenen Photosynthese wird für Reduktionen bei der Assimilation von Kohlenstoffdioxid Wasserstoff aus Wasser gewonnen und der nicht benötigte Sauerstoff des Wassers als molekularer Sauerstoff (O2) freigesetzt, den heterotrophe Lebewesen zur Atmung nutzen.
Chemoautotrophie
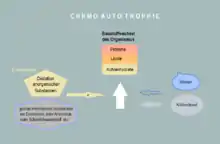
Chemoautotrophie ist die Nutzung von chemischer Energie für die Nutzung von CO2 zum Aufbau von Biomasse. Chemoautotrophie kommt bei Bakterien und Archaeen vor. Beispiele sind u. a. Schwefelbakterien, nitrifizierende Bakterien und einige Methanbildner. Die Reduktionsmittel für die CO2-Fixierung können solche Organismen aus anorganischen Stoffen gewinnen. Deshalb bezeichnet man sie als lithotroph („sich von Steinen ernährend“) oder in Kombination mit ihrer Chemoautotrophie als „chemolithoautotroph“.
Biochemie
Kohlenstoff-autotrophe Organismen verwenden für die Bildung organischer Baustoffe in der Regel Kohlenstoffdioxid CO2 als anorganische Kohlenstoffquelle. Bei einigen Wasserpflanzen konnte außerdem die Aufnahme von Carbonat-Ionen nachgewiesen werden. Die anorganischen Kohlenstoffverbindungen werden reduziert und der Kohlenstoff in organische Verbindungen eingebaut. Die wichtigsten biologischen Stoffwechselvorgänge, mit deren Hilfe Kohlenstoffdioxid assimiliert wird, sind
- der Calvinzyklus
- der Wood-Ljungdahl-Weg
- der reverse Citratzyklus und
- die Carboxylierung von Pyruvat.
Alle Pflanzen assimilieren Kohlenstoffdioxid mit Hilfe des Calvinzyklus, der gleichzeitig der energieaufwändigste ist. Einige Mikroorganismen verfügen über andere Wege der Kohlenstoffdioxid-Assimilation (zum Beispiel den reversen Citratzyklus).
Auch heterotrophe Organismen können geringere Anteile ihres Kohlenstoffbedarfs durch Kohlenstoffdioxid-Assimilation decken. Diese Reaktion erfolgt zum Beispiel bei der Carboxylierung von Pyruvat am Beginn der Gluconeogenese oder als anaplerotische Reaktion zur Auffüllung des Citratzyklus. Aus diesem Grunde gelten per definitionem nur solche Organismen als autotroph, die ihren Kohlenstoffbedarf ausschließlich aus anorganischen Quellen decken.
Weblinks
Literatur
- Daniel Boujard, Bruno Anselme, Christophe Cullin, Céline Raguénès-Nicol: Zell- und Molekularbiologie im Überblick. Springer Spektrum, Berlin, Heidelberg 2014, ISBN 978-3-642-41761-0, Kapitel Energetische Vorgänge in der Zelle, doi:10.1007/978-3-642-41761-0_9.