Polyvinylacetat
Polyvinylacetat (Kurzzeichen PVAC, manchmal auch nur PVA) ist ein thermoplastischer Kunststoff. Die Synthese des Polymers aus der Gruppe der Polyvinylester erfolgt mittels radikalischer Polymerisation. Neben dem reinen Homopolymer haben auch viele Co- und Terpolymere des Vinylacetats große technische Bedeutung.
| Strukturformel | |||
|---|---|---|---|
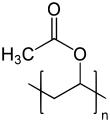 | |||
| n ≈ 100 bis 17000[1] | |||
| Allgemeines | |||
| Name | Polyvinylacetat | ||
| Andere Namen |
Essigsäureethenylesterhomopolymer | ||
| CAS-Nummer | 9003-20-7 | ||
| Monomer | Vinylacetat | ||
| Summenformel der Wiederholeinheit | C4H6O2 | ||
| Molare Masse der Wiederholeinheit | 86,09 g·mol−1 | ||
| Art des Polymers | |||
| Eigenschaften | |||
| Aggregatzustand |
fest | ||
| Löslichkeit |
Praktisch unlöslich in Wasser, leicht löslich in Ethylacetat, löslich in Ethanol[1] | ||
| Sicherheitshinweise | |||
| |||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||
Geschichte
Die Grundlagen für die Herstellung von Polyvinylacetat wurden im Jahr 1912 von Fritz Klatte in Deutschland entdeckt. Er erkannte die Polymerisationsfähigkeit der Vinylverbindungen im Sonnenlicht. In den Jahren 1912 und 1913 erfolgte dann auch die erste gezielte Herstellung von Polyvinylacetat und Polyvinylchloracetat durch Klatte. Seit den 1930ern wird von einigen Firmen eine ganze Reihe verschiedener Produkte in Form von Granulaten, Pulvern, Lösungen und Emulsionen für die verschiedensten Anwendungen hergestellt.
Herstellung und Gewinnung
Die Herstellung von Polyvinylacetat erfolgt aus Vinylacetat durch radikalische Polymerisation. Häufig wird jedoch mit Acrylsäure, Acrylaten, Crotonsäure, Vinyllaurat, Vinylchlorid oder Ethylen copolymerisiert. Dabei ist auf eine hohe Reinheit der Monomere zu achten, da die Fremdstoffe den Polymerisationsverlauf stark verlangsamen (z. B.: Crotonaldehyd, Vinylacetylen) oder zu unerwünschten Kettenübertragungen (z. B.: Essigsäure, Acetaldehyd, Aceton; Benzol, Toluol) führen. Ebenfalls unerwünscht sind Verunreinigungen mit zwei copolymerisierbaren Doppelbindungen (z. B.: Crotonsäurevinylester), da diese durch räumliche Vernetzung zur Bildung von unlöslichen Polymeren beitragen. Die Polymerisation wird meist mit radikalischen Initiatoren (Azoverbindungen, organische, anorganische und Hydroperoxide) gestartet. Photopolymerisation oder strahleninduzierte Polymerisation haben noch keine technische Bedeutung erlangt.
Als Polymerisationsverfahren zur Herstellung von Polyvinylacetat-Homopolymeren sind sowohl Substanz-, Lösungs-, Suspensions- bzw. Perl- und Emulsionspolymerisation möglich.
Polyvinylacetat ist ein notwendiges Vorprodukt für die Herstellung von Polyvinylalkohol und Polyvinylacetalen.
Struktur und Eigenschaften
Chemischer Aufbau
Im Homopolymer überwiegt die Kopf-Schwanz-Anordnung der Monomerbausteine. Durch Verringerung der Polymerisationstemperatur lässt sich der Anteil der Monomere in Kopf-Kopf-Anordnung weiter reduzieren. Der Polymerisationsgrad von Polyvinylacetat beträgt normalerweise 100 bis 5000.
Physikalische Eigenschaften
Polyvinylacetat ist ein amorpher, geruch- und geschmackloser Kunststoff mit hoher Licht- und Wetterbeständigkeit. Es ist brennbar, jedoch nicht leicht entflammbar. Die Glasübergangstemperatur des Homopolymeren schwankt in Abhängigkeit vom Polymerisationsgrad zwischen 18 und 45 °C. Die elektrischen, mechanischen und thermischen Eigenschaften sind ebenso in großem Maße vom Polymerisationsgrad abhängig.
Die Mindestfilmbildetemperatur von Homopolymerdispersionen beträgt etwa 15 bis 18 °C.
Chemische Eigenschaften
Die Estergruppen im Polyvinylacetat sind relativ leicht alkalisch verseifbar, wodurch das Polymer langsam in Polyvinylalkohol umgewandelt und dadurch hydrophil und wasserempfindlich wird. Diese Problematik ist der Grund für die häufige Copolymerisation mit anderen Monomeren.
Polyvinylacetat ist unlöslich in Wasser, Butanol, Diethylether, Petrolether, und aliphatischen Kohlenwasserstoffen, jedoch löslich in niederen Alkoholen, zahlreichen Ketonen, Estern, zyklischen Ethern, aromatischen und chlorierten Kohlenwasserstoffen.
Bei thermischer Zersetzung von Polyvinylacetat wird Essigsäure frei.
Verwendung, Verarbeitung

Polyvinylacetat wird in Form von Lösungen in organischen Lösungsmitteln oder als Dispersion verarbeitet.
Es wird als Bindemittel in Anstrichen und Lacken verwendet. Weitere Verwendung findet der Kunststoff als Weißleim (Holzleim), Tapetenkleister oder Klebstoff. Der in Deutschland bekannte Universalklebstoff Uhu ist eine vierzigprozentige Lösung von Polyvinylacetat in Aceton und Methylacetat. Auch einfacher Bastelkleber enthält oft überwiegend PVA und wird dann unter anderem als Vinylkleber bezeichnet.[3]
Andere Anwendungsgebiete sind die Papierherstellung und -beschichtung, Textilimprägnierung, Teppichrückseitenbeschichtung oder Modifizierung von Putz und Beton. Daneben ist es oft Bestandteil von Kaugummimassen und wird zur Beschichtung von Käse oder Wurst eingesetzt.
Handelsnamen von Polyvinylacetat sind beispielsweise Emultex F, Mowilith, Rhodopas, Vinamul oder Vinnapas.[4]
Umweltaspekte und Toxikologie
Untersuchungen auf Haut- und Schleimhautverträglichkeit im Tierversuch (LD50, Fütterung an Ratten, dermale Applikation) zeigten keine negativen Auswirkungen. Polyvinylacetat kann in Form von Dispersionen leicht ins Abwasser gelangen. Zwar ist es nach heutigem Wissen nicht toxisch, jedoch wurde es im wässrigen Milieu nur sehr schlecht abgebaut. Die Aufbereitung dispersionshaltiger Abwässer in Kläranlagen ist in der Regel kein Problem, sie sind leicht auszufällen und lagern sich dann im Klärschlamm ab, mit dem sie dann entsorgt werden können.
Nachweis
Das Abspalten von einfach nachweisbarer Essigsäure bei der thermischen Zersetzung kann als Hinweis auf das Vorhandensein von vinylacetathaltigen Polymeren und Copolymeren genutzt werden. Jedoch spalten auch Celluloseacetate Essigsäure bei der thermischen Zersetzung ab. Benetzt man Polyvinylacetat mit Iod-Iodkaliumlösung, entsteht eine purpurbraune Färbung, die sich durch Waschen mit Wasser noch verstärkt. Als weiteren Hinweis auf die Anwesenheit von Polyvinylacetat wird auch die Reaktion nach Liebermann-Storch-Morawski genutzt.
Siehe auch
Literatur
- Ernst Bartholomé, Ernst Biekert (Hrsg.): Ullmanns Encyklopädie der technischen Chemie. 4. Auflage. Verlag Chemie, Weinheim 1980, Band 19, ISBN 3-527-20019-3.
- Dietrich Braun: Erkennen von Kunststoffen – Qualitative Kunststoffanalyse mit einfachen Mitteln. Carl Hanser Verlag, ISBN 3-446-22425-4.
Weblinks
- Eintrag zu Polyvinyl acetate in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM)
Einzelnachweise
- Europäisches Arzneibuch – Grundwerk. 6. Auflage. Allgemeiner Teil, Monographiegruppen: Monographien K–Z. Deutscher Apotheker Verlag, Stuttgart 2008, ISBN 978-3-7692-3962-1, S. 3723–3724.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- So auf der Verpackung des "Weisser Vinylkleber, lösemittelfrei" der französischen Marke "Cléopâtre" zur Verwendung von Kindern ab 3 Jahren mit einer Abbindezeit von 30 Minuten.
- G. W. A. Milne: Gardner’s Commercially Important Chemicals: Synonyms, Trade Names, and Properties. Wiley-Interscience, Hoboken, N.J. 2005, ISBN 0-471-73661-9, S. 507.