Celluloseacetat
Celluloseacetat (Kurzzeichen CA, auch Zelluloseazetat[1][2], früher Acetylzellulose) ist eine Sammelbezeichnung für die Essigsäureester der Cellulose. Durch Einwirkung von Eisessig und Essigsäureanhydrid auf Cellulose (meist Zellstoff oder Baumwolllinters) unter Beisein von Katalysatoren (Schwefelsäure oder Zinkchlorid) muss zuerst das Cellulosetriacetat (Kurzzeichen CTA), das sogenannte Primäracetat, hergestellt werden, bei dem die drei Hydroxygruppen je Glucosebaustein verestert sind. Das ist notwendig, da eine partielle Veresterung auf direktem Weg nur zu Gemischen von nicht und vollständig acetylierter Cellulose führt. Da aber für die meisten Anwendungen das Cellulosetriacetat wegen seiner begrenzten Löslichkeit und schlechten Weichmacherverträglichkeit ungünstig ist, wird durch Wasserzugabe eine partielle Verseifung des Cellulosetriacetats vorgenommen, wobei je nach Temperatur und Einwirkungszeit Essigsäuregehalte von 41 bis 62,5 % im Ester eingestellt werden können. So werden verschiedene Typen von Sekundäracetaten (z. B. 2 ½ -Acetat und Diacetat) erhalten. In Abhängigkeit vom Veresterungsgrad verändert sich die Viskosität der Celluloseacetat-Typen (je höher der Veresterungsgrad, desto höher die Viskosität), wodurch sich ein breites Eigenschaftsspektrum und damit Produktspektrum erreichen lässt. Dieses reicht von Elektroisolierfolien, über Fasern für textile Zwecke und Faserkabel für Zigarettenfilter bis zu niedrigviskosen Zusatzstoffen für Klebstoffe und Textilhilfsmittel.[3][4][5][6]
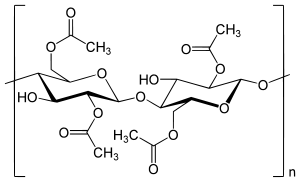
Celluloseacetat zählt zu den ältesten thermoplastischen Kunststoffen und wird als Derivat des Naturstoffes Cellulose zu den bio-basierten Kunststoffen gerechnet, die früher auch in ihrer Faserform als halbsynthetische Fasern bezeichnet wurden.[7]
Geschichte
Der Zeitraum von der ersten Darstellung bis zur ersten großtechnischen Erzeugung und Anwendung reichte von 1865 bis etwa Anfang/Mitte der 1920er Jahre.
- 1865 erzeugte Paul Schützenberger erstmals Celluloseacetat, indem er Cellulose in Form von Baumwollfasern mit Essigsäureanhydrid im geschlossenen Glasrohr auf 130 °C bis 140 °C erhitzte, bis es vollständig in Lösung ging. Nach Ausfällen mit Wasser, Waschen und Trocknen erhielt er ein weißes amorphes Pulver, das in Wasser unlöslich, aber in Alkohol und konzentrierter Essigsäure löslich war.[8][9]
- 1879 erfolgte eine Weiterentwicklung des Acetatverfahrens durch Antoine Paul Nicolas Franchimont, der herausfand, dass die Acetylierung der Cellulose durch Schwefelsäure oder Zinkchlorid katalysiert wird.[10]
- 1894 begann mit der Anmeldung des Britischen Patents Nr. 9676 durch Charles Frederick Cross und Edward John Bevan[11] die Einleitung einer neuen Periode in der Entwicklung, da in diesem Patent zum ersten Male der industrielle Wert und die technische Anwendung von Celluloseacetat erwähnt wurden.[12] Bei dem beschriebenen Verfahren wurden Cellulosehydrat und Acetylchlorid in Gegenwart eines Katalysators (Zinkchlorid) erwärmt und erstmals größere Mengen an Celluloseacetat erhalten, das in Chloroform löslich war. Durch Verdampfen des Lösungsmittels konnten zusammenhängende Häutchen erhalten werden, weshalb von den Erfindern das Celluloseacetat als Ersatz von Collodium in der Pharmazie und Chirurgie vorgeschlagen wurde.[13] Die Patente sind von Fürst Guido Henckel von Donnersmarck erworben und durch dessen eigene Patente[14][15] erweitert worden, so dass auf deren Grundlage in den Fürst Guido Donnersmarckschen Kunstseiden- und Acetatwerken in Sydowsaue bei Stettin (heute Szczecin-Żydowce, Polen) im Jahr 1898 das erste Celluloseacetat fabrikmäßig hergestellt werden konnte. Dort ist auch später in einer Versuchsanlage die erste, wenn auch nicht marktfähige Celluloseacetatseide produziert worden, nachdem Fürst Donnersmarck weitere Patente von Mork, Little und Walker erworben hatte.[16]
- Zwischen 1899 und 1901 meldete Leonhard Lederer Patente an,[17] die ebenfalls Grundlagen für eine industrielle Produktion von Celluloseacetat schufen, wobei immer noch von Hydratcellulose ausgegangen werden musste, was problematisch blieb.[10] Durch die Verwendung von Essigsäureanhydrid und Schwefelsäure war aber eine wesentlich niedrigere Reaktionstemperatur gegenüber Vorgängerverfahren möglich.
- 1901 startete eine Forschungsgruppe der Farbenfabriken vorm. Friedrich Bayer & Co, Elberfeld (heute Ortsteil von Wuppertal) unter Leitung von Arthur Eichengrün Entwicklungsarbeiten an einem Verfahren zur Herstellung hochwertiger Acetylcellulose. Es gelang erstmals Cellulosetriacetat auf Basis normaler Cellulose, also ohne den vorausgehenden Verfahrensschritt der Hydratisierung, herzustellen.[18] Dieses Celluloseacetat war leicht löslich in Chloroform, aber weniger löslich in Aceton.[19] Die vereinfachte Herstellung des Cellulosetriacetats hat aber die Erwartungen nicht erfüllt, so dass nach jahrelangen Versuchen seit etwa 1911 keine Produktion, auch nicht mehr versuchsweise, auf Basis dieses Verfahrenskonzepts stattfand.[20]
- 1904 meldete der Amerikaner George Wellington Miles ein Patent in den USA[21] und 1905 in Europa an, in dem die Gewinnung eines acetonlöslichen Celluloseacetats beschrieben wird. Allerdings gelang ihm keine großtechnische Verfahrensausführung und das erzeugte Acetat war durch starken Cellulosefaserabbau minderwertig.[22] 1904 wurde auch die BASF auf diesem Gebiet aktiv.[23] 1902 und damit vor Bekanntwerden der Patente von Miles war es jedoch schon bei Bayer den Chemikern Eichengrün und Becker gelungen, eine technisch verwertbare, acetonlösliche, nichtbrüchige, lagerbeständige Acetylcellulose zu produzieren.[24] Nach jahrelangem Rechtsstreit verkaufte Miles sein deutsches Patent an die Farbenfabriken vorm. Friedr. Bayer & Co, deren eigene Patentanmeldung zu diesem Sachverhalt letztlich mit diesem Patent[25] zusammengefasst wurde.[26] Das von den Erfindern als Cellulosehydroacetat erkannte Produkt wurde von den Farbenfabriken vorm. Friedrich Bayer & Co. unter dem Markennamen Cellit[27] in den folgenden Jahren fabrikmäßig produziert und zur Formulierung von Beschichtungsmassen für Flugzeuge und Luftschiffe, aber auch für die Herstellung von Beschichtungsträgern eines Sicherheitsfilms und von Acetatseide verwendet. Die Acetatseide wurde nach Vergabe der Lizenz für das von der Forschungsgruppe um Eichengrün im Jahr 1904 entwickelten und patentierten Trockenspinnverfahren[28] erstmals in der Kunstseidenfabrik Jülich 1907 produziert. Allerdings blieb die Bedeutung gering, da mit den bis dahin bekannten Farbstoffen diese Acetatseide nicht färbbar war und erst mit der Erfindung der Dispersionsfarbstoffe durch René Clavel im Jahr 1920 die breitere Nutzung der Acetatseide ermöglicht wurde.[29] Ebenfalls kaum an Bedeutung erlangte im ersten Jahrzehnt des 20. Jahrhunderts die von Eichengrün in seiner Tätigkeit als Leiter der Photofabrik Düsseldorf von Bayer vorangetriebene Herstellung von Kinofilmen auf der Basis des schwerentflammbaren Celluloseacetats, da sie im Gegensatz zu den zwar leichter entflammbaren Filmen auf Basis von Nitrozellulose zu dieser Zeit mechanisch weniger haltbar, teurer und schlechter klebbar waren. Eine Einführung dieser Sicherheitsfilme im Markt begann erst nach dem Ersten Weltkrieg Schritt für Schritt, umfassend sogar erst nach dem Zweiten Weltkrieg.[30]
- 1910/11 begann trotz einiger solcher Fehlschläge die Periode zunehmender fabrikmäßiger Erzeugung von verschiedenartigen Produkten auf der Basis von Celluloseacetat. Anteil daran hatten in Deutschland weiterhin die Forschungs- und Entwicklungsarbeiten von Eichengrün, die er ab 1909 in Berlin in seinem eigenen Laboratorium durchführte. Er entwickelte z. B. ein Verfahren, das es erlaubte, auf der Basis von Celluloseacetat ein dem Zelluloid ähnliches Produkt herzustellen. Die Rheinisch-Westfälische-Sprengstoff AG, Troisdorf, produzierte in Lizenz ab 1911 den Kunststoff Cellon, der durchsichtig, nicht brennbar und splitterfrei war. Anwendungen fand dieses Cellon für Gasmasken- und Fliegerbrillen, aber auch für Fensterscheiben im Boots-, Automobil-, Luftschiff- und Flugzeugbau. Außerdem erlangte die auf Eichengrüns Erfindungen beruhende Produktion von Celluloseacetatlacken eine große Bedeutung für die sich entwickelnde Flugzeug- und Luftschiffindustrie, wo sie zur Beschichtung der als Bespannung genutzten Leinen- und Baumwollgewebe eingesetzt wurden. Hergestellt wurden sie in Lizenz durch das Berliner Unternehmen Dr. Quittner Co. Selbst erzeugte er in seinem Berliner Unternehmen „Cellon-Werke Dr. Arthur Eichengrün“, das 1919 aus seinem Cellon-Laboratorium hervorgegangen war, vorrangig Celluloseacetat-Lacke für Isolationszwecke in der Elektrotechnik.[31] Ebenfalls von großer Bedeutung für die Ausweitung der Anwendungsgebiete des Celluloseacetats war die von Eichengrün 1919 entwickelte erste technisch brauchbare Spritzgussformmasse auf dieser Basis, die und deren daraus hergestellte Erzeugnisse später unter dem Markennamen Lonarit bekannt wurden. Der Berliner Mechanikermeister Hermann Buchholz baute 1921 in Zusammenarbeit mit Eichengrün die erste massenproduktionstaugliche Spritzgießmaschine für plastische Formmassen, auf der vorerst vor allem kleine Massenartikel wie Spulenkörper für die Elektroindustrie hergestellt wurden.[32]
- Einen bedeutenden Einfluss auf die Entwicklung der Celluloseacetatherstellung und von Produkten aus Celluloseacetat unterschiedlichster Art nahmen die Schweizer Gebrüder Camille und Henri (Henry) Dreyfus, die sich ab 1908 mit ihren Forschungs- und Entwicklungsarbeiten darauf konzentrierten und eine Vielzahl von Patenten anmeldeten, die für die Technik der Celluloseacetatherstellung von großer Bedeutung waren. Sie stellten z. B. den grundlegenden Zusammenhang zwischen hoher Viskosität, hoher Zugfestigkeit und Elastizität von Celluloseacetat dar.[33] Ende 1912 gründeten die Gebrüder Dreyfus mit Unterstützung des Unternehmers Alexander Clavel-Respinger die Cellonit Gesellschaft Dreyfus & Co. in Basel, in der Filme und Beschichtungslacke auf Celluloseacetatbasis, aber auch erste Mengen Acetatseide hergestellt wurden. Um den großen Bedarf an Acetatlacken für die Flugzeugindustrie zu decken, wurden durch die englische Regierung mit Hilfe der Gebrüder Dreyfus 1916 die British Cellulose and Chemical Manufacturing Co. in Spondon/Großbritannien aufgebaut. Um die kapitalintensiven Produktionsanlagen nach Ende des Ersten Weltkrieges und dem damit verbundenen stark rückläufigen Bedarf für die Flugzeuglacke weiter zu nutzen, konzentrierten sich die Gebrüder Dreyfus wieder auf die versuchsweise Herstellung von Acetatseide. Der Versuch war erfolgreich, weil es ihnen gelang, durch ein verbessertes Absorptionsverfahren eine nahezu vollständige Wiedergewinnung der bei der Herstellung anfallenden Lösungsmittel zu ermöglichen und damit die Herstellungskosten entscheidend zu senken. Gleichzeitig kam ihnen entgegen, dass der Schweizer René Clavel 1920 ein neues Färbeverfahren für Celluloseacetat gefunden hatte.[34] Die Gebrüder Dreyfus werden deshalb auch als die „Väter“ der Acetatseide angesehen.[35] Ab 1921 wurden an dem Standort Spondon des mittlerweile in British Celanese, Ltd, umbenannten Unternehmens ca. 500 kg Acetatseide pro Tag hergestellt. Sie kam unter dem Handelsnamen Celanese auf den Markt. Die Tagesproduktion wurde noch im gleichen Jahr verdoppelt und stetig erhöht. 1922 begann auch die Großproduktion der Acetatseide Celanese in den USA, anschließend auch in Werken in Europa.[36] In Deutschland wurde von der I.G. Farben und den Vereinigten Glanzstoff-Fabriken am 15. September 1925 die AcetA GmbH[37] für die Herstellung von Celluloseacetatfasern gegründet. In deren erweitertem Werk in Berlin-Lichtenberg wurde die Produktion nach dem Acetatverfahren 1927 aufgenommen.[38] Mitte der 1920er Jahre war damit die Produktionseinführung auf wesentlichen Anwendungsgebieten des Biokunststoffes Celluloseacetat erfolgreich abgeschlossen.
Herstellung
Bis heute existiert kein Verfahren, um Sekundärcelluloseacetate direkt herzustellen. Man wendet deshalb eine zweistufige Synthese an, da bei den Versuchen einer partiellen Veresterung der Cellulose ausschließlich ein Gemisch von nicht und vollständig acetylierter Cellulose entsteht. Cellulose wird zuerst immer vollständig zum Cellulosetriacetat und anschließend durch Hydrolyse in Celluloseacetate mit niederen Veresterungsgraden umgewandelt.
Die Herstellung unterteilt sich in folgende, meist durch direkten Stofffluss miteinander verbundene Prozessstufen:[39][40][41]
- Mechanische Aufbereitung des Zellstoffs: Der meist in Rollen- oder Plattenform bereitgestellte Zellstoff wird mittels unterschiedlicher Arten von Schreddern wie z. B. Hammermühle und Scheibenrefiner fibrilliert, wobei die aufeinanderfolgende Anordnung beider Schreddertypen eine optimale Auflösung bewirkt.
- Chemische Vorbehandlung: Die fibrillierte Cellulose wird mit Essigsäure (ggf. auch unter Zugabe geringer Mengen Schwefelsäure) unter mäßigem Umrühren bei 25 °C bis 50 °C für ca. 1 h behandelt, wodurch es zu einer kontinuierlichen Verdampfung und Kondensation der Essigsäure in den Zwischenräumen der Faserteilchen kommt. Dadurch quellen die Celluloseteilchen, was die Diffusion der Lösungsmittelteilchen in diese Teilchen während der folgenden Prozessstufe erleichtert. Neben dieser Essigsäuredampfvorbehandlung existiert auch eine Vorbehandlung in dünnbreiigem Zustand. Dabei wird der Zellstoff in große Mengen Wasser oder verdünnte Essigsäure eingebracht und intensiv umgerührt. Durch anschließende Verfahrensschritte wie Pressen oder Zentrifugieren wird die Konzentration der Cellulose im Brei immer weiter erhöht. Gleichzeitig wird Essigsäure in immer höherer Konzentration zugegeben. Der Vorteil dieses Verfahrens besteht in der Einsparung des Schredderns, da die Zellstoffschichten direkt in den Rührkessel zugegeben werden können.
- Acetylieren der Cellulose: Bei der kommerziellen Herstellung von Celluloseacetaten werden zur Acetylierung meistens das Eisessig-Verfahren oder das Methylenchlorid-Verfahren eingesetzt.
Bei Eisessig-Verfahren wird die vorbehandelte Cellulosemasse in einem Acetylierungsgemisch aus dem Lösungsmittel Eisessig mit einem Überschuss aus Essigsäureanhydrid, das als Veresterungsmittel dient, und mit Schwefelsäure als Katalysator unter intensiver mechanischer Durchmischung umgesetzt. Diese Reaktion ist stark exotherm und benötigt deshalb eine intensive Kühlung der Reaktionsbehälter. Der Veresterungsprozess wird durch Wasserzugabe beendet, wenn sich aus dem faserigen Brei eine hochviskose klare Reaktionsmischung herausgebildet hat. Diese Lösung (Dope) muss gelfrei sein und die angestrebte Viskosität aufweisen.
Beim Methylenchlorid-Verfahren wird im Acetylierungsgemisch Methylenchlorid als Lösungsmittel anstatt Eisessig eingesetzt. Da das niedrig siedende Methylenchlorid durch Destillation leicht abgeführt werden kann, ist eine Prozesssteuerung auch bei hochviskosen Lösungen sehr effektiv möglich. Selbst bei niedrigen Temperaturen kann es Cellulosetriacetat sehr gut lösen. Als Katalysator wird eine geringe Menge Schwefelsäure, aber häufig auch Perchlorsäure genutzt. Als Nebenprodukt der Reaktion wird allerdings meist auch Essigsäure gebildet, so dass das Lösungsmittel letztlich eine Mischung aus Methylenchlorid, Essigsäureanhydrid und Essigsäure ist.
Ein sehr seltenes heterogenes Verfahren ist das Faseracetat-Verfahren, das nur zur Herstellung von Cellulosetricacetat als Endprodukt verwendet wird. Dabei wird die Cellulose in einem Nichtlöser (wie z. B. Benzol) suspendiert und mit Essigsäureanhydrid unter Anwesenheit von Perchlorsäure als Katalysator verestert. - Partielle Verseifung (Hydrolyse): Um die gewünschten Sekundärcelluloseacetat-Typen zu erhalten, wird das gewonnene Cellulosetriacetat verseift. Dazu wird der Triacetatlösung unter Anwesenheit eines Säurekatalysator (meist Schwefelsäure) mittels Zugabe von Wasser unter Rühren und Erwärmen auf meist 60 bis 80 °C verseift. Über die Konzentration der Schwefelsäure, die Wassermenge und die Temperatur wird der Hydrolyseprozess so gesteuert, dass der gewünschte Molekülabbau erreicht wird. Der Hydrolyseprozess wird dann durch Zugabe von Salzen (z. B. Natrium- oder Magnesiumacetat), die den Säurekatalysator neutralisieren, abgebrochen. Vom Niveau der Einstellparameter hängt die Dauer des Hydrolyseprozesses ab.
- Ausfällen des Celluloseacetats: Wichtig beim Ausfällen des Celluloseacetats aus der Reaktionslösung mittels verdünnter Essigsäure ist es, gleichförmige und leicht waschbare Celluloseacetat-Flocken zu erhalten. Vor der Fällung muss das evtl. vorhandene Methylenchlorid vollständig abdestilliert werden. Die Essigsäure wird anschließend rückgewonnen.
- Waschen, Trocknen und Mischen der Flocken: Durch intensives Waschen, das meist im Gegenstromprinzip erfolgt, muss die Essigsäure bis auf geringste Spuren von den Flocken beseitigt werden, weil sonst Schädigungen („Ankohlen“) während des Trocknungsprozesses eintreten. Nach dem Abpressen der Waschflüssigkeit werden die Flocken auf einem von heißer Luft durchströmten Fließband-Trockner auf ca. 2–5 % Restfeuchte getrocknet. Für die spätere Herstellung von sehr hochwertigen, thermisch beständigen, farbhellen und farbstabilen thermoplastischen Formmassen werden die Celluloseacetatflocken vor dem endgültigen Trockenen in zusätzlichen Prozessschritten auch noch gebleicht und speziell stabilisiert, um thermischen Abbau und Verfärbung zu minimieren. Bevor die Celluloseacetatflocken in einen Sammelbehälter, von dem aus der Transport zu entsprechenden Verarbeitungsanlagen erfolgt, wird eine exakt gesteuerte Mischung der Flocken vorgenommen. Damit sollen Abweichungen der Celluloseacetate aus verschiedenen Herstellchargen ausgeglichen werden.
Für viele Weiterverarbeitungsprozesse werden die Flocken vorher meist zu feinen Pulvern gemahlen. Um das Celluloseacetat in thermoplastischen Kunststoffverarbeitungsverfahren wie z. B. Spritzgießen verwenden zu können, muss das Pulver außerdem mit geeigneten Weichmachern und anderen Zusatzstoffen, wie z. B. die Funktions-Zusatzstoffe zur Thermo-, Witterungs-, UV- und IR-Stabilisation,[42] gemischt werden. Die Mischungen können auf die entsprechenden nachfolgenden Verarbeitungsanforderungen abgestimmt werden. Aus dem durch Schmelzen fertiggestellten Compound wird Granulat hergestellt, das an die Kunststoffverarbeiter geliefert werden kann.
Eigenschaften
Celluloseacetat mit üblichen Substitutionsgraden ist löslich in Aceton, das Primäracetat hingegen nicht. Es lässt sich, anders als die reinen Zellulosefasern wie Baumwolle, Viskose und Lyocell, im Schmelzspinnverfahren verarbeiten. Es ist transparent, schwer entflammbar und leicht zu färben. Die Faser hat einen gelappten Querschnitt (was dem daraus hergestellten Gewebe aus Azetatseide ermöglicht, Luft einzuschließen und die Wärmeisolation zu fördern[43]), weist dadurch längsgerichtete Linien auf und hat einen seidenähnlichen Glanz. Bei 180 bis 200 °C ist Celluloseacetat thermoplastisch formbar. Bei Temperaturen über 85 °C leidet der seidenähnliche Glanz.
Die Trockenfestigkeit von Celluloseacetat liegt mit 10–16 cN/tex unter der von Viskose oder Cupro. Die Nassfestigkeit beträgt etwa 65–75 % der Trockenfestigkeit. Die Celluloseacetatfaser ist um ca. 30 % dehnbar. Da auch die reversible Dehnung relativ hoch ist, neigen Textilien aus Celluloseacetat weniger zum Knittern als z. B. Viskose.
Die Feuchtigkeitsaufnahme von Celluloseacetat ist mit ca. 6 % eher gering. Die Faser quillt wenig und trocknet schnell. Aufgrund der geringen Feuchtigkeitsaufnahme neigen Celluloseacetat-Textilien zur elektrostatischen Aufladung, obwohl der Kunststoff selbst wenig zur Aufladung neigt.
Die Fasern verbrennen mit leicht bläulicher Flamme und bilden Tropfen.
Verwendung
Celluloseacetat wird vor allem zu Textilfasern und Geweben verarbeitet. Textilien aus Celluloseacetatfaser, einer Form von Kunstseide, sehen Naturseide sehr ähnlich und fühlen sich fast ebenso weich an. Sie sind in der Regel knitterarm und pflegeleicht. Wegen der geringen Quellung und Wasseraufnahme ist das Gewebe für Regenmantel- und Schirmstoffe geeignet. Weiterhin werden daraus Blusen-, Hemden-, Kleider-, Futter-, Krawattenstoffe und Damenunterwäsche hergestellt.
In der Augenoptik wird Celluloseacetat für Brillenfassungen verwendet. Dank seiner thermoplastischen Eigenschaften lässt es sich gut anpassen.
In den optischen Schichten von Computerflachbildschirmen, Mobiltelefondisplays und anderen LC-Displays werden Folien aus Celluloseacetat – hier auch als Triacetat oder TAC-Film bekannt – verarbeitet. Ebenso besteht in den meisten Fällen die Ummantelung von Schnürsenkelenden aus Celluloseacetat.
Aufgrund seiner Schlagzähigkeit spielt Celluloseacetat in der Werkzeugindustrie seit Jahrzehnten eine bedeutende Rolle bei Schraubendrehergriffen, wenngleich in den letzten Jahren andere Materialien wie Polypropylen, Polyamid und thermoplastische Elastomere Celluloseacetat immer mehr verdrängen.
Celluloseacetat dient außerdem als Dielektrikum bei Metall-Lack-Kondensatoren.
Seit den 1910er Jahren löste Cellulose-Triacetat das Zelluloid als Träger für Filmmaterialien schrittweise ab, da es im Vergleich zum Zellulosenitrat nur schwer entflammbar ist. Zunächst wurden die Amateurfilmmaterialien auf CTA lanciert, in den Formaten 9,5 und 16. Filme mit einem Schichtträger aus Acetylzellulose trugen daher bis vor wenigen Jahren die Bezeichnung Safety Film oder Sicherheitsfilm. Heute ist der größte Anwendungsbereich der Celluloseacetatfaser die Herstellung von Zigarettenfiltern.
 Geöffneter Zigarettenfilter vor und nach dem Rauchen
Geöffneter Zigarettenfilter vor und nach dem Rauchen Geöffneter gebrauchter Zigarettenfilter – die Fasern aus Celluloseacetat sind braun gefärbt.
Geöffneter gebrauchter Zigarettenfilter – die Fasern aus Celluloseacetat sind braun gefärbt. Kosmetikstift aus Celluloseacetat
Kosmetikstift aus Celluloseacetat Transparente Würfel aus Celluloseacetat
Transparente Würfel aus Celluloseacetat Kugelschreiber aus Celluloseacetat
Kugelschreiber aus Celluloseacetat
Umweltbelastung und Abbaubarkeit


Da aktuell jährlich ca. 4,5 Billionen Zigarettenfilter aus Celluloseacetat in die Umwelt gelangen und sie damit in Verdacht stehen der häufigste Müll in der Umwelt überhaupt zu sein, geht von Celluloseacetat eine große Umweltbelastung aus.[44]
Anders als lange Zeit vermutet kann Celluloseacetat unabhängig vom Substitutionsgrad prinzipiell in der Natur abgebaut werden, wobei die Abbaurate stark vom Substitutionsgrad abhängt: Je höher der Substitutionsgrad, desto länger dauert der Abbau.[45] Außerdem hängt die Abbaugeschwindigkeit stark von den Umweltbedingungen ab. In stark biologisch aktiven Böden können CA-Fasern beispielsweise zwischen 4 und 9 Monaten komplett abgebaut sein[45], wohingegen der Abbau in anderen Bereichen mehrere Jahre[46] dauern kann.
Prinzipiell sind zwei Abbauwege zu unterscheiden: Der biologische Abbau über Mikroorganismen und der Photoabbau.[45]
Der biologische Abbau verläuft in zwei Schritten. Zunächst werden die Acetylgruppen über Acetylesterasen abgebaut, sodass Cellulose entsteht. Diese wird dann über Cellulasen komplett abgebaut.[45] Ein Grund für den langsameren Abbau von CA mit höherem Substitutionsgrad ist, dass Mikroorganismen diese ab einem Substitutionsgrad größer 1 nicht mehr als Nahrungsquelle wahrnehmen.[46]
Celluloseacetat absorbiert UV-Licht mit Wellenlängen von 280 nm oder weniger. Da das durch die Atmosphäre gefilterte Sonnenlicht keine kleineren Wellenlängen als 300 nm aufweist, ist kein direkter nennenswerter Photoabbau möglich. Allerdings kann ein indirekter Photoabbau durch sekundäre Effekte oder durch Zusatz von Photokatalysator wie TiO2 in der Natur induziert werden.[45]
Aufgrund der starken Umweltbelastung wird an zahlreichen Ansätzen geforscht, mit denen der Abbau von Celluloseacetat beschleunigt werden kann.[45][46] Ein Beispiel ist das Einbauen eines Säuredepots, welches Säure nach dem Rauchen einer Zigarette freisetzt. Durch die Säure kann der erste Abbauschritt der Deacetylierung beschleunigt werden.[46]
Pflege
Durch die chemische Modifikation ist Celluloseacetat gegenüber mikrobiellem Abbau beständiger als Cellulose. Hierbei hängt die Beständigkeit vom Substitutionsgrad der Cellulosefasern ab.[47] Schimmelpilze, Bakterien und auch Termiten bauen Celluloseacetat zu Kohlenstoffdioxid, Wasser, Sauerstoff und Humus ab. Die Lichtbeständigkeit ist gut, und dank der Unempfindlichkeit gegenüber Mikroorganismen ist Celluloseacetat auch gegenüber Witterungseinflüssen gut geschützt.
Sowohl gegenüber Säuren – hier insbesondere anorganische Säuren wie Schwefelsäure – als auch gegenüber Laugen ist die Faser sehr empfindlich. Gegenüber Oxidationsmitteln, wie sie in der Textilveredlung eingesetzt werden, ist die Faser beständig, nicht aber gegenüber den organischen Lösungsmitteln der chemischen Reinigung. Insbesondere ist Vorsicht bei Fleckenwasser geboten.
Aufgrund der Laugenempfindlichkeit sollten keine stark alkalischen Waschmittel eingesetzt werden. Die glatte Struktur der Faser und die damit verringerte Schmutzaufnahme machen eine Kochwäsche überflüssig. Um den seidenähnlichen Glanz nicht zu zerstören, empfehlen die meisten Hersteller, Stoffe aus Celluloseacetat nur mäßig warm (Stufe 1) im halbfeuchten Zustand auf der Rück- bzw. Innenseite zu bügeln.
Literatur
- A. Eichengrün: Acetylcellulose. (PDF; 54 MB) In: Ullmann’s Enzyklopädie der technischen Chemie. Band 1. 1914, S. 114–131
- Dissertation 1931 (PDF; 2,8 MB) über die Acetylierung von Baumwolle und anderer Cellulose
Weblinks
- Celluloseacetat. Material Archiv – Umfangreiche Materialinformationen und Bilder
- Generation Zero (PDF; 1,0 MB) Bioplastics Magazine
Einzelnachweise
- Duden | Zellulose | Rechtschreibung, Bedeutung, Definition, Herkunft. Abgerufen am 22. Januar 2022.
- Duden | Azetat | Rechtschreibung, Bedeutung, Definition, Herkunft. Abgerufen am 22. Januar 2022.
- Wilbrand Woebeken (Hrsg.): Kunststoff-Lexikon. Carl Hanser Verlag, München/Wien 1998, ISBN 3-446-17969-0, S. 78.
- Karl Oberbach (Hrsg.): Saechtling Kunststoff-Taschenbuch. Carl Hanser Verlag, München/Wien 2004, ISBN 3-446-22670-2, S. 551.
- Wolfgang Kaiser: Kunststoffchemie für Ingenieure – Von der Synthese bis zur Anwendung. 3. Auflage. Carl Hanser Verlag, München 2011, ISBN 978-3-446-43047-1, S. 346.
- Jürgen Falbe, Manfred Regitz (Hrsg.): Römpp – Lexikon Chemie. Band 1, 10., völlig überarb. Auflage. Georg Thieme Verlag, Stuttgart 1996, ISBN 3-13-107830-8, S. 638.
- Hans Beyer: Lehrbuch der organischen Chemie. S. Hirzel Verlag, Leipzig 1968, S. 341.
- Edward Chauncey Worden: Technology of Cellulose Esters. Volume Eight: Carbohydrate Carboxylates (Cellulose Acetate). D. Van Nostrand Company, New York 1916, S. 2530.
- Victor Emmanuel Yarsley: Über die Herstellung und physikalischen Eigenschaften der Celluloseacetate. Julius Springer Verlagsbuchhandlung, Berlin 1927, S. 5.
- Stefan Mecheels, Herbert Vogler, Josef Kurz: Kultur- & Industriegeschichte der Textilien. Wachter, Bönnigheim 2009, ISBN 978-3-9812485-3-1, S. 417.
- Patent GB9.676, angemeldet 17. Mai 1894
- Charles E. Mullin: Acetate Silk and its Dyes. D. Van Nostrand Company, New York 1927, S. 18 f.
- Edward Chauncey Worden: Technology of Cellulose Esters. Volume Eight: Carbohydrate Carboxylates (Cellulose Acetate). D. Van Nostrand Company, New York, 1916, S. 2534.
- Patent DE 105347 (angemeldet am 26. August 1898) (PDF) Commons
- Patent DE 112817 (angemeldet am 25. November 1898) (PDF) Commons
- Valentin Hottenroth: Die Kunstseide. 2., erweiterte Auflage. Verlag S. Hirzel, Leipzig 1930, S. 325.
- Patent DE118538 (angemeldet am 19. August 1899) (PDF) Commons. - Patent DE120713 (angemeldet am 18. August 1900). - DE163316 (angemeldet am 4. September 1901)
- Edward Chauncey Worden: Technology of Cellulose Esters. Volume 8: Carbohydrate Carboxylates (Cellulose Acetate). D. Van Nostrand Company, New York, 1916, S. 2536.
- Patent DE159524, angemeldet 2. August 1901
- Valentin Hottenroth: Die Kunstseide. 2., erweiterte Auflage. Verlag S. Hirzel, Leipzig 1930, S. 18.
- Miles-Patent US 838350 (angemeldet 23. November 1904)
- Valentin Hottenroth: Die Kunstseide. 2., erweiterte Auflage. Verlag S. Hirzel, Leipzig 1930, S. 19.
- BASF-Patent DE184201, angemeldet am 2. Oktober 1904
- Bayer-Patent US790565 (Triacetylcellulose) und Bayer-Patent US734123 (Acetylcellulose), beide angemeldet am 8. Januar 1902 von Arthur Eichengrün und Theodor Becker.
- Patent DE252706, angemeldet 30. September 1905
- Charles E. Mullin: Acetate Silk and its Dyes. D. Van Nostrand Company, New York 1927, S. 19.
- Bayer-Wortmarke DE412799 "Cellit" vom 17. Juni 1929, gelöscht am 5. April 2001. - Anm.: der Handelsname Cellit wurde von Bayer bereits ab 1905 benutzt.
- Patent GB 28.733, angemeldet 28. Dezember 1904
- Paul-August Koch, Günther Satlow: Großes Textil-Lexikon: Fachlexikon für das gesamte Textilwesen. Band A –K. Deutsche Verlags-Anstalt, Stuttgart 1965, S. 19.
- Elisabeth Vaupel: Lorbeer für Eichengrün – Hommage an einen vergessenen jüdischen Chemiker. In: Kultur & Technik. 1/2005, S. 48. deutsches-museum.de (PDF; 8,3 MB)
- Elisabeth Vaupel: Lorbeer für Eichengrün – Hommage an einen vergessenen jüdischen Chemiker. In: Kultur & Technik. 1/2005, S. 49. deutsches-museum.de (PDF; 8,3 MB) abgerufen am 6. November 2013
- Die historische Entwicklung der Spritzgiesstechnik. auf: mhborowski.de, abgerufen am 6. November 2013.
- Charles E. Mullin: Acetate Silk and its Dyes. D. Van Nostrand Company, New York 1927, S. 20.
- Valentin Hottenroth: Die Kunstseide. 2., erweiterte Auflage. Verlag S. Hirzel, Leipzig 1930, S. 19.
- Hermann Klare: Geschichte der Chemiefaserforschung. Akademie-Verlag, Berlin 1985, S. 55.
- Charles E. Mullin: Acetate Silk and its Dyes. D. Van Nostrand Company, New York 1927, S. 21.
- Edeltraud Hinkelmann: Vom Gasteer zu schillernden Farben – Zur Geschichte eines chemischen Unternehmens. In: Berlinische Monatsschrift (Luisenstädtischer Bildungsverein). Heft 7, 1999, ISSN 0944-5560, S. 31–32 (luise-berlin.de).
- Stefan Mecheels, Herbert Vogler, Josef Kurz: Kultur- & Industriegeschichte der Textilien. Wachter, Bönnigheim 2009, ISBN 978-3-9812485-3-1, S. 418.
- Ludwig Bottenbruch (Hrsg.): Kunststoff-Handbuch 3/1 – Technische Thermoplaste: Polycarbonate, Polyacetate, Polyester, Celluloseester. Carl Hanser Verlag, München/Wien 1992. ISBN 3-446-16368-9, S. 404–408
- Menachem Lewin (Hrsg.): Handbook of Fiber Chemistry. Third Edition. Taylor & Francis Group, Boca Raton 2007, ISBN 0-8247-2565-4, S. 778–784.
- Zakhar Aleksandrovič Rogowin: Chemiefasern: Chemie – Technologie. Georg Thieme Verlag, Stuttgart / New York 1982, ISBN 3-13-609501-4, S. 182–186.
- Hans Domininghaus (Hrsg.): Die Kunststoffe und ihre Eigenschaften. 6., neu bearbeitete und erweiterte Auflage, Springer-Verlag, Berlin/Heidelberg 2005, ISBN 3-540-21410-0, S. 1461
- Jürgen Thorwald: Die Stunde der Detektive. Werden und Welten der Kriminalistik. Droemer Knaur, Zürich und München 1966, S. 480 f.
- Florian Rötzer: Nicht Plastik, Zigarettenkippen sind der häufigste Abfall. Abgerufen am 8. Oktober 2019.
- Juergen Puls, Steven A. Wilson & Dirk Hölter: Degradation of Cellulose Acetate-Based Materials: A Review. In: Journal of Polymers and the Environment. Band 19, 2011, S. 152–165, doi:10.1007/s10924-010-0258-0.
- Raymond M. Robertson, William C. Thomas, Jitendrakumar N. Suthar & David M. Brown: Accelerated degradation of cellulose acetate cigarette filters using controlled release acid catalysis. In: Green Chemistry. Band 14, 2012, S. 2266–2272, doi:10.1039/c2gc16635f.
- Gottfried W. Ehrenstein, Sonja Pongratz: Beständigkeit von Kunststoffen. Hanser Fachbuch, 2005, ISBN 3-446-21851-3, S. 853–854.